115例胎龄≤32周早产儿喂养不耐受影响因素的病例对照分析
2019-07-02肖东凡陈蓉许天兰
肖东凡 陈蓉 许天兰
(贵州省人民医院,贵州 贵阳 550002)
近年来,随着NICU防治及抢救水平的不断提高,早产儿主要并发症及死亡原因有所改善,但新生儿坏死性小肠结肠炎(NEC)造成的早产儿死亡率较前有增加[1]。这可能与早产儿胃肠功能不成熟、肠道菌群的定植异常、胃肠道血液灌注异常有关[2-4];尤其是对胎龄≤32周的早产儿,其移行性运动复合波(MMC)呈低幅而无规律的收缩、吸吮及吞咽动作协调性尚未成熟[7],较晚期早产儿往往更易发生NEC[5]。FI是一种常见的的胃肠道疾病,为NEC的早期表现。至今我国关于胎龄≤32周早产儿FI的报告不多,除母乳喂养在减少胃肠道疾病有较强的证据外,其它疗效尚未得到认可[6]。本文主要分析胎龄≤32周的早产儿喂养不耐受影响因素,以期为FI的发生提供临床参考依据。
1 资料与方法
1.1一般资料 收集2014年1月至2016年12月于我院产科娩出、生后12h内入住我院NICU的胎龄≤32周早产儿的临床资料。排除消化系统畸形及先天性心脏病、未开奶自动放弃治疗或死亡、住院时间<7d、遗传代谢疾病、临床资料不全的患儿后,共收集115例患儿,住院期间早产儿的喂养量及添奶速度均参照2006年中国新生儿营养支持临床应用指南[7]。FI参照文献[8]中的诊断标准。耐受组41例,中位体质量1 585(1 367.5,1 807.5) g,中位胎龄为31.14(30.28,31.78)周;不耐受组74例,中位体质量为1 400(1 175,1 620) g,中位胎龄为30.71(29.35,31.64)周,发病时间于生后0.41~19.5 d,中位发病时间为2.5(1.45,4.35) d。另将所有患儿的相关研究因素按产前、产时、产后三部分收集,即,(1)产前因素:母亲妊娠期疾病、母孕期地塞米松的使用、抗生素的使用;(2)产时因素:包括宫内窘迫、羊水异常、胎盘异常、脐带异常、胎膜早破、多胎、胎龄、出生体质量;(3)产后因素:①产后基本情况:首次开奶时间、首次胎便排出时间、胎便排尽时间。②生后疾病及干预情况:新生儿窒息、感染性疾病、灌肠、呼吸机的使用、肺表面活性物质的使用、甲基黄嘌呤类药物的使用、输血、口服益生菌。两组患儿一般资料的比较差异无统计学意义(P>0.05)。
1.2方法 所有入选对象的临床资料均由专门培训过的调查人员使用统一的信息采集表进行收集,并对收集的资料进行全面检查、核对。然后,采用双人双录入的方式输入计算机中。专业技术控制:喂养不耐受的判定由管床护士发现后报告管床医生,请示我科两名副主任以上医师后按喂养不耐受诊断标准统一给予诊断或排除。
2 结 果
2.1产前因素对喂养不耐受的影响 单因素分析结果显示,两组患儿在母亲妊娠期疾病、母孕期地塞米松使用、抗生素的使用上差异无统计学意义(P>0.05)。见表1。
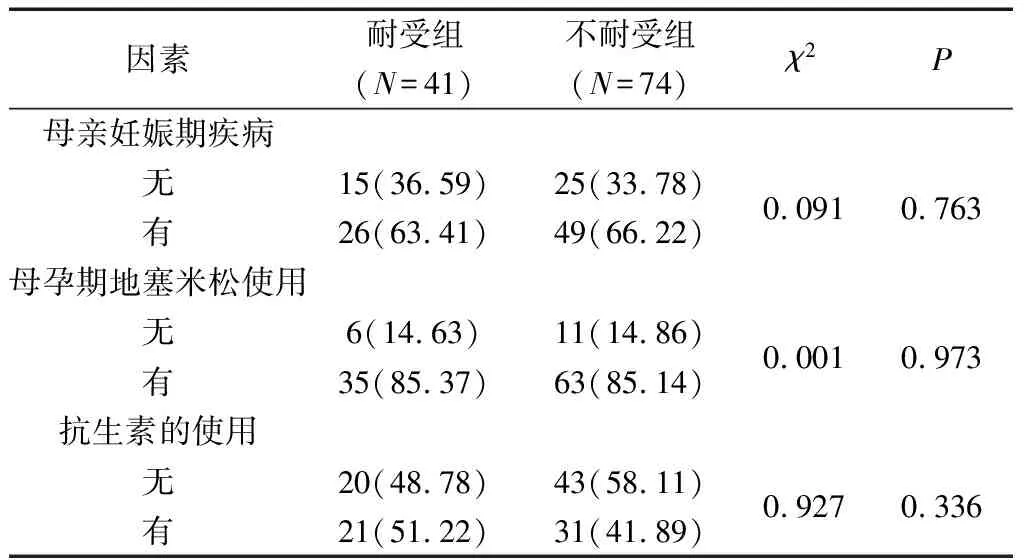
表1 两组的产前因素比较[n(%)]
2.2产时因素对喂养不耐受的影响 单因素分析结果显示,两组在脐带异常、多胎、出生体质量上差异具有统计学意义(P<0.05)。Logistic分析结果显示,出生体质量是FI的产时独立影响因素(P<0.05),出生体质量与FI受呈负相关。见表2~3。

表2 耐受组与不耐受组的产时异常比较[n(%)]
注:*以中位数(四分位数间距)表达。

表3 产时因素的二元Logistic回归分析
2.3产后因素对喂养不耐受的影响 单因素分析结果显示,胎便排尽时间、感染性疾病、呼吸机的使用、甲基黄嘌呤类药物的使用、口服金双歧与FI相关(P<0.05),其余各因素在两组间比较差异无统计学意义(P>0.05)。Logistic分析结果显示,胎便排尽时间、口服金双歧是FI的产后独立影响因素(P均<0.05)。其中,胎便排尽时间是FI的危险因素,口服金双歧是FI的保护因素。见表4~7。

表4 两组的产后基本情况比较

表5 两组在窒息等级上的差异分析[n(%)]
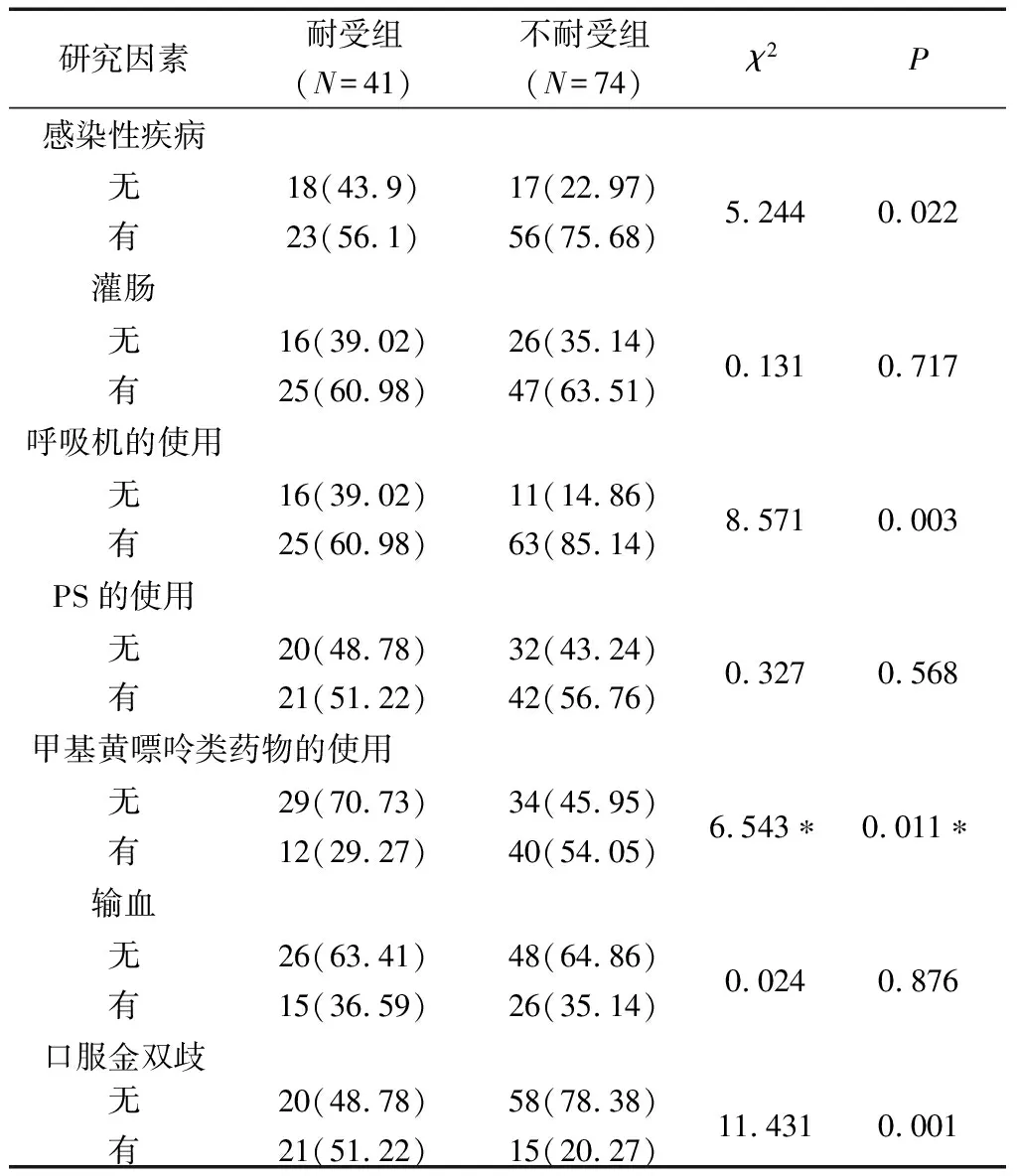
表6 两组在生后疾病及干预情况上的差异分析[n(%)]
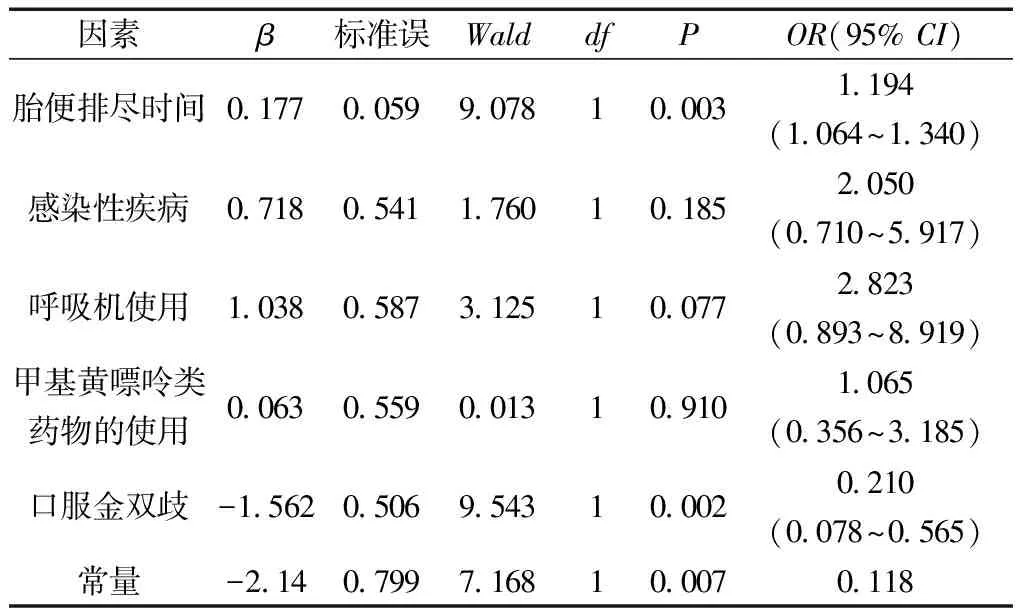
表7 产后因素的二元logistic回归分析
2.4诊断价值 出生体质量、胎便排尽时间这两个指标的曲线下面积与AZ=0.5比较,差异有统计学意义(P值均<0.05)。见图1。出生体质量≤1405g为受试者工作特征(ROC)曲线的最佳临界值,对应的特异性为73.17%,敏感性为54.05%;胎便排尽时间≥11天为ROC曲线的最佳临界值,对应的特异性为73.17%,敏感性为66.22%。见表8。

图1 出生体质量、胎便排尽时间的ROC曲线

项目胎便排尽时间出生体质量AUC0.7210.660SE0.05000.051395% CI0.629~0.8010.566~0.746P0.0000.0013临界值≥11d≤1 405 g敏感性/%66.2254.05特异性/%73.1773.17
3 讨 论
1996年R.A.Ringer等[9]研究表明,胎龄<29周的所有早产儿均发生了FI。近年来,随着喂养问题被不断关注,早产儿喂养不耐受的发生率有所下降,但仍作为非常早产儿的常见病之一。有报道[10-11]显示,胎龄≤32周的喂养不耐受发生率分别为67.6%、67.4%,与本文结果显示FI发生率(64.3%)相近。FI可造成住院时间延长、院内感染发生、肠外营养相关肝损害等,也造成神经系统功能发育受累、孤独症等不良事件,给家庭和社会带来了巨大的经济负担及精神压力。因此,研究喂养不耐受的影响因素对临床工作的指导有一定的必要性。
本文结果中未发现母亲妊娠期疾病、抗生素的使用是FI的高危因素(P>0.05)。地塞米松作为一种肾上腺糖皮质激素,于产前使用可以促进早产儿胃肠器官的发育成熟;抑制IL-1β刺激胎儿肠上皮细胞(IEC)释放炎症因子(IL-6、IL-8)的过程,维持肠道内稳态,增强肠粘膜的屏障功能,对不成熟的肠道具有一定保护作用[12];同时其亦可以促进血浆胃动素(MOT)水平升高,降低FI的发生率。本文结果显示,母亲孕期地塞米松的使用与胎龄≤32周早产儿FI的发生无相关性。原因可能与多数具有早产儿风险的母亲产前仅单疗程使用地塞米松,且其使用的时间距早产儿出生时间相差7 d以上或小于48 h,引起激素对胎儿促成熟方面的药理作用减弱、消失,可能导致相应的器官出现可逆性改变或未发育成熟有关[13]。本文结果还显示,出生体质量是胎龄≤32周FI的保护性因素。推测原因如下[14-16]:(1)出生体质量越低,早产儿胃肠动力越不成熟,越易出现消化道症状。(2)出生体质量越低,乳酸酶、肠激酶活性越低且含量越少,胆汁酸浓度越低,肠管长度越短,绒毛膜体质量减轻以及肠道隐窝的深度变浅等,不利于肠道内营养物质吸收。(3)出生体质量越低,免疫系统越不成熟,抵抗病原菌的能力越弱。另外,大多数非常早产儿,住院期间的侵入性操作、氧中毒以及其他病理原因,均易造成肠道菌群紊乱、增殖细胞加速凋亡等,从而导致FI发生。本文结果显示,出生体质量的曲线下面积AUC在机会线以上,且以1 405 g作为最佳临界值时,特异性为73.17%,敏感性为54.05%。提示出生体质量≤1 405 g对FI患儿可能具有一定的诊断预测价值。说明在临床工作中需加强对有早产儿风险孕妇的随访,努力减少体质量≤1 405 g的新生儿娩出;同时需警惕体质量≤1 405 g的早产儿消化道症状、减少不必要的侵入性操作、动作轻柔,同时严格遵守无菌操作,以减少喂养不耐受的发生。
研究[17]显示,缩短胎便排出时间,有利于肠内营养物质的吸收,这可能与胃肠蠕动相对较快,减少了喂养困难的发生有关,与本文的结果相似。此外,本文对胎便排尽时间行诊断价值运算时发现,胎便排尽时间≥11 d对FI具有较好的诊断预测价值。然而喂养不耐受常开始出现于生后6~8 d内[18],本文显示75%的FI患儿发病时间处于生后4.35 d之前,故将其作为预测FI的指标,临床意义并不大。若能早期使用更直观的指标(如胃电图、胃动素等)反应早产儿胃肠蠕动可能更有临床价值。本文结果中,口服金双歧是胎龄≤32周FI的保护性因素,且使用期间未见药物相关败血症、器官功能障碍等不良反应。因此,临床实践中,对未存在免疫功能缺陷的早期早产儿,新生儿医师可预防性使用口服益生菌来减少喂养不耐受的发生。但在使用益生菌期间,需警惕那些不明原因导致相关感染指标升高以及临床表现不佳的早产儿存在其相关感染的可能性,必要时应行厌氧菌培养。
综上所述,非常早产儿的喂养不耐受与早产儿消化系统本身的成熟度相关,在临床工作中需加强对出生体质量≤1 405 g早产儿的喂养耐受性的监测。口服益生菌、缩短胎便排尽时间可减少喂养不耐受的发生率,但因本研究样本量少,发病机制尚不明确,有待于今后进一步研究。
