精细化营养支持护理路径在腹腔镜下胃部恶性肿瘤切除术围术期患者中的应用效果▲
2019-06-19金鲜珍廖春艳乔莉娜
樊 慧 金鲜珍 廖春艳 乔莉娜
(西安交通大学第一附属医院普外科,陕西省西安市 710061,电子邮箱:332801757@qq.com)
营养不良可增加患者的住院时间、并发症和病死率[1],Lew等[2]研究认为,危重症患者常伴有严重代谢紊乱,其营养不良发生率高于普通疾病患者。随着自然环境及人类饮食结构的改变,胃部恶性肿瘤患病率逐年增加,以手术切除病灶为主的综合疗法是其主要治疗方法[3]。随着腹腔镜技术的快速发展,目前切除胃部恶性肿瘤多选用腹腔镜下手术,由于患者术前存在癌肿过度消耗、组织蛋白质分解水平亢进、负氮平衡和水电解质代谢紊乱等原因,导致术后并发症发生率上升,不利于康复,影响治疗效果[4]。施行精细化营养支持治疗有利于患者平稳度过围术期[5],利于患者营养平衡,降低不良反应发生率[6-8]。营养支持分为肠内营养支持和肠外营养支持,肠内营养支持对术后康复起着关键作用[9-11]。我院对接受腹腔镜下胃部恶性肿瘤根治术的患者,在围术期给予精细化营养支持护理路径,收到较好效果,现将结果报告如下。
1 资料与方法
1.1 临床资料 选取2017年4月至2018年5月在我院普通外科接受腹腔镜下胃部恶性肿瘤根治术的患者140例作为研究对象。入选标准:(1)经组织病理学检查确诊为胃部恶性肿瘤;(2)年龄18~82岁;(3)择期在腹腔镜下行胃部恶性肿瘤根治术;(4)签署知情同意书。排除标准:(1)并发严重的心、脑、肾、肝疾病及精神疾病,存在沟通障碍患者;(2)孕期及哺乳期妇女;(3)有严重营养不良、低蛋白血症者;(4)合并其他恶性肿瘤;(5)并发上消化道出血、麻痹性肠梗阻等不宜施行胃肠道营养支持者;(6)有咽喉部疾病史者。采用随机数字表法将患者分为两组,每组70例。观察组男43例,女27例,年龄19~77(44.6±7.8)岁;体质量44~70(59.8±1.3)kg;组织病理类型均为腺癌;原发肿瘤-区域淋巴结-远处转移(tumor-node-metastasis,TNM)分期:Ⅰ期14例,Ⅱ期34例,Ⅲ期22例。对照组男39例,女31例,年龄18~82(46.3±6.9)岁;体质量45~67(59.4±1.1)kg;组织病理类型均为腺癌;TNM分期:Ⅰ期13例,Ⅱ期36例,Ⅲ期21例。两组患者性别、年龄、体质量、病理类型、TNM分期资料比较,差异均无统计学意义(均P>0.05),具有可比性。本研究获得医院伦理委员会审批通过。
1.2 方法 两组患者均给予胃部疾病和腹腔镜手术常规护理,包括入院宣教,完善相关检查及心理护理等。观察组围术期给予精细化营养支持护理路径方案[6,12-13]:(1)建立精细化营养支持护理路径小组:由主管医师、主管护师、护师等数人组成,由主治医师对小组成员进行精细化营养支持方案内容培训,由主管护师对护师进行护理路径内容及相关知识培训;参考相关文献由我院肠内营养专人制定腹腔镜下胃部恶性肿瘤切除术精细化营养支持护理路径表格,小组成员严格按照该表格内容要求对患者施行精细化营养支持干预。(2)精细化营养支持干预:入院时对患者进行全面的营养评估,根据个体评估结果,小组讨论后分别制定个体化的精细营养支持干预方案并填入表格,严格按照干预方案要求施行精细化营养干预:① 术前:向患者及家属详细讲解肠内营养支持的目的、作用、人体适应过程及其在治疗中可能会出现反流、误吸、鼻饲导管阻塞或脱落、鼻咽部和胃肠道不适等并发症及其处理方法;讲解胃肠导管的使用、护理方法及注意事项;进行术前饮食宣教和心理护理。② 手术后当天:按常规方法行胃肠插管,按术前制定个体化的精细化营养支持方案给予肠内营养支持,用微泵匀速持续泵入营养剂,观察营养支持治疗过程中出现的肠道不耐受等并发症情况。③ 术后第2天:再次评估患者肠道耐受情况,及时调整肠内营养液用量;观察有无不良反应,若出现不良反应及时报告医生处理;指导患者在床边活动,观察肠鸣音和肛门排气情况。④ 术后第3~6天:再次评估肠道耐受情况,及时调整肠内营养液用量;术后第6天,给予饮食指导,试行流质饮食,密切观察进食后反应。⑤ 术后第7天:开展营养专题讲座,与患者共同制订出院后饮食和康复计划。
1.3 观察指标 (1)血清白蛋白、前白蛋白和血红蛋白水平及其体质量:采集患者术前、术后第7天空腹肘部静脉血5 mL,置入肝素抗凝管,以2 500 r/min,离心10 min,取血清,应用日立公司生产的全自动生化分析仪(型号:TBA-40FR)检测血清白蛋白、前白蛋白水平;采用ABX Micros 60(MDSIN公司,法国)生化分析仪检测血红蛋白水平,均严格按照说明书进行操作和判读。(2)并发症发生率:包括术后反流误吸所致的吸入性肺炎、腹胀呕吐及胃潴留等。患者呕吐物为4~6 h以前摄入的食物,或空腹时间>8 h,胃内残留量>200 mL时判定为胃潴留。(3)患者对护理工作满意度:患者出院时采用自制的满意度调查问卷对患者进行调查,按“满意”“基本满意”“不满意”评定,总满意率=(基本满意+满意)例数/总例数×100%。
1.4 统计学分析 采用SPSS 20.0统计学软件进行统计学分析。计量资料以(x±s)表示,组间比较采用t检验,组内治疗前、后的比较采用配对t检验。计数资料以例数(百分比)表示,比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者体质量、血清白蛋白、前白蛋白及血红蛋白水平比较 手术前,两组患者体质量、白蛋白、前白蛋白及血红蛋白水平比较,差异均无统计学意义(均P>0.05),手术后第7天时,对照组血清白蛋白、前白蛋白及血红蛋白水平低于治疗前(t=5.176、7.213、6.332,均P<0.001),并且低于观察组(均P<0.05),但是观察组患者的白蛋白、前白蛋白及血红蛋白水平与手术前水平比较,差异均无统计学意义(t=2.220、0.956、1.223,P=0.192、0.069、0.517),见表1。
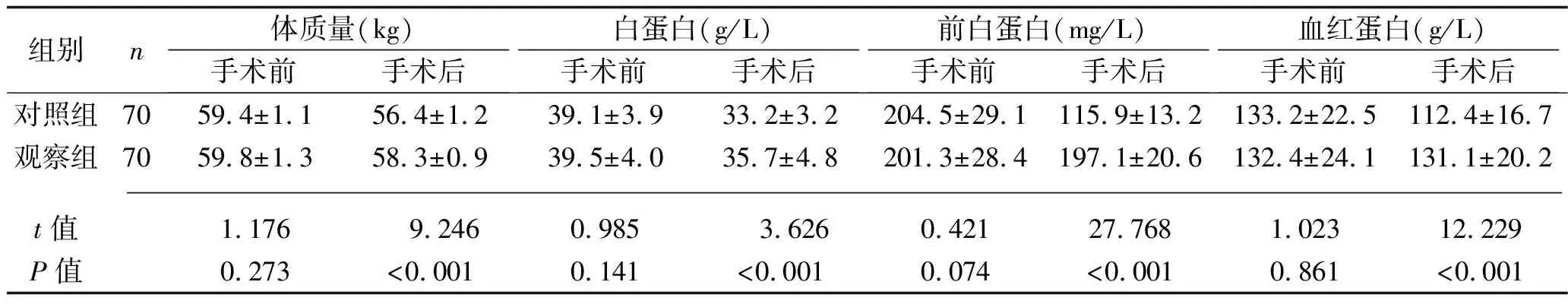
表1 两组患者手术前、后体质量、白蛋白、前白蛋白及血红蛋白水平比较(x±s)
2.2 两组患者并发症发生率比较 观察组不良反应发生率均低于对照组(均P<0.05)。见表2。

表2 两组患者术后并发症发生率比较[n(%)]
2.3 两组患者满意率比较 观察组患者对护理工作的总满意率高于对照组(χ2=9.856,P=0.002)。见表3。

表3 两组患者对护理服务满意度比较[n(%)]
3 讨 论
目前,胃肠道恶性肿瘤最有效的治疗方法仍然是外科手术,手术前后给予营养支持可提高治疗效果[3]。Sullivan等[14]报道,肠内营养支持可增加患者胃肠道血流量,促进胃肠道蠕动,维持胃肠黏膜的完整性和基本功能。有学者[15]认为胃肠道恶性肿瘤术后患者给予肠内营养支持治疗可改善肠道功能,促进营养吸收。Simpson等[16]研究发现,营养支持治疗对维持术后患者血液谷氨酞胺水平的稳定有重要作用,并有保护患者胃肠黏膜完整性、促进肠黏膜再生的作用。阮戈[17]观察发现,胃肠道恶性肿瘤患者术前营养不良发生率较高,营养不良严重影响预后,围术期给予精细化营养支持有助于改善患者生活质量,促进术后康复。Arends等[18]认为营养状况是影响恶性肿瘤患者术后愈后的重要因素之一,建议对胃肠道恶性肿瘤术后患者给予低糖、高脂肪类营养支持辅助治疗。Vashi等[19]认为精细化营养支持护理路径能改善患者术后营养状况,提高患者生存质量。本研究结果显示,手术后第7天时,对照组患者血清白蛋白、前白蛋白及血红蛋白水平低于手术前及观察组(均P<0.05),但观察组患者上述指标与手术前水平比较,差异均无统计学意义(均P>0.05),提示精细化营养支持护理路径可有效改善腹腔镜下胃部恶性肿瘤切除术患者围术期的营养状况。
随着现代医疗技术的日益发展,肠内、肠外营养支持方案被广泛应用于各种手术后患者的辅助治疗,并具有积极的作用。Fujiya等[20]认为肠内、肠外营养支持均可提高营养不良患者的机体免疫功能。本研究结果显示,给予腹腔镜下胃部恶性肿瘤切除术患者精细化的营养支持治疗,能改善患者的营养状况,并且术后不良反应发生率低,患者满意度高(均P<0.05)。
总之,精细化营养支持护理路径对腹腔镜下胃部恶性肿瘤切除术患者有积极作用。
