Pringle法和选择性半肝阻断法对肝细胞癌患者术后预后的影响
2019-06-19黄正锋黄文文李立志唐毓林张涌泉黄国振许景洪
黄正锋 黄文文 李立志 唐毓林 张涌泉 黄国振 许景洪
(广西壮族自治区民族医院暨广西医科大学附属民族医院肝胆胃肠外科,南宁市 530021,电子邮箱:50805564@qq.com)
肝细胞癌是世界五大常见的恶性肿瘤之一,其发生隐匿,进展迅速,早期诊断困难,预后较差,给社会及患者带来严重的经济负担[1]。肝切除术是有效提高肝细胞癌患者生存率主要手段,术中控制出血是保证手术安全的重要措施之一[2],术中、术后大出血和输血可增加肝切除术后患者的死亡率。研究发现肝脏血流阻断能够影响肝细胞癌术后肝功能[3-4],但关于其影响肝细胞癌远期生存率的报道较少。本研究探讨不同阻断肝脏血流方法对肝癌患者长期生存率的影响,现报告如下。
1 资料与方法
1.1 临床资料 收集2012年3月至2015年3月在我院确诊为肝细胞癌的184例患者的临床资料,所有患者均采用根治性手术治疗,且术后病理证实为肝细胞癌。纳入标准:(1)肿瘤数目不超过3个;(2)所有肿瘤局限于肝脏一段或者半肝。排除肝外转移等手术禁忌证。根据肝门阻断方式不同,将患者分为Pringle组122例和选择性半肝阻断组62例。Pringle组:间歇性阻断肝门,每次可连续阻断肝门15 min,然后开放5 min,可重复3次。选择性半肝阻断组:根据肿瘤所在肝位置选择性阻断一侧肝脏。两组患者的性别、年龄、体质指数、HBsAg、肝细胞癌家族遗传史、胆红素、血清总蛋白、白蛋白、ALT、AST 、凝血时间、血小板、肿瘤大小、甲胎蛋白、抗病毒治疗、是否合并肝硬化、切除方式、是否输血、出血量、肿瘤包膜完整性、切除肿瘤边缘、Edmondson分级以及巴塞罗那分期等一般资料比较,差异均无统计学意义(均P>0.05)。见表1。

续表1
1.2 随访 所有患者术后第1个月返院复查,以后每3个月随访1次,2年后每6个月随访1次。通过住院或门诊、书信及电话等方式对患者进行随访,随访内容包括肝功能、血清甲胎蛋白水平、腹部超声、CT或MRI检测结果。随访终点事件为患者死亡,截止日期为2017年3月。
1.3 统计学分析 采用SPSS 20.0软件进行统计分析。符合正态分布的计量资料以(x±s)表示,比较用t检验;非正态分布的计量资料资料采用中位数以及四分位数[M(P25,P75)]表示,比较采用秩和检验;计数资料以例数和百分比表示,比较采用χ2检验;两组累计生存率和复发率比较采用Kaplan-Meier法,采用Cox回归模型分析影响患者预后的因素。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者术后累计生存率比较 Pringle组的术后中位生存期为27.3个月,术后1年、2年、3年累计生存率分别为83.6%、66.4%、50.7%;选择性半肝阻断组的术后中位生存期为28.5个月,术后1年、2年、3年累计生存率分别为80.3%、71.0%、51.4%。两组术后生存率比较,差异无统计学意义(χ2=0.094,P=0.759)。见图1。
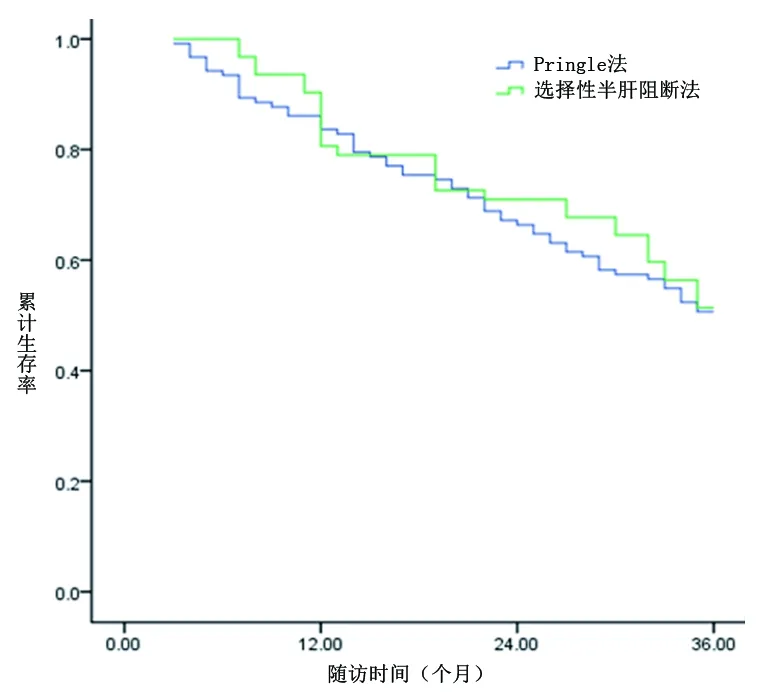
图1 两组患者术后生存率的Kaplan-Meier曲线
2.2 两组患者术后复发率比较 Pringle组术后1年、2年、3年复发率分别为27.2%、47.9%、58.7%;选择性半肝阻断组术后1年、2年、3年复发率分别为22.6%、38.7%、51.6%。两组术后复发率比较,差异无统计学意义(χ2=1.173,P=0.279)。见图2。

图2 两组患者术后复发率的Kaplan-Meier曲线
2.3 导致肝细胞癌术后死亡的因素 以患者的预后为因变量(死亡=1,存活=0),以AST、甲胎蛋白及输血情况为协变量(赋值情况见表2),采用Cox回归模型对肝细胞癌的术后预后进行单因素分析,然后将单因素分析中具有统计学意义的变量作为协变量做多因素分析。结果显示,AST≥70 U/L、甲胎蛋白≥400 ng/mL及输血治疗是影响肝细胞癌患者术后预后的独立危险因素(均P<0.05)。见表3~4。
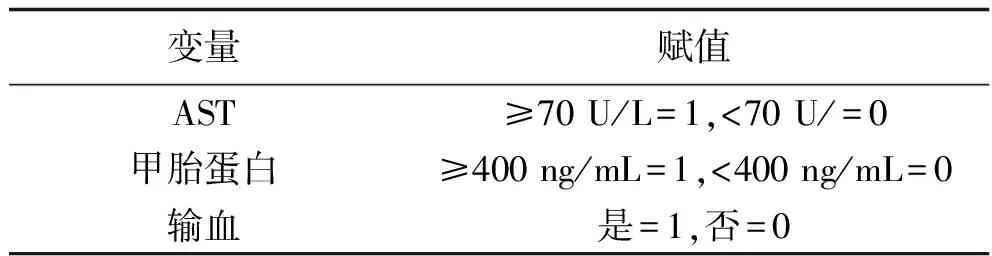
表2 变量赋值情况
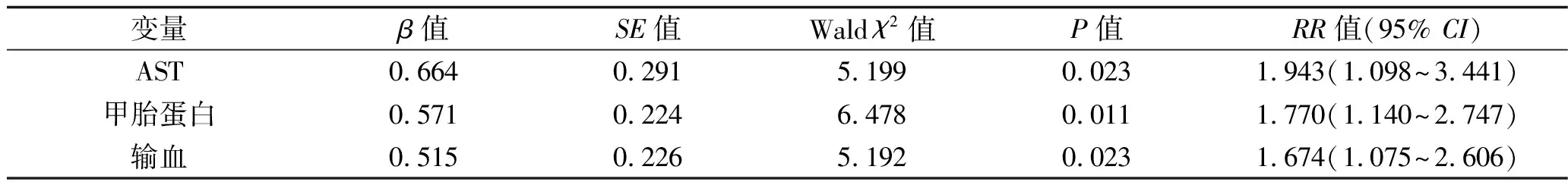
表3 导致肝细胞癌患者术后死亡的单因素分析
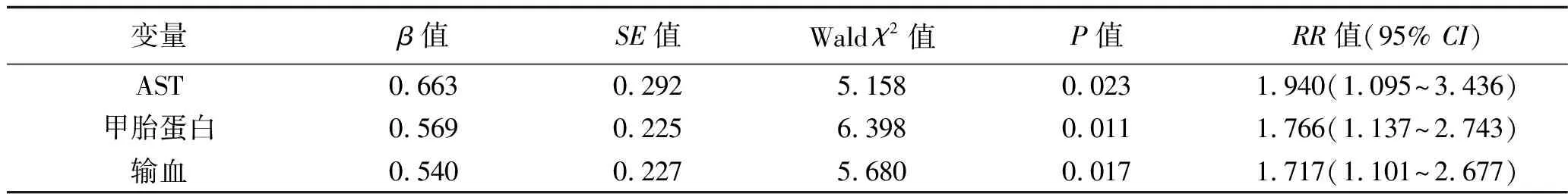
表4 导致肝细胞癌患者术后死亡的多因素分析
2.4 肝细胞癌术后复发的因素分析 以患者的复发情况为因变量(复发=1,不复发=0),以AST、血小板计数、甲胎蛋白水平、肿瘤大小、肿瘤数目、巴塞罗那分期、出血量及输血情况为协变量(赋值情况见表5)。采用Cox回归模型对肝细胞癌的术后复发情况的影响因素进行单因素分析,然后将单因素分析中具有统计学意义的变量作为协变量做多因素分析。结果显示,血小板计数<100×109/L、肿瘤大小≥5 cm、肿瘤个数为2~3个以及输血量≥1 000 mL是导致肝细胞癌患者术后复发的独立危险因素(均P<0.05)。见表6~7。

表5 变量赋值情况
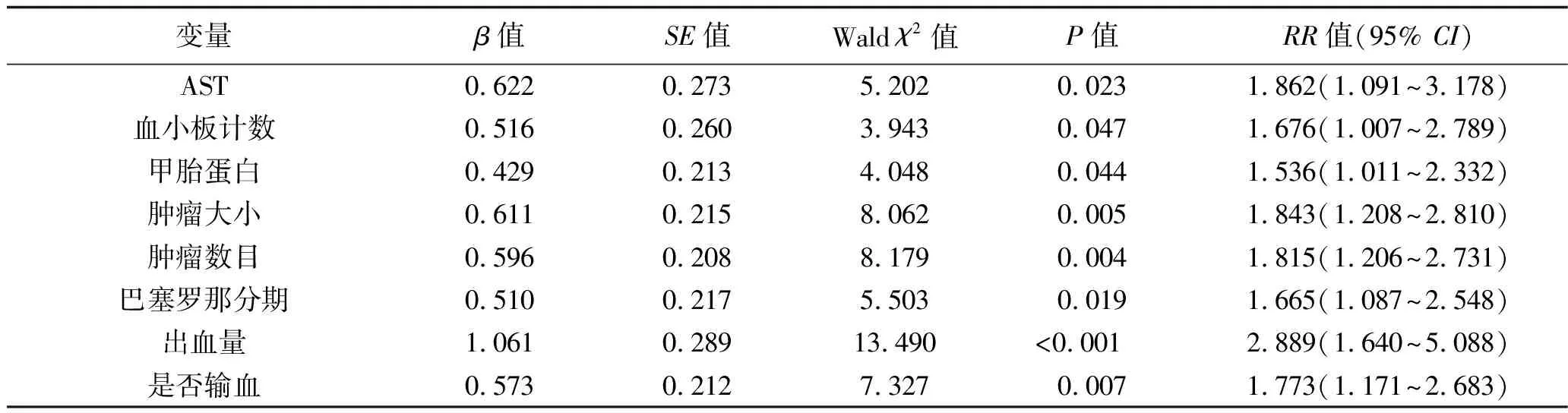
表6 导致肝细胞癌患者术后复发的单因素分析
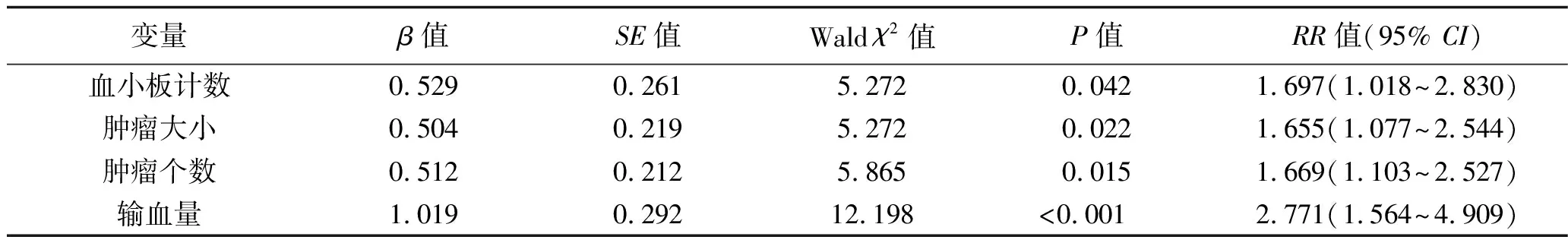
表7 导致肝细胞癌患者术后复发的多因素分析
2.5 亚组分析 对于肿瘤最大径≥5 cm的患者:Pringle组和选择性半肝阻断组的1年、2年、3年累计生存率分别为87.0%、62.3%、46.6%和78.4%、70.3%、48.6%;两组生存率比较差异无统计学意义(χ2=0.064,P=0.800),见图3。对于甲胎蛋白≥400 ng/mL的患者:Pringle组和选择性半肝阻断组的1年、2年、3年累计生存率分别为83.7%、69.6%、55.3%和88.6%、79.5%、52.3%;两组比较差异无统计学意义(χ2=0.014,P=0.907),见图4。对于巴塞罗那分期为A期的患者:Pringle组和选择性半肝阻断组的1年、2年、3年累计生存率分别为84.3%、68.5%、52.7%和84.0%、74.0%、55.7%;两组比较差异无统计学意义(χ2=0.302,P=0.582),见图5。对于HBsAg(+)患者:Pringle组和选择性半肝阻断组的1年、2年、3年累计生存率分别为81.9%、64.8%、48.4%和88.5%、73.1%、57.5%;两组比较差异无统计学意义(χ2=1.291,P=0.256),见图6。
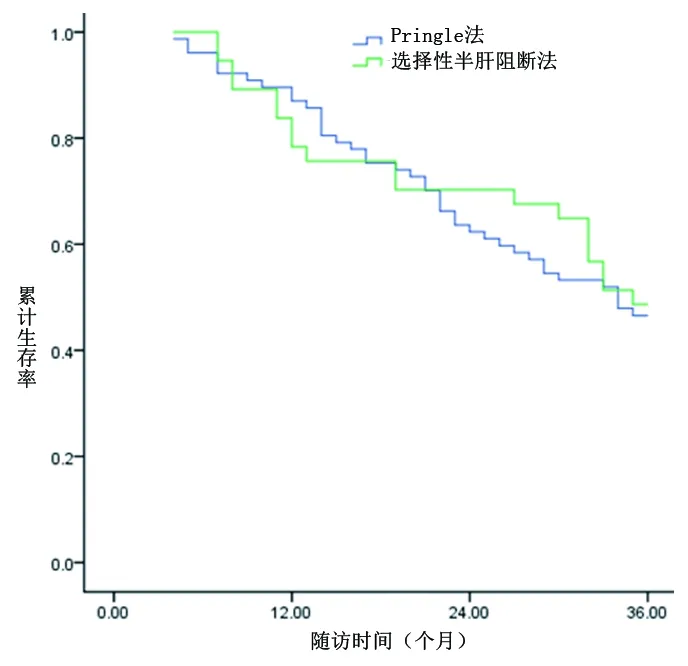
图3 肿瘤最大径≥5 cm时两组患者累计生存率比较
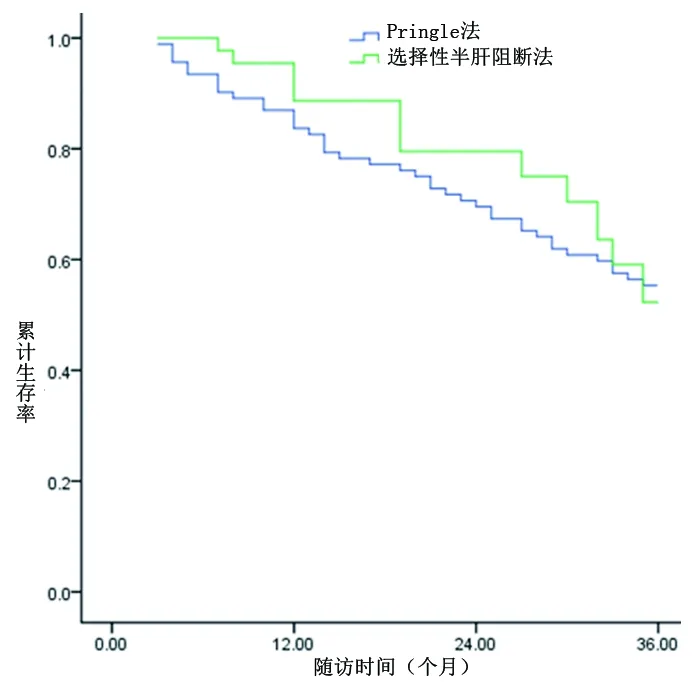
图4 甲胎蛋白≥400 ng/mL时两组患者累计生存率比较

图5 巴塞罗那分期为A期时两组患者累计生存率比较
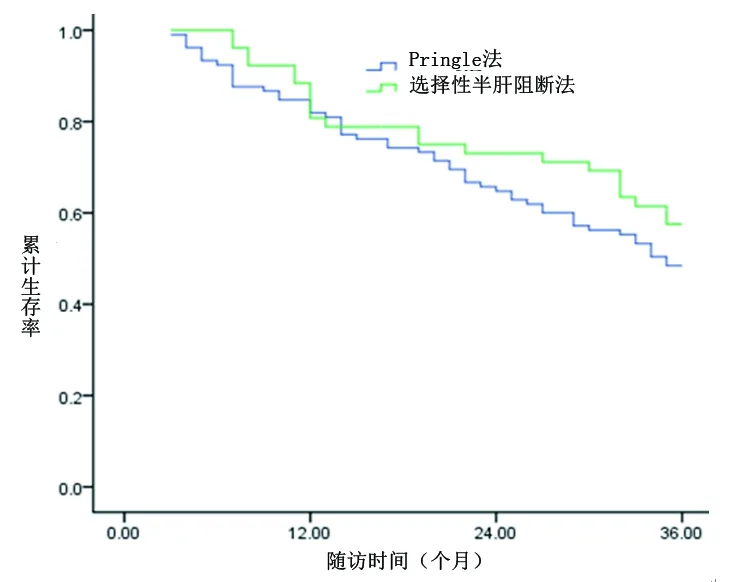
图6 HBsAg(+)时两组患者累计生存率比较
3 讨 论
尽管原发性肝癌的治疗手段逐渐增多,但外科根治性肝切除仍然是治疗该病的主要方法[5]。有研究指出术中出血量以及术后输血可能影响肝癌患者的远期生存率[6]。而Pringle法、选择性半肝阻断法、全肝阻断法以及超声刀等手术器械的应用,大大减少肝切除出血量[3-4]。
Pringle法是一种间歇性肝门阻断方式,肝血流重新恢复的过程可能引起严重的缺血再灌注损伤,从而导致肝动脉压升高、术后肝功能受损、细菌移位以及内毒血症等。选择性半肝阻断主要是根据肿瘤所在的位置选择阻断一侧入肝血流,其能够显著减少肝实质缺血再灌注损伤[3-4]。Pringle法和选择性半肝血流阻断均可能导致患者术后肝功能异常,但对患者术后累计生存率及复发率的影响尚不清楚。有学者指出Pringle法治疗是原发性肝癌早期肝内复发的危险因素之一,该方式能够促进肝癌细胞脱落和肿瘤复发[7]。动物实验研究发现,肝门阻断造成的肝脏缺血再灌注损伤能够促进肿瘤肝内复发和转移[8]。有研究推测Pringle法可导致肝脏缺血再灌注损伤进而影响肝细胞癌患者预后,但结论尚未明确[2,4,9-10]。本研究结果显示,两组患者术后1年、2年、3年累计生存率以及复发率比较,差异均无统计学意义(均P>0.05)。因此,我们认为虽然选择性半肝阻断对患者远期生存率和复发率并不优于Pringle法,但是在手术过程中,根据肿瘤的位置考虑采用选择性阻断入肝血流,可以减少对肝脏的缺血再灌注损伤。同时选择性半肝阻断避免了入肝血流反复阻断和开放,减少手术时间,一定程度上提高了手术的安全性。
本研究结果显示,对于肿瘤最大径≥5 cm、甲胎蛋白≥400 ng/mL、巴塞罗那分期为A期以及HBsAg(+)的肝细胞癌患者,Pringle法与选择性半肝阻断控制入肝血流法治疗的累计生存率比较,差异均无统计学意义(均P>0.05)。提示在上述情况下Pringle法以及选择性半肝阻断治疗对肝细胞癌患者术后累计生存率影响差异不大。但对于HBsAg(+)的患者,选择性半肝阻断治疗的累计生存率稍高于Pringle法,因此在条件允许的情况下应尽可能考虑行选择性半肝阻断法。肝细胞癌患者在手术过程中能够激活HBsAg病毒,Pringle法能够引起肝脏的缺血再灌注损伤,进一步加重肝脏负担,有可能在HBsAg病毒激活过程中发挥促进作用,但该设想还有待进一步研究证实。
本研究结果显示,AST≥70 U/L、甲胎蛋白≥400 ng/mL以及输血治疗是导致肝细胞癌患者术后死亡的独立危险因素;血小板计数<100×109/L、肿瘤大小≥5 cm、肿瘤个数为2~3个以及出血量≥1 000 mL是导致肝细胞癌患者术后复发的独立危险因素,与既往研究结果一致[11-12]。因此,对于具有上述危险因素的患者,术后需注意定期随访,及时发现肿瘤复发和转移病灶,进而进行后续辅助治疗以提高远期生存率。
本研究存在以下不足:首先,本研究为回顾性研究,虽然基线资料统计学无差异,但仍可能存在选择性便偏倚;其次,本研究纳入的研究对象相对较少,缺乏相关随机对照研究。
综上所述,Pringle法和选择性半肝阻断法对肝细胞癌患者术后远期生存率和复发率的影响差异不大,但是选择性半肝阻断法引起肝功能损伤程度弱于Pringle法,对局限于半肝的肿瘤及HBsAg(+)患者应优先考虑采用选择性半肝阻断。
