以索非布韦为基础的口服直接作用抗病毒药物治疗终末期肾病合并丙型肝炎病毒感染的血液透析患者的疗效及安全性
2019-06-19叶德辉李德新
叶德辉 刘 静 李德新 王 凡
(首都医科大学附属北京佑安医院血液透析室,北京市 100069,电子邮箱:dehui0532@sina.com)
慢性肾脏病(chronic kidney disease,CKD)是威胁全球健康的公共卫生问题之一,全球CKD患病率高达11%~13%[1],而中国约有近1.2亿成年CKD患者[2],CKD发展至终末期常需要血液透析治疗[3]。丙型肝炎病毒(hepatitis C virus,HCV)感染亦是全球性的公共卫生问题,其感染率达2.5%[4]。我国血液透析患者中HCV感染率接近41.1%[5],输血、透析器重复使用及透析年限较长等是血液透析患者感染HCV的危险因素[4]。目前,HCV感染促进肾功能损害的机制尚不明确,可能包括多种免疫机制、病毒的直接细胞毒性、合并用药的影响等[6]。研究发现,存在HCV感染的血液透析患者肝病相关死亡率、心血管死亡率和感染相关死亡率均明显升高[7-8],HCV感染是CKD进展的独立危险因素,血液透析合并HCV感染患者应尽早行抗病毒治疗以改善预后[9]。但是血液透析患者对干扰素的耐受性差,存在诱发排斥反应的风险。近年来,针对HCV生活周期中病毒蛋白靶向特异性治疗的直接作用抗病毒药物(directly acting antivirals,DAAs)的研究发展迅速,DAAs通过抑制HCV基因组编码的复制相关蛋白(非结构蛋白区)编码蛋白酶、RNA聚合酶的活性而发挥抑制病毒复制的效应,包括非结构蛋白3/4A蛋白酶抑制剂、非结构蛋白5A抑制剂和非结构蛋白5B聚合酶抑制剂等。本研究探讨血液透析患者应用以索非布韦为基础的DAAs方案抗HCV的疗效及其安全性,现报告如下。
1 资料与方法
1.1 临床资料 回顾性分析2015年8月至2018年1月在我院诊治的5例终末期肾病合并HCV感染患者的临床资料,均行血液透析治疗,HCV诊断参考文献[10]中的丙型病毒性肝炎诊断标准。纳入标准:(1)治疗前6个月肝肾功能基本稳定;(2)排除合并乙型肝炎病毒、梅毒螺旋体、人类免疫缺陷病毒等其他类型病原体的感染;(3)治疗依从性好;(4)无服用DAAs禁忌证。其中男4例,女1例,年龄41~69岁;1例为失代偿期肝硬化患者,1例为代偿期肝硬化患者,3例为慢性丙型肝炎患者;服用抗病毒药物前检测HCV基因型,其中4例为1b型,1例为2a型;抗病毒治疗前血清HCV-RNA水平均>103IU/mL。
1.2 DAAs抗病毒治疗及血液透析方案 DAAs治疗方案参考2015版《丙型肝炎防治指南》[11],均不给予干扰素治疗。DAAs药物均购自印度NATCO公司,包括索非布韦(400 mg×28片,批号:1900474)与达拉他韦(60 mg×28片,批号:1900452)。具体治疗方案见表1。
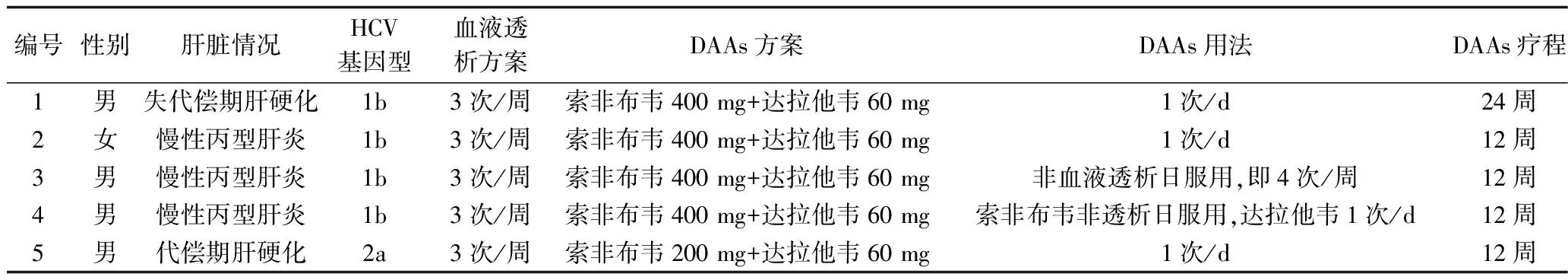
表1 5例血液透析合并丙型肝炎患者的DAAs抗病毒治疗情况
1.3 随访及观察指标 所有患者均随访5个月以上,分别于治疗前、治疗后第2周、治疗后第4周及治疗后第12周复查血常规、肝功能、肾功能及血清HCV病毒载量,观察患者DAAs抗病毒治疗期间的血常规、肝功能、尿素清除指数、尿素下降率的变化情况,以及不良反应(如恶心、呕吐等)发生情况。患者HCV-RNA转阴则判定为治疗有效。
2 结 果
所有患者均获得快速病毒学应答,均无HCV感染复发,均未出现病毒学突破(即在未更改治疗的情况下,病毒定量水平比治疗中最低总上升1 log值,或一度转阴后又转阳)见表2。DAAs抗病毒治疗期间所有患者的白细胞、血小板、血红蛋白、尿素清除指数、尿素下降率均较治疗前无明显变化,肝功能均正常。1例患者于抗病毒治疗开始的第1周出现食欲不振,未予特殊处理逐渐自行好转,其余4例患者无不良反应发生。

表2 5例患者抗病毒治疗前后血清HCV-RNA水平情况(IU/mL)
3 讨 论
DAAs药物于2011年在欧美市场上市,其对血液透析治疗的终末期肾病合并HCV感染患者疗效显著[12-15]。DAAs直接作用于HCV的蛋白酶、RNA聚合酶等病毒复制的重要环节,有效抑制病毒复制。由于干扰素存在较高的诱发排斥反应的风险,改善全球肾脏病预后组织指南不推荐将干扰素联合利巴韦林用于肾移植术后HCV感染患者的抗病毒治疗[16]。2015年版《丙型肝炎防治指南》[11]指出,合并肾损害的丙肝患者应首选无干扰素和利巴韦林的DAAs方案。达拉他韦等药物均在肝脏代谢,可用于合并肾功能不全的患者,而约90%索非布韦经过肾脏代谢,目前尚无证据证明估计肾小球滤过率(estimated glomerular filtration rate,eGFR)<30 mL/(min·1.73 m2)及终末期肾病患者可使用索非布韦[11]。欧洲肝病学会丙型肝炎治疗指南也提出在eGFR<30 mL/(min·1.73 m2)的重度肾功能不全和终末期肾病患者中需谨慎使用索非布韦,暂无推荐剂量[17]。目前我国已上市的索非布韦的药品说明书中对于eGFR<30 mL/(min·1.73 m2)或需要血液透析的终末期肾病患者,同样无明确安全性及适当推荐剂量。然而有研究发现,以索非布韦为基础的DAAs用药方案在治疗eGFR<30 mL/(min·1.73 m2)的CKD患者中,持续病毒学应答可达88%~96%[18-19]。
本研究观察5例终末期肾病合并HCV感染患者采用索非布韦联合达拉他韦的DAAs抗病毒治疗效果,结果显示,末次随访时所有患者均获得快速病毒学应答,5例患者的DAAs抗病毒治疗情况均存在差异,但最终都得到比较满意的结果。索非布韦是目前唯一经肾脏代谢的DAAs类药物,其在血液透析合并HCV感染患者中的安全性引起学者的注意。索非布韦药品说明书中对其不良反应的分析主要基于对索非布韦与利巴韦林合用的研究,最常发生的药物不良反应为疲劳、头痛、恶心与失眠,未发现索非布韦的特异性不良反应。本研究中,5例患者口服索非布韦的频率参考肾功能正常患者的服药频率,治疗期间未出现生化指标异常及严重不良反应,仅有1例患者出现轻微的食欲不振,可自行缓解。但是由于DAAs药物上市时间尚短,其远期疗效及安全性还有待进一步研究,加之DAAs药物价格不菲,加重长期透析治疗的患者的经济负担,且部分患者因合并其他疾病不能与DAAs药物同时服用,因而不能全面评估其疗效及安全性,建议行血液透析的终末期肾病合并HCV感染患者采用DAAs抗病毒治疗时,应密切检测肝肾功能的变化。
