药物共晶的制备表征及体外释放的研究进展
2019-06-11张亚晴吕宝兴牛景梅何文彬李玉琴
张亚晴,吕宝兴,牛景梅,何文彬,李玉琴
药物共晶的制备表征及体外释放的研究进展
张亚晴,吕宝兴,牛景梅,何文彬,李玉琴*
(泰山医学院 药学院,山东 泰安 271016)
药物共晶作为药物活性组分的新的固体形态之一,以其能够改善药物理化性质而不影响药物内部结构,晶型药物的稳定性和可操作性方面比之其他剂型更具优势,且临床治疗效果更佳,受到药学领域的各个研究机构及学者的密切关注,成为新药开发的一个重要方向。根据国内外的研究现状,作者对药物共晶的制备、表征以及体外释放进行检索,并对药物共晶近几年的研究进行系统的综述。
药剂学;体外释放研究;综述;药物共晶;制备方法;表征方法
共晶广义上是指两个或两个以上的不同分子被包含在同一个晶体结构中而形成的晶体或混合晶体,在药学上共晶则是指一种共晶形成物作为药物活性成分(active pharmaceutical ingredient, API)与共晶配体(cocrystal conformers, CCF)按照固定的化学计量配比以氢键、π-π堆积作用或其他非共价键的作用下形成新的结晶物[1-2]。虽然到目前为止,人们对药物共晶的研究尚不深入,但是关于醌氢醌药物共晶的研究报导早在1844年就出现了。近年来伴随着药物共晶在引入新成分并不改变药物疗效、改善自身溶解度及稳定性等方面的优点不断显现,药物共晶被广泛关注并不断涌现诸多新的共晶类药物诸如吡罗昔康-苯甲酸共晶[3]、氢氯噻嗪共晶[4]、姜黄素共晶[5]等。本文作者结合近几年药物共晶的研究现状,对其制备方法、表征及体外研究进行综述,并对其发展进行了展望,为以后药物共晶在医学领域的应用提供有效的借鉴。
1 研究现状
改善难溶性药物溶解度和生物利用度的方法主要是制备新的药物剂型,如微乳、脂质体、共晶等。关于共晶报道已有一百多年的历史,但近21年才开始应用于药物领域[6-7]。药物共晶是指一个共晶形成物作为药物活性成分(active pharmaceutical ingredient, API)与另一个或多个共晶形成物(cocrystalcoformers, CCF)在氢键、范德华力或其他非共价键的作用下形成新的结晶。药物共晶技术可以通过引入CCF改变API的诸多理化性质,如增溶、改善稳定性、提高生物利用度等,还可提高药物的药理活性。图1统计了近20年关于共晶论文发表与专利授权情况。由图1可见,关于共晶的研究已经达到了一个新的阶段。
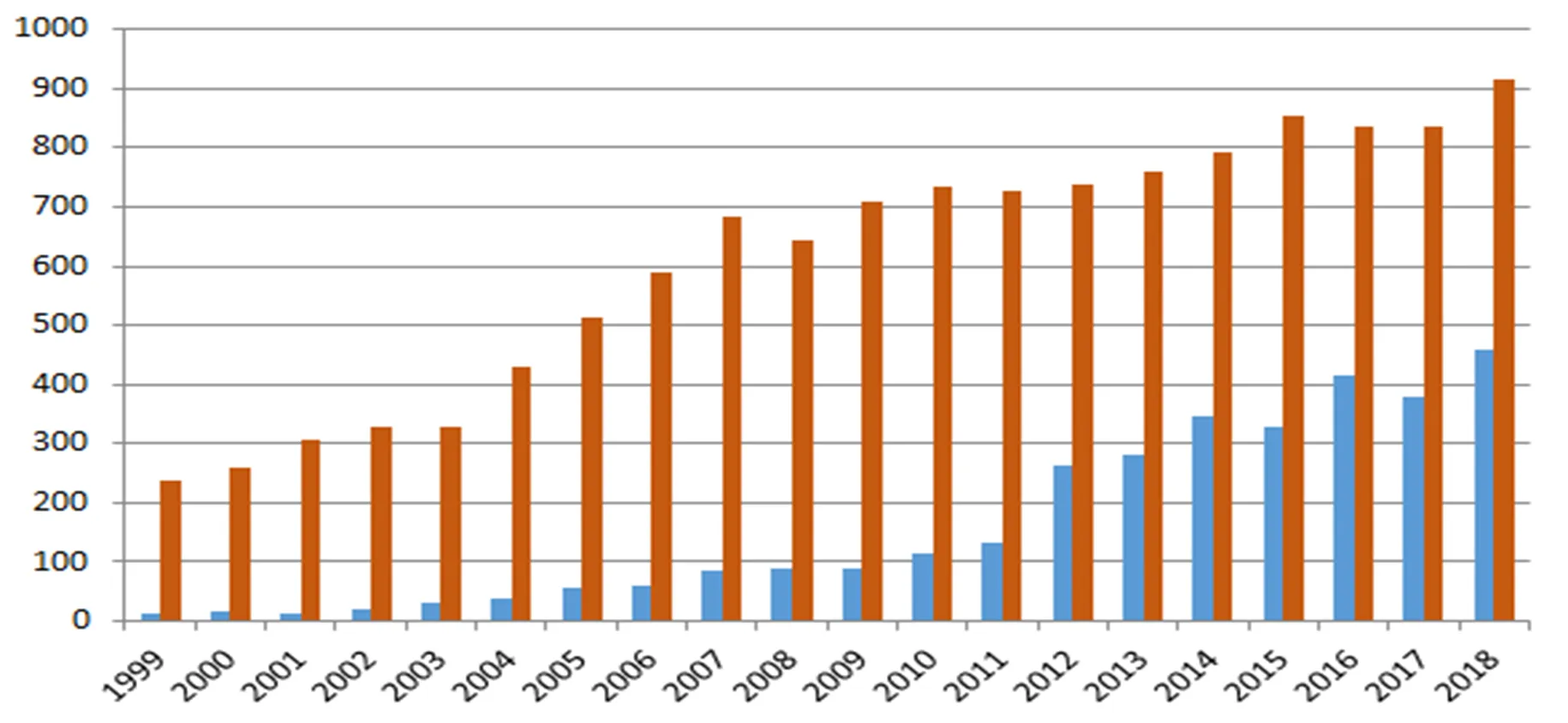
—Article; —Patent
为了实现 API 在制药领域的实际应用,药物共晶的出现为其展开了一个广阔的前景,对其性质的改善成为药物研究者们关注的热点之一。随着药物共晶在制药领域的逐渐成熟,人们把目光从最初的结构设计转向其性质研究上来,力求找到结构与性质之间的关系,即探究什么样的结构会给共晶的性质带来一定程度的提升。
2 药物共晶制备方法
2.1 溶液合成法
溶液合成法主要包括蒸发结晶法、冷却结晶法、溶析结晶法和反应结晶法等,上述方法也是目前制备药物共晶应用最广泛的方法之一。林锋等[8]采用混悬液结晶法,以西洛他唑和对羟基苯甲酸为原料,硝基甲烷或乙腈为溶剂,室温条件下快速搅拌1 h,抽滤干燥得到西洛他唑-对羟基苯甲酸共晶。杨金锁[9]通过对巴比妥酸-尿素共晶在甲醇中的热力学分析得到两种晶型在22~25 ℃时具有相似的性质(随着温度的升高,共晶溶解度增加),结果表明可以通过冷却结晶法制备出巴比妥酸-尿素共晶。邱培燊等[10]采用溶剂挥发法,将摩尔比为1∶1的对乙酰氨基酚和阿德福韦酯加入乙腈中,充分搅拌后置于通风处挥发溶剂,制备出了阿德福韦酯-对乙酰氨基酚共晶。运用溶剂挥发法制备药物共晶时,要注意使溶液中的API与CCF形成一种分子间强作用力,避免其他新组合(API-API,CCF-CCF)成分形成,还要注意各个药物单晶之间溶解度差异,以防药物析出。
2.2 固体合成法
固体合成法主要包括研磨法、升华法和熔融法等。研磨法一般分为无液干研磨(neat grinding,NG)和液体辅助研磨(liquid-assisted grinding,LAG)。易涵等[11]将伊曲唑康与丙二酸按照摩尔比1∶1的配料比置于研磨罐中,加入直径2 mm的氧化锆50 g进行无液研磨10 min,制备出伊曲唑康-丙二酸共晶。结果表明,新形成的药物共晶比伊曲唑康具有更好的溶解度和溶出度。
2.3 超声法
超声法优点在于操作简便和产率高,其原理是利用超声波较高的频率加速微粒间的相互作用以及接触几率。杨欢[12]将双苯氟嗪和苯甲酸按照一定配比加入到2 mL无水乙醇中,利用超声法制备了双苯氟嗪-苯甲酸共晶。相比于研磨制备,室温超声作用下制备的复合共晶物远多于单纯研磨法,因而超声可以加速共晶的合成。
2.4 超临界流体法
超临界流体技术的出现使得药物共晶制备工艺有了更深入的发展。超临界流体同时具有部分相似的液体和气体性质,可以通过升温或降压的方式改变物质的溶解度,从而分离超临界流体中溶解的物质。该技术一般常用超临界CO2作为溶剂,通过减压达到饱和以析出药物共晶。Padrela等[13]用超临界流体技术制备了吲哚美辛-糖精、茶碱-糖精、咖啡因-糖精、磺胺甲嘧啶-糖精、阿司匹林-糖精和卡马西平-糖精的药物共晶。
2.5 高速气流法
高速气流法是一种新思路,为药物共晶的批量制备提供了极大的便利。高压喷射出的高速气流速度高达300~1 000m∙s-1,药物活性成分在此气流中具有极高的运动速度,让API、CCF与档板之间相互冲撞摩擦,使API、CCF快速粉碎并随着气流按照不同的层级被收集。孙炳扬等[14]首次应用高速气流法,按照摩尔比1∶1的比例将茶碱分别与戊二酸、水杨酸、肉桂酸、苯甲酸等充分混合放入空气压缩机中进行高速混合收集,最后通过表征得到了茶碱-戊二酸、茶碱-水杨酸、茶碱-肉桂酸和茶碱-苯甲酸四种药物共晶。
3 药物共晶表征方法
3.1 X-射线衍射法(XRD)
X-射线衍射法是物质表征和质量控制必不可少的一种方法,同时也是一种最重要的无损分析工具,适用于流体粉末以及完整的晶体,分为粉末衍射和单晶X-射线衍射两种。
粉末衍射法是一种能够得到晶体结构的方法,常用来检测结构未知的物质,将得到的衍射数据同衍射数据国际中心(International Centre for Diffraction Data, ICDD)数据库中的数据进行比对,用以确定新物质的结构。庞丽丽[15]对来那度胺和烟酰胺制备的共晶物质进行X-粉末衍射表征,结果表明原料物质的特征峰都不同程度的减弱或消失,共晶的RXD图谱中2角为12.2°和22.1°的地方出现了新的特征峰,以此说明了三种不同的制备共晶方法都产生了新的药物共晶。
单晶X-射线衍射法是测定晶体组成的一种方法,其依据的原理是单位晶体对X-射线的衍射效应,即如果有一束单色X-射线照射到晶体上面,那么按照一定规律排列组合的原子之间的间隔距离和入射的X-射线波长有着一样的数量级,因此不一样的原子散射出的X射线之间将会产生互相干涉效果,在一定的方向上会产生强X射线的衍射,又因为衍射线在空间当中排布的位置和强度,和晶体的组成结构有着紧密的联系,故而不同种类的晶体产生的衍射样式都能够表现出这种晶体当中原子分布的规律[16]。此方法可依照记录形式的不同来区分为照相法和衍射仪法两类。
3.2 傅里叶红外光谱分析法(FTIR)
傅里叶红外光谱法大因其信噪比和灵敏度高、通光量大,以及光谱范围广和分辨率高,在药物共晶的表征中得到了广泛的应用。叶婵娟[17]运用傅里叶红外光谱法对吡嗪酰胺和氢氯噻嗪进行了表征,将吡嗪酰胺或氢氯噻嗪、柠檬酸以及共晶的红外光谱图进行比较,结果表明有新的配合物产生。宋亚茹等[18]用FTIR对新型蓝光材料进行了表征,结果证明有新的配合物产生。Stott P W等[19]通过红外光谱分析对布洛芬与七种萜类皮肤渗透促进剂形成的共晶体系进行比较实验,结果表明只有与布洛芬作用形成氢键的萜烯才会生成共晶体系。
3.3 热分析法
热分析法主要包括热重法(TGA)、差示扫描量热法(DSC)、差热分析法(TDA),其中以DSC和TGA最为重要也最为常用。Phaechamud T等[20]对布洛芬和薄荷醇-樟脑共晶采用差示扫描量热法进行了表征,分析表明薄荷醇-樟脑体系共晶点接近1∶1、共晶的熔点为-1 ℃。
4 体外释放研究
体外释放研究是考察药物的溶解度、溶出度和生物利用度的一项技术,其实质是利用改变外界温度、搅拌、酸碱度等因素来模拟体内的复杂代谢过程在体外进行的药物释放实验。药物形成共晶后,可显著改善药物单体的溶解度,进而提高药物的溶出度和生物利用度。通过体外释放研究,可以初步考察药物共晶的成药性。Phaechamud T等[20]对布洛芬和薄荷醇-樟脑共晶进行了体外释放研究,研究结果发现布洛芬共晶的溶解度为(282.11±6.67) g∙L-1,药物水溶性提高了4倍,生物利用度得到明显提高。
测量API的平衡溶解度是目前为止药物共晶溶解度测量研究中最常用的方法,但是该方法极易受到药剂的种类、溶解时间及温度、药物颗粒大小等因素的影响。孙晓伟[21]探究了吲哚美辛-烟酰胺、卡马西平-烟酰胺、布洛芬-烟酰胺三种共晶在水中的溶出速率,发现当共晶溶于水使氢键迅速打开,共晶配体烟酰胺被释放到水溶液中,由于晶型的瞬间崩塌,致使药物活性成分呈现出无定型状态(即此时药物保留共晶状态时增加了溶解度的性质),增大了三种共晶的溶解度。
药物的溶出速率直接决定药物在体内释放与吸收的程度。有鉴于此,邱培燊[10]等人采用桨法对阿德福韦酯-对乙酰氨基酚共晶进行了溶出速率测定,并通过HPLC分析得到形成共晶后的药物,结果发现阿德福韦酯-对乙酰氨基酚共晶的溶解度及溶出速率均得到了显著改善。Ivo M. Aroso等[22]对氯化胆碱、薄荷醇与乙酰水杨酸、苯甲酸和苯乙酸所形成的药物共晶进行了溶解速率研究,研究表明在磷酸盐缓冲溶液中,共晶形式的药物活性成分比单纯药物活性成分的溶出速率尤为快速。这两次实验的结果均说明了药物共晶增大溶出速率的特点在药物递送系统的开发中拥有巨大的潜力。
5 发展前景
药物共晶技术是新型的固体形态技术,结合了制药工程与晶体工程学的优势,为难溶性药物的临床应用局面打开了新的方向,拉近了晶体工程学与医药产业的距离。对于我国来说药物共晶的新型固体形态可以在创新方面突破原有药物研发专利的封锁,打破西方国家的专利垄断,降低药物以及治疗成本,造福公共医疗,缓解看病贵的难题,这也使得药物共晶技术在医药市场具有极大的价值和潜力,但是目前我国对药物共晶的研究尚不深入,类如溶剂的选择以及最佳共晶配体的筛选等问题仍然困扰着研究者,还需要广大从事药物研究人员更加深入的开展研究,才能把握先进的科学发展方向和发展机遇。
[1] 胡盛福, 宋胜杰, 丁泽杰, 等. 药物共晶制备方法研究进展[J]. 浙江化工, 2018, 49(7): 1-3, 15.
[2] MORISSETTE S L, ALMARSSON O, PETERSON M L, et al. High-throughput crystallization: polymorphs, salts, co-crystals and solvates of pharmaceutical solids[J]. Advanced Drug Delivery Reviews, 2004, 56(3): 275-300.
[3] 张跃勇, 田佳鑫, 吕琳, 等. 吡罗昔康-苯甲酸共晶的制备与体外释放研究[J]. 中国新药杂志, 2018, 27(1): 91-96.
[4] 王小兵, 黄世铭, 廖静怡, 等. 氢氯噻嗪药物共晶的制备、表征及量化计算[J]. 江西师范大学学报: 自然科学版, 2015, 39(3): 240-245.
[5] 程桂林, 邓彩赟, 蒋成君. 姜黄素共晶研究进展[J]. 浙江化工, 2017, 48(12): 12-17.
[6] 吴其国, 胡叶青, 刘慧娟, 等. 中药活性成分的共晶形成物研究进展[J]. 广西中医药大学学报, 2017, 20(3): 73-76.
[7] 张晓明. 药物共晶的合成、表征与性质研究[D]. 长春: 吉林大学,2016: 1-7.
[8] 林锋, 赵玉梅, 郑志兵, 等. 西洛他唑-对羟基苯甲酸共晶制备新工艺[J]. 中国药物化学杂志, 2015, 25(1): 45-49.
[9] 杨金锁. 巴比妥酸-尿素共晶多晶型及其共结晶过程研究[D]. 上海: 华东理工大学, 2017: 23-41.
[10] 邱培燊, 高静, 钱帅, 等. 对乙酰氨基酚通过共晶形成提高阿德福韦酯的溶出及肠吸收[J]. 药学学报, 2018, 53(6): 993-1001.
[11] 易涵, 尹亚妹, 赵秀丽, 等. 伊曲康唑共晶的制备与表征[J]. 沈阳药科大学学报, 2014, 31(3): 161-168.
[12] 杨欢. 双苯氟嗪-苯甲酸共晶的研究[D]. 石家庄: 河北医科大学, 2013: 10-19.
[13] PADRELA L, RODRIGUESA M A, VELAGAB S P, et al. Screening forpharmacticalcocrystals using the supercritical fluid enhanced atomization process[J]. J Supercrit Fluids, 2010, 53(1-3): 155 - 164.
[14] 孙炳扬, 彭汝芳, 梁华, 等. 一种批量制备药物共晶的新方法-高速气流法[J]. 安全与环境学报, 2017, 17(3): 1081-1087.
[15] 庞丽丽. 来那度胺-烟酰胺共晶的制备与表征[D]. 无锡: 江南大学, 2015: 13-16.
[16] 孔庆云. X-射线单晶衍射法的原理及应用[J]. 西北民族学院学报, 1997(2): 60-62.
[17] 叶婵娟. 吡嗪酰胺和氢氯噻嗪的共晶研究[D]. 南昌: 南昌大学, 2014: 40-45.
[18] 宋雅茹, 吴红, 王德, 等. 新型发蓝光材料的合成和光谱表征及光致和电致发光性能的研究[J]. 光谱学与光谱分析, 2000, 20(5): 730-731.
[19] STOTT P W, WILLIAMS A C, BARRY B W. Transdermal delivery from eutectic systems: enhanced permeation of a model drug, ibuprofen[J]. Journal of Controlled Release Official Journal of the Controlled Release Society, 1998, 50(1-3): 297.
[20] PHAECHAMUD T, TUNTARAWONGSA S, CHAROENSUKSAI P. Evaporation behavior and characterization of eutectic solvent and ibuprofen eutectic solution[J]. Aaps Pharmscitech, 2016, 17(5): 1213-1220.
[21] 孙晓伟. 药物共晶热力学相图及溶解行为研究[D]. 天津: 天津大学, 2015: 53-58.
[22] AROSO I M, SILVA J C, MANO F, et al. Dissolution enhancement of active pharmaceutical ingredients by therapeutic deep eutectic systems[J]. European Journal of Pharmaceutics & Biopharmaceutics, 2016, 98: 57-66.
Progress in preparation, characterization andrelease of drug eutectics
ZHANG Yaqing, LV Baoxing, NIU Jingmei, HE Wenbin, LI Yuqing*
(,,271016,)
Drug eutectics, as one of the new solid forms of the active components of drugs, has been paid close attention by various research institutions and scholars in the field of pharmacology, and becomes an important direction of new drug development. Drug eutectics can improve the physical and chemical properties of the drug without affecting its internal structure. The stability and operability of drug eutectics are superior to other dosage forms, and the clinical treatment effect is better. According to the research status at home and abroad, the preparation, characterization andrelease of drug co eutectics are searched. In this paper, the recent research on drug eutectics is systematically reviewed. According to the research status at home and abroad, the authors searched for the preparation, characterization and in vitro release of drug eutectic, and systematically reviewed the research of drug eutectic in recent years.
Pharmaceutics;release study; summary; drug eutectics; preparation method; characterization method
2019-01-13
国家级大学生创新训练项目(201810439073)
张亚晴(1997-), 女(汉族), 山东威海人, 本科, 主要从事药物分析方面的研究,Tel. 18263818631, E-mail 540011206@qq.com;
李玉琴(1968-), 女(汉族), 山东泰安人, 教授, 博士,硕士生导师, 主要从事药物分析方面的研究,Tel. 0538-6229751, E-mail liyuqin@tsmc.edu.cn。
(2019)03–0077–06
10.14146/j.cnki.cjp.2019.03.006
R94
A
(本篇责任编辑:赵桂芝)
