Ce改性Co/SEP催化剂对乙醇重整制氢的影响
2019-06-03汪春生王一双陈明强汤志远杨忠连
汪春生, 王一双,2, 陈明强,*, 汤志远, 张 涵, 杨忠连, 王 君
(1. 安徽理工大学 化学工程学院, 安徽 淮南 232001;2. 安徽理工大学 能源与安全学院, 安徽 淮南 232001)
近年来,在全球能源短缺和清洁能源兴起的背景下,生物质热解转化成液体燃料技术的发展使生物质分散加工成生物油和生物油催化重整制氢成为可能。生物油成分复杂、富含上百种含氧有机化合物,利用生物油直接催化重整制氢不利于探索其制氢机理以及催化剂失活机理。因此,乙醇作为生物质发酵产物和热解生物油中醇类代表性组分,以其高氢密度、无毒、经济、催化重整的相对可行性而备受青睐,被广大学者选为生物油模型物来研究其催化重整制氢机理。并且,利用生物乙醇进行重整制氢,不仅可以提高生物质的利用效率,还可以解决传统制氢方法的不可再生性[1-3]。利用乙醇为原料进行催化蒸汽重整制氢反应已经得到了大量研究,研究结果证明,乙醇催化蒸汽重整制氢过程包含一个复杂的反应网络,主要平行反应有[4-6]:
乙醇蒸汽重整
C2H5OH+3H2O →6H2+2CO2
(1)
乙醇分解
C2H5OH → CH4+ CO + H2
(2)
乙醇脱水
C2H5OH → C2H4+ H2O
(3)
乙醇脱氢
C2H5OH → C2H4O + H2
(4)
甲烷化
CO + 3H2→ CH4+ H2O
(5)
水煤气可逆变换
CO + H2O ↔ CO2+ H2
(6)
甲烷水蒸气重整
CH4+H2O → CO + 3H2
(7)
积炭
2CO → CO2+ C
(8)
CH4→ C + 2H2
(9)
C2H4→ coke
(10)
因而,为达到生物乙醇高效催化蒸汽重整制氢的目的,具有特定选择性的催化剂被广泛应用于乙醇蒸汽重整(Ethanol steam reforming, ESR)反应中,贵金属基(Pt、Pd、Rh和Ru等)和Ni基催化剂因其具有优异的C-C和C-H断键能力得到大量的研究。但是,贵金属的经济性限制了它们的工业化应用[1,2,7-11]。值得注意的是在ESR中苛刻的重整条件下Ni基催化剂具有很强的亲碳性和易烧结性,会导致催化剂表面严重积炭以及活性金属位点损失[7-11]。文献[12-14]以芳香族化合物为原料,在低水/碳比(S/C)的条件下研究了Ni基催化剂失活机理,发现Ni基催化剂失活通常被认为是:Ni活性位点被封装炭包裹;纤维炭的形成使Ni颗粒从载体表面剥离;不可逆的金属相烧结。而钴基催化剂在C-C键裂解和氢选择性方面表现出了与镍基相似的高效率,还可以在一定程度上促进水煤气变换反应和甲烷水蒸气重整反应提高氢气产率[15],被认为是一种具有工业应用前景的ESR催化剂,但是催化剂稳定性是其工业应用的重要评价指标。其中,催化剂表面含碳中间物种的快速移除是提高催化剂稳定性的主要方式。近年来,研究者发现,CeO2具有较好的Ce4+/Ce3+氧化还原循环和较高的氧物种迁移率,可以有效地移除含碳中间物种,并且将CeO2加入Co基催化剂中,Co活性金属颗粒附近的积炭能被CeO2的晶格氧所气化,达到瞬时移除积炭的性能,同时,Co-Ce间的相互作用可以增强Co金属表面分散度和还原性,提高催化剂储释氧能力[16,17]。另外,在催化剂物理化学性质方面,载体扮演着多重角色,其不仅可以通过酸碱性位点影响反应路径,还可以利用自身多孔性、水热稳定性来锚定金属活性位点。天然海泡石(sepiolite,简称SEP)是一种水热稳定性良好、表面硅羟基富集的水合硅酸镁盐,其理想化学公式为Mg8Si12O30(OH)4(OH2)4·8H2O,由两个四面体硅片层和一个中心氧化镁片层组成,呈片层状和多孔结构,经酸化处理移除部分水镁石八面体层后,其多孔性和八面体空位得到增加,有利于金属相的稳定掺杂和传质吸附[18]。
1 实验部分
1.1 试剂与实验装置
乙醇(C2H5OH)、六水合硝酸钴(Co(NO3)2·6H2O)、六水硝酸铈(Ce(NO3)3·6H2O)和氢氧化钠(NaOH),均为AR。实验所用试剂均购于国药集团化学试剂有限公司。乙醇蒸汽重整实验装置示意图见图1,其中,固定床内径为25 mm,长度为300 mm。
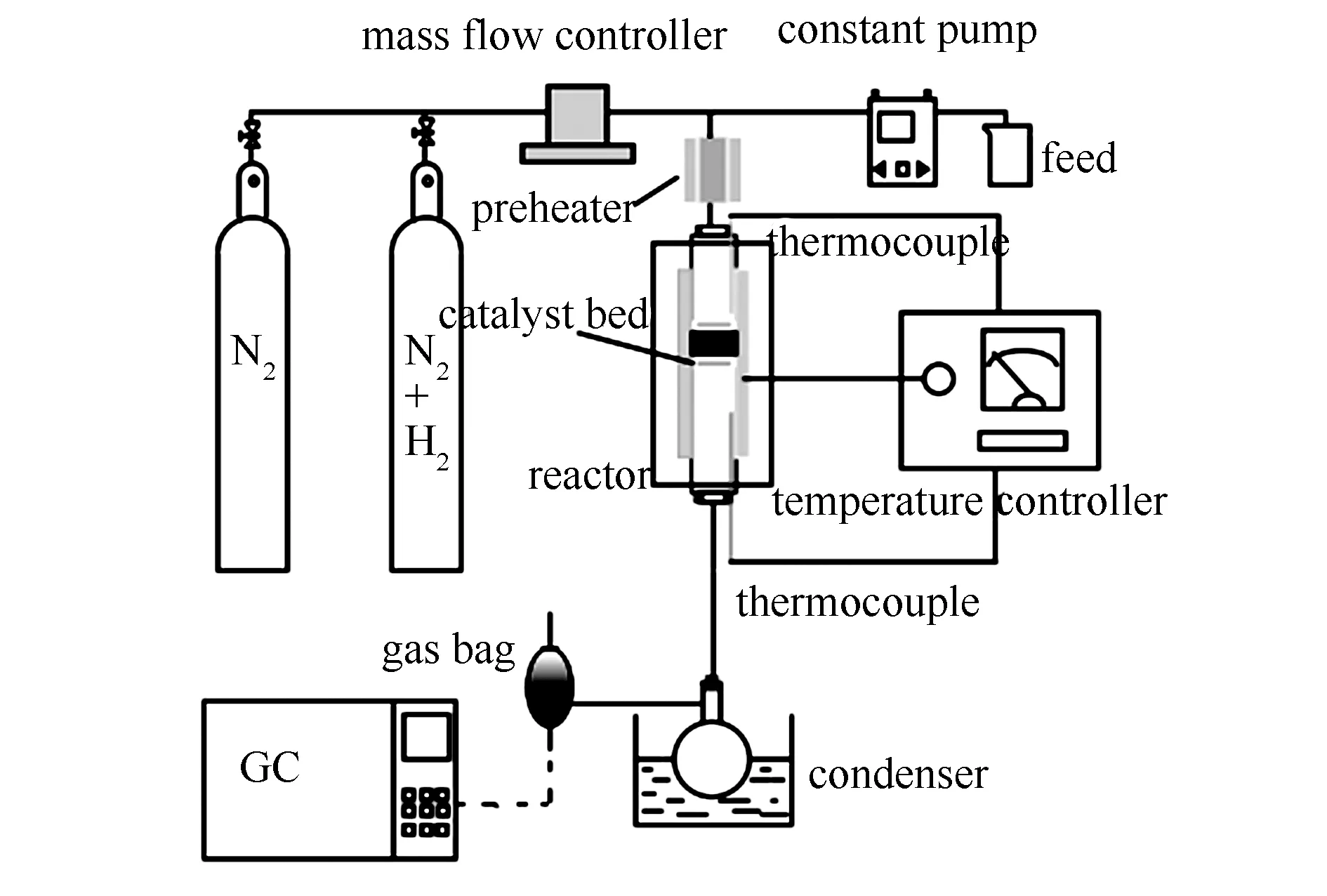
图 1 实验装置示意图
1.2 催化剂的制备
Co/SEP和Co-Ce/SEP两种催化剂通过沉淀法制得,Co金属负载量为10 %(质量分数)、Ce与Co物质的量比为0.3。称取2.45 g Co(NO3)2·6H2O 和1.11 g Ce(NO3)2·6H2O于200 mL烧杯中加入100 mL去离子水形成水溶液,再称取4.06 g硝酸酸化预处理的SEP加入上述水溶液中,置于水浴锅中恒温(60 ℃)磁力搅拌2 h后,逐滴滴加沉淀剂(5 mol/L NaOH)调节pH值至10±0.2,搅拌 2 h后恒温静置老化12 h。然后将老化后的悬浊液进行抽滤用去离子水洗2-5次,滤饼于烘箱中105 ℃干燥12 h,研磨并用80目网筛过筛。将过筛后粉末置于管式炉中,在空气氛围下以4 ℃/min的升温速率升至700 ℃恒温煅烧4 h,即制得煅烧后Co-Ce/SEP催化剂。Co/SEP的制备方法同上文一致。再将上述制备的煅烧后催化剂置于管式炉中,通入0.4 L/min的10% H2/N2还原气以4 ℃/min的升温速率升至700 ℃恒温还原2 h即可制得还原后Co/SEP和Co-Ce/SEP催化剂。
1.3 催化剂的表征
XRD谱图由日本Rigaku公司的SmartLab(3 kW) X射线衍射仪在操作电压为40 kV和操作电流为40 mA条件下,以CuKα辐射为辐射源进行测量,5°-80°扫描,步长为0.02°。
在配备有热导检测(TCD)的Auto ChemII 2920仪器上进行了H2-温度程序升温还原(H2-TPR)测定。在200 ℃下用Ar气体(40 mL/min)处理50 mg催化剂2 h,冷却至50 ℃,再在5% H2/Ar流量下(40 mL/min)还原至900 ℃,加热速率为10 ℃/min。
采用FEI生产Tecnai G2 F20场发射透射电子显微镜观测催化剂的结构形貌特征,其操作电压为200 kV。
1.4 实验步骤
实验中液相进料为乙醇和水不同物质的量比(1∶3-1∶18)的混合物。首先将少许石英棉置于固定床中(如图1所示)后称取1.00 g催化剂铺撒在石英棉上,在催化剂上方另置一层石英棉压紧催化剂。然后,常压下以0.24 L/min通入高纯N2吹扫15 min,打开温控升温加热,通入0.4 L/min 10% H2/N2,在700 ℃下恒温2 h还原催化剂。催化剂活化后切换0.24 L/min N2载气流,将温度控制在600 ℃。温度恒定后,由恒流泵以11.3 g/h流速通入不同物质的量比的乙醇/水混合物。出口气经过冷凝装置后由气袋收集,并在华爱GC-9160气相色谱仪上用TCD检测器和TDX-01色谱柱分析气相产物组成,具体测定条件参见文献[21]。乙醇转化率、氢气产率和C1产物选择性计算公式如下[15,22]:

在实施过程中,“课程套餐”的内容可以根据学生的发展诉求以及阶段性的培养目标灵活调整,做到因需组合、因势调整。
(12)
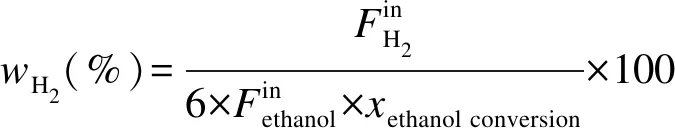
(13)

(14)

2 结果与讨论
2.1 催化剂的表征
2.1.1 XRD分析
煅烧和还原后样品的XRD谱图见图2,在17.6°、19.7°和26.5°处的衍射峰属于SEP(JCPDS 26-1226)的特征衍射峰,并且在煅烧和还原后的Co/SEP和Co-Ce/SEP催化剂中均能观察到SEP的特征衍射峰,说明作为载体SEP具有出色的热稳定性。

图 2 Co/SEP和Co-Ce/SEP两种催化剂煅烧和还原后的XRD谱图
另外,在图2 (a)中,Co/SEP和Co-Ce/SEP在31.3°、65.2°的衍射峰对应的是Co3O4(JCPDS 43-1003),而Co-Ce/SEP在28.6°、47.4o和56.4°处出现明显的CeO2(JCPDS 34-0394)衍射峰,说明Co和Ce两种组分都成功负载在载体SEP上。由图2(b)可知,Co/SEP和Co-Ce/SEP催化剂经过还原活化后在44.3°和51.5°出现明显的Co(JCPDS 15-0806)金属峰以及在36.5°和42.4°处微弱的CoO衍射峰(JCPDS 48-1719),这可能是由于氧化钴物种本身的难还原性或其与载体有较强的相互作用难以被完全还原。另外,由表1可知,在Co-Ce/SEP中的Co0颗粒粒径更小,说明CeO2的加入提高了金属Co的分散度、抑制活性金属的团聚[23,24]。

表 1 反应前催化剂的物化性质
%;
b/c: derived from diffraction peak in XRD corresponding to the Co3O4(440) plane at 65.2° or Co0(111) plane at 44.2° by the Scherrer formula
2.1.2 H2-TPR分析
煅烧后Co/SEP和Co-Ce/SEP催化剂的H2-TPR谱图见图3。由图3可知,在250-450 ℃低温区,Co/SEP和Co-Ce/SEP都出现了两个还原峰,其对应于与载体具有较弱相互作用的Co3O4先还原成CoO、再由CoO还原成金属Co的过程。随着温度的升高,在700 ℃左右高温区出现一个较强的不对称的还原峰,其对应于与载体相互作用较强的Co3O4颗粒或Co2+离子的还原[24]。相比于Co/SEP,Co-Ce/SEP的还原峰整体向低温区迁移。结合催化剂不同温度区域氢气消耗量和其理论还原度(见表1)可以看出,Co/SEP低温区氢气消耗量和还原程度都低于Co-Ce/SEP,这些都说明添加的CeO2促进了钴氧化物的还原,明显改善了催化剂的还原性,从而暴露出更多表面金属活性位点。另外,在Co-Ce/SEP的谱图中接近800 ℃的肩峰,是由体相CeO2的还原所造成,而在低温区微弱的表面Ce还原峰通常被遮盖[25,26]。
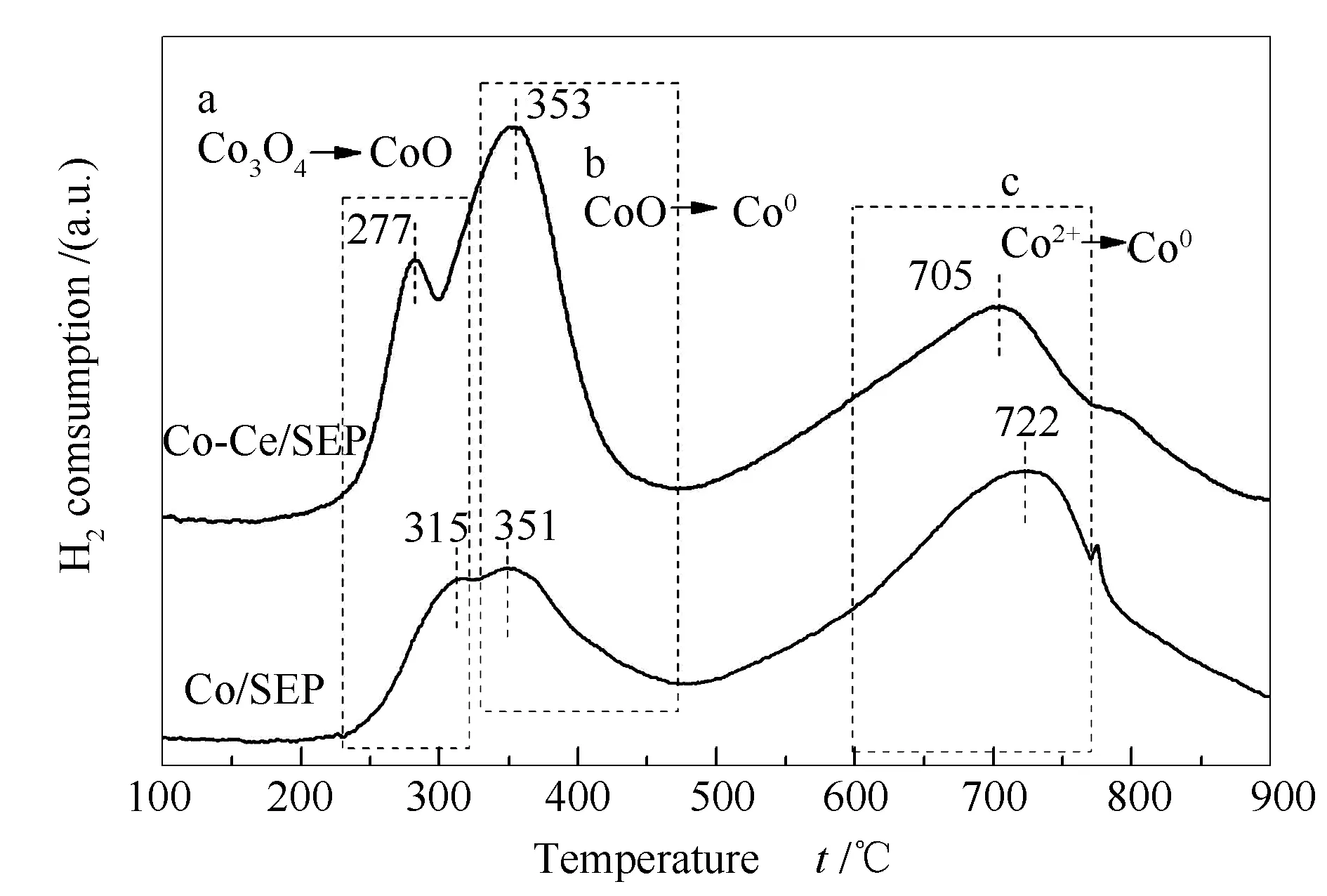
图 3 Co/SEP和Co-Ce/SEP催化剂的H2-TPR谱图
2.1.3 TEM分析
图4显示了两种还原后催化剂的微观结构形貌。

图 4 还原后催化剂的TEM照片
由图4(a)可知,还原后Co/SEP催化剂中出现大量被深灰色区域所包围的黑色颗粒,这些黑色颗粒代表钴金属颗粒,其直径约为40 nm。Ce加入Co/SEP中后,这些黑色颗粒直径约为10 nm,见图4(b)。这说明Co-Ce/SEP中Ce的添加明显减小了钴金属颗粒粒径、提高了活性金属分散度,与XRD表征结果相一致。
2.2 催化剂对乙醇催化重整制氢的影响
分别取1.00 g Co/SEP、1.00 g Co-Ce/SEP和1.00 g SEP催化剂置于固定床中部,在常压,WHSV=20.5 h-1,S/C=3和600 ℃条件下,考察10 h反应时间内两种催化剂对乙醇催化重整制氢性能影响,结果见图5。
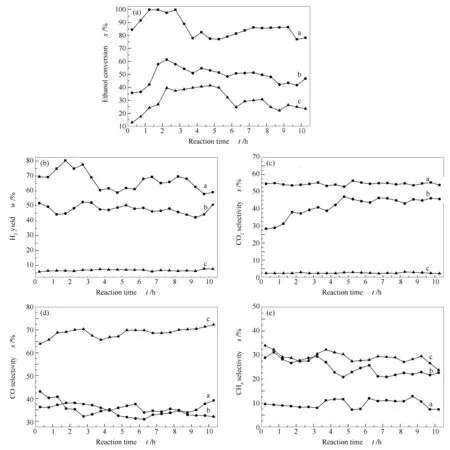
图 5 10 h反应时间内催化剂对乙醇蒸汽重整制氢的影响
由图5可知,载体SEP几乎无重整活性,在重整测试过程中主要发生了乙醇分解反应(2)和乙醇脱氢反应(4),因而表现出了较低的乙醇转化率和氢气产率以及一定的CO、CH4选择性,而几乎无H2和CO2产生。
对于Co/SEP催化剂来说,在反应初期乙醇转化率由35%升至60%,CO和CH4的选择性逐渐增加;随着反应的进行,Co/SEP逐渐失活,其乙醇转化率最终降至42%,而CO选择性为30%至35%,CO2选择性最终稳定在45%,氢气产率在45%附近波动,另外反应后期甲烷选择性保持在24%。这都说明,Co/SEP的乙醇催化重整制氢活性不高且稳定性差,金属位烧结带来表面活性位点大量减少和大幅度失活。作为重整反应(1)产物的CO2始终保持着较低选择性,说明相对较高的H2产率、CH4和CO选择性主要源自乙醇脱氢反应(4)和乙醇分解反应(2)。
相比于Co/SEP,Co-Ce/SEP在反应初期即达到最大活性,乙醇转化率在最初3 h内保持在100%,但随后乙醇转化率骤降至78%,氢气产率也由75%降至55%,CO选择性逐渐降低至后期的33%,CO2选择性(55%)比较稳定且相对较高,以上现象表明,Co-Ce/SEP在反应3 h后发生一定程度失活。然而,反应4 h后Co-Ce/SEP的活性又有所恢复,乙醇转化率恢复至约85%,氢气产率也升高至约65%,甲烷选择性则在10%左右波动。反应中期时活性得到一定恢复是因为Ce的添加,缓解了金属Co纳米颗粒的烧结,同时促进乙醇重整反应(1)和WGS反应(5),抑制了甲烷的生成。综上,CeO2添加进Co/SEP后,提高了其稳定性,使催化剂能保持相对较高的活性[27-29]。
2.3 温度对乙醇催化重整制氢的影响
取1.00 g Co-Ce/SEP催化剂置于固定床中部,在常压,WHSV=30.3 h-1和S/C=3条件下,在500-700 ℃条件下反应4 h考察温度对Co-Ce/SEP的催化重整制氢性能影响,结果见图6。
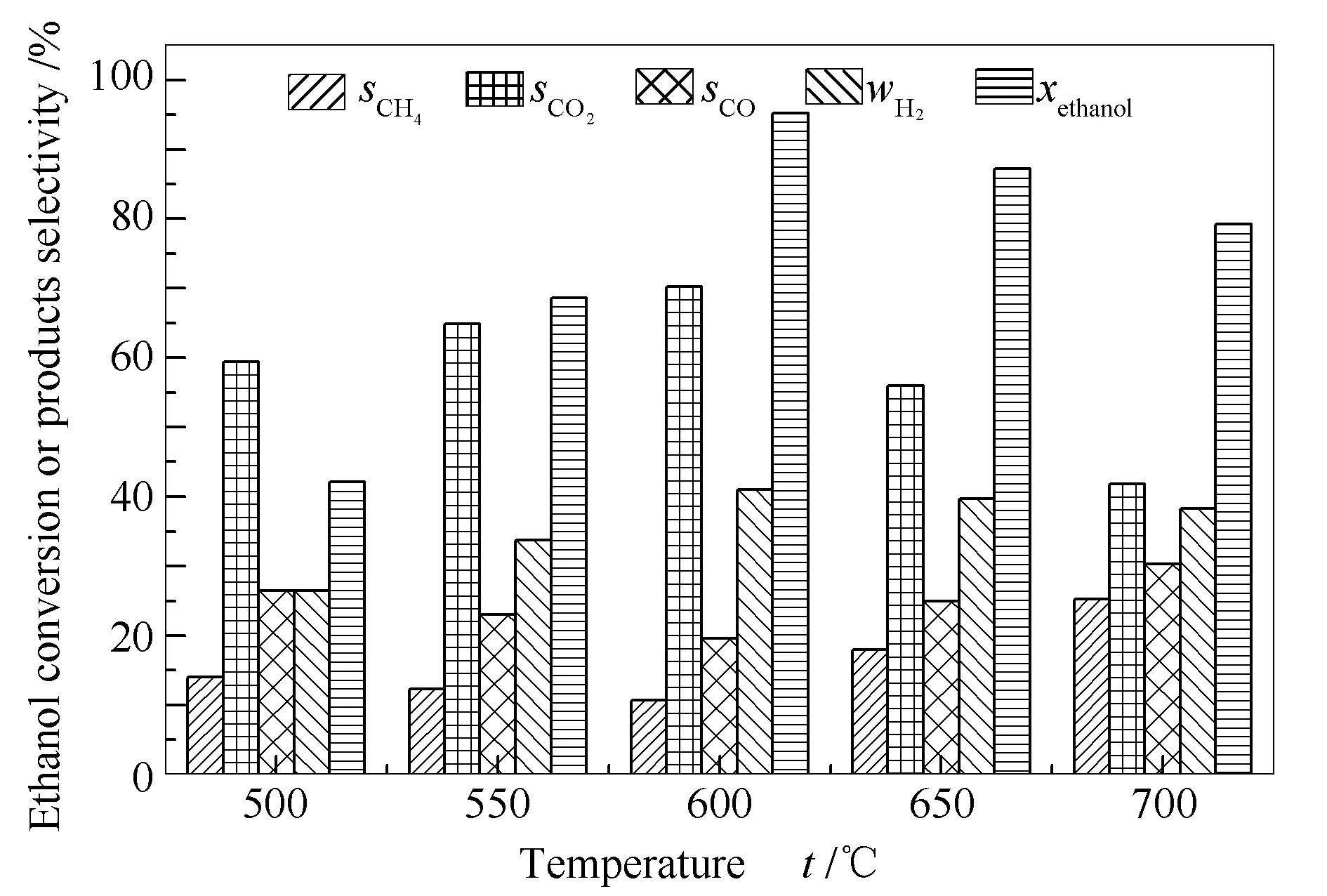
图 6 温度对乙醇催化重整制氢的影响
由图6可知,500-600 ℃时,乙醇转化率、H2产率和CO2选择性随着温度升高而升高,而CH4和CO选择性随之下降;而当温度超过600 ℃后,乙醇转化率、H2产率和CO2选择性随之下降,并伴随着CH4和CO选择性的上升。这种现象说明温度对乙醇重整反应过程有着明显的影响。在低温区中温度升高明显促进了反应(1)、(6)和(7)的进行,提高H2的产率、抑制CH4和CO的形成。而当温度过高时,由于热力学的限制,使水汽变换反应向逆向进行并且乙醇的分解反应也占据了主导地位,会降低H2产率[30-32]。因此,在此实验条件下,Co-Ce/SEP最佳催化重整乙醇制氢的反应温度为600 ℃。
2.4 S/C比对乙醇催化重整制氢的影响
取1.00 g Co-Ce/SEP催化剂置于固定床中部,在常压,WHSV=30.3 h-1和600 ℃条件下,考察4 h反应时间内S/C比对Co-Ce/SEP的催化重整制氢性能影响,结果见图7。

图 7 S/C比对乙醇催化重整制氢的影响
由图7可知,根据乙醇重整反应(1),S/C比的理论值为1.5,但如图7所示,当进料S/C比为1.5时,水蒸气仍不够充足,一部分乙醇会发生分解反应(2),导致CH4和CO选择性较高;H2产率较低。因此,在此基础上适当增加S/C比有助于促进乙醇重整反应(1)。当S/C比由1.5升高至3.0时,乙醇转化率由52%升至95%,同时氢气产率也由32%升高至41%,而CH4和CO的选择性降到最低值。然而,进一步增加S/C比导致乙醇转化率和氢气产率持续下降,当S/C比为9时,乙醇转化率和氢气产率分别降至76%和15%,CO2选择性升至63%,而CH4和CO的收率始终保持在较低水平,这可能是由于过量的水蒸气会在催化剂活性位点上与乙醇发生竞争吸附,阻碍活性位点催化转化乙醇,同时过高的S/C比会明显促进水气变换反应(6)和甲烷水蒸气重整反应(7),推高CO2收率。另一方面,根据Zou等[30]的研究发现,高S/C比条件下,过量蒸汽输入会加剧金属活性相的烧结和表面活性位点的减少。因此,适当的S/C比能促进乙醇重整制氢,带来较高的乙醇转化率和氢气产率,但过高的S/C比会阻碍乙醇的催化重整[30-33]。因此,对Co-Ce/SEP催化重整制氢而言最佳S/C比为3。
3 结 论
本研究考察了Co-Ce/SEP和Co/SEP催化剂催化重整制氢的性能。由表征结果证明,Ce的加入显著改善了Co-Ce/SEP的分散度和还原性,同时能增强催化剂的抗烧结能力和稳定性。通过多组实验得知,Co-Ce/SEP在WHSV=20.5 h-1,S/C比=3和600 ℃条件下达到最优活性,在10 h稳定性测试中能保持较高的乙醇转化率和氢气产率,分别为85%和65%。
