低温等离子体协同Cu-Mn-Ce-Zr/TiO2催化降解甲苯
2019-06-03豆宝娟赵晨晨闫宁娜杨德宇郝庆兰
豆宝娟, 赵晨晨, 张 庆, 闫宁娜, 杨德宇, 郝庆兰
(天津科技大学, 天津 300457)
挥发性有机化合物(VOCs)是造成空气污染日益严重的主要污染源之一,已引起社会各界的广泛关注[1]。甲苯属于典型的VOCs气体,主要来源于石油化工、有机溶剂、油漆等,严重危害空气和人体健康。低温等离子体方法因具有可在常温常压下反应、投资费用低和操作简单等优点,已成为VOCs末端处理技术的研究热点之一[2,3]。但单独使用低温等离子体技术降解VOCs时,能量利用率低、副产物种类多且不可控,容易造成二次污染[4]。利用催化氧化技术CO2选择性高的优点,与低温等离子体相结合,可有效抑制副产物的产生,是一种新型的无害化处理VOCs的方法[5-7]。Dou等[4]发现,采用低温等离子体协同CuCeZr/TiO2催化剂将甲苯完全降解为CO2时对应的放电功率为40 W,而采用单独等离子体完全降解甲苯的放电功率为80 W,且CO2选择性仅为43%。
以铜、锰等过渡金属为主要活性组分的氧化物催化剂在低温等离子体协同催化技术中受到广泛的关注。关绣娟等[8]对介质阻挡放电-催化降解甲苯进行了研究,发现Mn、Fe、Al、Co和Ti催化剂降解甲苯的活性与分解O3的能力成正相关关系,其中,Mn具有最优的O3分解能力,在相同的条件下,甲苯去除率比其他催化剂高15%-33%。复合过渡金属氧化物作为一类反应活性高、易于制备的低成本催化材料,在催化降解VOCs的应用方面受到越来越多研究者的关注[9-12]。李洪芳等[12]采用反相微乳法制备了CuO、ZrOx、FeOx和CoOx掺杂的Mn系列催化剂,发现Mn-CuOx催化剂降解甲苯的活性最高,其完全转化温度为220 ℃。但该类催化剂在等离子体协同催化领域的应用报道较少。
添加具有不完全占有4f轨道和空5d轨道的稀土金属助剂,可明显改善过渡金属催化剂的性能[7,13]。掺杂丰富氧空位和高储氧释氧能力的CeO2[4,9,12,14]和热稳定性好的ZrO2[15]形成CuO-CeO2-ZrO2固溶体,在改善Cu催化剂热稳定性的同时,可以增加了CuO-CeO2氧化物的氧的扩散率和存储容量,显著提升催化剂的活性[9]。本研究采用等体积浸渍法制备CuxMn1-xCe0.75Zr0.25/TiO2(x=1.0、0.75、0.5、0.25、0)复合氧化物催化剂。课题组前期研究证明,该系列催化剂的热催化活性顺序为CuCe0.75Zr0.25/TiO2>Cu-MnCe0.75Zr0.25/TiO2>MnCe0.75Zr0.25/TiO2[16]。在此基础上,本实验通过研究低温等离子体协同催化反应器上催化剂的活性,与单独低温等离子体降解甲苯的效率进行比较,对低温等离子体协同催化降解甲苯的作用进行了分析。
1 实验部分
1.1 催化剂的制备
选用Cu和Mn为主金属,Ce和Zr为助剂,TiO2为载体,采用等体积浸渍法制备系列CuxMn1-xCe0.75Zr0.25/TiO2(x=1.0、0.75、0.5、0.25、0)催化剂(记为CuxMn1-xCZ/T)。以(CuO)x(MnO2)1-x占4%(质量分数)为基准,将Cu(CH3COO)2、Mn(CH3COO)2、Ce(NO3)2和Zr(NO3)2按比例溶于去离子水中,待充分溶解后,加入到TiO2载体中,制得催化剂前驱体,随后在105 ℃下干燥6 h,550 ℃下焙烧4 h,得CuxMn1-xCZ/T催化剂。最后在20 MPa压力下压片、制粒、过筛,取10-12 目颗粒备用。
1.2 催化剂的表征
X射线衍射(XRD)由DX-2700型X射线衍射仪测定,Cu靶作为衍射源(λ=0.1541 nm),扫描步长0.06°。催化剂的程序升温还原(H2-TPR)使用PCA-140化学吸附仪测定。200 mg催化剂经Ar预处理后,用5%H2/Ar(50 mL/min)还原,以10 ℃/min的升温速率由室温升至800 ℃。O2程序升温脱附(O2-TPD)在相同的化学吸附仪上进行测定,200 mg催化剂在O2气氛下(30 mL/min)以20 ℃/min升至550 ℃吹扫30 min,降至室温后切换Ar气氛(50 mL/min),以10 ℃/min速率升至1000 ℃。X衍射光电子能谱(XPS)数据使用Perkin-Elmer PHI-1600 ESCAX射线光电子能谱仪进行测定,X射线源为Mg阳极靶(350 eV)。各个物种的结合能值以C 1s(Eb=284.8 eV)为内标校正。
1.3 催化剂的评价
1.3.1 等离子体联合催化实验评价装置
研究以甲苯为目标污染物。等离子体联合催化实验评价装置示意图见图1,主要由配气系统、反应系统和检测系统组成。
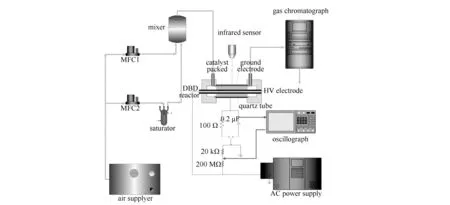
图 1 等离子体协同催化降解甲苯评价装置示意图
配气系统利用空气夹带甲苯蒸气来模拟甲苯废气(150 mg/m3),采用D08系列质量流量计(北京七星华创电子股份有限公司)控制配气系统中的气体流量,气体总流量控制为4 L/min;反应系统包括等离子体发生器和DBD反应器(石英玻璃),DBD电源采用型号为CTP-2000 K低温等离子体实验电源(Coronalab公司),信号输出为正弦波,频率输出为3-100 kHz,电压调节为0-100 kV。实验中的放电过程用时较短,反应器温度的变化较小,可以忽略温度对实验结果的影响。检测系统包括气相色谱仪和放电参量检测器。将催化剂(10-12目)装入内径为14 mm的石英反应器中,使样品充满整个放电区域。进出口处的CO2用AE. Porapak N填充柱分析,TCD检测;VOCs采用DB-35MS毛细柱分析,FID检测;研究不同放电功率下的甲苯降解效率。
1.3.2 催化剂转化率、选择性与比能密度(SED)的计算方法
催化剂的活性以甲苯的转化率表示,计算公式见式(1):
(1)
式中,x为甲苯的转化率,%;cin、cout分别为反应器进口和出口处甲苯的质量浓度,mg/m3。
CO2选择性计算式为(2):
(2)
式中,s为催化剂的CO2选择性;c1为尾气中的CO2的质量浓度(已扣除背景气体中CO2浓度),mg/m3;n为甲苯的碳原子数,7。
比能密度的计算公式见式(3):
(3)
式中,P为放电功率,W;qv为气体流量,L/min;SED为比能密度,J/L。
2 结果与讨论
2.1 催化剂的表征
2.1.1 XRD表征
CuxMn1-xCe0.75Zr0.25/TiO2催化剂以及纯氧化物CuO、MnO和载体TiO2的XRD谱图见图2。由图2可知,所有催化剂均出现载体TiO2的特征衍射峰,即25.2°、37.8°、48.1°、55.1°和62.8°处为锐钛矿晶型TiO2的强衍射峰,28.7°、36.8°和38.6°处为金红石晶型TiO2的弱衍射峰,XRD没有检测到CuO、MnO、CeO2、ZrO2的特征衍射峰,说明金属氧化物在载体表面高度分散或超出检测范围[16],且催化剂均很好地保留了实验用载体TiO2的形貌特征。
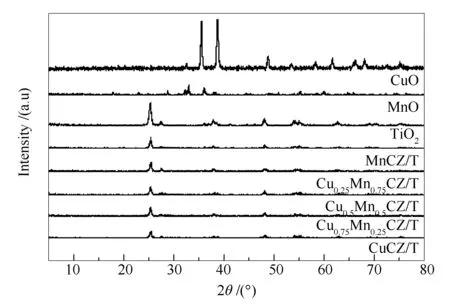
图2 CuxMn1-xCZ/T催化剂的XRD谱图
2.1.2 H2-TPR表征
图3为催化剂的H2-TPR谱图。
由图3可知,单一主金属的MnCZ/T催化剂在200-500 ℃仅出现了一个较弱的还原峰,对应着MnO2的还原[16]。其他CuxMn1-xCZ/T(x=1.0、0.75、0.5、0.25)催化剂均有两个还原峰,分别为α峰和β峰。低于200 ℃的α峰归属于进入到CeO2的晶格中且与Ce有强相互作用的CuO的还原峰[17]。CuO与CeO2之间的相互作用越强,会使CeO2的晶格发生扭曲,从而产生更多的氧空位,这有助于提高催化剂的活性[4]。催化剂的H2-TPR谱图中高于200 ℃的β峰为铜锰氧化物的还原峰[17]。随着Mn/Cu比的增加,Cu、Mn双金属CuxMn1-xCZ/T催化剂α峰的还原温度向高温偏移,是由于Mn的加入削弱了铜铈之间的相互作用所致;而β峰的还原温度向低温偏移,这是因为CuO加入锰氧化物后可以形成晶格缺陷和氧空位,从而促进彼此的还原能力[16]。
2.1.3 O2-TPD表征
图4为CuxMn1-xCZ/T催化剂样品的O2-TPD谱图。
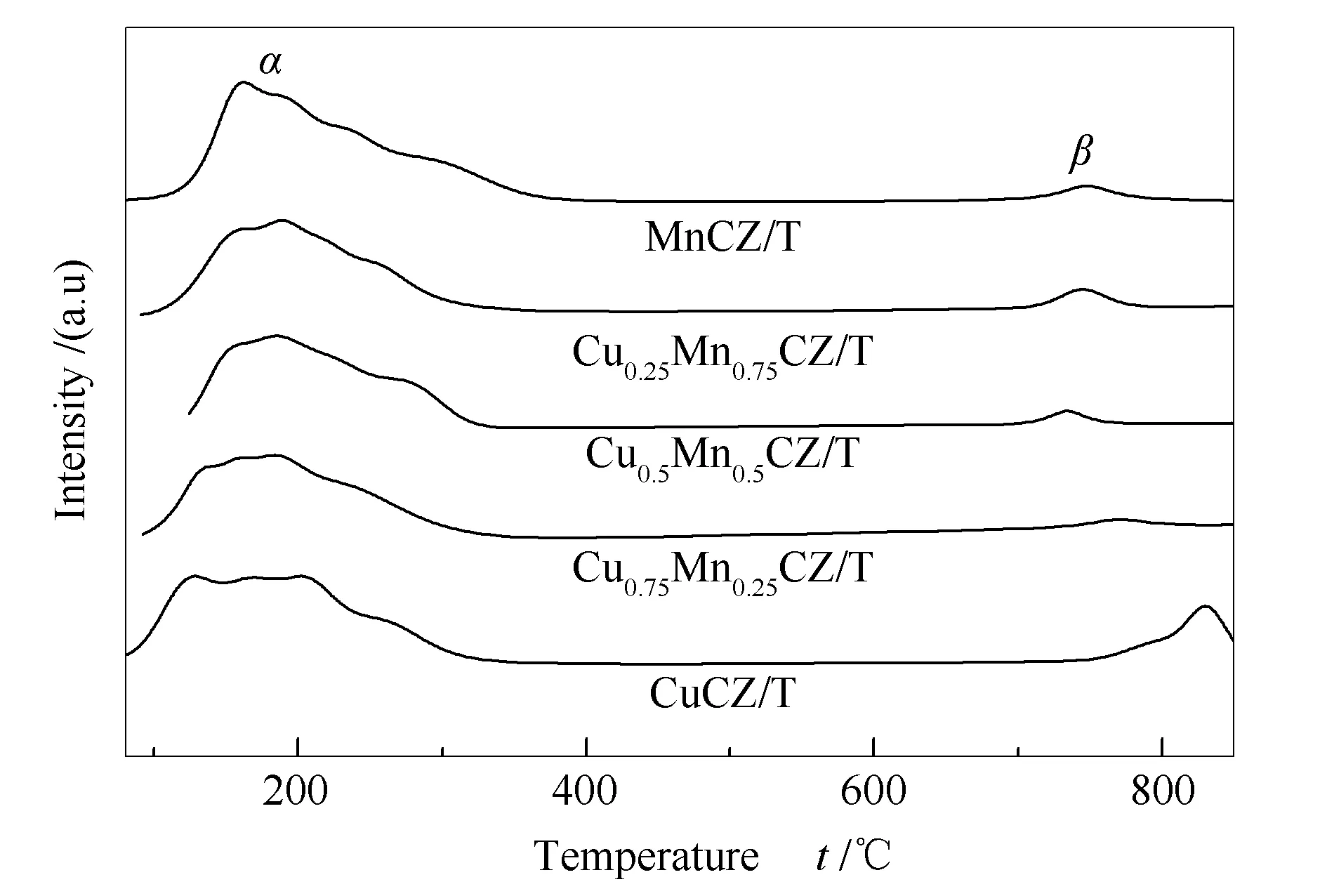
图 4 CuxMn1-xCZ/T催化剂的O2-TPD谱图
由图4可知,CuxMn1-xCZ/T催化剂均出现了两个O2的脱附峰,100-400 ℃的α峰为催化剂物理吸附氧(O2)和化学吸附氧(O-)的脱附峰;700-900 ℃的β峰为催化剂晶格氧(O2-)的脱附峰,其中,包含了表面晶格氧和体相晶格氧。
CuxMn1-xCZ/T催化剂上的甲苯催化氧化反应遵循MvK机理[16],参与反应的主要氧物种为晶格氧,其含量与催化剂的活性成正相关。因此,通过对晶格氧的β峰进行积分可知,CuCZ/T的晶格氧含量最高,为7.0 μmol/g,结合XPS结果(见2.1.4部分)可知,CuCZ/T催化剂中Ce3+浓度较高,可以产生更多的氧空位,从而促进晶格氧的迁移[18]。MnCZ/T催化剂的晶格氧含量(3.0 μmol/g)仅次于CuCZ/T催化剂,这是由于锰具有多个价态,易在催化剂中产生晶格缺陷,从而增强氧的流动性。
2.1.4 XPS表征
图5为CuxMn1-xCZ/T催化剂不同元素的XPS谱图。
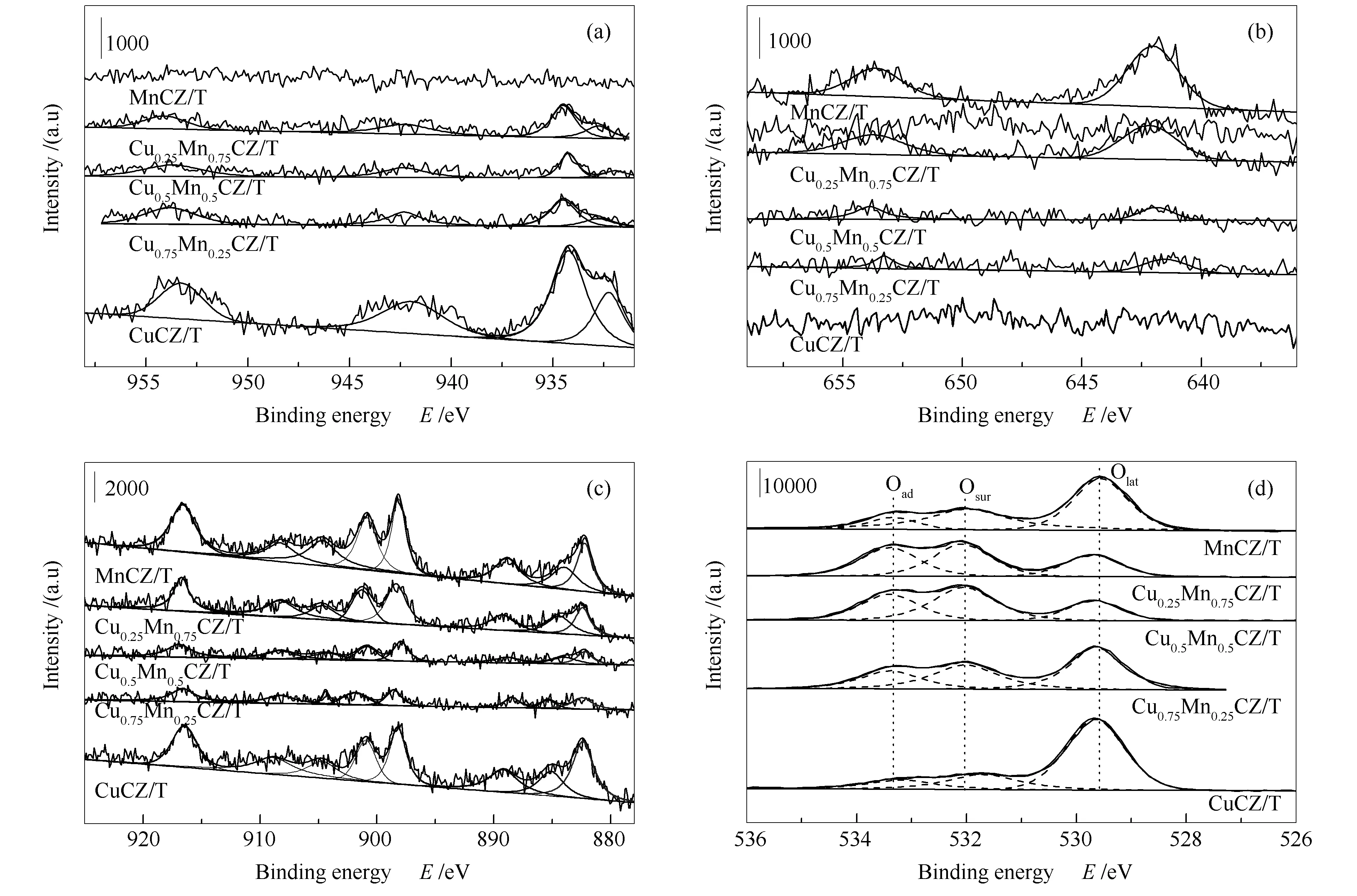
图 5 CuxMn1-xCZ/T催化剂的XPS谱图
由图5(a)可知,Cu 2p的XPS谱图中有明显的Cu 2p3/2(933.6 eV)和Cu 2p1/2(953 eV)特征衍射峰,在937.6-945.4 eV为卫星峰,证明有Cu2+的存在。Cu 2p3/2(933.6 eV)的特征衍射峰可分为两个峰,分别对应Cu+(933.5 eV)和Cu2+(934.5 eV)。图5(b)为拟合后的 Mn 2p谱图,其结合能位于643.4和657.2 eV分别对应于Mn 2p3/2和Mn 2p1/2,前者主要对应于Mn3+和Mn4+[19]。图5(c)为CuxMn1-xCZ/T催化剂Ce 3dXPS谱图,Ce元素 XPS谱图的复杂性是由Ce的4f轨道与配体氧的2p轨道杂化以及4f轨道被反馈的电子部分占据的结果。每个样品的谱图均可拟合为八个亚谱峰, 结合能从小到大依次用v、v1、v2、v3和μ、μ1、μ2、μ3表示。其中,v1和μ1为代表Ce3+的Ce 3d5/2和Ce 3d3/2的特征峰,其余为Ce4+的特征峰[20]。图5(d)为CuxMn1-xCZ/T催化剂的O 1sXPS谱图。其中,结合能位于 527.8-530.3 eV的 O 1s对应于表面晶格氧(-O);位于530.6-531.1 eV的O 1s归属于表面氧(β-O);位于532.1-534.3 eV的O 1s归因为吸附氧(-O)[21]。
表1给出了与XPS表征相对应的CuxMn1-xCZ/T催化剂表面物种的相对含量。由表1可知, 所有催化剂表面的Cu、Mn含量均小于理论负载量,说明Cu和/或Mn进入CeO2-ZrO2晶格中形成晶格缺陷。由Ce3+/Ce4+比可知,CuCZ/T催化剂的Ce3+/Ce4+比最高(0.35),这有利于Cu2++Ce3+和Cu++Ce4+的转换,从而提高催化剂的氧化还原能力。这与H2-TPR的结果相一致。此外,催化剂中的Ce3+取代Ce4+会形成缺陷结构,导致催化剂表面出现氧空位和不饱和化学键,使得CeO2中更多的化学吸附氧转移到晶格氧物种中[22]。而Mn的加入抑制了Cu和Ce之间的相互作用,从而使得其他催化剂的Ce3+/Ce4+值降低。比较催化剂的晶格氧(Olat)和吸附氧(Oad)比例可知,单金属催化剂含有的Olat多于双金属催化剂,表明催化剂中Cu-Mn之间的相互作用,阻碍了Cu进入CeO2晶格中,从而减少了Olat的比例,降低了催化剂的氧化能力[22]。XPS表征的催化剂表面晶格氧含量结果与O2-TPD得到的晶格氧含量相一致。
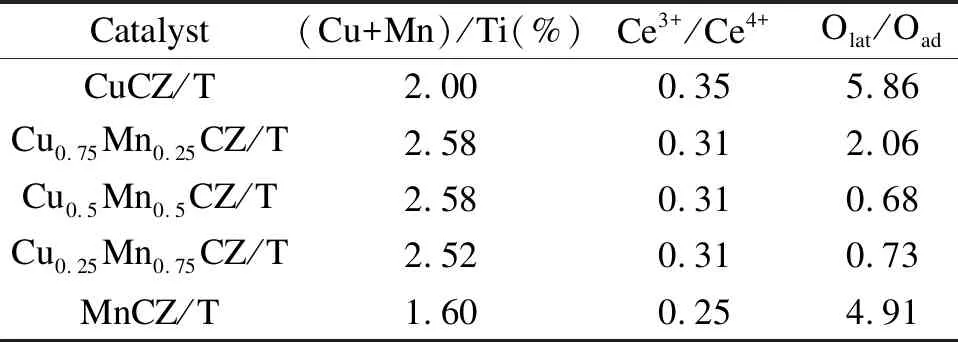
表1 CuxMn1-xCZ/T催化剂的表面物种
2.2 等离子体协同催化降解甲苯评价实验
单独等离子体和等离子体协同催化降解甲苯的转化率和CO2选择性见图6,相应的甲苯转化率为99%时对应的SED值见表2。
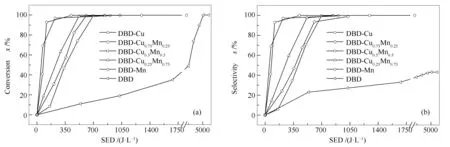
图 6 催化剂甲苯降解率(a)和CO2选择性(b)与比能密度的关系

表 2 CuxMn1-xCZ/T催化剂上甲苯转化率为99%时对应的SED值
由图6和表2可知,等离子体协同催化的甲苯降解效果明显高于单独等离子体作用下的效果;随着放电功率的增大,甲苯降解率和CO2选择性增加。值得注意的是,单主金属催化剂CuCZ/T和MnCZ/T的活性相近,在SED小于350 J/L时,甲苯就实现了90%的转化,明显优于双主金属催化剂。结合表征结果可知,CuCZ/T催化剂的低温还原性好、晶格氧含量高,且Ce3+/Ce4+值较其他催化剂较大,可以产生较多的氧空位有利于甲苯的活化,使得其在等离子体的作用下仍然具有较好的活性;等离子体在放电过程中会产生臭氧,放电功率越高,臭氧产生量越多[23]。当SED增加到一定值后,CuxMn1-xCZ/T催化剂(x=0.75、0.5、0.25、1.0)降解甲苯的效率开始凸显,使得其甲苯转化率达到99%时对应的SED值低于CuCZ/T催化剂(见表2)。这是由于这些催化剂中存在锰物种,Mn具有较强的分解O3的能力,可以将其分解为具有高活性的O·,从而促进反应的进行[14]。其中,MnCZ/T催化剂中锰含量最多,弥补了其相对较弱的氧化还原性能和较低的晶格氧含量的缺陷,使其降解甲苯效果与CuCZ/T催化剂基本一致。而双金属催化剂由于其(Cu+Mn)/Ti的比值较大,Ce3+/Ce4+值较小,说明催化剂中的氧物种主要为吸附氧且主金属和二氧化铈之间的相互作用力较小,使得双金属催化剂的活性低于单金属催化剂的活性,这也与其较差的低温还原性和较低的晶格氧比例的表征结果相对应。
由图6(b)的CO2选择性可知,在等离子体协同催化作用下,CO2选择性与甲苯转化率相对应,降解的甲苯完全转化为CO2和H2O,没有副产物生成。但是在单独等离子体作用下,甲苯的降解伴随着副产物的生成。随着SED的增加,甲苯的转化率是增大的,当SED增大到5100 J/L时,甲苯的转化率达到了100%,但CO2选择性仅为43%。这说明当有催化剂存在时,等离子体产生的高能电子和具有强氧化性的自由基通过吸附在催化剂活性中心上,提高了催化剂的氧化还原性能,从而提高了催化剂的CO2选择性。
3 结 论
Cu、Mn之间的相互作用削弱了Cu-Ce之间的相互作用,导致催化剂的还原能力和晶格氧含量降低,使得Cu-Mn双主金属催化剂的活性低于Cu、Mn单主金属催化剂。
在等离子体协同催化的条件下,CuCZ/T的活性较高依然与其具有较好的低温还原性和较多的氧空穴、晶格氧有关;当SED增加到一定值后,CuxMn1-xCZ/T催化剂(x=0.75、0.5、0.25、1.0)表现出更高的活性,表明含Mn催化剂可以与等离子体过程中产生的O3相互作用,从而增强了催化剂的活性。
