注射用单硝酸异山梨酯细菌内毒素检查法研究
2019-05-27曹霞飞何华红
曹霞飞 何华红
(1 广州市食品检验所,广东 广州 511405;2 广州市药品检验所,广东 广州 510160)
注射用单硝酸异山梨酯(Isosorbide Mononitrate for Injection)是新一代长效硝酸酯类抗心绞痛药物,为硝酸异山梨酯的主要活性代谢产物。本品主要释放一氧化氮使环鸟苷酸(CGM)增加而致血管扩张,降低肺动脉高压,减少回心血量,减轻心脏负荷,从而减少心肌耗氧量;同时还可通过提高血小板内环磷酸腺苷水平抑制肺血管微血栓形成,降低肺循环阻力[1],减轻心脏负荷,改善缺血区血流供应。近年来,该药物已广泛应用于心绞痛及充血性心力衰竭等心血管疾病的治疗。本品尚未收载于中国药典,国家食品药品监督管理局国家药品标准(试行)YBH05182003对其药物的质量控制采用家兔法进行热原检查;而国家食品药品监督管理局国家药品标准WS1-(X-022)-2005Z中规定注射用单硝酸异山梨酯内毒素限值为不大于3.2 EU/μg。本实验针对现有资料中,该药物存在方法、标准不统一且限度偏低等问题进行修订,以考察其进行细菌内毒素检查的可行性,并提出将其限度提高至更安全合理的范围,力求降低其在临床使用中的热原反应率。研究如下。
1 仪器与试药
1.1 仪器:恒温水浴(SW22型),德国Julabo公司;旋涡混合器(MSI型),广州IKA公司。所用玻璃用具和耐热材料置于热空气烤箱中经250 ℃干热2 h除去热原。
1.2 试药:注射用单硝酸异山梨酯(瑞阳制药有限公司,规格:每瓶50 mg,批号:12043006;山东新时代药业有限公司,规格:每瓶20 mg,批号:033120201;浙江普洛康裕制药有限公司,规格:每瓶20 mg,批号:20100705B;海南新中正制药有限公司,规格:每瓶50 mg,批号:120201;武汉华龙生物制药有限公司,规格:每瓶25 mg,批号:20120503。
1.3 细菌内毒素工作标准品规格:批号:150601-201174,160 EU/支,中国食品药品检定研究院提供。
1.4 细菌内毒素检查用水(BET水)规格:批号:1105060,50 mL/支,湛江安度斯生物有限公司产品。
1.5 鲎试剂(TAL)A:湛江安度斯生物有限公司产品,批号:1202151,灵敏度(λ):0.25EU/mL,规格:0.1mL/支;鲎试剂(TAL)B:厦门市鲎试剂实验厂有限公司产品,批号:110603,灵敏度(λ):0.25 EU/mL,规格:0.1 mL/支。
2 方法与结果
2.1 内毒素限值(L)的确定[2]:注射用单硝酸异山梨酯临床最大有效剂量为7毫克/次,依据剂量来确定,非经肠道药品的内毒素限值L等于K/M,K是人每千克体质量的内毒素阈值,注射剂K=5 EU/(kg·h);M是人每千克体质量在1 h内的最大注射剂量,按成人体质量60 kg计算,根据“化学药品注射剂安全性检查法应用指导原则”的要求安全系数定为3,经计算得到注射用单硝酸异山梨酯的细菌内毒素限值为14 EU/mg。以此为依据,做以下可行性研究。
2.2 灵敏度复核试验:按照中国药典2015年版四部通则细菌内毒素检查法,复核实验所用鲎试剂的灵敏度测试值(λc)是否在其标示灵敏度(λ)的可接受范围内,根据不同厂家不同规格鲎试剂灵敏度的标示值,将细菌内毒素工作标准品用BET水溶解,在旋涡混合器上混匀30 min,分别制成2倍稀释系列,即2λ、λ、1/2λ和1/4λ四个浓度的内毒素标准溶液,试验包括阴性对照。将溶液直接加入和等量容积(0.l mL)装有冻干粉试剂的单次试管中,恒温孵育一段时间[(37±1)℃,(60±2)min],避免振动,将每支试管按顺序从恒温器中直接取出并轻轻翻转180°观察结果,如果内容物形成坚实凝胶并在试管翻转后保留在原处,则记为阳性;如果未形成完整的凝胶,则结果为阴性,最低浓度的内毒素标准溶液的所有平行管都为阴性结果试验才为有效试验。
结果见表1,由表1可见,两批鲎试剂经用细菌内毒素工作标准品检查,λc/λ均在0.5~2.0,结果均符合规定。
2.3 干扰初筛试验[3]
2.3.1 最大有效稀释倍数是样品的最大允许稀释倍数,在MVD下,内毒素限值可以被判断,此方法适应于注射液或非经肠道的以溶解或稀释形式给药的药品溶液,MVD的计算公式如下:MVD=cL/λ,L=14 EU/mg,因此可计算出注射用单硝酸异山梨酯进行细菌内毒素检测时,使用目前常用于药品检验的0.25~0.03 EU/mL的鲎试剂所对应的最大有效稀释倍数分别为56、112、224、448、896倍,对应的最低有效浓度为0.036 mg/mL、0.018 mg/mL、0.009 mg/mL、0.0045 mg/mL、0.002 mg/mL。

表1 鲎试剂灵敏度复核试验结果
2.3.2 初筛试验:取5批注射用单硝酸异山梨酯,用细菌内毒素检查用水(BET水)进行稀释,使其质量浓度分别为0.036 mg/mL、0.018 mg/mL、0.009 mg/mL、0.0045 mg/mL、0.002 mg/mL将以上系列浓度溶液标记为供试品组(NPC),用上述梯度的BET水稀释液作为溶剂,与4λ浓度内毒素标准品等比混合的方法制备含有2λ浓度内毒素的供试品,标记此系列溶液为供试品阳性对照组(PPC),取灵敏度为0.25 EU/mL的两个不同厂家的鲎试剂进行试验,每一稀释浓度制备两管,同时按常规分别设细菌内毒素阳性对照组(PC)和BET水阴性对照组(NC)各两管,结果见表2。

表2 样品干扰初筛试验结果
从表2结果可见,所用的5批注射用单硝酸异山梨酯浓度稀释到0.018 mg/mL或以下时,两个厂家的鲎试剂与细菌内毒素反应均未见增强或抑制的干扰作用。
2.4 干扰试验:用灵敏度为0.25 EU/mL,两个不同厂家的鲎试剂按中国药典2015年版四部通则的细菌内毒素检查法进行试验,取不同厂家5批注射用单硝酸异山梨酯用BET水将样品稀释至0.018 mg/mL,用BET水和供试品稀释液将对应的细菌内毒素工作标准品稀释成2λ、λ、1/2λ和1/4λ浓度的PPC系列和供试品稀释液NPC系列,每一稀释浓度平行4管,同时用上述供试品稀释液和BET水各做两管阴性对照管,按公式计算BET水和供试品稀释液反应终点浓度的几何平均值(Es和Et),Es=lg-1(Xs/4),Et=lg-1(Xt/4),结果见表3。
从表3可知,5批注射用单硝酸异山梨酯用两个厂家生产的鲎试剂进行试验,结果注射用单硝酸异山梨酯0.018 mg/mL稀释溶液对两个厂家生产的鲎试剂测得的灵敏度在0.5λ~2.0λ,表明此浓度样品溶液无干扰作用。
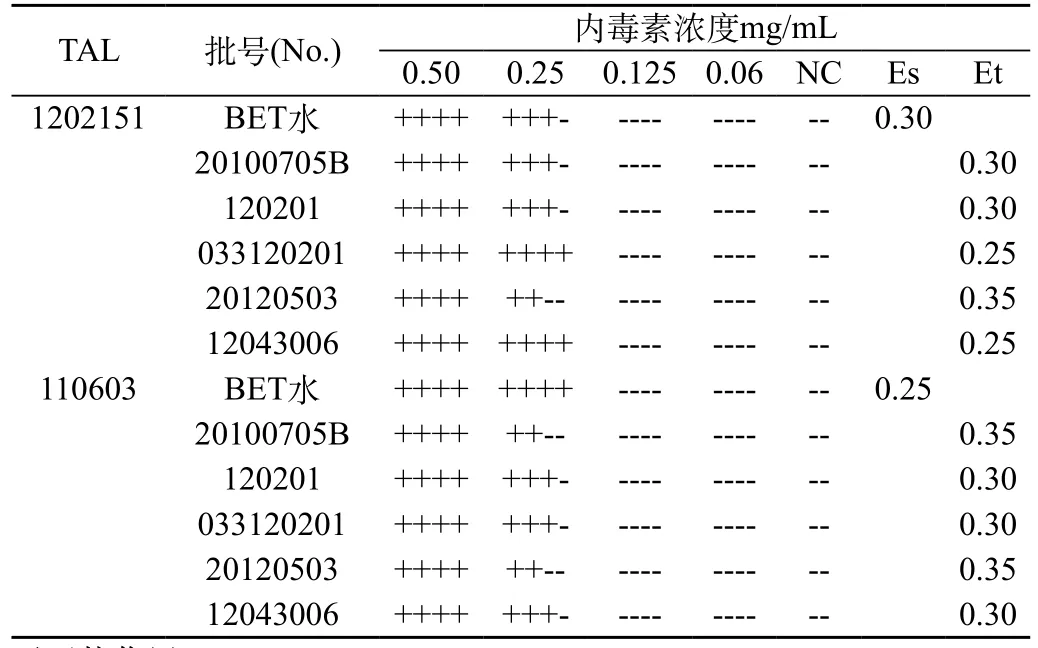
表3 样品(终浓度为0.018mg/mL)干扰试验结果
2.5 样品细菌内毒素检查:取5批注射用单硝酸异山梨酯,稀释方法同2.4制成供试品溶液,使用λ=0.25 EU/mL的两个厂家的鲎试剂进行细菌内毒素检查,并用此稀释液将细菌内毒素工作标准品稀释为2λ的溶液,作为供试品的阳性对照,另外以BET水建立阳性对照和阴性对照,按中国药典2015年版二部细菌内毒素检查法检查,结果见表4。

表4 样品细菌内毒素检查结果
从表4结果可见,阴性对照组(NC)均为阴性,供试品阳性对照组(PPC)和阳性对照组(PC)均为阳性,实验有效;供试品组(NPC)均为阴性,表明样品中所含细菌内毒素未超过限度规定,5批注射用单硝酸异山梨酯的细菌内毒素检查均符合规定。
3 讨 论
本研究通过比较鲎试剂与内毒素在水溶液和供试品溶液中反应的差异程度,确定供试品在某一浓度下是否对细菌内毒素检查有增强或抑制。采用了不同厂家共5批样品与鲎试剂的相容性进行筛查试验,确定其无干扰浓度范围。将注射用单硝酸异山梨酯的0.036 mg/mL、0.018 mg/mL、0.009 mg/mL、0.0045 mg/mL、0.002 mg/mL稀释液与批号为1202151,灵敏度0.25 EU/mL(由湛江安度斯生物有限公司提供)和批号为110603,灵敏度0.25 EU/mL(由厦门市鲎试剂厂有限公司提供),两个厂家生产的鲎试剂进行试验。内毒素干扰预试验结果表明注射用单硝酸异山梨酯为0.018 mg/mL或以下浓度稀释液时对以上两个厂家的鲎试剂无干扰作用。
随后进行正式干扰试验,5批注射用单硝酸异山梨酯0.018 mg/mL稀释液与以上两批次鲎试剂(批号同干扰筛查试验)进行干扰试验,结果对两个厂家生产的鲎试剂均无干扰作用,Es/Et均在0.5~2.0,表明注射用单硝酸异山梨酯0.018 mg/mL稀释液对以上两个厂家鲎试剂无干扰作用。
研究表明,注射用单硝酸异山梨酯可按《中国药典2015年版四部》通则第一法(凝胶法)进行细菌内毒素检查,确定限值为:14 EU/mg是可行的。
