猪毛角蛋白降解菌的分离筛选及其降解特性研究
2019-05-21尹红梅刘惠知
刘 标,尹红梅,刘惠知
(湖南省微生物研究院,长沙 410009)
0 引 言
随着中国生猪养殖和加工业的快速发展,每年产生了大量的废弃猪毛,大部分猪毛被填埋或焚烧处理,这些处理方法对生态环境造成了严重的污染。猪毛富含 α-角蛋白,含量高达95%以上[1],如果对这些废弃蛋白进行降解回收利用,不仅可以改善生态环境,其降解产物可广泛用于饲料蛋白源及有机肥。
角蛋白在分子内和分子间存在二硫键、氢键、配位键和范德华力等多种键能,三维构象高度交联,性质稳定,不容易被普通的蛋白酶(胃蛋白酶、胰蛋白酶)水解,因此给资源化利用带来了困难。根据文献报道[2],猪毛角蛋白的二级结构主要为 α-螺旋,半胱氨酸的含量高(二硫键多),比羽毛角蛋白(β-螺旋)结构更稳定,更难降解。研究表明,自然界中的某些微生物能够将角蛋白降解成小肽、氨基酸等动物可以消化利用的成分,利用微生物对角蛋白废弃物进行无害化处理是一种高效、环保、低成本的转化方式。近年来,利用微生物降解角蛋白引起了研究工作者的广泛关注,目前已报道能降解羽毛角蛋白的微生物包括细菌、真菌、放线菌[3-14],如枯草芽孢杆菌、金黄色节杆菌、淡拟紫青霉和链霉菌等菌种,但专门针对猪毛角蛋白高效降解的微生物仅有少数报道[15-16]。因此,本研究从生猪屠宰场周边土壤中取样,筛选到一株高效降解猪毛角蛋白的微生物菌株,并对其进行了分类鉴定及降解特性的研究,旨在丰富降解猪毛角蛋白的微生物资源,为猪毛废弃物的无害化处理和资源化利用提供技术支持。
1 材料与方法
1.1 材料
1.1.1 菌株分离样品
长沙市某生猪屠宰场周围长期堆积废弃猪毛处的土壤样品。
1.1.2 角蛋白材料
各种废弃毛发的获取:收集屠宰场周边废弃的猪毛、鸡毛、鹅毛、鸭毛、羊毛,用蒸馏水冲洗干净,60 ℃烘干水分至恒定质量。
猪毛粉制备:将烘干后的猪毛粉碎,过80目筛后即制成猪毛粉。
1.1.3 培养基
选择培养基:猪毛粉 10.0 g/L,KH2PO40.5 g/L,K2HPO41.0 g/L,NaCl 0.5 g/L,pH值为7.0。降解培养基:猪毛 10 g/L,KH2PO40.5 g/L,K2HPO41.0 g/L,NaCl 0.5 g/L,pH值为7.0牛肉膏蛋白胨培养基:牛肉膏5.0 g/L,蛋白胨10.0 g/L,NaCl 5.0 g/L,pH值为7.0。以上所有培养基均121 ℃高温灭菌20 min待用。
1.2 试验方法
1.2.1 高效猪毛角蛋白降解菌的分离及筛选
称取1.1.1中采集的土壤样品10.0 g置于内含90 mL无菌水的锥形瓶中,充分振荡混匀。取5 mL混合液置于内含100 mL选择培养基的锥形瓶中,30 ℃,180 r/min振荡培养。取驯化培养96 h的菌液梯度稀释后,涂布在固体选择培养基(选择培养基中添加2%琼脂)平板上培养3 d,筛选生长良好的单菌落,利用四分区划线法进一步纯化,牛肉膏蛋白胨试管斜面低温保存各菌株。
1.2.2 初筛菌株猪毛角蛋白降解率的测定
将初筛获得的角蛋白降解菌接种至牛肉膏蛋白胨培养基中培养24 h(30 ℃,180 r/min)获得种子液,调节各种子液的活菌数约为3.0×108CFU/mL。将各种子液以2%接种量分别接种到以猪毛为唯一碳氮源的降解培养基中,30 ℃,180 r/min培养,观察猪毛的降解状况,接种等量无菌水作为对照。分别在第 3、5、7天,采用失质量法测定猪毛的降解率[16],即将培养液利用滤纸过滤,收集残渣至干燥箱内干燥至恒定质量,称量残渣质量,计算各菌株的猪毛角蛋白降解率。降解率的计算公式如下
猪毛降解率=(对照猪毛干质量-试验组猪毛残渣干质量)/对照猪毛干质量×100% (1)
1.2.3 高效猪毛角蛋白降解菌X-3的菌种鉴定
菌株形态及生理生化鉴定:在牛肉膏蛋白胨培养基上培养48 h后观察菌落形态特征,在油镜下观察菌体形态。菌株生理生化性质的鉴定参照《微生物学实验教程》(第2版)[17]。
菌株16S rDNA序列分析:用DNA提取试剂盒提取菌株X-3的基因组DNA,采用16S rDNA通用引物27F : 5′-AGAGTTTGATCCTGGCTCAG-3′, 1492R :5′-GGTTACCTTGTTACGACTT-3′进行 PCR 扩增。PCR反应条件:95 ℃预变性3 min;95 ℃变性45 s,56 ℃退火45 s,72 ℃延伸90 s,反应进行30个循环;最后72 ℃延伸10 min,4 ℃终止。将PCR产物回收纯化后委托上海生物工程股份有限公司测序。
PCR产物测得的序列在NCBI中运用Blast进行同源性分析,利用Mega 5.0软件中Neighbor-Joining法构建基于16S rDNA序列的系统发育树,重复取样1 000次进行bootstrap检验,确定该菌的种属。
1.2.4 菌株X-3对不同来源角蛋白的降解效果分析
为了探究菌株 X-3对几种常见角蛋白底物的降解效率,分别在降解培养基中添加猪毛、鸡毛、鸭毛、鹅毛、羊毛进行降解试验,降解培养基中各种毛发的添加量均为10 g/L,接种量为2%(体积分数),30 ℃,180 r/min培养,在第7 d采用失质量法测定降解率,以接种等量无菌水为对照,降解率的计算方法同1.2.2中所述。
1.2.5 菌株X-3降解猪毛角蛋白机理的初步研究
1)菌株X-3降解猪毛角蛋白产物分析
接种一环菌株X-3到牛肉膏蛋白胨培养基中,30 ℃,180 r/min培养24 h制成种子液,调节种子液的活菌数约为3.0×108CFU/mL。以2%接种量接种种子液到选择培养基中,30 ℃,180 r/min培养,分别在第1、2、3、4、5、6、7天测定角蛋白的降解率、发酵上清液中胞外角蛋白酶活、胞外二硫键还原酶活性、可溶性蛋白含量、各种含硫化合物(巯基化合物、硫酸盐、亚硫酸盐)含量,每个处理重复3次。
2)各成分分析测定方法
发酵液4 ℃、5 000×g离心10 min后,经0.22 μm过滤器过滤后即制成胞外粗酶液。胞外角蛋白酶活性、二硫键还原酶活性、可溶性蛋白含量的测定参照齐治国等[18]研究中介绍的方法进行,发酵上清液中各种含硫化合物的含量测定参照黄林等[19]研究的方法进行。
1.3 数据分析
试验数据利用Microsoft Excel 2003进行初步计算,以平均值±标准差表示,并绘图;利用软件SPSS 18.0对数据进行统计分析,数据间差异显著性比较采用One-way ANOVA方法进行分析。
2 结果与分析
2.1 高效猪毛角蛋白菌株的分离筛选
经驯化筛选后,共分离筛选到 6株能够利用猪毛粉作为碳氮源生长的细菌菌株,分别编号为X-1、X-3、X-4、X-6、X-7、X-8。将6株菌株接种到降解培养基中发酵培养,第 7天时各培养基中的猪毛都有被降解的现象,其中,接种菌株 X-3的锥形瓶中猪毛降解程度最高,培养液明显变浑浊,菌株生长旺盛(图1)。6株菌株在不同时间点对猪毛角蛋白的降解率如表 1所示,结果显示,菌株X-3在各时间点对猪毛的降解率均为最高,第7天时,降解率达77.3%,降解效果显著强于其他菌株。因此,选取菌株X-3进行下一步深入研究。
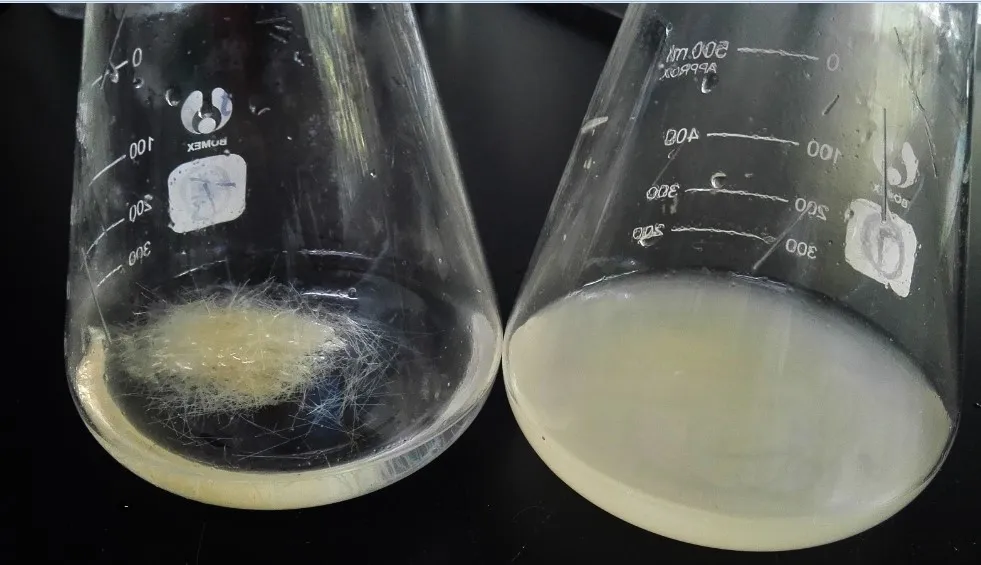
图1 菌株X-3对猪毛底物的降解效果Fig.1 Pig hair degradation effect of strain X-3

表1 不同菌株对猪毛角蛋白的降解率Table 1 Degradation rate of different strains to pig hair keratin%
2.2 高效降解菌X-3菌种鉴定
2.2.1 菌株形态学观察及生理生化试验结果
将菌株X-3接种在牛肉膏蛋白胨平板上,30 ℃培养48 h后,可以观察到菌落正面呈白色,反面呈淡黄色,边缘不整齐,表面干燥光滑(图 2a)。在油镜下观察,菌株X-3营养体呈杆状,单个排列,可形成芽孢(图2b)。菌株生理生化试验结果如表 2所述,与已报道的凝结芽孢杆菌的生化特征相符合。
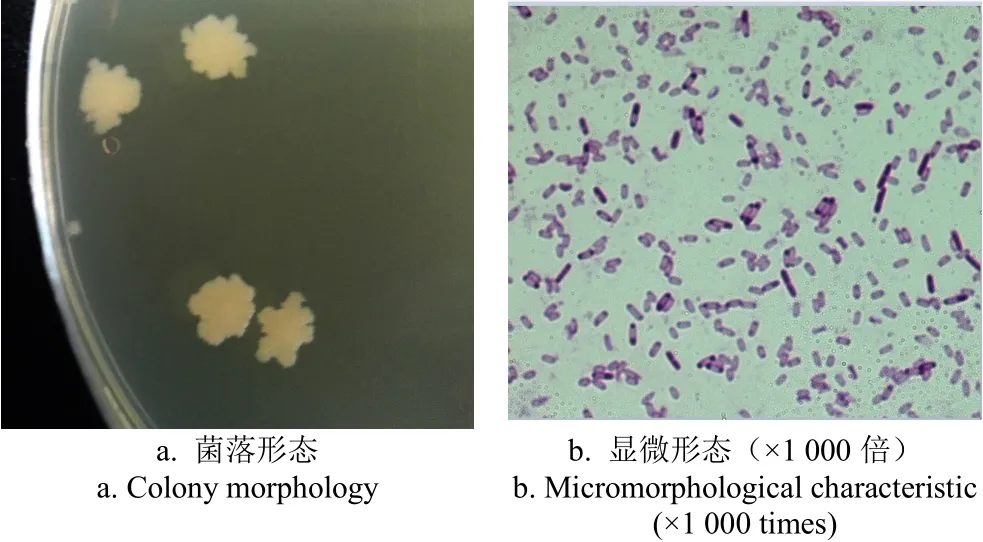
图2 菌株X-3菌落形态及显微形态特征Fig.2 Colony morphology and micromorphological characteristics of strain X-3

表2 菌株X-3的生理生化特征Table 2 Physiological and biochemical characteristics of strain X-3
2.2.2 菌株16S rDNA序列分析结果
测序结果显示,菌株 16S rDNA扩增序列长度为1 456 bp,将其序列提交到 Genbank数据库(登录号MK182787),并在NCBI数据库中进行Blast分析,根据同源性比对结果,利用 Mega 5.0软件构建基于 16S rDNA序列系统进化树,结果如图3所示,菌株与凝结芽孢杆菌的进化距离最近。结合菌株形态学特征、生理生化特征和 16S rDNA序列分析的结果,初步将菌株 X-3鉴定为凝结芽孢杆菌(Bacillus coagulans)。

图3 基于菌株X-3 16S rDNA序列的系统发育树Fig.3 Phylogenetic tree based on 16S rDNA sequences of strain X-3
2.3 菌株X-3对不同来源角蛋白的降解能力
图4 结果表明,发酵培养7 d后,菌株X-3对鸡毛、鹅毛的降解率分别为86.7%、88.4%,显著优于对其他 3种角蛋白底物的降解率(P<0.05)。菌株对猪毛、羊毛、鸡毛、鹅毛、鸭毛等角蛋白底物的降解率均大于 60%,说明其对不同来源的角蛋白均具有较好的降解效果,是一株广谱的角蛋白降解菌。

图4 菌株X-3对不同角蛋白的降解效果Fig.4 Degradation effect of strain X-3 to different keratins
2.4 菌株X-3降解猪毛角蛋白的机理初探
2.4.1 角蛋白降解率与角蛋白酶活性、二硫键还原酶活性的变化趋势
图 5结果显示,在以猪毛角蛋白为唯一碳氮源的培养基中,菌株X-3摇瓶发酵7 d时间内,猪毛角蛋白的降解率、角蛋白酶活性和二硫键还原酶活性均表现出先增大后保持稳定的变化趋势。前5 d,猪毛角蛋白的降解率、角蛋白酶活性和二硫键还原酶活性均随着培养时间的延长而逐渐增大,此后,无显著性变化。猪毛角蛋白降解率与角蛋白酶活、二硫键还原酶活之间均呈显著的正相关关系,相关系数分别为0.964、0.975,说明猪毛角蛋白的降解依赖于菌株 X-3产生的角蛋白酶和二硫键还原酶活力的大小。

图5 菌株X-3发酵过程中角蛋白降解率与角蛋白酶活性、二硫键还原酶活性的变化Fig.5 Keratinase, disulfide reductase activity and keratin degrading rate during fermentation by strain X-3
2.4.2 菌株X-3降解角蛋白过程可溶性蛋白及各种含硫化合物的变化
表3结果表明,菌株X-3在降解猪毛角蛋白的过程中,产生了大量的可溶性蛋白,角蛋白中的硫元素也随之转化为硫酸盐、亚硫酸盐和巯基化合物等多种形式的含硫化合物。发酵前5 d,可溶性蛋白的含量不断增加,质量浓度最高达863.4 µg/mL,此后稍有下降,推测是后期微生物对可溶性蛋白的利用速度大于可溶性蛋白生成的速度导致。角蛋白中二硫键中的硫主要转化为硫酸盐,其含量显著高于同时期亚硫酸盐、巯基化合物的含量(P<0.05)。

表3 角蛋白降解过程中可溶性蛋白及含硫化合物质量浓度变化Table 3 Content change of soluable protein and sulfur compounds during degradation of keratin
3 讨 论
利用微生物降解猪毛角蛋白不仅能够有效改善生态环境,而且可以增加蛋白质饲料的供给[20-21]。本研究以含二硫键较多的 α-角蛋白(猪毛)为降解对象,分离筛选到的凝结芽孢杆菌X-3对α-角蛋白和β-角蛋白均具有较好的降解效果,应用范围广。凝结芽孢杆菌(Bacillus coagulans)是中国农业农村部和美国食品药品监督管理局批准可用于动物饲料添加的安全微生物菌种,它可以维持肠道微生态平衡、提高动物的免疫力,同时由于其能产生芽孢,具有抗逆性强、易储存等优点,该菌种在益生菌领域成为了研究热点[22-24]。根据文献检索,目前未见有将凝结芽孢杆菌用于降解角蛋白方面的报道。因此,本研究筛选到的Bacillus coagulans X-3丰富了猪毛角蛋白降解的菌种资源,在废弃角蛋白的资源化利用方面具有较好的应用前景。
根据文献报道[25],微生物降解角蛋白的过程可分为以下 2个步骤:首先,角蛋白结构中二硫键遭到破坏,角蛋白分子变得疏松,角蛋白初步变性;然后,在蛋白水解酶或别的物理化学因素的作用下将变性的角蛋白水解,最终降解成肽段、氨基酸等小分子物质。角蛋白中二硫键起主要稳定作用,降解角蛋白的关键步骤是二硫键的断裂。
目前,研究工作者总结出 3种主要的角蛋白二硫键断裂途径,即二硫键还原酶裂解途径、真菌菌丝体机械穿透裂解途径、亚硫酸盐裂解途径[26]。本研究筛选获得的菌株 X-3在降解角蛋白过程中能够分泌胞外二硫键还原酶,而且其酶活与角蛋白降解率存在较强的相关性,说明该菌株主要依靠二硫键还原酶断裂二硫键,然后由角蛋白酶进一步水解变性的角蛋白。根据已有的文献报道[18,27-28],目前仅在放线菌、真菌等能够产生菌丝体的微生物中发现有机械力破坏角蛋白二硫键的机制,而凝结芽孢杆菌X-3是细菌,显然不具有类似能力。
关于亚硫酸盐裂解途径,有学者在研究真菌降解角蛋白的试验中得出结论:菌株首先会分泌亚硫酸盐断裂二硫键,然后变性的蛋白质进一步被蛋白酶降解[29-30]。菌株 X-3在降解角蛋白二硫键的过程中也伴随着亚硫酸盐的生成,亚硫酸盐是否在二硫键的断裂过程中起到作用,本研究没有进一步深入,因此,下一步计划添加不同浓度的亚硫酸盐到菌株 X-3的降解培养基及胞外粗酶液中,检测对角蛋白降解效率的影响。
为了进一步挖掘该菌在降解角蛋白方面的潜能,还有许多的工作需要进一步深入研究,如优化该菌株的最佳产酶及降解角蛋白的环境条件、X-3降解角蛋白的分子机理也有待进一步深入。
4 结 论
本研究筛选到一株高效的猪毛角蛋白降解菌株X-3,其对猪毛降解率高达77.3%。综合菌株形态学、生理生化特征及16S rDNA系统发育分析结果,初步鉴定该菌株为凝结芽孢杆菌(Bacillus coagulans)。菌株X-3对α-角蛋白(猪毛、羊毛)和 β-角蛋白(鸡毛、鹅毛、鸭毛)的降解率均大于 60%,是一株高效的广谱角蛋白降解菌。菌株对猪毛角蛋白的降解依赖于其产生的角蛋白酶和二硫键还原酶活力的大小,在降解过程中产生了大量的可溶性蛋白,二硫键中的硫也随之转化为硫酸盐、亚硫酸盐和巯基化合物,表明菌株 X-3在利用角蛋白的过程中存在酶降解途径,但是否具有亚硫酸盐降解途径有待进一步验证。
本试验筛选的高效安全降解菌株 X-3可将猪毛角蛋白降解成易被动物体消化利用的可溶性蛋白、多肽、氨基酸等产物,可用于废弃猪毛角蛋白的资源化利用,具有广阔的应用潜力。
