一步合成法制备双金属有机骨架材料及其低温选择性脱硝催化性能
2019-05-21曲殿利郭玉香魏原驰孙文静杨雨静
姚 焯,曲殿利,郭玉香,魏原驰,孙文静,杨雨静
(1.辽宁科技大学材料与冶金学院,鞍山 114051;2.辽宁科技大学高温材料与镁资源工程学院,鞍山 114051;3.辽宁丰华实业有限公司,营口 115103;4.辽河石油勘探局有限公司石油化工分公司,盘锦 124022)
1 引 言
在现代社会中,汽车尾气等移动源和火电厂等固定源都会排放出大量的氮氧化物(NOx)从而导致一系列严重的环境问题,例如:光化学烟雾、酸雨、臭氧分解以及温室效应等。NH3选择性脱硝催化还原法是一种有效的治理火电厂等固定源的NOx尾气排放技术[1-2]。然而,目前在工业化应用中最广泛的催化剂是以V2O5-WO3/TiO2为代表的催化剂。通常来说,该类催化剂的工作温度为300~400 ℃。为了避免重新对烟气进行加热同时保证催化剂的工作温度,SCR装置被安装在脱硫和静电除尘装置之前。然而这会造成一系列的问题,例如把烟气中的SO2氧化成SO3进而腐蚀其它设备以及管路,并且由于大量的烟尘及生成的碱金属覆盖在催化剂的表面造成催化剂中毒失活。因此开发出一种低温SCR催化剂可以有效的提升催化剂的寿命以及保护后端设备,这引起了研究者们的广泛关注。
近年来,负载的锰基催化剂以及锰复合催化剂由于其优秀的低温选择性脱硝催化性能、环境友好、成本低而被广泛的研究[3-4]。研究者们对铜分子筛催化剂也进行了广泛而深入的研究,发现Cu是做为催化活性中心而存在于催化剂中,孤立的Cu2+和Cu-O-Cu二聚体在SCR反应中起着决定性的作用[5-6]。目前,金属有机骨架材料(MOFs)由于其具有可调节的孔道结构,巨大的比表面积和孔隙率,优异的热稳定性而在催化反应[7-8]、气体的吸附和分离[9-10]、药物传输[11-12]、能量储存[13-14]等领域有着广阔的应用前景。
Cu3(BTC)2(H2O)3(CuBTC)由于其具有丰富的孔结构、适宜的孔径还有大量的不饱和金属活性位点,因此是一种理想的低温SCR催化剂。在本实验中,采用一步合成法将Mn纳米粒子有效的负载到了CuBTC表面,制备了一系列Mn-Cu-BTC催化剂,采用TG、XRD、FESEM、BET等手段对其进行表征,确定了催化剂的物相,热稳定性和微观结构,根据在固定实验台上对模拟烟气的催化效果,讨论了Mn-Cu-BTC系列催化剂的低温脱硝性能。
2 实 验
2.1 试 剂
三水合硝酸铜(阿拉丁试剂),N-N-二甲基甲酰胺(DMF;阿拉丁试剂),无水乙醇(北京化工厂),均苯三甲酸(阿拉丁试剂),四水合氯化锰(阿拉丁试剂),去离子水(实验室自制)。
2.2 催化剂的制备
2.2.1 CuBTC的制备
将15 mL 去离子水,15 mL 无水乙醇,15 mL DMF倒入烧杯中混合后再加入4.5 mmol(1.087g)Cu(NO3)2·3H2O与4.5 mmol (0.525 g)H3BTC并超声30 min直到溶液中沉淀完全溶解。将烧杯中溶液转移到带有聚四氟乙烯内衬的水热反应釜中,在120 ℃下保温12 h。反应结束后,使水热反应釜自然冷却到室温后用乙醇洗涤沉淀。在100 ℃下干燥12 h。
2.2.2 Mn-Cu-BTC的制备
取相应质量的Cu(NO3)2·3H2O和MnCl2·4H2O放入烧杯中,加入4.5 mmol (0.525 g) H3BTC、15 mL 去离子水、15 mL DMF、15 mL 无水乙醇。将溶液转移到带有聚四氟乙烯内衬的水热反应釜中,在120 ℃下反应12 h。用去离子水洗涤沉淀在100 ℃下干燥12 h。所得样品记为Mn-Cu-BTC/x(x为Mn与CuBTC质量比)。
2.3 样品表征
采用德国耐驰公司的STA449F3型同步热分析仪,在氮气气氛下对制备的催化剂进行综合热分析,初始温度40 ℃,终止温度为750 ℃,升温速率为10 ℃/min。采用X' Pert Powder型号X射线衍射仪对催化剂进行物相分析,测试角度为5°~50°,光源为CuKα射线(λ=0.15406 nm);催化剂的比表面积采用北京精微高博公司生产的JW-BK112型比表面积和微孔分析仪进行分析,催化剂首先在200 ℃下真空脱附处理2 h,以 N2为吸附质,在-196 ℃下进行测试。利用Brunauer-Emmett-Teller (BET)模型计算催化剂的比表面积,采用Barrett-Joyner-Halenda(BJH)分析其比孔容及孔分布方程;采用德国蔡司公司生产的Zeiss-∑IGMA HD型场发射扫描电子显微镜对催化剂进行微观形貌表征。
2.4 SCR脱硝性能测试
在固定床反应器上进行SCR脱硝性能测试,实验台示意图见图1。反应温度为150~300 ℃。每次测试中催化剂填充量为2 mL,相应的反应空速(GHSV)为30000 h-1。模拟烟气中包含500 ppm NO,500 ppm NH3,5vol% O2,N2为平衡气体。青岛众瑞烟气分析仪(ZR-3200)用来分析出口烟气中NO和NO2的浓度。在各个温度下,待反应达到平稳状态之后开始记录反应数据。SCR反应中NO转化率公式如下所示:
(1)


图1 SCR实验台示意图Fig.1 Schematic diagram of the analyzer bed for SCR

图2 CuBTC和Mn-Cu-BTC/x催化剂样品的XRD图谱Fig.2 XRD patterns of CuBTC andMn-Cu-BTC/xcatalysts
3 结果与讨论
3.1 XRD分析
图2为所制备催化剂CuBTC和Mn-Cu-BTC/x(x=0.01~0.2)的XRD图谱。由图可见,所制备的CuBTC及Mn-Cu-BTC样品在2θ=5.9°(111)、 6.8°(200),9.5°(220)、 11.7°(222)、 13.5°(400)、14.7°(331)、16.5°(422)、17.6°(511)和19.1°(440)位置呈现典型的特征峰,这些特征峰与之前文献报道的标准图谱一致吻合,证明所制备的样品具有完整的晶体结构。但是随着样品中Mn离子量的逐渐增多,样品的衍射峰强度减弱,样品的结晶程度也逐渐减弱,这也证明了Cu-Mn离子之间存在着相互作用从而使得样品向无定形态转变。在Mn-Cu-BTC/x系列样品中在41.5°和42.6°出现两个微弱的Mn3O4特征峰,这也进一步证明了Mn离子成功的引入到了CuBTC晶体之中。
3.2 热稳定性分析
所制备的不同催化剂样品的TG曲线如图3所示。可以看出所制备的催化剂样品热稳定性相似,升温过程中存在着3个失重阶梯。升温到130 ℃时,CuBTC样品约有10%的质量损失,Mn-Cu-BTC/0.25样品质量损失约为13%,这归因于催化剂样品表面的吸附水以及孔道内残留的乙醇分子。在130 ℃到265 ℃区间为第二个失重台阶,此时CuBTC和Mn-Cu-BTC/0.25样品质量损失分别为5%和2%,这主要是由于催化剂样品内部与Cu结合的水分子的移除。在此温度范围内大量的Cu活性位点暴露出来,此时催化剂的SCR反应活性最佳。在265 ℃到300 ℃范围内为第三个失重台阶,此时有机骨架开始逐渐分解。最后在300 ℃以上时催化剂样品剧烈失重,对应着样品内部的结晶有机材料的分解,因此在300 ℃以上时催化剂样品的SCR活性剧烈下降。
3.3 N2物理吸附结果分析
所制备的催化剂样品是一种多孔材料,拥有比较大的比表面积和丰富的孔道结构,同时众多研究表明在NH3-SCR反应中催化剂的比表面积和孔道结构对催化效率具有重要影响[15-16]。CuBTC和Mn-Cu-BTC/0.25样品的氮气吸附脱附等温线如图4所示。有图可见,所制备的样品均属于LangmuirⅠ型吸附等温线,意味着在低压区,随着相对压力升高,氮气吸附量急剧增加,当相对压力增大到一定程度之后,随着相对压力的继续增加,氮气吸附量增加的趋势大幅降低。同时可以发现,CuBTC样品的氮气吸附量远高于Mn-Cu-BTC/x材料。但是一步合成法制备的Mn-Cu-BTC样品的等温线出现了很小的回环,表现出了介孔的性质。通过BET方程计算得到所制备催化剂的比表面积,依据BJH模型分析确定其比孔容和孔径,所得结果总结于表1。CuBTC样品表现出了最大的BET比表面积为1460 m2/g,随着Mn离子引入量的的增加,样品的比表面积呈现下降的趋势。但是所制备的样品的平均孔径有所增加。

图3 CuBTC和Mn-Cu-BTC/0.25催化剂样品的TG曲线Fig.3 TG curves of CuBTC andMn-Cu-BTC/0.25 catalysts samples
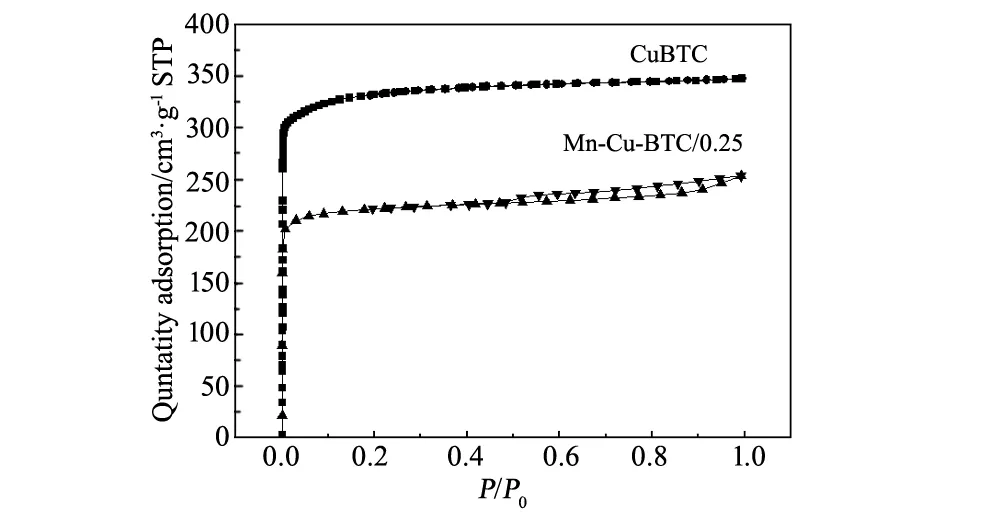
图4 CuBTC和Mn-Cu-BTC/0.25催化剂样品的氮气吸附脱附等温曲线Fig.4 Nitrogen adsorption/desorption isothermsof the CuBTC and Mn-Cu-BTC/0.25 catalysts samples

表1 CuBTC和Mn-Cu-BTC/x催化剂样品的N2吸附测试Table 1 N2adsorption-desorption of CuBTC and Mn-Cu-BTC/xcatalysts samples
3.4 SEM分析
CuBTC和Mn-Cu-BTC/0.25样品的SEM照片如图5所示。所制备的CuBTC样品呈现完整的八面体晶体结构,在晶体表面有孔道结构存在。由一步合成法制备的Mn-Cu-BTC/0.25 样品中,Mn与BTC结合呈现微小的球状,均匀分布在CuBTC的表面。由图5c可见所形成的Mn-BTC结构类似于花瓣状,其存在也为NH3-SCR反应中提供了大量的不饱和金属位点,进一步提高了催化剂的低温反应活性。

图5 所制备催化剂样品的SEM照片(a)CuBTC ×2000倍;(b)Mn-Cu-BTC/0.25 ×2000倍;(c)Mn-Cu-BTC/0.25 ×8000倍Fig.5 SEM images of the as-synthesized samples (a)CuBTC; (b)Mn-Cu-BTC/0.25 ×2000;(c)Mn-Cu-BTC/0.25 ×8000
3.5 SCR脱硝性能分析

图6 CuBTC和Mn-Cu-BTC/x催化剂在不同温度下的NO转化效率;反应条件:500ppm NO,500ppm NH3,5vol% O2,N2为平衡气,GHSV=30000 h-1Fig 6 NO conversion efficiency for CuBTC and Mn-Cu-BTC/x catalysts at different temperatures. Reaction conditions:500ppm NO, 500ppm NH3, 5vol% O2, and N2balance, GHSV=30000 h-1
图6为一步合成法制备的Mn-Cu-BTC/x催化剂样品作为低温NH3-SCR脱硝反应催化剂时,NOx浓度随着温度的变化曲线。对于所有的催化剂样品来说,NO转化率在150 ℃以下时均相对较低,然而当温度升高到150~220 ℃范围内时NO转化率呈指数式增长。NO转化率在220~260 ℃内达到了最高值接近94%。随着反应温度继续增加,由于有机骨架的分解导致NO转化率急剧下降,这一结果也与TG测试结果一致。在CuBTC材料中,两个Cu离子簇与4个羧基集团共价结合,形成了浆轮状的结构。其中Cu2+之间以微弱的键位相连,剩余轴向的配位空隙中被微弱的水分子键所充满。在适宜的热处理温度下,水分子很容易被移除进而产生大量的Lewis酸性位和不饱和的Cu活性位点暴露出来,因此提升NH3-SCR反应活性[17]。在150 ℃以下时较低的NO转化率是由于不饱和Cu活性位点没有形成。由于Mn离子引入到催化剂中,Mn离子也提供了大量的活性位点以及适宜的孔径结构,因此催化剂的NH3-SCR反应温度得以进一步降低。
4 结 论
采用一步合成法成功的制备出Mn-Cu-BTC催化剂。通过优化Mn/Cu的质量比例,催化剂样品的孔径结构被精细的控制。与CuBTC催化剂相比,在200 ℃下,催化剂Mn-Cu-BTC/1较Cu-BTC的NO转化率提升了接近30%;在220~260 ℃范围内,催化剂Mn-Cu-BTC/0.25较Cu-BTC的NO转化率提升了大约20%,Mn-Cu-BTC/0.25样品的转化率达到94%。获得如此优越的NH3-SCR脱硝性能主要由适合的孔径尺寸、适当的铜锰离子摩尔比、催化剂中Mn和Cu离子协同效应而共同决定的。
