组合类和固态电解质锂空气电池的研究进展
2019-05-07许林成郝占忠
许林成,郝占忠
(内蒙古科技大学 包头师范学院 化学学院,内蒙古 包头 014000)
逐年递增的原油消耗加快了全球变暖,不符合可持续发展的理念;为实现绿色能源的全面发展,探索新型可再生能源已成为当前的主要研究方向。以二次电池作为能量来源,满足绿色环保的性能需求,且结构简单利于循环使用,在生活中发挥很大优势。具有最负电极电位的锂金属[1],和空气(氧气)组成的电池,在同等条件下全包装后能量密度(600 Wh/kg[2])接近于化石燃料的燃烧值(700 Wh/kg)[3],因而作为研究重点。但锂氧电池目前的能量密度和稳定性与这些理论值相距甚远,电子转移和传质效率的限制和放电/充电过程中不可预测的副反应,是导致锂空气电池电化学反应迟滞和不可持续的主要原因[4]。电解质作为两极之间离子的导电路径,又是溶解和释放反应产物的“场所”,与上述因素密切相关。就电解质体系而言,锂空气电池分的四类:水系、非水系、有机-水系以及固态。水系电解液是最早被研究的电解质,由于水与阳极接触产生氢气,且间歇循环过程中的稳定性差等,而限制的发展[5]。目前锂空气电池常用电解质为非水系[6],又分为有机电解液和离子液体,有机电解液易挥发,不能保证空气阴极化学反应和电化学过程的稳定性,难以提供实际意义上锂氧化物溶解度和足够高的氧气传输能力;而离子液体宽温度范围、不易挥发、较大的极性可调控行为成近年来的研究热点,但由于氧溶解度有限,反应物迁移率低,性能也有待提高[7]。
组合(有机混合、有机-水、固态混合)电解质选用有利两极的不同溶剂提高离子的传输导体,同时增加介电常数减缓不可逆产物的沉积量,进而显著改善电池性能。固体电解质则通过两相紧密接触防止外界因素的干扰,且一定的机械强度避免枝晶的穿透。但该新型电解质的出现也引入其他不利因素;对该系列锂空气电池进行总结和分析,为进一步设计优化电解质提供依据。
1 有机混合液

各类有机电解液存在的不足,使研究转向两种及以上单一液相电解液的混合,组合各成分的优点,能够呈现协同效应[2]。Xu等[17]混合了PC(propylene carbonate)和EC(ethylene carbonate)溶剂体系,研究表明该体系在PC/EC的质量比7∶3~2∶8及LiTFSI(bistrifluoromethanesulfonimide lithium salt)的浓度0.7~1.0 mol/L范围内具有较为平坦的最大放电容量,而且有利于电池的稳定性。有机混合电解质在一定程度上改善了电池的稳定性,但限制有机混合电解质性能的另一因素——金属锂枝晶,同样有待进一步解决。常用聚烯烃类添加剂[18]的有助于表面生成SEI膜,但同时溶液的润湿性差,阻止了金属锂的充放电反应。Zheng等[19]在常用的碳酸盐基电解质中加入三嵌段聚醚(Pluronic P123)作为添加剂,结果表明,在电解质中加入0.2%~1%(按重量计)P123可以有效地提高电解质的润湿性(如图1),同时,P123在锂金属表面的吸附生成人工固体电解质界面层,抑制锂枝晶的生长,起到双功能作用。在大电流密度为1.0,3.0 mA/cm2时具有较长的循环稳定性(如图2)。



图2 不含和含P123的电解质中以0.1 mA/cm2放电时锂在Cu衬底上沉积15 h的电压-时间曲线[19]Fig.2 Voltage-time curve of lithium deposited on Cusubstrate at 0.1 mA/cm2 discharge in electrolytenot containing and containing P123 for 15 h

通过有机类电解质的混合,实现离子电导率和电化学稳定性的提高,并在一定程度上降低不可逆放电产物(过氧化锂、氧化锂等)的堆积,改善电池的性能。但仍存在电解质稳定性差,与反应中间体作用生成沉淀,且多种溶液的混合可能增大了黏度,使传质受阻,从而降低反应速率。因此,针对这些限制因素选择合适功能化添加剂,在不影响自身平衡的情况下弥补缺陷,提高电池性能。
2 有机-水混合液
为了有效溶解产生的放电产物,开发新型有机-水锂空气电池(工作示意图见图3),有机和水系电解质分别位于锂阳极和空气阴极一侧;但需用能通过Li+的隔膜隔开,避免混合后的副反应发生。理想隔膜保证Li+通过性,同时又能阻止H2O和CO2进入;一定的机械强度,而又与两种电解质有较好的相容性[6],因此采用含锂型隔膜。
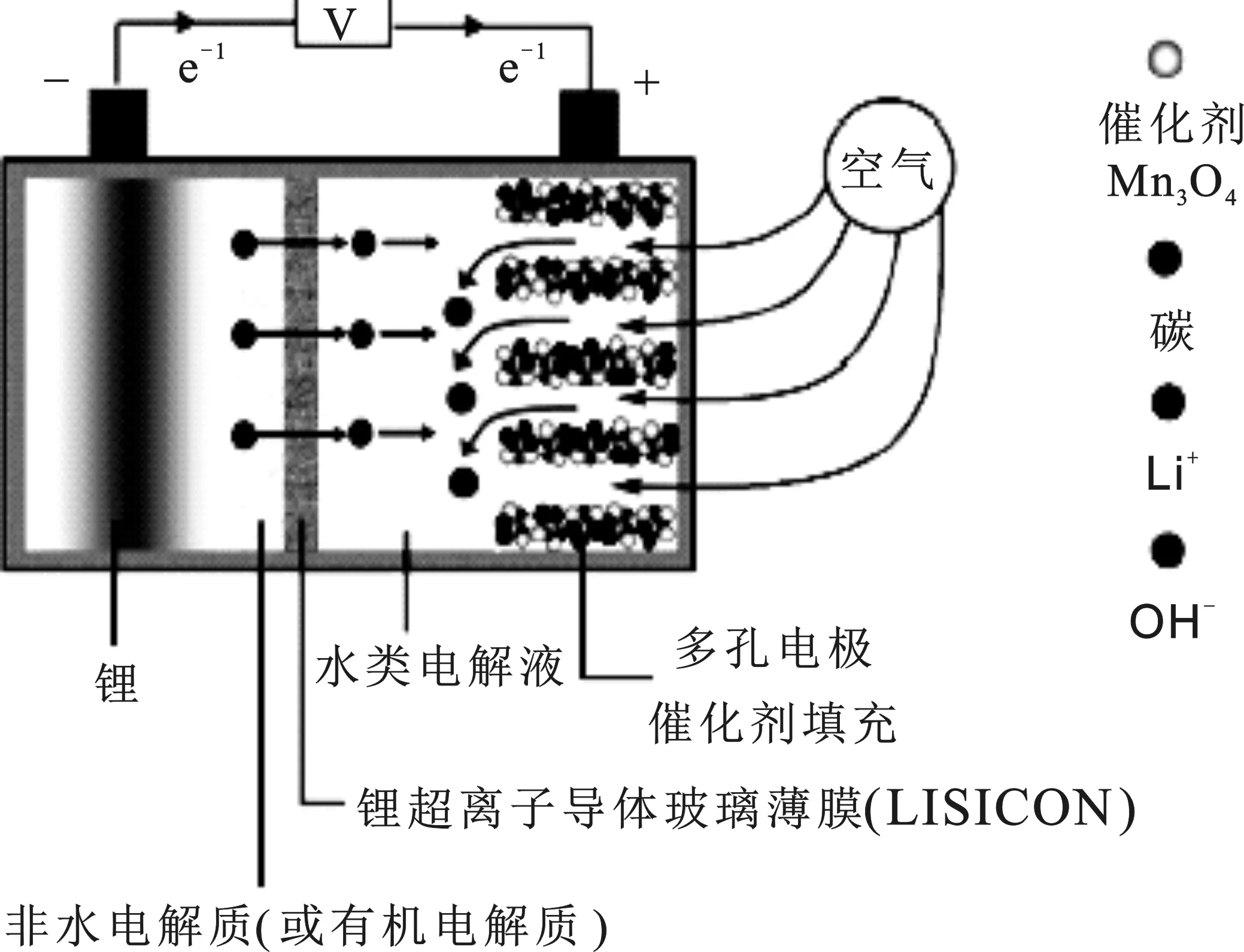
图3 有机-水电解质锂空气电池工作示意图[23]Fig.3 Working diagram of organic-waterelectrolyte lithium air battery
Wang等[23]首先提出了有机-水组合电解质型锂-空气电池,设计为金属锂阳极直接接触1 mol/L LiClO4/EC+ DMC有机电解质,阴极直接接触的是LiOH水溶液,两相之间以LISICON(Li14ZnGeO4)隔开。该体系放电时,金属锂被氧化生成锂离子溶解在有机电解质中(1),氧气则在LiOH溶液中发生还原生成OH-(2)。
负极:Li-e-→Li+(-3.04 V vs.SHE)
(1)
正极:O2+2H2O+4e-→4OH-(0.40 V vs.SHE)
(2)
充放电测试显示,电极总质量一定时,该电池可以持续放电500 h以上,比容量可达50 000 m Ah/g(放电曲线如图4)。研究结果表明,氧气在该体系的空气阴极上还原成可溶于水的LiOH,避免有机体系的放电产物堵塞电极微孔。但充电时常温常压下达到LiOH 5.25 mol/L[24]的溶解度后产生沉淀,直接降低电池的能量密度;若再对沉淀加水溶解或循环分离,则造成装置复杂[25]。He等[26]提出了从水电解质中分离LiOH放电产物的循环运行模型(如图5),该模型可以分离的LiOH,且有望提取锂金属并进行再利用。更进一步的研究显示[27],LiOH浓度的大小对电池功率密度影响很小,当功率密度达到最大时,LiOH的浓度达到0.5 mol/L。
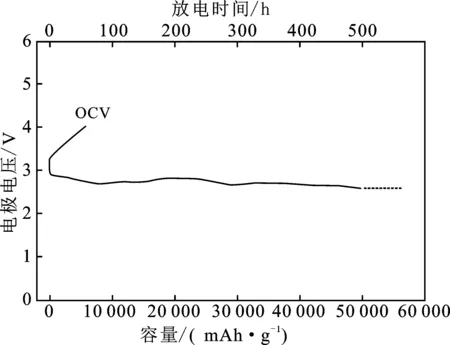
图4 组合电解质锂空气电池长时间放电曲线[23]Fig.4 Combined electrolyte lithium air batterylong time discharge curve

图5 含能量转换单元和产品回收单元锂-空气电池系统的原理图[26]Fig.5 Schematic diagram of lithium-air battery system withenergy conversion unit and product recovery unit
同时电解质隔离膜的稳定性,是限制电池性能另一关键因素,Wang等[23]又将水相电解质一端用阳离子交换膜分隔成两室,靠近隔板一侧用LiNO3溶液,空气电极一侧则填充LiOH溶液,利用这类装置可以富集和回收放电产物LiOH。该设计又能有效防止OH-对LISICON的腐蚀,进而提高锂空气电池的能量密度[27-28]。Zhang等[29]则考虑把LiOAc饱和溶解在90%(体积百分数)的HOAc溶液中,制备一个缓冲阴极;结果显示,该电池中使用的LISICON板在缓冲溶液中是稳定的。这种新型电池保持可充电能力为250 mAh/g,可以提供400 Wh/kg以上的特殊能量密度,这比传统的石墨/LiCoO2电池优越(见图6)。

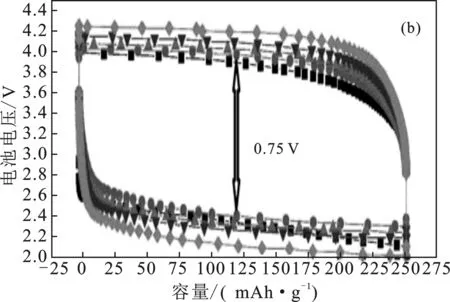
图6 使用缓冲溶剂有机-水锂空气电池充放电曲线[28]Fig.6 Charge-discharge curves of organic water lithiumair batteries using buffer solvents cycle 5; cycle 15
有机-水电解质的应用,使金属锂阳极与水直接接触的危险得到抑制,又可以避免一定阴极不溶放电产物生成,因此该体系的连续放电时间远远高于有机型锂-空气电池。而且空气中除氧气以外的其他组分(如 H2O 等)不会对该体系造成显著影响,故与单一有机体系相比,电池的反应机理变得更加简单。但该类电池体系仍过于复杂(有机相电解质产生的不溶放电产物,需特殊装置溶解[25-26]),有待进一步研究。
3 固态电解质
液态电解质存在的漏液、容量低、副产物多等诸多问题,难以满足锂空气电池的长远发展。采用致密的固体电解质可以避免空气与金属阳极接触,一定的机械强度又避免枝晶的穿透。目前,用于锂空气电池的固态电解质为:无机固态以及高分子聚合物电解质。
3.1 无机(陶瓷)固态电解质
常用无机固态电解质是NASICON结构的Li1+xAlyGe2-y(PO4)3(LAGP)或Li1+x+yAlxTi2-x(PO4)3(LATP),室温下该锂离子导体具有较高电导率(LAGP:5.08×10-3S/cm[30];LATP:7×10-4S/cm[31]),且低温烧结能够形成致密的陶瓷电解质。王章俊等[32]以Li7La3Zr2O12材料为固体电解质,样品在850 ℃下即可生成标准立方相石榴石结构,可用于阻止氧气等向阳极处扩散,同时两者的接触也有助于减少界面传输电荷的电阻。但样品在1 350 ℃高温下煅烧,会造成锂的流失,转变为La2Zr2O7。若使电池保持较好的倍率性能和循环性能,后期可以通过补锂重新转回Li6.6La3Zr1.6Ta0.4O12,以稳定锂离子较高电导率。Kitaura等[33]以LAGP为无机固态电解质,在2.0~4.2 V (vs.Li/Li+)电压范围内,500 mA/g的电流密度下首次放电容量和充放电容量达到1 700 mAh/g和900 mAh/g(见图7)。观察到在3.1 V(vs.Li)附近的电化学氧化还原电位,表明电池中Li2O2的形成和分解。此外,在低电流密度下,充放电曲线之间的总极化为0.2 V(如图8),证明使用稳定的固体电解质可以改善在有机液体电解槽中的大极化。同时研究发现,该类电解质出现与锂金属直接接触把Ge4+、Ti4+还原而致失效的缺点。为了减缓固体电解质与锂阳极之间的反应,加入过渡层——聚合物导电膜,但也带来了界面电阻增大和耐氧化性变差两方面影响,同样降低电池效率[34]。

图7 500 mA/g的电流密度下电池首次充放电容量[30]Fig.7 500 mA/g initial charge-discharge capacity of thebattery at current density

图8 10 mA/g电流密度下电池充放电曲线[30]Fig.8 10 mA/g current density cell charge-discharge curve
针对上述因素,Kumar等[35-36]以Li2O和氮化硼(BN)为掺杂剂的聚合物陶瓷(PC)材料,作为阳极电荷转移反应催化剂、SEI稳定剂和良好的锂离子传输介质,适合于电池阻抗降低和与金属锂的电化学相容性。在锂金属与气相色谱板之间掺杂Li2O的聚合物电解质阻止了锂与气相色谱的反应,而氮化硼(BN)聚合物在气相色谱与复合空气阴极之间增强了接触,防止了水分和CO2,但电池内阻还是有所增加。而Zhang等[37]采用陶瓷电解质和由单壁碳纳米管和1-乙基-3-甲基咪唑双(三氟甲基磺酰基)酰亚胺组成的交联网络凝胶(CNG)空气阴极,将电解质与电极之间的界面电阻成功降低。使该电极具有优越的电子、离子和氧的三维连续通道,使三相阴极反应不依赖于液体电解质的渗透,放电容量和充电容量分别达到56 800 mAh/g和53 900 mAh/g。
3.2 固体聚合物电解质
聚合物电解质之所以成为近年研究的重点,是因其安全性能高、稳定性好和易加工的特点。固体聚合物电解质一般是通过将锂盐分散到聚丙烯腈(PAN)、聚碳酸醚(PCE)、聚环氧乙烷(PEO)或PVdF-HFP等聚合物基体中制备的。Scrosati等[38]制备了一种不含阴极催化剂,由PEO、ZrO2和LiCF3SO3组成的固体电解质。组装后的电池,过电位间隙为400 mV,远低于液相电解质锂空气电池,但电池的功率密度未超过20 μA/cm2相对较低,这主要是由于PEO在室温下离子电导率低所致。因此,离子电导率是影响固体聚合物类锂空气电池性能的关键因素,而阴极与电解质接触界面产生降解过程[4]又是导致离子电导率较低的主要原因。
EIN-Eli等[39]合成了一种类似的PEO基固体聚合物电解质,应用于含有阴极催化剂的锂空气电池中。在80 ℃下,与乙二醇二甲醚为基础的液体电解质电池相比,该类电池放电电压提高了80 mV,充电电压降低了400 mV。当以0.1 mA/cm2电流密度放电时,电池的放电比容量为1 481 mAh/g;在0.2 mA/cm2电流密度下放电时,电池在40周循环后,仍保持稳定。Lu等[40]制备了一种LiBF4盐溶于PCE基的电解质,由于聚合物玻璃化温度低,使电解质具有较高离子电导率(1.57 mS/cm)。0.1 mA/cm2电流密度下放电时,电池的容量为2 200 mAh/g,同等条件下接近于TEGDME/LiBF4的电池容量(2 600 mAh/g)。故合适的阴极催化剂和聚合材料可以避免聚合物的降解,提高电池的离子电导率,维持稳定的电池充放电容量。
3.3 固体混合电解质
同样采用多种电解质的复合,结合不同固态电解质的优点,综合实现所需的力学性能、稳定性等。因此无机固体和高分子聚合物的复合,高分子聚合物和氧化物纳米粉体(如 SiO2)以及液态电解质(如吡咯基离子液体PYR14TFSI)的复合等[41-44]也开始被研究。最近,Kumar等[45]报道了一种三层结构的陶瓷层-聚合物层-陶瓷层固体电解质隔膜,通过电子线蒸发沉积技术将LAGP包覆在聚乙烯(PE)膜的两面,形成 LAGP-PE-LAGP 结构。这种复合电解质隔膜和锂金属接触后界面阻抗较低,室温下在1.3 mA/cm2的电流密度下对锂金属进行充放电循环,极化较低。但是这种隔膜在使用前需要在含有锂盐的电解质中浸润,其表现出的对锂金属的稳定性不确定是否与浸润的电解质有关,具体的性能有待进一步研究,不能说是真正的固态电解质。
综上所述,固态电解质锂空气电池仍处于研究阶段,这种电池具有在中等和高温下运行的潜力,是作为电动汽车动力电池的应用优势。但液态水系和非水系的锂离子电导率比固体电解质高,锂阳极、空气阴极在电池组装过程中与固态电解质接触时,界面阻抗大,能量消耗高。因此,抗氧化性优异(能抵御氧自由基和LiOx等的氧化)、界面电阻低、又耐非氧组分(如水气、CO2)侵蚀等是固态电解质用于锂空气电池必须具有的特性[46]。
4 结论与展望
高理论比能量的锂空气电池,是人们迫切需要的能源装置,如果能实现商业化,可有效缓解能源匮乏和污染问题。相同条件下,组合类和固态电解质是获得高效稳定性能电池的较好选择,但仍有较多弊端需克服:
(1)明确电池可逆循环工作机制。目前对于电极和电解质内部、界面以及“双电层”之间反应产物生长、演变和溶解的相关机制还不够明确。除此之外,外界因素引起的副反应对电池反应机理的影响程度,如何使副产物有效分解等规律是首要探究内容。
(2)补锂。电解质多次运行过程中产生的一些不可逆锂盐,以及高温下无机固体电解质锂的流失,造成电池逐渐终止。有效的补锂方法可以保持较高的离子导电率,从而使电池长期循环。
(3)电池的性能。针对不同体系电解质在锂空气电池中的应用,探明限制电池性能的关键因素,据此在不破坏原平衡的基础上,提出相应的解决方案(如催化剂、增塑剂、导电剂等),使电池倍率性能和循环性能得到显著提高。
