反复气胸伴双肺弥漫性囊性病变1例
2019-04-27孙宛君高梦茹费广茹胡晓文
孙宛君 高梦茹 费广茹 韦 炜 胡晓文
Birt-Hogg-Dubé综合征(Birt-Hogg-Dubé syndrome, BHDS)是一种罕见的常染色体显性遗传的单基因疾病,主要表现包括皮肤纤维性脂肪瘤,多发性肺部囊性病变、复发性气胸和肾细胞癌[1]。肺部囊性病变是BHDS常见的表现,在高达85%的患者中可见,临床上易与其他囊性肺病如肺淋巴管肌瘤病(lymphangioleiomyomatosis, LAM)等混淆[2]。尤其当患者缺乏特征性皮损或肾脏疾病时,常常会发生漏诊甚至误诊。现报道一例延误诊断半年的BHDS,以提高认识。
临床资料
患者女,45岁,农民。因“突发胸闷伴左侧背部针刺样疼痛1周”于2016年5月7日就诊于当地医院,入院前1周提重物后突然起病,病程中无咯血、发热等症状,辅助检查:胸片示左侧气胸。予左侧胸腔闭式引流后症状缓解,复查胸部CT示左侧肺复张,左侧见多发囊腔,右侧可见少量气胸,予拔除胸腔引流管。2016年5月16日患者无诱因下再次出现胸闷,胸部CT示右侧气胸,双肺弥漫性囊性病变,见图1,给予右侧胸腔闭式引流术后患者胸闷症状缓解。其后1个月内患者两次发生右侧气胸,均经胸腔闭式引流后缓解。2016年7月12日患者因右侧气胸复发,外院诊断考虑肺淋巴管肌瘤病可能,行胸膜摩擦固定术和电视辅助胸腔镜下楔形切除术,术中见右肺较大肺大泡,病理结果回报示右肺中叶、右肺尖、右下叶内外后侧基底段肺大泡,肺组织显慢性炎,部分肺泡扩张、肺间隔断裂,肺泡腔融合,纤维组织增生。病理结果排除淋巴管肌瘤病,但未能明确气胸病因。2016年11月2日患者因反复气胸原因未明于我院就诊,复查胸部CT双肺见弥漫性囊性病变,大小不一,以双肺基底部多见,见图2。患者既往体健,否认任何基础疾病、过敏史,无吸烟史或接触刺激性气体,病程中完善多项辅助检查:风湿、肿瘤和免疫指标阴性,头颅MRI和腹盆腔CT、超声心动图未见异常。追问病史,患者母亲有左侧反复气胸病史,一位舅舅有左侧气胸病史,其哥哥和子女未见明显异常,见图3。鉴于患者中年女性,气胸反复发作,结合胸部影像学弥漫性囊性病变和气胸家族史,考虑罕见病BHD,行血液基因检测FLCN突变阳性,其基因突变为c.1165G>T,患者最终确诊为BHDS。本例患者行胸膜固定术后随访2年气胸未再发生,肺功能检查基本正常,复查胸部CT示无明显变化。经检查,本例患者并无皮肤和肾脏受累。
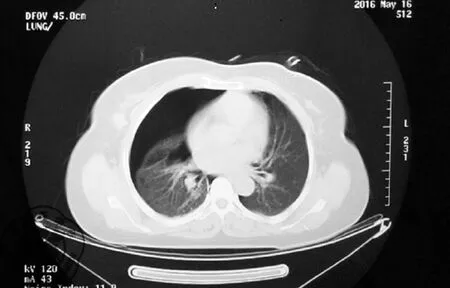
图1 2016年5月16日胸部CT示右侧气胸,双肺多发囊性病变
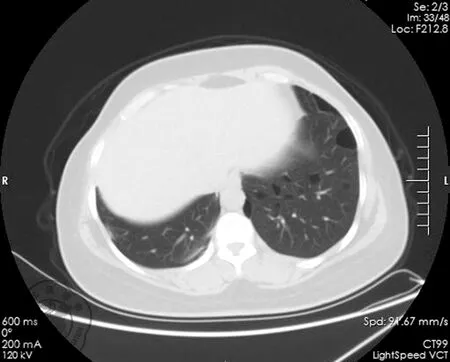
图2 2016年11月2日胸部CT示双肺散在多发囊性病变
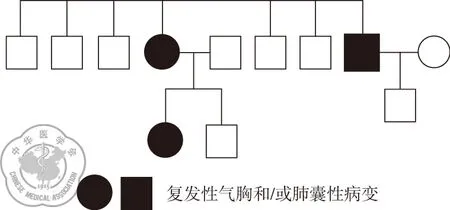
图3 患者家族遗传谱中母亲左侧复发气胸及舅舅左侧气胸病史
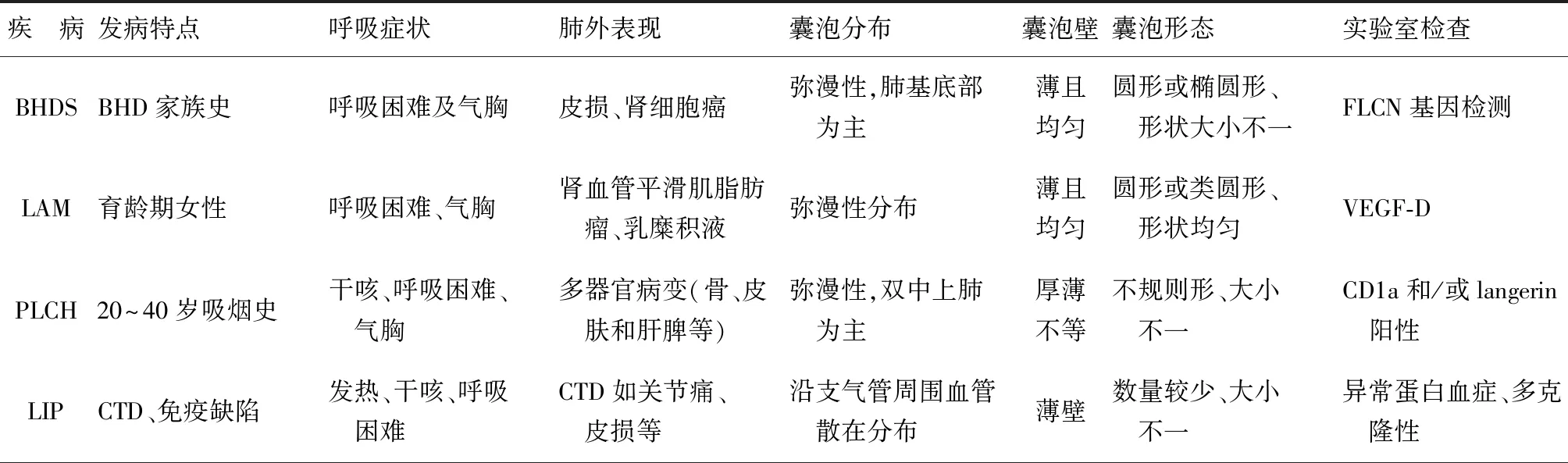
表1 弥漫性囊性肺病临床和影像学特点
注:BHDS:Birt-Hogg-Dubé综合征;CTD:结缔组织病;LAM:淋巴管平滑肌瘤病;PLCH:肺朗格汉斯细胞组织细胞增生症;LIP:淋巴细胞性间质性肺炎;VEGF-D:血管内皮生长因子-D
讨 论
BHDS由三位加拿大医生Birt、Hogg和Dubé等于1977年首次报道[3]。截至2017年,根据BHD基金会统计的文献数据,全世界超过600个家系诊断有BHDS。其中,报道确诊BHDS的患者大多来自欧美,约占3/4,其次为亚洲约占1/4,在报道的亚洲患者中又以日本占大多数(73%)。最新一项研究报道2014年至2017年确诊27例BHDS,显示国内仍较为罕见[4]。
BHDS是一种常染色体显性遗传病,2001年首次发现BHD相关基因位于染色体17p11.2上,随后研究发现在BHDS患者FLCN基因突变失活,FLCN基因编码的卵泡蛋白在皮肤、肺泡上皮和肾单位表达,具有肿瘤抑制作用[5-7]。2016年2月全世界已发现183种不同的FLCN突变,包括插入,缺失,错义和无义突变。2017年来自中国BHDS患者FLCN基因突变筛查报告在27例确诊患者中发现14个新突变,提示中国BHDS患者可能有不同于欧美患者的突变位点[4]。
BHDS常见三联表现包括皮肤异常病变、肾脏恶性肿瘤和肺部病变,Tong等[8]发现BHDS患者通常在20~30岁出现多发的白色小丘疹,主要分布在面部和颈部。Murakami等[9]回顾总结62例亚洲BHDS患者,发现亚洲患者发生皮肤病变不足1/3。BHDS患者肾脏病变可发展为肾细胞癌,严重威胁生命,包括嫌色细胞癌、透明细胞癌和混合型等多种组织病理学,BHDS患者患肾癌的风险可能在15%~30%[10-12]。本例未发现肾脏病变,建议成年患者每年定期行影像学检测以尽早发现肾脏恶性肿瘤[1]。
肺部病变是BHDS患者最常见的表现之一,Gupta等[2]研究发现104例患者中85%的BHDS患者发现肺部囊性病变,与Murakami等[9]回顾性分析亚洲BHDS患者结果相近。BHDS患者囊性病变对其肺功能通常无显著影响,即使胸部CT表现为多发囊性病变,但BHDS患者可能无胸闷和呼吸困难等表现,肺功能结果对BHDS诊断意义不大[13]。胸部HRCT可协助诊断BHDS,其特点如下[14]:①双侧多发的圆形或椭圆形囊状阴影,形状大小不一;②可见囊壁,薄且均匀;③弥漫性分布,以肺基底部为主;④受累部分肺实质基本正常,部分可能发生气胸,不伴有肺结节和磨玻璃影。本例患者影像学上主要表现为反复发作的气胸,双肺散在分布的多发囊状阴影,以圆形或类圆形为主,大小不一,壁薄且均匀,主要分布在双肺基底部,高度符合上述特点。BHDS胸部CT常表现为弥漫性囊性病变,其作为重要诊断线索之一,需与其他肺部弥漫性囊性病变相鉴别[15-16],见表1。
Gupta等[2]报道BHDS患者发生自发性气胸风险为76%,其中超过一半的气胸患者出现复发,平均首次发病年龄为36.5岁。自发性气胸患者的研究结果示BHDS导致的气胸占5%~10%,且大多数患者无皮肤病变或肾细胞癌[17-18]。在后续调查中,研究者发现4例患者有气胸家族史。气胸家族史是有别于其他肺部囊性的重要线索之一。Murakami等[9]发现仅有不到5%的亚洲BHDS患者出现所有3种症状。本例患者以气胸为首发表现,有气胸家族史,通过查体和腹部CT也未发现皮疹和肾细胞癌。所以,有气胸家族史的患者出现肺部弥漫性囊性病变,即使无皮疹和肾细胞癌等提示性肺外表现,仍需高度怀疑BHDS。
治疗:除了肾癌的常规筛查,主要为气胸的处理。对于气胸首次发作且未确诊的患者,若症状较重且影像学提示肺压缩面积>30%,通常采取胸腔穿刺抽气或闭式引流等保守治疗[19]。由于BHDS引起的气胸复发率高,需尽早采用胸膜固定术或胸腔镜手术治疗。相对内科保守治疗,胸膜固定术可显著降低气胸复发的风险[2]。胸膜覆盖技术是一种用于治疗气胸并减少其复发的新手术方法。Ebana 等[20]报道了1例BHDS复发性气胸患者在胸腔镜下成功应用胸膜覆盖技术治疗气胸。然而目前这项技术尚未完全成熟,仍缺乏相应数据支持。本例术前3个月内共发生4次气胸,胸膜固定术后随访2年气胸未再复发。
从本例患者诊治过程中得到的启示: ①对于反复自发性气胸患者,应及时完善胸部HRCT检查;②病因不明的反复气胸伴双肺弥漫性囊性病变患者,临床医师不能忽视询问家族史;③疑似BHDS的患者应接受FLCN基因检测。
