老年高血压病人外周血TLR4表达与血压昼夜节律的关系探讨
2019-04-17,,,,
,, ,,
高血压作为全球常见的慢性病一直被认为是导致心脑血管事件甚至死亡的最主要危险因素之一[1]。近年来随着对高血压发病机制研究的深入,认为慢性炎症和机体免疫功能的异常可能参与了高血压及其靶器官损害过程[2]。Toll样受体4(TLR4)是人类发现的第一个TOLL样受体(toll like receptors,TLRs)家族成员,目前研究表明TLR4可在血管平滑肌细胞(VSMCs)和内皮细胞等心血管相关细胞中表达,在心血管炎症病理发展过程中发挥了重要作用[3]。本研究旨在观察老年高血压病人外周血TLR4表达与血压昼夜节律的关系,从而探讨老年高血压靶器官损伤的机制。
1 资料与方法
1.1 研究对象 纳入2018年1月—2018年10月在我院门诊和老年病科住院的未经正规治疗的老年高血压病人80例, 年龄≥60岁。所有入选病例均采用 1999 年世界卫生组织(WHO)/国际高血压学会(ISH )高血压诊断标准。同时选取血压正常、年龄≥60岁的老年人30名作为对照组。所有入选者均排除继发性高血压、血液病、糖尿病、恶性肿瘤, 严重心、脑、肺、肝、肾疾患和近期感染者。
1.2 研究方法
1.2.1 生化检测 所有病人于06:00~08:00采集空腹静脉血检测总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)等指标。所有化验均在山西医科大学第一医院检验中心完成。
1.2.2 动态血压监测 血压曲线分为杓形和非杓形, 夜间收缩压(SBP)和/或舒张压(DBP)下降10%~20%为正常杓型动态血压节律,否则为非杓型动态血压节律[4]。
1.2.3 流式细胞术检测TLR4 抽取新鲜的外周血100μL,加入红细胞裂解液1mL室温下孵育10min,1 500 r/min离心10~15 min后弃上清,用磷酸缓冲盐溶液(PBS)悬浮细胞调节浓度至1×106细胞/mL, 取100 μL 细胞悬液加入流式细胞管中,加入5 μL TLR4-FITC荧光抗体,同时设置阴性对照管(加入等量PBS)。充分混匀,室温避光孵育30~40 min,每管分别加1 mL PBS重悬,1 500 r /min离心 10 min,弃上清。 再次加入1 mL PBS重悬细胞重复离心后弃上清,加入 200 μL PBS 重悬细胞用流式细胞仪上机检测。

2 结 果
2.1 老年高血压组与对照组基础资料比较 两组在性别、体质指数、TC、TG、LDL-C、HDL-C方面比较差异无统计学意义(P>0.05);老年高血压组24 h、白昼、夜间收缩压(SBP)、舒张压(DBP)、脉压(PP)均明显高于对照组(P<0.05)。详见表1、表2。
注:两组各项比较P>0.05

表2 老年高血压组和对照组血压指标和TLR4表达比较(±s)
注:dSBP为白昼收缩压;dDBP为白昼舒张压;nSBP为夜间收缩压;nDBP为夜间舒张压;dPP为白昼脉压;nPP为夜间脉压;与对照组比较,1)P<0.05
2.2 老年高血压组与对照组TLR4表达比较 老年高血压组TLR4表达阳性率为(7.86±1.87)%,明显高于对照组的(5.16±1.48)%,两组比较差异有统计学意义(P<0.05)。详见表2。
2.3 非杓型高血压组与杓型高血压组一般资料和TLR4表达的比较 老年高血压组根据血压昼夜节律分为杓型高血压组和非杓型高血压组,两组在性别、体质指数、TC、TG、LDL-C、HDL-C方面比较差异无统计学意义(P>0.05); 非杓型高血压组TLR4表达的阳性率明显高于杓型高血压组,两组比较差异有统计学意义(P<0.05)。详见表3。
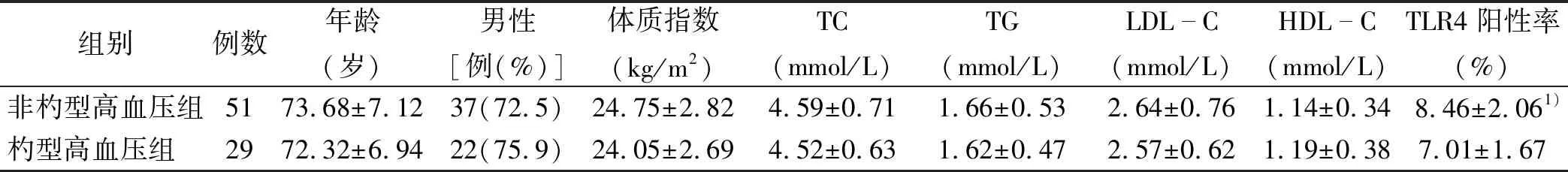
表3 非杓型高血压组、杓型高血压组及对照组一般资料和TLR4表达的比较
与杓型高血压组比较,1)P<0.05
3 讨 论
全球疾病负担研究(GBD2015)数据显示,在全球死亡率下降速度快于预期的基础上,心血管疾病所导致的死亡率却是增加的[1],其中高血压是心血管疾病最主要的危险因素[2],易导致心、脑、肾等靶器官损害,甚至诱发心脑血管事件的发生[5],严重威胁着人类健康。原发性高血压(EH)的发病机制尚不清楚,遗传、体液、环境及神经生物学机制等均参与了高血压的发生发展。新近研究认为,高血压病是一种慢性炎症性疾病,国内外文献均证实高血压的发生、发展及转归与炎症密切相关,而高血压的血流动力学异常又加重其炎症反应[6]。血管内存在多个炎症因子和炎症通路,而TLRs尤其是 TLR4 介导的炎症通路参与了高血压的病理过程[7],Marketou等[8]研究表明TLR4的激活与原发性高血压密切相关。本研究显示老年高血压组TLR4表达的阳性率明显高于对照组,说明TLR4信号转导通路及炎症机制可能参与了老年高血压的发生发展。
有研究证实,TLRs信号通路的激活可诱发高血压心肌重构和纤维化,导致心肌结构和功能的改变[9]。谭丽华等[10]发现高血压大鼠出现明显的左室肥厚时,伴有心肌TLR4、NF-κB、肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)等免疫炎症因子表达的增多,证实了免疫-炎症反应参与了高血压大鼠左室肥厚的发展。Bomfim等[11]通过对自发性高血压大鼠的研究发现,抑制TLR4可以直接降低血压,缓解血管异常收缩,认为抗TLR4药物对于直接控制血压有重要作用。张世魁等[12]研究表明高血压肾损害病人外周血单核细胞TLR4表达及血清TNF-α水平均明显升高,证实了TLR4信号通路天然免疫和炎症反应在高血压肾损害中的重要作用。总之,TLR4与高血压的靶器官损害密切相关,可能是高血压的独立危险因子。而老年高血压病人常伴有血压昼夜节律的异常,血压变异与靶器官损害、心脑血管事件及死亡率的相关性尤为密切。本研究结果显示非杓型老年高血压病人TLR4表达的阳性率明显高于杓型老年高血压病人,说明TLR4信号通路的过度激活和TLR4表达的增多可能是老年高血压病人血压节律异常导致靶器官损害明显的机制之一。
总之,TLR4 及其介导的炎症免疫反应与老年高血压病的发生发展密切相关[13]。TLR4可以通过炎症机制引起内皮功能紊乱及组织损伤,造成血管重构、心肌纤维化等,最终导致靶器官损害[14]。而干预TLR4的表达对于改善血压及相应的并发症可能有一定的疗效[15]。因此,研究TLR4在高血压发生发展及靶器官损害中的作用,可为高血压的治疗提供思路,以减少和预防心脑血管并发症的发生,从而达到长期改善高血压病人生活质量的最终目的。
