用于高效产氢的多功能Co-B催化剂
2019-04-11李佳璇王临才仲鸣慎
李佳璇,王临才,仲鸣慎
(上海第二工业大学 a.电子废弃物研究中心;b.上海电子废弃物资源化协同创新中心;c.资源循环科学与工程中心,上海201209)
0 引言
氢能是化石燃料的替代能源,可作为安全和清洁能源,为了满足其未来的巨大需求,实用和环保型产氢技术的需求显著增加[1]。碱性硼氢化物溶液水解(例如NaBH4,NH3BH3)和碱性水电解是两种不产生CO2的环保型制氢工艺且被广泛研究[2]。大部分研究集中在探索高效和低成本的催化剂上,可通过降低阴极上析氢反应(HER)和阳极析氧反应(OER)的过电位[3],来提高硼氢化物水解时的氢生成速率(HGR)。Co、Ni及其合金 (Co-P、Co-B[5-6]、Co-C-rGO[7]、Ni-B[8]、Co-Ni-P[9])等催化剂可用于水解反应,同时 Ni-B[10]、Co-B[11]、Co-Mo-B[12]、Ni-Co[13]、Co2B[14]、Co-Ni/MoS[15]2等催化剂也可用于水电解。Co-B已被证明是多功能催化剂,从而引起人们的广泛关注。其为化学稳定的化合物,具有多种组成形式,如:CoxB(x=1,2···)[16]。此类非贵金属基催化剂具有特殊的电磁特性,如磁性Co-B催化剂可以在使用后磁性分离[5]。其在水解反应以及电化学水分解反应中也表现出较高的催化活性[17-18]。
制备Co-B的常规方法为元素合成和还原金属氧化物两种,但合成温度较高使催化剂价格昂贵且具有挑战性[19-20]。在室温条件下,溶液沉淀法制备无定形钴硼合金的研究始于20世纪50年代[21],后来溶液沉淀法被证明是制备各种形态纳米级Co-B的简便和普遍的方法[22]。尽管溶液沉淀法在Co-B的组成调节方面也具有相当大的潜力,但所研究的大多数 Co-B,n(Co:B)约为 2[21-23]。
前期研究表明,制备Co-B的方法和反应溶剂对其催化活性起着决定性的作用,但仍然不明确。期望进一步研究,有助于开发出更有效的Co-B催化剂复合材料,替代贵重催化剂用于产氢技术中。
本文利用溶液沉淀法,在水(H2O),四氢呋喃(THF)及乙醇(C2H5OH)溶剂中,CoCl2与NaBH4简单反应,制得纳米Co-B催化剂。研究表明,Co-B在水解反应和电化学水解反应中的催化活性与Co-B的制备溶剂密切相关。
1 实验部分
1.1 材料
CoCl2·6H2O(AR) 和NaBH4(AR,98%) 购自Sigma-Aldrich。聚乙烯吡咯烷酮(PVP,AR),Naf i on(AR),C2H5OH(AR,99.5%),THF(AR,99.5%)和氢氧化钠(NaOH,AR)均购自Aladdin。H2O(DI,18.0 MΩ·cm)为超纯水。
1.2 催化剂的制备
在H2O、C2H5OH和THF 3种不同体系中通过化学还原法制备Co-B催化剂。将0.7138 g CoCl2·6H2O和0.3 g PVP加入100 mL烧瓶中,然后加入20 mL THF溶剂。室温搅拌1 h,将0.264 8 g NaBH4迅速滴加到烧瓶中,控制温度0℃,搅拌(450 r/min)反应2 h,反应完毕,将黑色沉淀用H2O和C2H5OH交叉洗涤3次以除去未反应的物质和可溶性副产物,收集制得的材料在70℃下干燥。采用上述同样的方法,制备H2O和C2H5OH体系的Co-B催化剂。
1.3 表征方法
电感耦合等离子体光谱仪(ICP,Perkin-Elmer Optima 5300)分析催化剂的化学组成。X射线衍射仪(XRD,D8-Advance,Cu Kα辐射,16 kW)和扫描电子显微镜(SEM,Hitachi S4800)分别研究Co-B的晶态和无定形结构。X射线光电子能谱(XPS)测定表面电子态,所有样品在纯氩(Ar)气氛中预处理以避免氧化。Co-B催化剂的磁性表征是在25℃下使用磁强计(MagLab-12,Oxford)进行的,并且样品的质量小于2 mg。利用CHI660D电化学分析仪(CH Instruments,Inc,上海)以标准三电极配置在1.0 mol/L KOH水溶液电解质中进行电化学测试。
1.4 Co-B用于NaBH4水解
Co-B用作NaBH4水解反应的催化剂。在室温下将0.01 g Co-B粉末置入试管中,然后用针管快速注入5 mL,含有质量分数5%的NaBH4和质量分数2%的NaOH的水溶液,产生的H2积聚在与气压计相连的倒梯度量筒中,计算HGR[L/(min·g)]和活化能(Ea,kJ/mol)。HGR的计算公式如下:
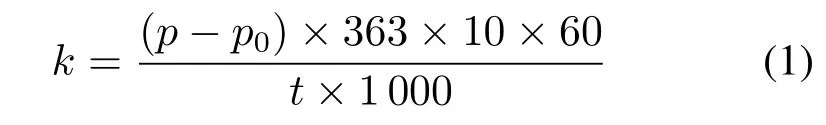
式中:k为HGR[L/(min·g)];p0和p分别为初始压力和总压力(Pa);t为催化时间(s);363为梯度量筒体积(mL)。
在不同的温度下测定NaBH4水解反应的Ea,且符合:
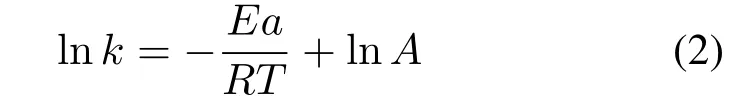
式中:T为绝对温度(K);A为预指数因子;R为常数 [8.314 J/(K·mol)]。
1.5 电化学测试
先制备Co-B在钛(Ti)箔上的工作电极(Co-B@Ti),将5 mg的Co-B催化剂粉末在975µL C2H5OH和25µL质量分数5%的Naf i on的混合物中制备催化剂溶液,超声处理30 min。取10µL该混合溶液移液至预先经过抛光和清洁的Ti箔(1 cm×1 cm)上以形成催化剂膜,并在65℃下干燥10 min,负载量为1.2 mg/cm2。在析氢和析氧测试之前,使H2和O2在1 mol/L KOH电解液中持续通气30 min,确保H2-H2O和O2-H2O平衡。然后,Co-B@Ti作为工作电极,石墨棒作为对电极,饱和甘汞电极(SCE)作为参比电极。同时,与商业性的Pt/C和IrO2做对比。Pt-C/Ti(1.2 mg/cm2)、IrO2/Ti(1.2 mg/cm2)电极与Co-B@Ti制备方法相同。电流都没有针对欧姆电位下降进行校正,使用以下等式将测量的电位校准至可逆氢电极(RHE):
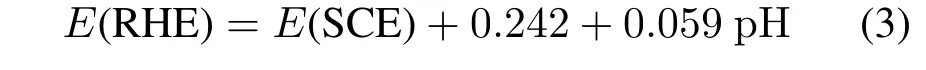
使用扫描速率为5 mV/s的线性扫描伏安法获得极化曲线。
2 结果与讨论
2.1 结构特点
Co-B催化剂是NaBH4分别在H2O、C2H5OH、THF溶剂中还原CoCl2所得到的,分别表示为 Co-B(H2O)、Co-B(C2H5OH)、Co-B(THF)。利用XRD、SEM分析Co-B黑色粉末的晶体结构和表面形貌。图1所示为Co-B在不同溶剂体系中的XRD,没有明显的杂质峰,说明Co-B催化剂是非晶态。由图2(a)~(c)的SEM中可见,Co-B催化剂为纳米颗粒,其直径为50~80 nm。所得纳米粒子在表面分布不均匀,随机生长在催化剂表面,可以为NaBH4的催化水解提供丰富的活性位点。

图1 不同体系中Co-B催化剂的XRD图谱Fig.1 XRD patterns of the Co-B catalyst in different systems

图2 Co-B(H2O)、 Co-B(C2H5OH)和 Co-B(THF)的SEM图像Fig.2 SEM images of Co-B(H2O),Co-B(C2H5OH)and Co-B(THF)

图3 Co-B(THF)的磁性光学照片Fig.3 Magnetic optical photographs of Co-B(THF)
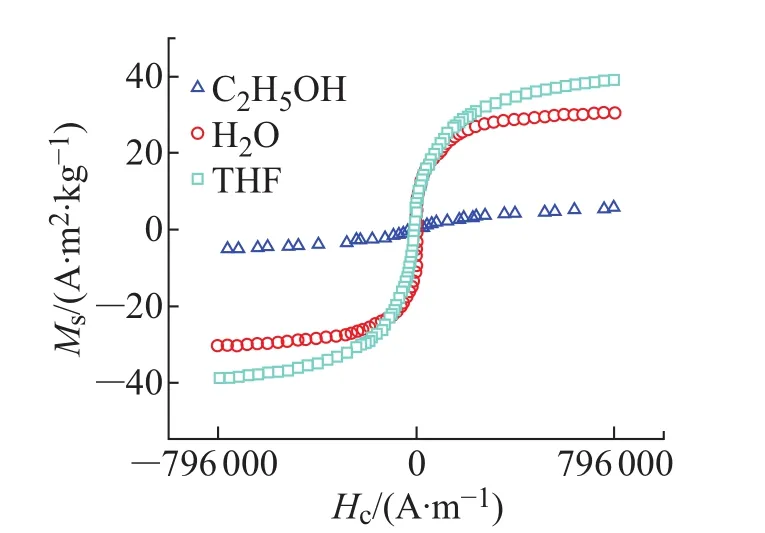
图4 298 K时Co-B的磁滞回线Fig.4 The hysteresis loop of Co-B catalysts at 298 K
图3 所示为Co-B(THF)的磁性光学照片,可以看出催化剂完全被磁铁吸附,溶液变为无色透明。图4所示为298 K时Co-B催化剂在不同体系的磁滞回线。Co-B(THF)的饱和磁化强度(Ms)值为39.2 A·m2/kg,而 Co-B(H2O)和 Co-B(C2H5OH)的Ms则为30.1 A·m2/kg和5.2 A·m2/kg,这种现象归因于THF体系制得的Co-B催化剂有较大的比表面积,而永磁场中磁性粒子的能量通过单个磁畴中的磁性分子的数量与其体积成比例[24]。此外,纳米材料在磁性催化剂的表面上缺乏完全配位,并且自旋也是无序的。这也是导致Co-B(THF)的Ms值增大的另一个因素[25]。Co-B(H2O)的矫顽力(Hc)(1 990 A/m)高于Co-B(THF)(0 A/m)。这表明Co-B(THF)具有优异的磁性[26]。
所制备的Co-B的组成不同,对 NaBH4的催化水解有着强烈影响。由表1可知,当n(CoCl2:NaBH4)为 3:7 时,Co-B(THF)的 HGR为 7.45 L/(g·min);同时 ICP分析表明,所制备的催化剂 Co与 B的原子比为 1.80:1。另外,Co-B(THF)的最高HGR为7.45 L/(min·g)。H2O和C2H5OH体系中最高HGR分别为4.21 L/(min·g)和 6.00 L/(min·g)。Co-B(H2O)作为对照组,在相同n(CoCl2:NaBH4)条件下,其催化剂的HGR总是低于Co-B(THF)和Co-B(C2H5OH)。这是由于Co-B(THF)的B可以在CoCl2与NaBH4还原反应期间与Co结合,所述还原剂能够改善Co碱的催化剂活性。
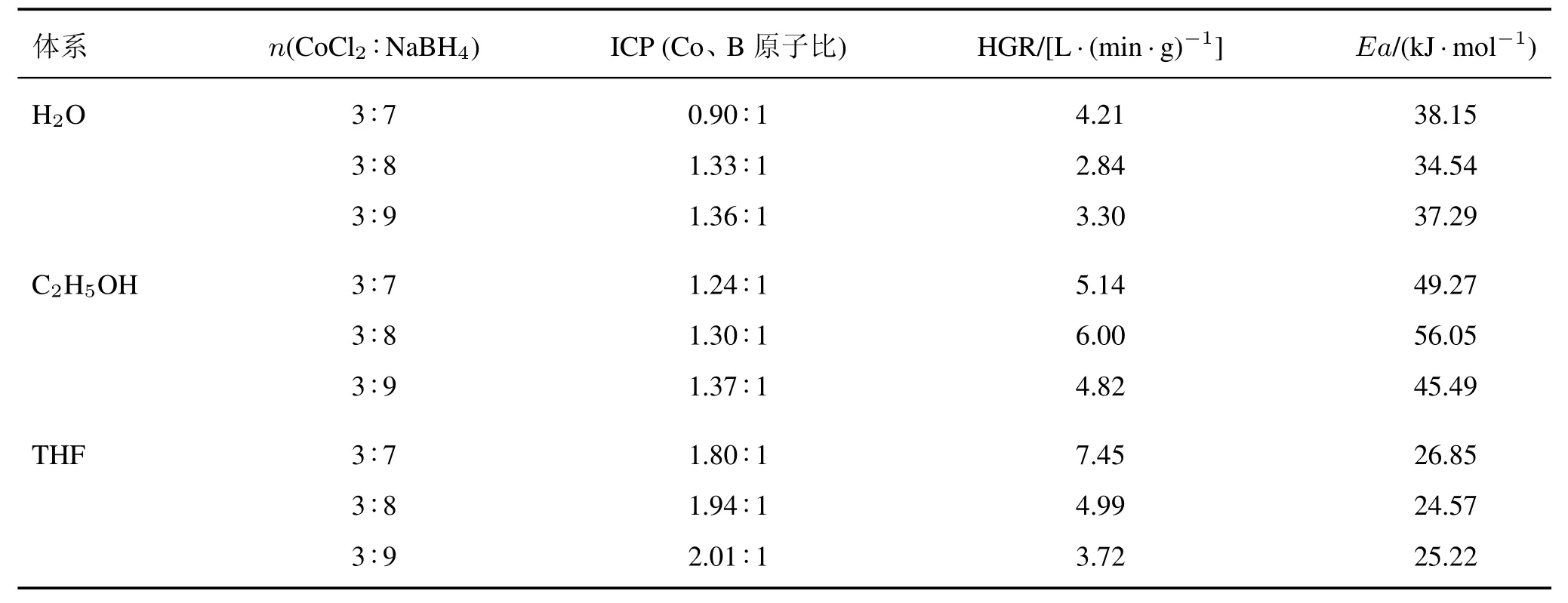
表1 298 K时所制备催化剂的条件、组成及性质Tab.1 The conditions,composition and property of the as-prepared catalysts at 298 K
2.2 NaBH4水解与电化学性能
298 K 时,Co、Co-B(H2O)、Co-B(C2H5OH)和Co-B(THF)催化剂的NaBH4水解曲线如图5所示。可以看出,在不同体系中的产氢率几乎与反应时间成线性比例。
反应温度是影响催化反应的重要因素。图6所示为温度在283~313 K范围内对催化反应的影响。其中,产氢率为NaBH4在不同体系中Co-B水解制氢时的实际产氢量与理论产氢量之比。3个体系的产氢率随着温度的升高急剧增加,根据式(1)和(2)计算,Co-B(H2O)的HGR从 293 K时的 2.20 L/(min·g)到 313 K的7.15 L/(min·g),Ea 为 39.48 kJ/mol。Co-B(C2H5OH)的Ea为56.05 kJ/mol。298 K时,Co-B(THF)的HGR为 7.45 L/(min·g),303 K 时为 11.50 L/(min·g),Ea较低,为26.85 kJ/mol。这是由于Co-B催化剂,特别是Co-B(THF)加速了NaBH4分子的运动,导致越来越多的有效碰撞达到能量阈值。
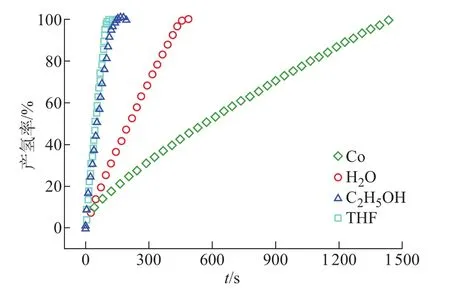
图5 298K 时 Co、 Co-B(H2O)、 Co-B(C2H5OH) 和Co-B(THF)的NaBH4水解曲线Fig.5 Hydrolysis curves of NaBH4of Co,Co-B(H2O),Co-B(C2H5OH)and Co-B(THF)at 298 K

图6 Co-B(H2O)、Co-B(C2H5OH)、Co-B(THF)在不同温度下水解NaBH4的产氢率图。插图:对NaBH4水解进行线性拟合Fig.6 Hydrogen yield rate of hydrolyzing NaBH4in Co-B(H2O),Co-B(C2H5OH)and Co-B(THF)at various temperature.Inset:Linearfit to NaBH4hydrolysis
不同溶剂制备出的Co-B@Ti在氮气饱和的1.0 mol/L KOH电解液中评估其电催化HER、OER性能。HER和OER初始数据没有进行IR校正[23]。如图7(a)所示,Ti箔上负载量相同的商业Pt/C显示出优异的催化活性,忽略裸Ti箔向HER提供的还原电流,需要113 mV过电位才能提供100 A/m2的电流密度。从表2可知,在HER中,Co-B@Ti(H2O)和Co-B@Ti(C2H5OH)在100 A/m2时的过电位分别为420和380 mV,而Co-B@Ti(THF)在相同的电流密度展现了更小的过电位(270 mV)。图7(b)所示为Ti箔,IrO2@Ti,Co-B@Ti(H2O)和 Co-B@Ti(THF)的OER。可观察到,IrO2@Ti显示出优异的OER活性,且Ti箔对OER贡献较小。从表2中可知,Co-B@Ti(H2O)和Co-B@(THF)在电流密度为100 A/m2时具有相同的过电位310 mV。由图7(c)、(d)及表2可知,Co-B@Ti(THF)的HER的Tafel斜率为282.6 mV/dec,OER的Tafel斜率为226.30 mV/dec,而Pt-C/Ti HER的Tafel斜率为90.3 mV/dec以及IrO2/Ti OER的Tafel斜率为103.6 mV/dec,说明商业型的Pt-C和IrO2在电子传输以及HER、OER具有更加优异的性能,但Pt和IrO2属于贵金属,价格昂贵,不能广泛应用于实验中。
2.3 XPS分析
用XPS表征Co-B的结合能(BEs),归一化后的谱图如图8所示。在图8(a)中观察到THF体系中Co的2p(1/2)和2p(3/2)XPS峰位于800.5 eV和784.6 eV以及宽肩部在806.0 eV和789.2 eV,这是由于制备过程暴露在空气中而无意地形成CoO或Co主要以Co(II)态的形式存在于化合物中。Co-B(THF)的Co 2p(3/2)峰在784.6 eV处,相对于Co-B(H2O)和Co-B(C2H5OH)的正电化学位移约为0.5 eV,因此THF溶液具有可以调节电子的性质。B 1s的BEs出现在188.0 eV[28],但Co-B(H2O,C2H5OH和THF)的B分别出现在194.2、194.1和194.4 eV,如图8(b)所示。它表明高氧化态和氧化态为B(III)[28]。
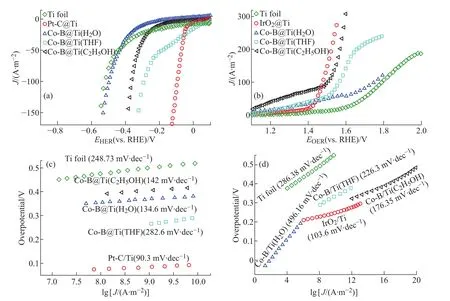
图7 (a)、(b)极化曲线;(c)、(d)HER和OER的LSV曲线所对应的塔菲尔斜率Fig.7 (a),(b)Polarization curves;(c),(d)Tafel slopes corresponding to the LSV curves of HER and OER
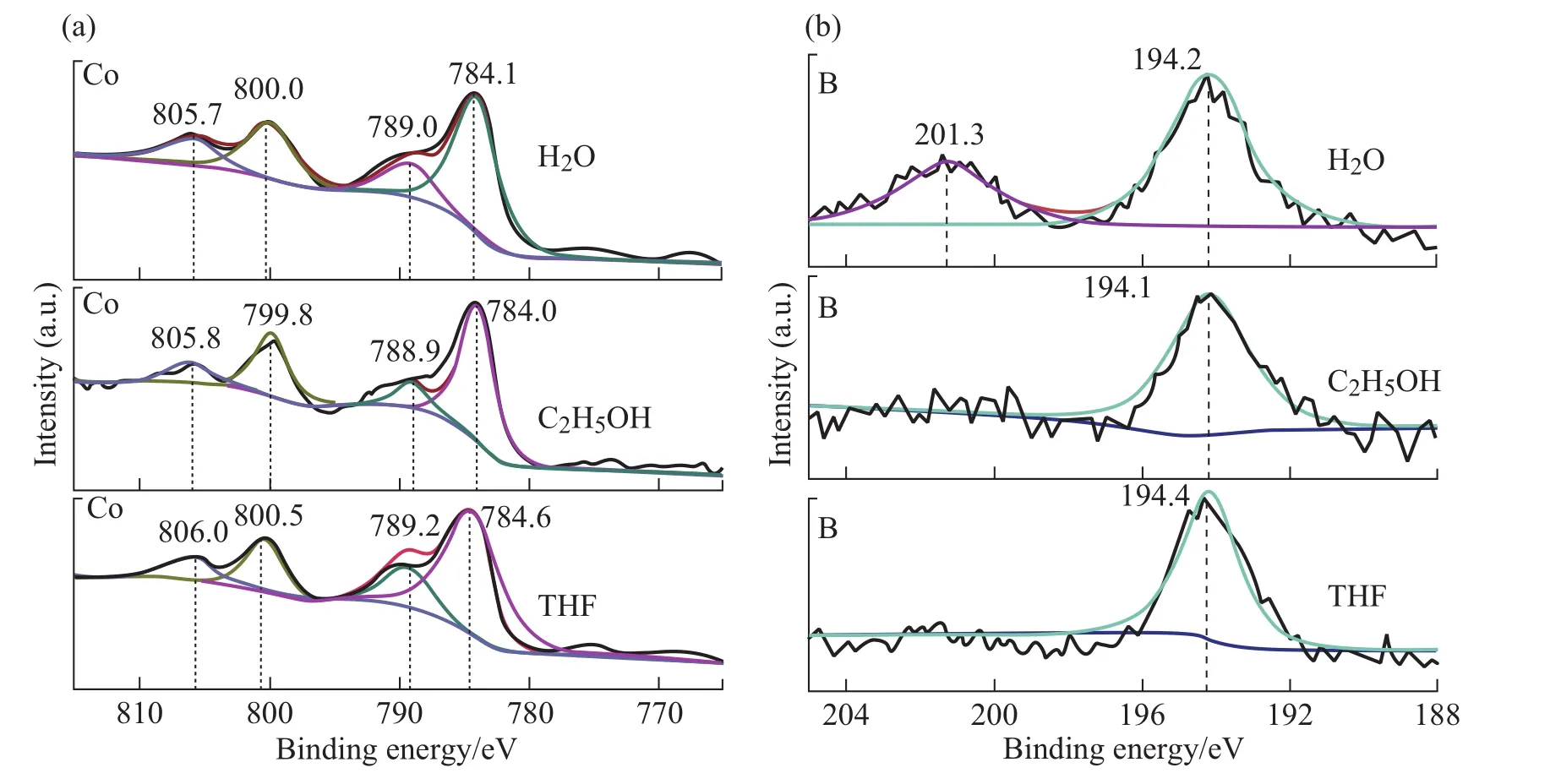
图8 在H2O,C2H5OH和THF体系中(a)Co 2p高分辨率的XPS光谱(b)B 1s核心水平光谱Fig.8(a)Co 2p high resolution XPS spectra of Co-B in H2O,C2H5OH and THF systems(b)B 1s core level spectra
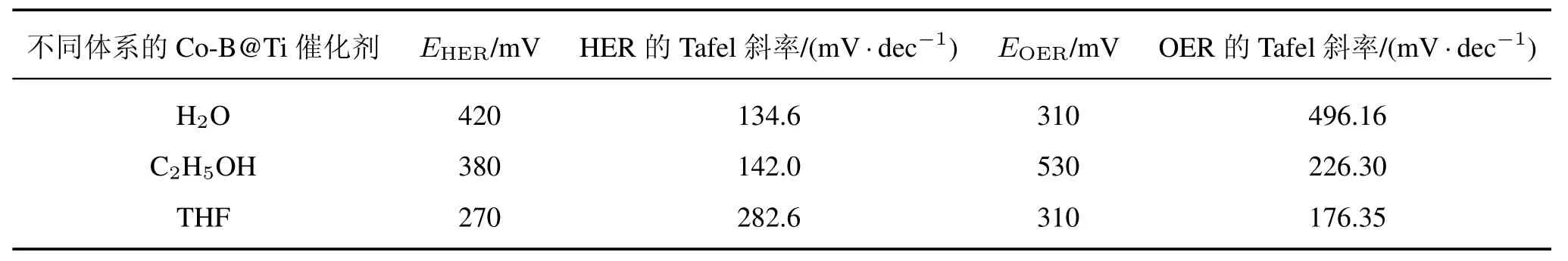
表2 不同体系Co-B@Ti催化剂在1 mol/L KOH中的HER和OER性能Tab.2 HER and OER performance of Co-B@Ti catalysts in 1 mol/L KOH under different systems
3 结 语
本文采用溶液沉淀法制备多功能Co-B催化剂,方法简单且成本较低。因此,该方法可以推广至其他具有不同元素组成的催化剂的制备中。用于碱性NaBH4溶液水解的Co-B催化剂是一种高效且稳定的催化剂,特别是在THF体系中。在298 K时,Co-B(THF)的HGR的最大值为7.45 L/(min·g),Ea为26.5 kJ/mol。同时,Co-B(THF)也具有优良的电化学和磁性能。Co-B@Ti(THF)在1.0 mol/L KOH电解液中,电流密度为100 A/m2时HER和OER过电位分别为270 mV和310 mV。
