康柏西普与雷珠单抗治疗非缺血型视网膜分支静脉阻塞继发黄斑水肿的对比观察
2019-04-11赵旭丽阳光张娣廖凯袁安
赵旭丽 阳光 张娣 廖凯 袁安
(四川省成都市第二人民医院眼科 成都 610017)
视网膜静脉阻塞(retinal vein occlusion, RVO)是眼科常见的视网膜血管病变,发病率仅次于糖尿病视网膜病变[1]。与高血压、动脉硬化、心脑血管疾病及糖尿病等全身因素密切相关,与开角型青光眼局部因素相关。临床上根据静脉阻塞发生的部位分为视网膜中央静脉阻塞、视网膜分支静脉阻塞 (branch RVO, BRVO) 和视网膜半侧中央静脉阻塞。其中BRVO的发病率约占RVO的80%[2]。
静脉阻塞后,由于沿静脉分布区域的视网膜循环障碍,缺血、缺氧导致视网膜血管屏障破坏,血管内皮受损,眼底微血管病变导致渗漏。当病变累及黄斑时,即引起黄斑水肿。BRVO继发黄斑水肿的发生率为30%~66%[3]。对于RVO继发黄斑水肿的治疗,首选抗血管内皮生长因子(vascular endothelial growth factor, VEGF)药物[4],国内临床上多采用的抗VEGF药物有康柏西普和雷珠单抗,给药模式为按需治疗,3+PRN或1+PRN。本研究中,我们只对非缺血型BRVO引起的黄斑水肿进行观察,给药模式为1+PRN,随访12个月比较2种药物的疗效及注射次数。
1 资料与方法
1.1 资料 收集2016年1月~2017年1月在我院确诊为非缺血型BRVO继发黄斑水肿患者共38例(38眼)。所有患者均完善视力、裂隙灯、散瞳检眼镜(眼底镜)、眼底照相、光学相干层析成像(optical coherence tomography, OCT)及荧光素眼底血管造影(fundus fluorescein angiography, FFA)检查,并确诊为非缺血型BRVO继发黄斑水肿。按照治疗药物不同分为2组。康柏西普组22例,其中男性12例、女性10例;平均年龄为(56.87±11.36)岁;平均病程为(2.83±1.65)个月;伴高血压16例、高血脂8例、糖尿病4例。雷珠单抗组16例,其中男性9例、女性7例;平均年龄为(58.13±12.70)岁;平均病程为(3.04±1.81)个月;伴高血压11例、高血脂6例、糖尿病3例。2组间性别、年龄、病程及高血压、高血脂、糖尿病等高危因素比较差异均无统计学意义(P>0.05),资料具有可比性。
病例纳入标准:①视力下降或视物变形,眼科常规检查及FFA、OCT检查确诊为BRVO继发黄斑水肿;②OCT检查显示黄斑中心凹隆起,囊样水肿,平均黄斑中心凹厚度(central macular thickness, CMT)>250 μm;③FFA检查示早期视网膜静脉充盈迟缓,血管迂曲,黄斑区荧光素积存,未见无灌注区。
病例排除标准:①合并全身严重心脑血管疾病或手术禁忌证者;②曾有玻璃体切除手术史、抗VEGF药物或曲安奈德眼内注射史、眼底激光治疗史患者;③合并有糖尿病视网膜病变、病理性近视等其他视网膜疾病者;④合并白内障、严重玻璃体积血等屈光介质不清的患者;⑤有高眼压、青光眼病史的患者。
1.2 方法 BCVA检查:标准照明条件下,采用国际标准对数视力表进行检查,转换为LogMAR视力便于统计,视力数指为0.01(2.0 logMAR),手动为0.001(3.0 LogMAR)。
OCT检查:采用德国Zeiss公司的OCT 5000行黄斑OCT检查。仪器自动测量中心凹视网膜内界膜至视网膜色素上皮层之间的垂直距离即为CMT。
FFA检查:采用德国海德堡血管造影系统,将20%荧光素钠3 mL溶于2 mL无菌注射用水,自肘静脉快速推入,动态观察造影全过程,造影时长≥10 min。所有患者检查前均签署知情同意书。
玻璃体腔注射:所有手术均在我院眼科层流手术室内进行,术前签署知情同意书。术前连续3 d予0.5%左氧氟沙星滴眼液滴眼,严格消毒和无菌操作,丙美卡因表面麻醉3次。开睑器开睑,使用专用注射针头于角巩膜缘后3.5 mm处进针,向球心方向刺入并确保针头位于玻璃体腔内,注入康柏西普或雷珠单抗的剂量均为0.5 mg(0.05 mL)。退针后用棉棒压迫针眼1 min,术毕结膜囊内涂左氧氟沙星眼膏包术眼。术后第1天即可打开术眼,继续用0.5%左氧氟沙星滴眼液滴眼3 d预防感染。
1.3 观察指标 术后每月随访,完善BCVA、裂隙灯、眼压、检眼镜、眼底照相、黄斑OCT等检查,若病情需要,则每3个月完成FFA检查。
重复治疗标准:① BCVA下降且OCT显示黄斑有水肿;②复查OCT显示 CMT 较前次随访时增加≥100 μm;③持续性CMT,即初始治疗后CMT下降不明显。重复治疗的注射药物及剂量同首次注射。
对比观察2组患者治疗前和治疗后12个月时BCVA、CMT的变化及总注射次数。

2 结果
2.1 治疗前后BCVA情况 康柏西普组与雷珠单抗组治疗前的BCVA(LogMAR)分别为0.70±0.18、0.73±0.20,差异无统计学意义(P=0.887);2组治疗后1、3、6、12个月的BCVA分别与治疗前相比均有明显提高(P<0.05),各随访时间点组间比较差异均无统计学意义(表1)。
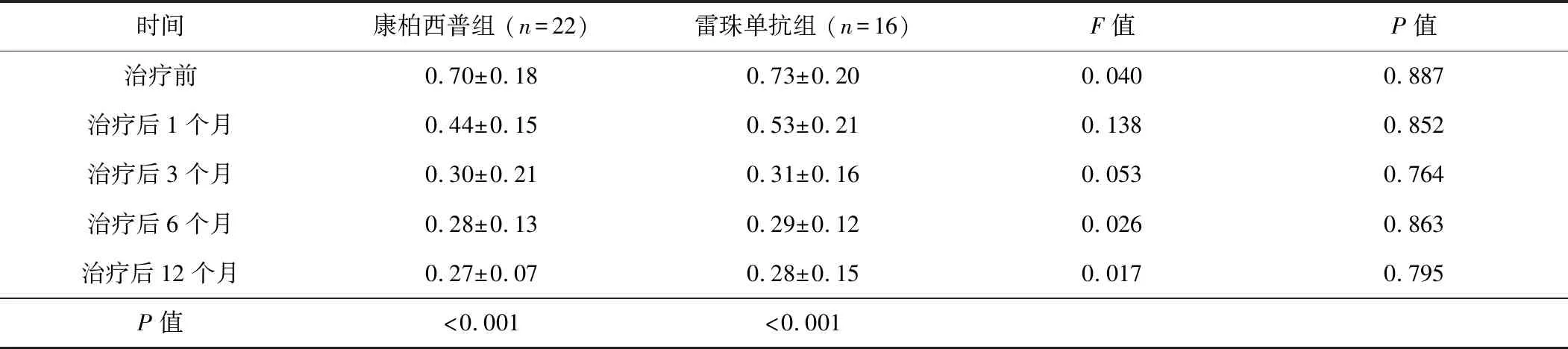
表1 2组患眼治疗前后BCVA(LogMAR)变化
2.2 治疗前后CMT比较 2组患眼治疗后1、3、6、12个月时的CMT与治疗前相比,均有明显降低,差异有统计学意义(P<0.05);各随访时间点组间比较差异均无统计学意义(表2)。
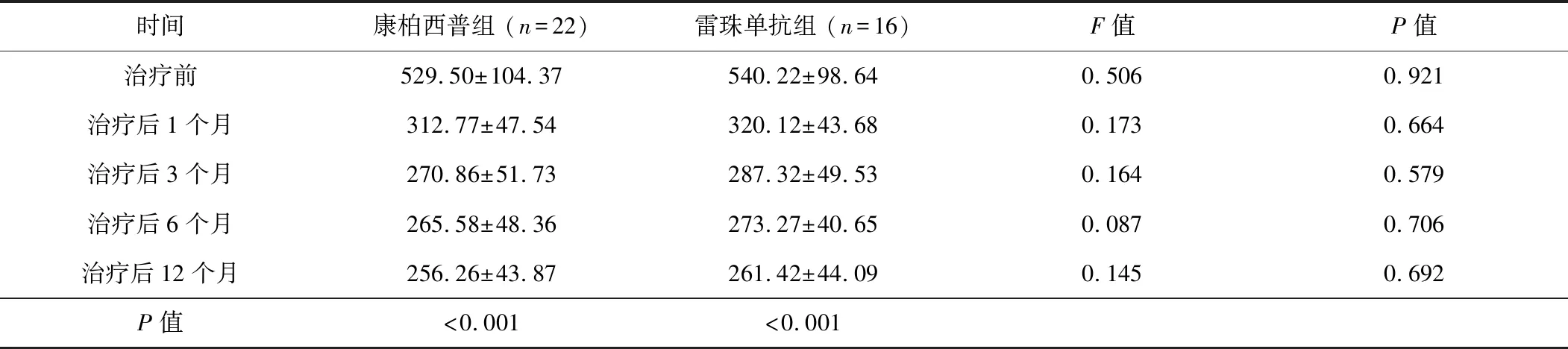
表2 2组患眼治疗前后CMT变化
2.3 注射次数比较 随访12个月,康柏西普组22眼共注射36次,患者接受注射次数为1~3次,平均(1.64±0.70)次;雷珠单抗组16眼共注射30次,患者接受注射次数为1~3次,平均(1.88±0.67)次;康柏西普组的注射次数少于雷珠单抗组,差异有统计学意义(t=3.471,P=0.023,P<0.05)。
2.4 术后不良反应 2组患者在治疗及随访过程中,均未发现眼压升高、眼内炎、继发性青光眼等眼部并发症。2组均有1例发生球结膜下出血,未经特殊处理自行吸收。2组均未见由于治疗引起的全身不良反应。
3 讨论
视网膜在静脉阻塞的情况下,会导致视网膜组织回流障碍、缺血、缺氧,生成并释放大量细胞因子,如VEGF、胎盘生长因子(placental growth factor, PIGF)、炎性因子(IL-6、IL-8)等导致血-视网膜屏障破坏,继发黄斑水肿[5]。有研究[6-7]发现,视网膜静脉阻塞后患眼玻璃体腔VEGF水平明显升高;VEGF及其受体的过度表达与血清蛋白渗出、视网膜增厚、黄斑水肿密切相关。
对于RVO继发黄斑水肿的治疗,目前首选抗VEGF药物。如果多次玻璃体腔注射治疗效果不佳,可选择长效激素治疗[4]。目前对于抗VEGF治疗RVO继发黄斑水肿尚缺乏指导性的意见。瑞士的一项针对抗VEGF 药物治疗RVO继发黄斑水肿的研究表明, 1+PRN组和3+PRN组间比较,术后 1、2、3、6 个月BCVA和CMT 差异均无统计学意义。富莉莉等[8]比较玻璃体腔注射康柏西普1+PRN模式和3+PRN模式治疗RVO继发的黄斑水肿,随访6个月,差异无统计学意义。反复玻璃体腔注射抗VEGF药物治疗湿性老年性黄斑变性,有增加远期黄斑区地图样萎缩、视网膜色素上皮萎缩及脉络膜毛细血管萎缩的风险[9]。同时由于抗VEGF治疗所带来的经济负担,目前国内临床上对于RVO所致黄斑水肿,一般采用1+PRN的治疗模式。
雷珠单抗是一种新型重组人IgGlk单克隆抗体片段,能够选择性与VEGF-A结合,抑制眼内新生血管生成,减少视网膜内渗液释放,从而达到促进渗液吸收和消除水肿的作用。Pece等[10]采用雷珠单抗治疗视网膜静脉阻塞,可迅速阻断VEGF-A,提高视力,使黄斑厚度明显下降。而国产抗VEGF药物康柏西普是一种融合蛋白,不仅能阻断 VEGF-A 的所有亚型,还能同时阻断 VEGF-B 和 PIGF,其作用范围比雷珠单抗更广泛[11]。 有研究[7,11]表明,对雷珠单抗治疗无效的患者,康柏西普可能会有效。
有文献[12-13]对RVO黄斑水肿患者进行一次玻璃体腔注射康柏西普或雷珠单抗治疗,随访6个月时比较2组的视力和黄斑厚度,康柏西普均明显好于雷珠单抗。而本研究采用1+PRN的治疗模式,结果显示,康柏西普组和雷珠单抗组的治疗效果与治疗前比较,差异均有统计学意义,各随访时间点组间比较BCVA和CMT方面的效果却相当,与文献报道不同。因为雷珠单抗与康柏西普作为抗VEGF药物,均不能摧毁渗漏的毛细血管,只能在一定时间内抑制液体渗漏,且2种药物的作用时间较短,康柏西普半衰期为4.2 d,雷珠单抗半衰期为2.88 d,玻璃体腔内药物浓度降低后,黄斑水肿可再次发生,需要重复注射。因此治疗期间应注意每月按时随访,及时再次给药,2种药物均能达到相同疗效。
在注射次数方面,HORIZON研究用玻璃体腔注射雷珠单抗治疗BRVO继发黄斑水肿患者,12个月后0.3 mg、0.5 mg组及安慰剂组平均注射次数分别为2.4、2.1、2.0次[14]。我们的研究结果显示,随访12个月康柏西普组的平均注射次数为(1.64±0.70)次,雷珠单抗组的平均注射次数为(1.88±0.67)次,康柏西普的注射次数更少,与雷珠单抗相比较差异有统计学意义。分析原因可能是:①康柏西普分子结构与VEGF有更强的亲和力,结合后其复合物结构更稳定,代谢率较缓慢;②虽然2组患者治疗前基线资料相比较差异无统计学意义,但我们的样本量较小,不排除患者的全身情况及个体对药物的敏感度差异因素所致。本研究为回顾性非随机对照临床研究,相对于前瞻性随机对照研究存在一定偏倚,有待大样本的随机对照研究来证实。
我们认为,对于非缺血型RVO继发黄斑水肿,选择玻璃体腔注射康柏西普可在不增加并发症风险的前提下,有效减少注射次数。但RVO病因复杂,病程、眼底出血及黄斑区受累情况均会影响患者的视力预后,且患者之间存在很大的个体差异。治疗应从病因入手,注重个体差异,合理使用抗VEGF药物。
