自动电位滴定直接测定含锰粗钴盐中常量钴
2019-04-04
(1.国家镍钴新材料工程技术研究中心,兰州 730101;2.兰州金川新材料科技股份有限公司, 金昌 737100;3.金川集团有限公司检测中心,金昌 737100)
国内钴企业的原料很大一部分来自非洲的钴铜矿,钴铜原矿经湿法冶金处理后,钴以粗制碳酸盐或粗制氢氧化物形式销往国内,这两种形式的原料通常被统称为粗钴盐,钴作为其重要的有价金属元素,准确测定含量至关重要。
常量钴的测定方法有亚硝酸钴钾重量法[1]、EDTA滴定法[2]、亚硝基红盐分光光度法[2,3]和电位滴定法[4-10]。亚硝酸钴钾重量法分析流程长,不易掌握,在日常工作中很少采用;EDTA滴定法则适合于共存干扰组分少的样品;分光光度法主要应用于较低含量钴的测定;而电位滴定法测定钴量,测定范围宽,分析精度高,但共存的锰(Ⅱ)少量即干扰其测定,采用将锰生成二氧化锰沉淀消除干扰的方法[11],二氧化锰沉淀会吸附少量的钴,使测定结果系统偏低,需要进行补正。而采用离子交换法分离锰等组分后再测定钴量[4],方法操作冗长,当试样中的铁量高时,对树脂还需特殊处理;实际分析工作中,也采用电位滴定法测定钴锰合量,采用AAS或ICP测定锰含量,通过差减法得出钴的含量,这样操作比较繁琐,同时可能造成分析误差的扩大。
根据锰在电位滴定中价态的变化,试验了在高氯酸、磷酸存在下,将锰氧化生成稳定的磷酸锰,消除了共存锰的干扰,该方法共存的其他元素不干扰钴的测定,实现了电位滴定法对粗氢氧化钴和粗碳酸钴中钴量的直接测定。方法分析结果准确度高、精密度好,满足粗氢氧化钴、粗碳酸钴原料中钴量的测定要求。
1 试验部分
1.1 仪器及试剂
自动电位滴定仪(Metrohm 905 Titrando 型),附Pt-Titrode 电极,140型复合电极。
盐酸(ρ1.19 g/mL);硝酸(ρ1.42 g/mL);高氯酸(ρ1.67 g/mL);磷酸(ρ1.69 g/mL);氨水(ρ0.90 g/mL);柠檬酸铵溶液(300 g/L);氟化氢铵;上述试剂均为分析纯试剂。
锰标准溶液[ρMn=10.000 mg/mL]:准确称取2.0000g金属锰(wMn≥ 99.95%),慢慢加入20mL硝酸(1+1),低温溶解后,取下冷却,用水清洗表皿及杯壁,冷却后移入200mL容量瓶中,以水定容。此溶液1mL含锰10mg。
钴标准溶液[ρCo=8.000 mg/mL]:准确称取4.0000g金属钴(wCo≥ 99.95%),加入30mL硝酸(1+1),低温溶解后,取下冷却,用水清洗表皿及杯壁,冷却后移入500mL容量瓶中,以水定容。此溶液1mL含钴8mg。
钴标准滴定溶液[ρCo=1.000 mg/mL]:准确称取1.0000g金属钴(wCo≥ 99.95%),加入20mL硝酸(1+1),低温溶解后,加入10mL硫酸(1+1),加热至冒尽大量白烟后,取下冷却,用水清洗表皿及杯壁,加热溶解盐类,冷却后移入1000mL容量瓶中,以水定容。此溶液1mL含钴1mg。
铁氰化钾标准溶液(ρ[K3Fe(CN)6]=5.6 g/L),配制后用钴标准滴定溶液在自动电位滴定仪上标定,计算铁氰化钾对钴的滴定系数,输入自动电位滴定仪计算公式中。
1.2 试验方法
分取一定量的钴标准溶液置于400mL烧杯中,加入5mL高氯酸、10mL磷酸,在360℃~400℃左右温度下加热至高氯酸浓白烟减少,液面出现大量密集的气泡时,取下表皿,继续加热至气泡逐渐消失,直至沿杯壁的液面无小气泡时,即刻取下,稍冷3 min~5min,用水冲洗表皿及杯壁,在不断摇动下加热煮沸溶解盐类后,取下冷却,移入200mL容量瓶中,以水定容。于200mL烧杯中,事先加入30mL柠檬酸铵溶液,30mL氨水,准确加入一定量的铁氰化钾标准溶液(以铁氰化钾标准溶液过量2mL~10mL为宜),混匀,然后分取25.00mL 试液至该烧杯中,在全自动电位滴定仪上,将Pt-Titrode电极放入烧杯,不断搅拌下用钴标准滴定溶液滴定过量的铁氰化钾标准溶液,按仪器设定的程序,自动滴定至电位突跃最大即为终点,自动计算结果。
2 结果与讨论
2.1 滴定介质及用量的选择试验2.1.1 柠檬酸铵用量选择试验
柠檬酸铵用量选择采用试验方法制备的钴试液进行试验。于1组200mL烧杯中,加入不同量的柠檬酸铵溶液,30mL氨水,准确加入25.00mL铁氰化钾标准溶液,混匀,分别移入25.00mL钴试液,按试验方法测定终点电位,结果见表1。

表1 柠檬酸铵用量试验
从表1可知,柠檬酸铵溶液(300g/L)用量在≥15mL时,滴定体系的终点电位一致,本试验选择加入30mL柠檬酸铵溶液。
2.1.2氨水用量选择试验
于1组200mL烧杯中,加入30mL柠檬酸铵溶液,不同量的氨水,准确加入25.00mL铁氰化钾标准溶液,混匀,分别移入25.00mL按试验方法1.2.1处理后的钴试液,按试验方法1.2.2测定。结果见表2。
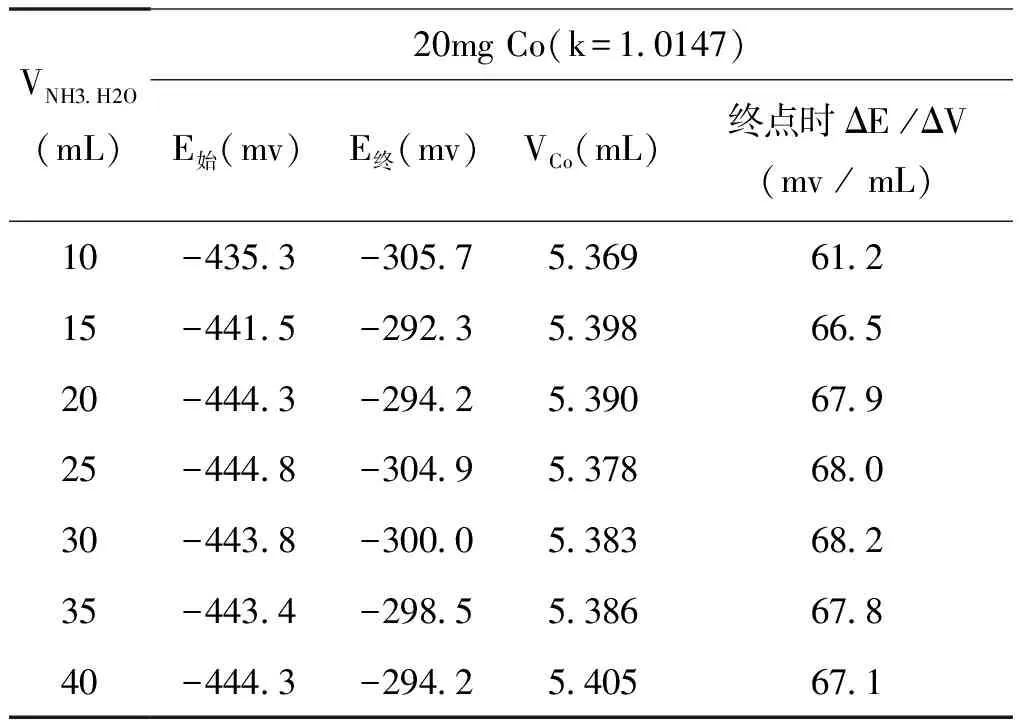
表2 氨水用量试验
从表2可知,氨水用量对终点电位及终点突跃电位的影响较为显著,在20~35mL时,滴定体系的终点电位突跃更为显著。本试验选择加入30mL氨水。
2.2 共存元素干扰情况的考察2.2.1 考察Mn2+的干扰消除情况
由文献[7-9]可知,不进行分离或掩蔽,少量的锰即干扰钴的测定。按样品中含钴量,试验分取不同量的钴标准,加入一定量的锰,按试验方法1.2.1加入5mL高氯酸和10mL磷酸冒烟处理后,按1.2.2进行测定,考察锰的干扰消除情况,结果见表3。

表3 Mn2+干扰消除考察试验
由表3可知,按试验方法处理样品后,共存80mg Mn2+不干扰钴的测定。粗氢氧化钴和粗碳酸钴样品中共存的锰量通常都小于10%(相当于试液中含Mn 40mg),因此,采用本法掩蔽共存的锰,可直接测定样品钴含量,能够满足样品分析要求。
2.2.2 其他共存元素干扰试验
分别移取10.00mg 和20.00mg的钴标准于一组烧杯中,加入下列不同量的共存元素,按试验方法1.2.1处理后,分取25.00mL试液,按1.2.2滴定。结果见表4。
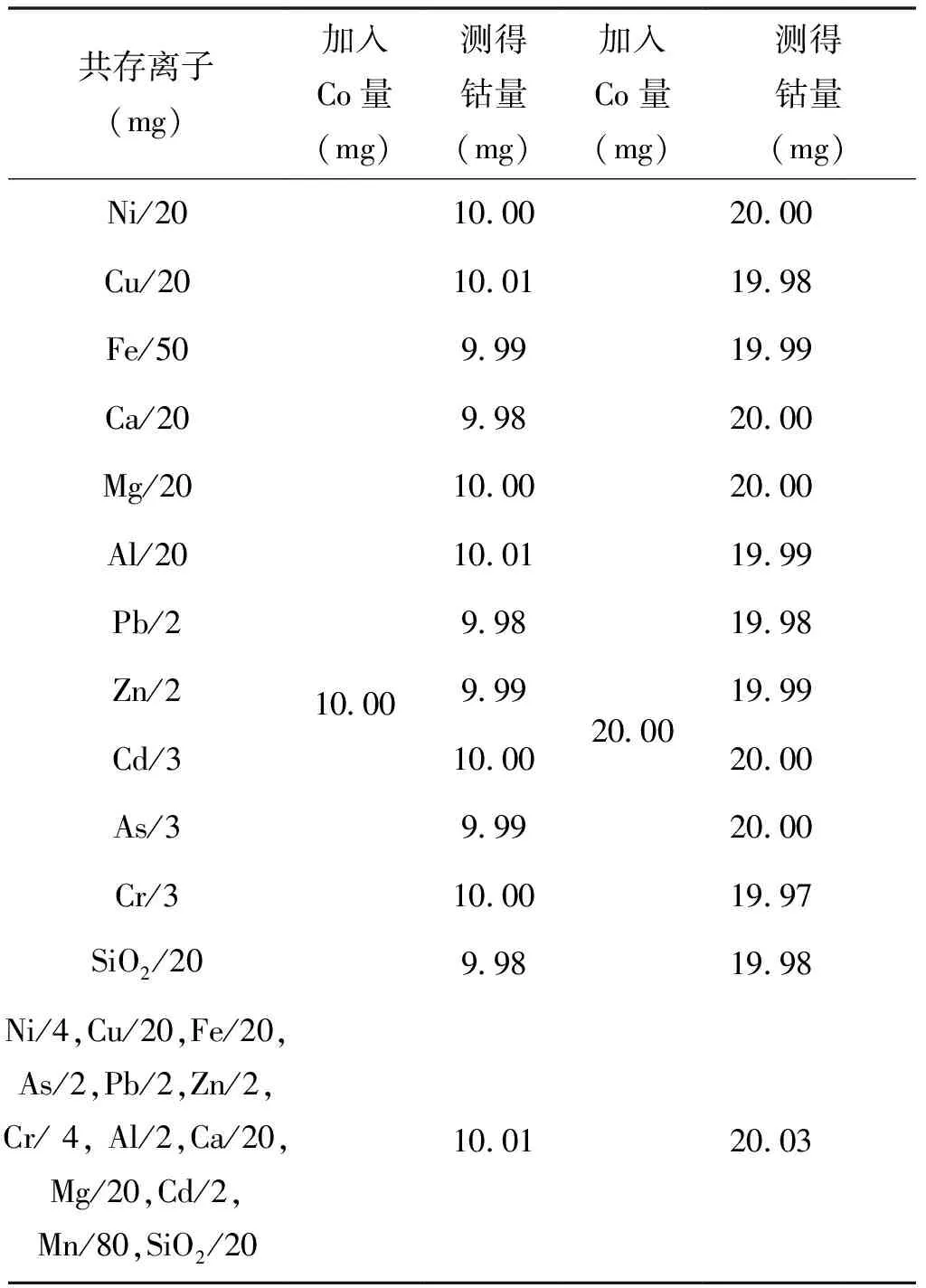
表4 共存元素干扰试验
2.3 试液加入顺序的选择
将25.00mL按试验方法处理的钴标准试液(1.2.1)及样品试液先移入烧杯中,再依次加入30mL柠檬酸铵溶液、30mL氨水和25.00mL铁氰化钾溶液,当加入氨水后,出现白色沉淀,随着钴标准滴定溶液的加入沉淀逐渐减少并消失;而样品溶液在最后加入则无沉淀出现。由文献[7]可知,先加入样品还会出现结果偏低且不稳定现象。因此,试验选择样品溶液在柠檬酸铵溶液、氨水和铁氰化钾溶液后加入。
3 试样分析
3.1 拟订分析步骤
称取试样0.4000g置于400mL烧杯中,以少量水润湿样品,加入约0.2g氟化氢铵,加入20mL盐酸(1+1),盖上表皿,低温溶解样品,加入5mL高氯酸、10mL磷酸,以下操作按照试验方法进行,测定样品中钴量。
按下式计算样品中的钴含量:
式中:k——铁氰化钾标准溶液对钴标准滴定溶液的滴定系数;
V0—— 试液的总体积, mL;
V1—— 返滴定所消耗钴标准溶液毫升数,mL;
V2—— 加入铁氰化钾标准溶液毫升数,mL;
V3—— 分取试液的体积, mL;
ρCo—— 钴标准溶液的质量浓度,mg/mL。
m—试料量,g;
3.2 精密度试验
取钴锰含量不同的样品,按照拟订的分析步骤对粗碳酸钴、粗氢氧化钴样品中的钴进行11次测定,测定结果见表5。
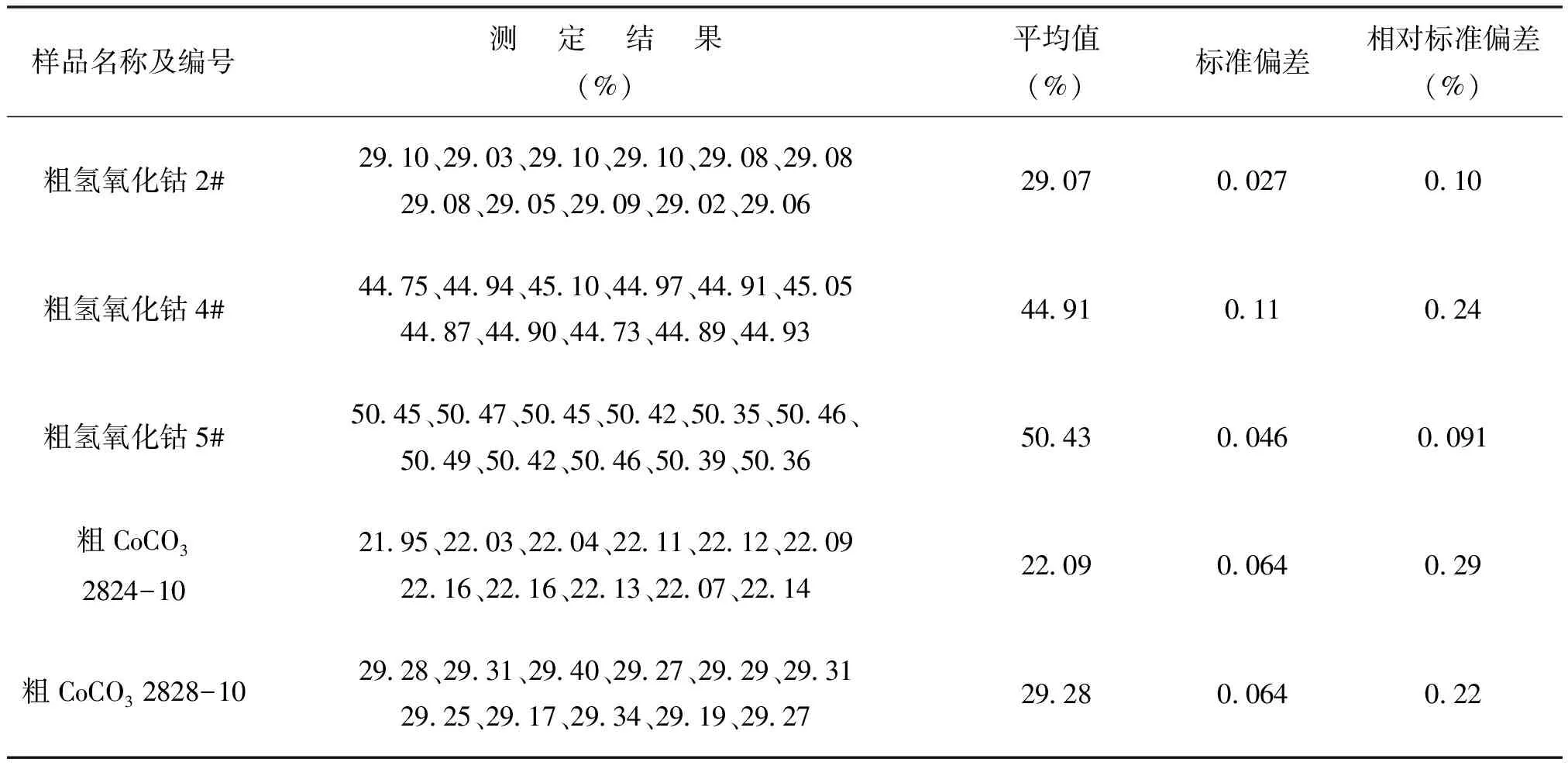
表5 精密度试验
3.3 准确度试验3.3.1 加标回收试验
为了考察本方法的准确度,对粗氢氧化钴和粗碳酸钴样品加入不同的钴量,按拟订的分析步骤进行回收率试验,测定结果见表6。
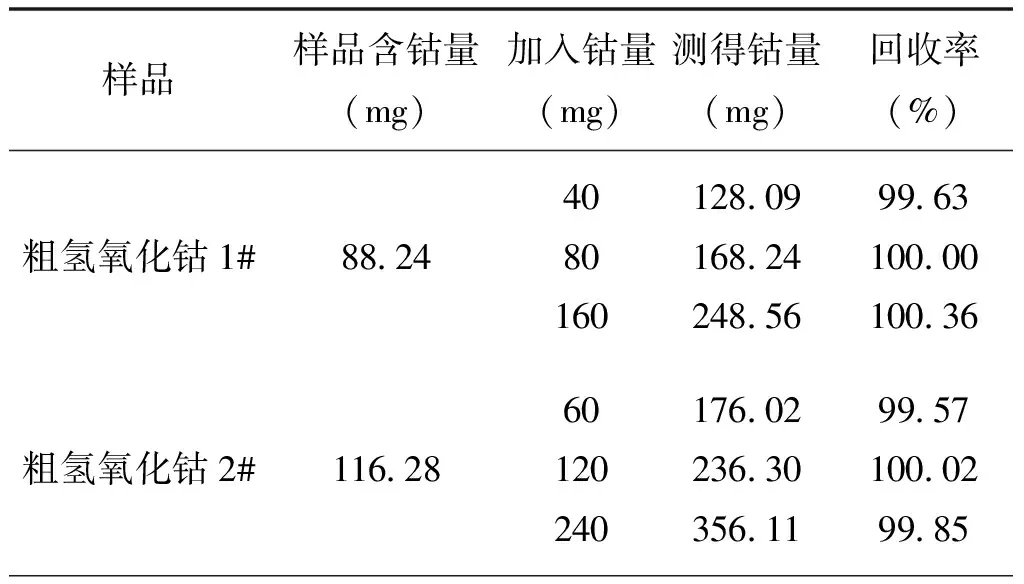
表6 样品加标回收试验
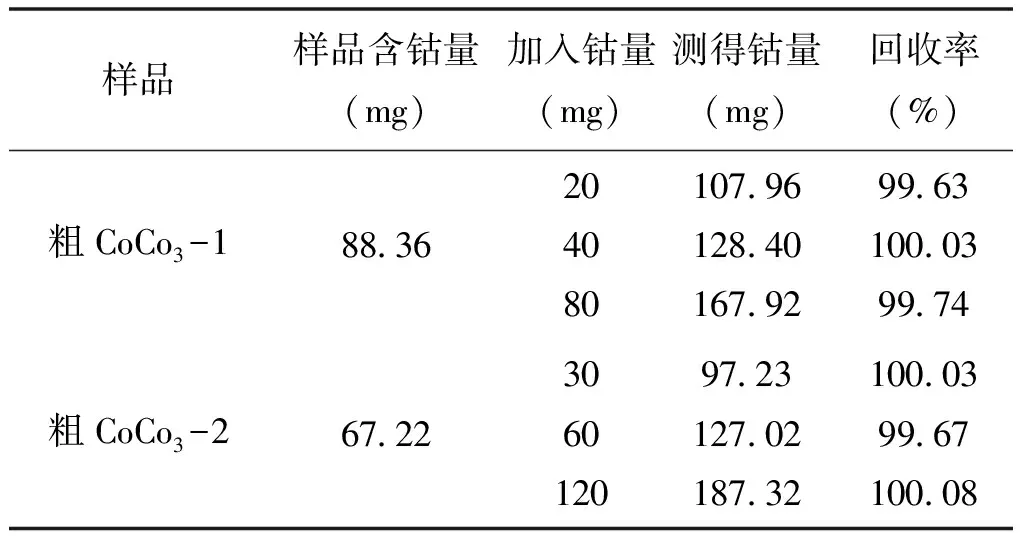
续表6
3.3.2 不同方法对照试验
在选定的测定条件下,按照拟订的分析步骤,选择不同含量的试样,采用不同的分析方法测定,与本方法的结果进行对照。结果见表7。
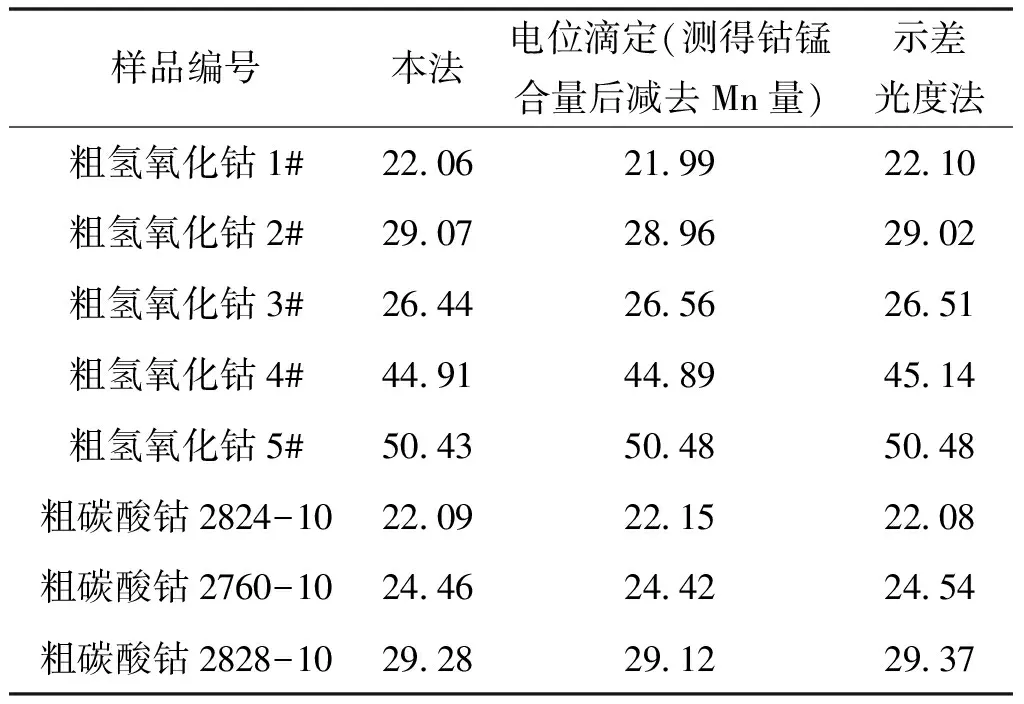
表7 对照分析试验
4 结论
由以上试验结果可以看出,通过冒高氯酸及磷酸烟掩蔽锰,利用电位滴定法直接测定粗氢氧化钴和粗碳酸钴中的钴量是可行的。样品测定的相对标准偏差为0.092%~0.32%之间,样品加标回收率为99.56%~100.15%。本方法结果准确度高、精密度好,满足分析要求。
