HPLC-CAD法测定硫酸新霉素中新霉素B、新霉素C、新霉胺及其他有关物质
2019-03-29刘庄蔚朱健萍梁秋霞蒋洁杨欣智
刘庄蔚 朱健萍 梁秋霞 蒋洁 杨欣智
(广西壮族自治区食品药品检验所,南宁 530021)
硫酸新霉素(neomycin sulfate)是首个被发现的氨基糖苷类抗生素,它是1949年Waksman等[1]从新霉素链霉菌代谢产物中分离得到的混合物。其抗菌谱较广,对革兰阳性菌、革兰阴性菌、结核杆菌等均有抑制作用[2],由于新霉素有显著的肾毒性和耳毒性,故常被制备成乳膏剂、软膏剂和滴眼液等外用制剂供患者使用。据文献报道,硫酸新霉素的主要成分为新霉素A、B、C 3种,新霉素A(新霉胺)仅微量,是新霉素B、C的降解产物之一[1]。中国药典2015年版二部采用薄层色谱法控制了硫酸新霉素中新霉胺的含量,方法专属性较差且分离能力较低,无法对其各组分及有关物质进行深入分析。目前文献报道测定硫酸新霉素或降解杂质新霉胺,多采用高效液相-柱前衍生化法[3-4]、高效液相-蒸发光散射法[5-6]、高效液相-脉冲安培检测法[2]。但柱前衍生化法操作繁琐,影响结果的因素较多;蒸发光散射法灵敏度较低,不利于微量杂质的检出;脉冲安培检测法,稳定性较差,色谱条件严格。电喷雾检测器是一种新型的高效液相色谱通用性检测器[1],灵敏度较高,通用。其原理是基于雾化-气溶胶的HPLC 检测器,通过Corona电晕针使氮气带电,而后将带电氮气与经干燥过的洗脱液中的溶质颗粒逆向充分混合,带电氮气的电荷转移,使溶质颗粒带电后,进入静电计检测电信号值。该检测信号响应不依赖于化合物的化学结构,与溶质质量成正比关系[7]。目前尚未见采用高效液相色谱-电喷雾检测器法测定硫酸新霉素各组分及有关物质的文献报道。
本文建立了测定硫酸新霉素中新霉素B、C、新霉胺和有关物质的高效液相-电喷雾检测法,专属性强,灵敏度较高。与现行标准收载的薄层色谱法比较,测定的杂质更多,可为硫酸新霉素的质量控制提供新的技术手段。
1 仪器与试药
1.1 仪器
Thermo Ultimate-3000高效液相色谱仪(赛默飞世尔公司);电喷雾检测器(赛默飞世尔公司);XA205DU电子天平(Mettler-toledo)。
1.2 对照品
硫酸新霉素标准品(批号:1 2 8 4 5 8,D r.Ehrenstorfer GmbH公司,新霉素B含量:80.0%,主要杂质新霉素C相对含量:9.6%,水分:0.5%),新霉胺对照品(批号:130411-200908,中国食品药品检定研究院提供),新霉素B六乙酸酯(批号:18-MAR-159-1,Toronto research chemicals公司提供),新霉素C六乙酸酯(批号:19-MAR-20-1、Toronto research chemicals公司提供)。
1.3 试剂
三氟乙酸(Fisher Scientific,批号:066963,试剂纯),水为超纯水。
1.4 样品
17批硫酸新霉素原料,分别来自企业A和B。
2 试验方法及结果
2.1 HPLC-CAD条件
色谱柱:Waters Xselect HSS T3(4.6mm×250mm,5μm),流动相:0.15mol/L的三氟乙酸溶液,流速:1mL/min,进样量:10μL,柱温:30℃,CAD检测器雾化温度:45℃。
2.2 溶液的制备
供试品溶液:取本品适量,加水溶解并稀释成浓度为1mg/mL的溶液,摇匀,作为供试品溶液。
自身对照溶液:精密量取供试品溶液1mL,置于20mL容量瓶中,用水稀释至刻度,即得浓度为0.05mg/mL自身对照溶液。
新霉胺对照品溶液:精密称取新霉胺对照品10mg,置于100mL容量瓶中,加水溶解并稀释至刻度,摇匀,作为新霉胺对照品储备溶液。精密量取2mL,置于10mL容量瓶中,用水稀释至刻度,即得2μg/mL的对照品溶液。
2.3 系统适应性试验
精密称取硫酸新霉素标准品10mg,再精密量取“2.2”项下的新霉胺对照品储备液2mL,置于10mg容量瓶中,用水稀释至刻度,摇匀,作为系统适用性试验溶液。称取新霉素B六乙酸酯对照品及新霉素C六乙酸酯对照品约1mg,分别置于10mL容量瓶中,用水溶解并稀释至刻度,摇匀,即得新霉素B与C定位用溶液。分别精密量取10μL,注入液相色谱仪,按照“2.1”项下条件分析,结果见图1~3。色谱图中,新霉素B和C的分离度为2.8,新霉素A与其周围的杂质峰也能达到基线分离,分离度为1.5,见图1,满足分析要求。
2.4 专属性试验
取溶剂水照“2.1”项下条件分析,结果显示空白溶剂不干扰样品测定,方法专属性好。
2.5 破坏性试验
取硫酸新霉素原料进行破坏,考察其降解情况。精密称取硫酸新霉素原料504.24mg,置于50mL容量瓶中,加水溶解并稀释至刻度,摇匀,作为储备液。精密量取储备液1mL,置于10mL容量瓶中,用水稀释至刻度,摇匀,作为未破坏的供试品溶液。
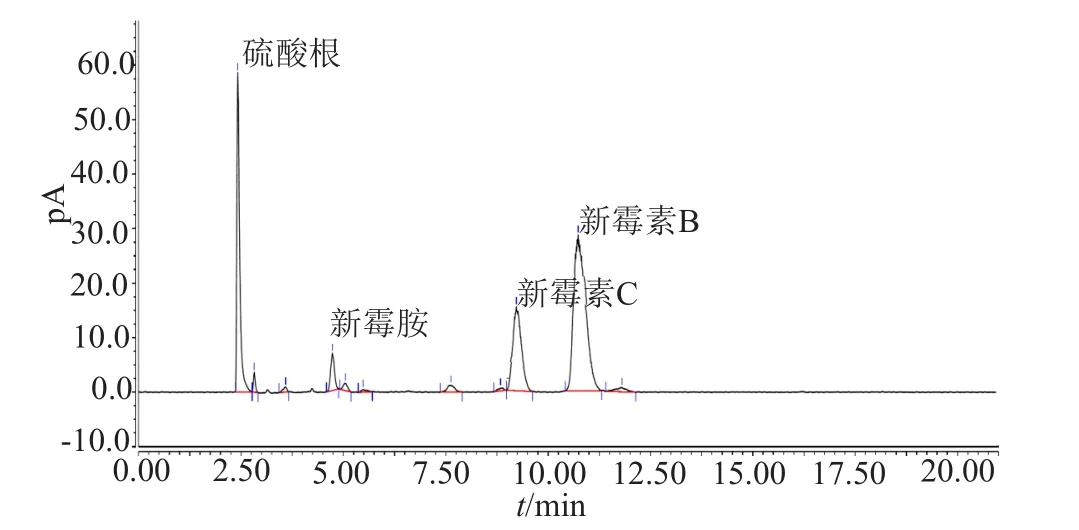
图1 系统适用性图谱Fig.1 Chromatograms in system suitability test
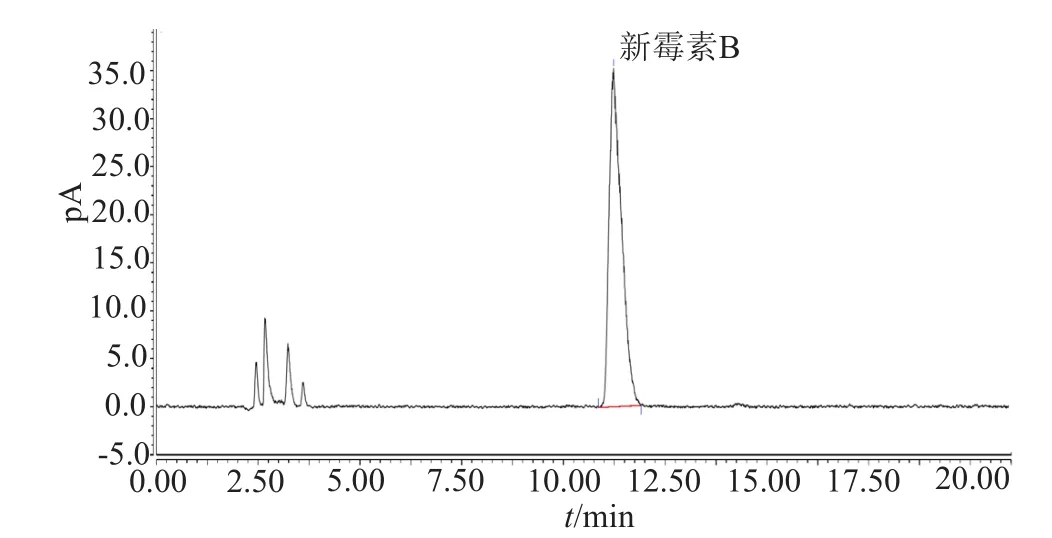
图2 新霉素B色谱图Fig.2 Chromatograms of neomycin B
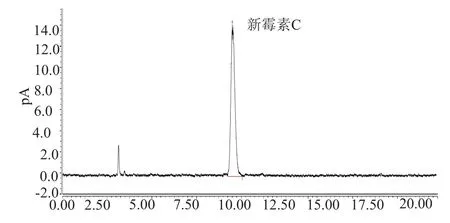
图3 新霉素C色谱图Fig.3 Chromatograms of neomycin C
(1)酸破坏:精密量取上述储备液1mL,置于10mL容量瓶中,加6mol/L的盐酸溶液1mL,放置16h后,用2mol/L的氢氧化钠中和,并用水稀释至刻度,摇匀。
(2)碱破坏:精密量取上述储备液1mL,置于10mL容量瓶中,加2mol/L的氢氧化钠溶液1mL,放置16h后,用6mol/L的盐酸中和,并用水稀释至刻度,摇匀。
(3)氧化破坏:精密量取上述储备液1mL,置于10mL容量瓶中,加双氧水1mL,放置16h后,用水稀释至刻度,摇匀。
(4)高温破坏:精密量取上述储备液1mL,置于10mL容量瓶中,置于沸水浴中加热3h后,取出,冷却,并用水稀释至刻度,摇匀。
(5)光照破坏:精密量取上述储备液1mL,置于10mL容量瓶中,置于强光4000Lx 48h后,取出,用水稀释至刻度,摇匀。
取上述溶液照“2.1”项下的色谱条件测定,图4为硫酸新霉素原料未破坏及破坏试验后的色谱图。
试验结果表明,硫酸新霉素在酸破坏的条件下,杂质新霉胺的含量增加。在氧化破坏的条件下,产生了新的降解杂质,新霉素B、C和新霉胺分别与相邻杂质的分离度为2.1和2.6、1.4和1.6、3.9和0.9。除新霉胺与其后面的杂质分离度较小外,新霉素B与C均能与破坏试验产生的杂质峰分离良好,系统基本可行。其他破坏条件下均无新的降解杂质产生,说明硫酸新霉素在碱性、高温、光照的条件下稳定。
2.6 检出限与定量限
取硫酸新霉素标准品和新霉胺对照品适量,分别加水溶解并逐级稀释成系列稀释溶液,按信噪比为3:1测定检测限,新霉素B检测限为0.02μg,新霉胺检测限为0.003μg。按信噪比为10:1测定定量限,新霉素B检测限为0.07μg,新霉胺检测限为0.012μg。
2.7 线性关系考察
2.7.1 硫酸新霉素B和C线性关系考察
精密取称硫酸新霉素标准品11.09mg,置于10mL容量瓶中,用水溶解并稀释至刻度,摇匀,作为硫酸新霉素对照品贮备液(新霉素B浓度:0.8828mg/mL,新霉素C浓度:0.1059mg/mL)。再精密量取0.1、0.2、0.4、0.5、0.6、1.6和2.0mL,分别置于10mL容量瓶中,用水稀释至刻度,摇匀,即得标准曲线溶液1~7。照“2.1”项下的色谱条件测定,结果表明新霉素B、C在测定范围内线性关系良好(表1),满足方法学要求。
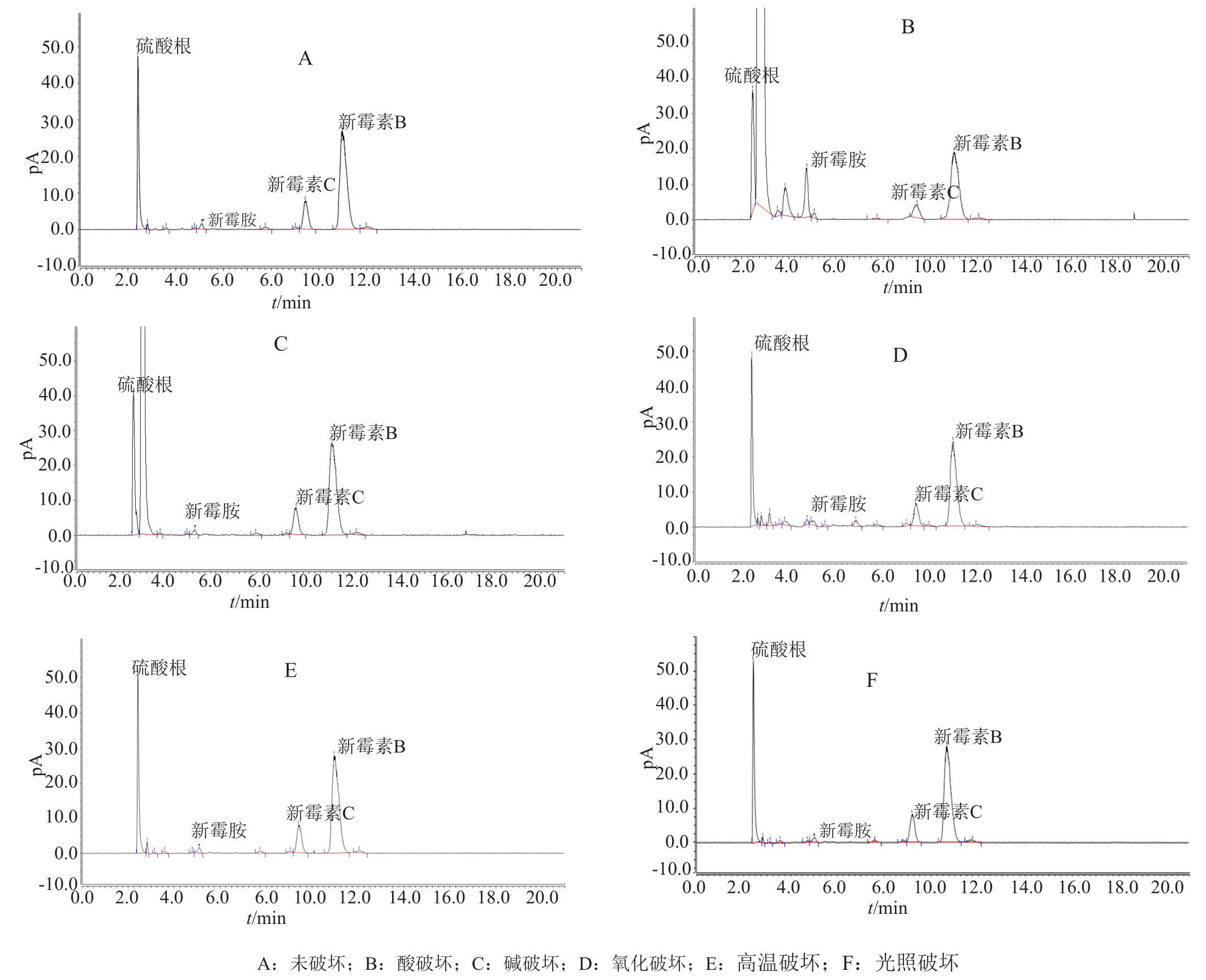
图4 供试品溶液原液及5种方式破坏溶液的色谱图Fig.4 Chromatograms of original samples solution and sample solution destroyed by fi ve ways
2.7.2 新霉胺线性关系考察精密称取新霉胺对照品10.36mg,置于100mL容量瓶中,用水溶解并稀释至刻度,摇匀,作为新霉胺对照品储备液(浓度为:0.1036mg/mL)。再精密量取0.1、0.25、0.5、1.0、1.5、2.0、2.5和3.0mL,分别置于10mL容量瓶中,用水稀释至刻度,摇匀,即得标准曲线溶液1~8。按照“2.2”项下的色谱条件测定,结果表明新霉胺在测定范围内线性关系良好(表1),满足方法学要求。
2.8 溶液稳定性考察
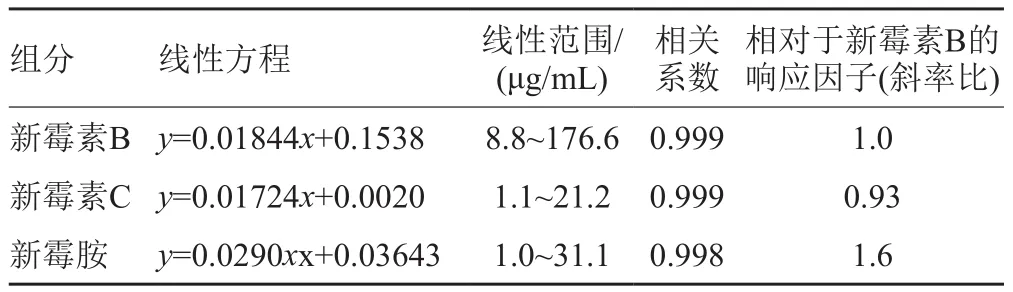
表1 线性关系实验结果Tab.1 Results of linear relationships
取供试品溶液分别在放置0、2、4、8、12和16h后进样测定,测定新霉素B、C、新霉胺的峰面积和其他杂质的总峰面积,结果表明供试品溶液在16h内稳定,新霉素B峰面积的RSD为0.8%、新霉素C峰面积的RSD为1.4%、新霉胺峰面积的RSD为1.6%、其他杂质总峰面积的RSD为4.1%。
2.9 进样精密度
分别取“2.7.1”项下的标准曲线溶液4和“2.7.2”项下的标准曲线溶液6连续进样6次,分别以新霉素B和新霉胺的峰面积考察仪器精密度,结果新霉素B峰面积的RSD为1.4%,新霉胺峰面积的RSD为1.1%,表明仪器精密度良好。
2.10 重复性实验
取一批硫酸新霉素原料分别制备6份供试品溶液,计算新霉胺的含量,结果6份样品中新霉胺含量的RSD为2.8%,符合方法学的要求。
2.11 新霉胺回收率试验
取一批硫酸新霉素原料做加样回收实验,称取9份,每份约10mg,精密称定,置于10mL容量瓶中,标记为回收率1~9,回收率1~3精密加入“2.2”项下的新霉胺对照品储备溶液1mL,回收率4~6精密加入“2.2”项下的新霉胺对照品储备溶液2mL,回收率6~9精密加入“2.2”项下的新霉胺对照品储备溶液3mL,用水稀释并定容至刻度,摇匀,即得。按上述方法进样测定,结果表明,平均回收率为93.1%(表2),符合方法学要求。
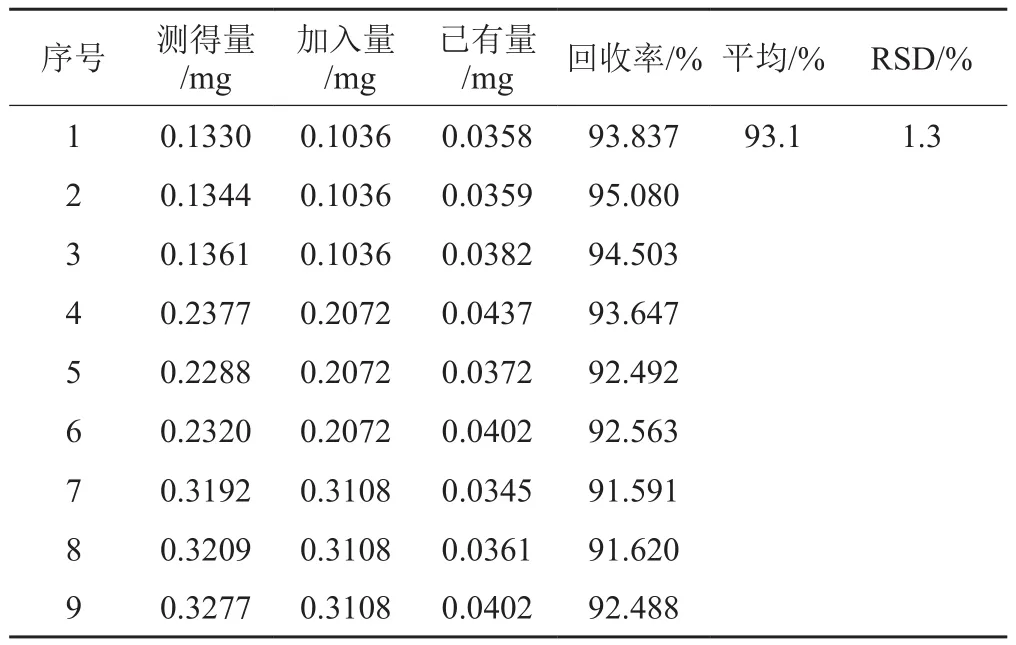
表2 回收率实验结果Tab.2 Results of recovery test
2.12 样品的测定
分别取17批原料,按“2.2”项下方法制备供试品溶液、自身对照溶液及新霉胺对照品溶液,按照“2.1”项下条件进样测定。杂质新霉胺的含量按外标法计算,新霉素C组分及其他杂质按自身对照法计算,结果见表3。
3 讨论
3.1 色谱条件的选择
硫酸新霉素是强极性化合物,极易溶于水,在反相色谱柱中几乎无保留,需采用离子对试剂提高新霉素在色谱柱中的保留行为。电喷雾检测器对流动相有特殊的要求,需采用挥发性的试剂。参考相关文献,尝试采用三氟乙酸水溶液-甲醇系统为流动相。试验发现,当有机相甲醇的比例为5%时,新霉素B和新霉素C无法分离,随着甲醇比例的减少,新霉素B和新霉素C的分离度开始增加。当用纯水相时,新霉素B和新霉素C的分离度能达到3.0左右,同时新霉胺也能与相邻杂质达到基线分离。因此,采用三氟乙酸水溶液100%作为流动相。此外,我们还对三氟乙酸的浓度进行了筛选,考察了0.1、0.15和0.2mol/L的三氟乙酸溶液,试验发现,这3种浓度的三氟乙酸均能使新霉素B和C达到基线分离,随着三氟乙酸浓度的增加,新霉素B和C的分离度也相应的增加。但当浓度为0.1mol/L时,新霉胺与相邻杂质无法达到基线分离,当浓度为0.15mol/L时,新霉胺与相邻杂质基本达到分离,分离度为1.5,当浓度为0.2mol/L时,新霉胺与相邻杂质的分离度为1.8。考察了0.15和0.2mol/L的三氟乙酸水溶液的pH值,分别为1.12和0.9,0.2mol/L的三氟乙酸水溶液对柱子的损伤相对较大。综合比较,采用0.15mol/L的三氟乙酸水溶液做为流动相。同时由于采用了酸性较强的纯水相作为流动相,本研究选择了亲水且耐酸的色谱柱Waters Xselect HSS T3(4.6mm×250mm, 5μm)对样品进行测定。
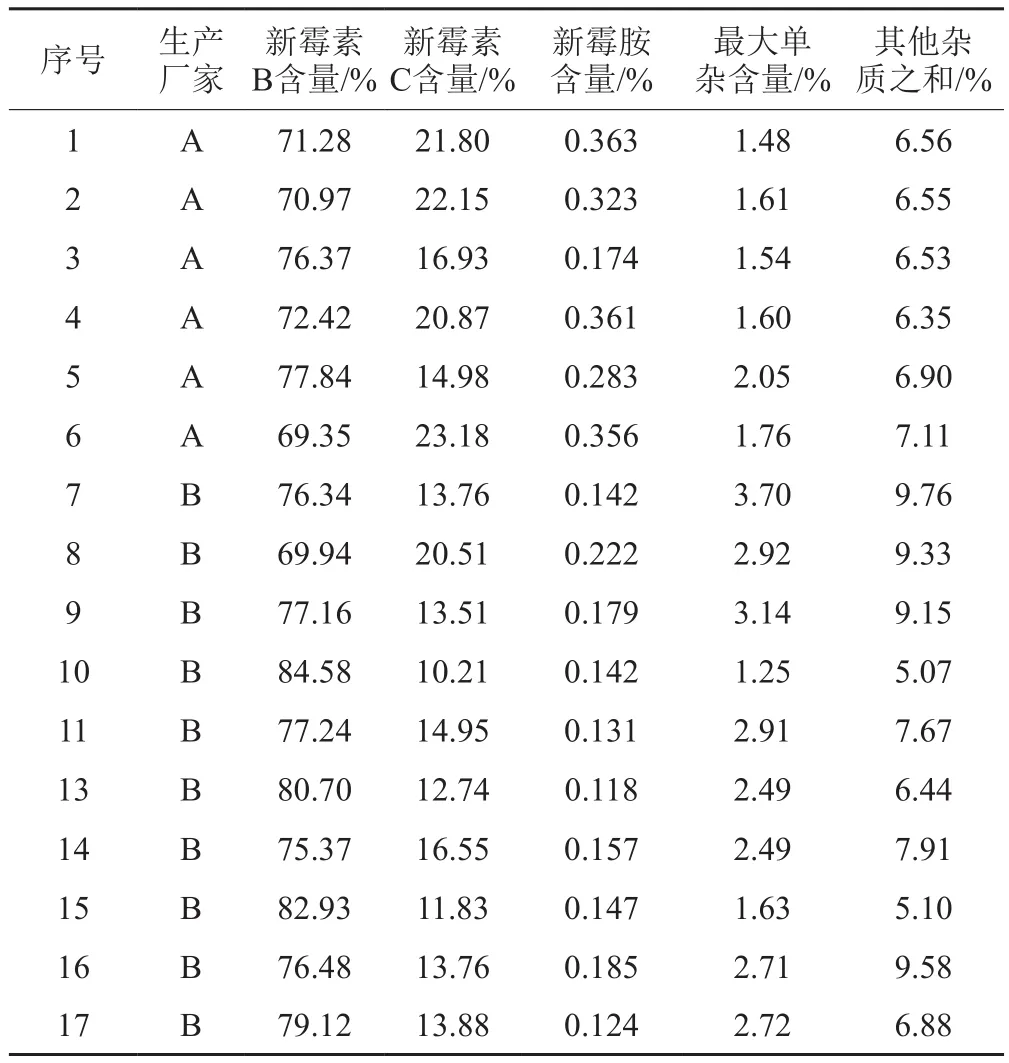
表3 样品测定结果Tab.3 Results of the determination
3.2 定量方式的选择
电喷雾检测器是继蒸发光散射检测器后的一款通用性质量检测器,它的响应值与化合物的结构无关,对质量相近的化合物响应值基本相同,在低浓度范围内响应值与浓度呈线性关系,可通过标准曲线法或外标法直接定量,无需采用双对数标准曲线[8-9]。新建立的方法中新霉素B、C和新霉胺在一个数量级内具良好的线性关系,相关系数均在0.998以上。新霉素B和新霉素C在欧洲药典中有确定结构式,两者为立体异构体[10];实验结果显示新霉素C的响应因子为0.93,与新霉素B基本一致。新霉胺和新霉素B的分子量相差较大,实验结果显示新霉胺的响应因子为1.6。因此,新霉素C的含量可根据对新霉素B对照品或标注有新霉素B含量的硫酸新霉素标准品直接进行折算;新霉胺的含量计算需用新霉胺对照品外标法计算或硫酸新霉素标准品校正因子法折算。
3.3 样品测定结果分析
利用建立的方法测定了17批硫酸新霉素原料中的新霉素B、新霉素C、新霉胺及其他有关物质。结果显示,主组分新霉素B的含量在69.35%~84.58%之间;新霉素C的含量在10.21%~23.18%之间;新霉胺的含量在0.118%~0.363%之间;其他最大单杂的含量在1.25%~3.70%之间;其他杂质总量在5.07%~9.76%之间。由于国内药典未对硫酸新霉素的组分进行控制,17批硫酸新霉素原料主成分含量变化范围过宽。欧洲药典采用高效液相-脉冲安培电化学检测法对硫酸新霉素中的有关物质进行了控制,其中新霉胺不得过2.0%,新霉素C为3.0%~15.0%,其他最大杂质不得过5.0%,其他总杂质不得过15.0%。参考欧洲药典的要求,有7批原料中新霉素C含量超过了限度。对测定结果进行分析发现,大部分样品当新霉素C含量较高时,主组分新霉素B的含量相应降低。据文献报道,新霉素是由发酵产生的多组分抗生素,新霉素B和新霉素C的比例与发酵工艺有关,主要产物新霉素B相对其他组分而言活性强、毒性低,是发酵过程中需要监测的主要组分[2]。但由于试验条件有限,没有分离到新霉素B和新霉素C的纯品进行效价的测定,具体硫酸新霉素的组分及杂质和效价的关系还需进一步深入研究。
4 小结
本文建立了测定硫酸新霉素组分B、C及有关物质的HPLC-CAD方法。该方法较现行标准方法(薄层色谱法)和ELSD法提高了灵敏度和分离度,能更好地测定硫酸新霉素的有关物质及组分。因此,新建立的HPLC-CAD方法可以更好地控制硫酸新霉素的质量,也为今后研究新霉素组分与效价之间的关系奠定了基础。
