脂必泰胶囊溶出度测定的方法研究
2019-03-29施磊,叶隽,宋磊
施 磊,叶 隽,宋 磊
(1.上海市静安区食品药品检验所,上海 200435; 2.上海市交通大学医学院附属同仁医院,上海 200050)
高脂血症是指由于脂肪代谢或运转异常使血浆中总胆固醇(TC)、三酰甘油(TG)和低密度脂蛋白胆固醇(LGL-C)中一种或几种脂质高于正常,表现为高胆固醇血症、高三酰甘油血症、混合型高脂血症[1]。临床上可为原发性或继发于其他疾病,是导致动脉粥样硬化、动脉血管内斑块形成、冠心病和脑卒中的高危因素。因此,控制血脂、改善血管内皮功能、稳定斑块成为一级预防的手段之一。脂必泰胶囊消痰化瘀、健脾和胃。主治痰瘀互结、气血不利所致的高脂血症。症见头昏、胸闷、腹胀、食欲减退、神疲乏力等。脂必泰胶囊质量标准收载于新药转正标准中药第64册。查阅文献发现,有多篇文章对脂必泰胶囊中红曲的有效成分洛伐他汀的含量测定进行了研究[2-4],没有对其溶出度进行方法学验证。本研究建立了HPLC 法测定脂必泰胶囊的溶出度,并进行了方法学验证。
1 仪器和试药
1.1 仪器
Agilent 1260系列高效液相色谱仪(包括G1311B型二元泵、G1329B型自动进样器、G4212B DAD检测器、Agilent openLAB色谱工作站,美国安捷伦),STAT智能溶出度仪(SOTAX AT7),CPA225D型电子天平(精度0.01 mg,德国赛多利斯公司)。
1.2 试剂和药品
洛伐他汀对照品(批号:100600-201504,含量为 99.4%,中国食品药品检定研究院),脂必泰胶囊(0.24 g/粒,批号:170206、160706、160511、160307,成都地奥九泓制药厂),甲醇(色谱纯,德国Merck公司),磷酸、十二烷基硫酸钠、氢氧化钠(均为分析纯,国药集团化学试剂有限公司),高纯去离子水(上海市静安区食品药品检验所自制)。
2 方法和结果
2.1 色谱条件
ZABAX-C18(250 mm×4.6 mm,5 μm);流动相为甲醇-0.05%磷酸(80∶20);流速1.0 ml/min;柱温 30 ℃;检测波长238 nm;进样量 10 μl。
2.2 溶液制备
2.2.1对照品溶液
精密称取洛伐他汀对照品溶液10.24 mg,置50 ml容量瓶中,加少量乙腈溶解并稀释至刻度,摇匀,作为储备对照溶液。
2.2.2供试品溶液
取样品(批号:170206)6粒,分别置200 ml容量瓶中,分别加1%十二烷基硫酸钠的磷酸盐溶液(pH 7.0)超声溶解,冷却,加溶剂至刻度,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,作为供试品溶液。
2.2.3阴性对照溶液
根据脂必泰胶囊处方配制,除去红曲,按生产工艺制备阴性样品,同供试品溶液制备方法,即得阴性对照溶液。
2.3 系统适应性试验
取洛伐他汀对照品溶液、供试品溶液及阴性对照品溶液,用流动相制成浓度为40 μg/ml的溶液作为系统适应性试验溶液。按“2.1”项下色谱条件测定,得液相色谱图(图1),洛伐他汀的保留时间为10.22 min,理论塔板数为10 500。结果表明,本次分析使用的色谱系统是有效、适用的。
2.4 线性关系考察
分别精密吸取按“2.2.1”项下配制的对照储备液0.2、0.5、1.0、2.0、3.0、5.0、10.0、15.0 ml,置25 ml的容量瓶中,分别加1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)稀释至刻度,摇匀,即得系列对照品溶液(浓度分别为1.63、4.073、8.143、16.29、24.43、40.72、81.44、122.2 μg/ml)。按“2.1”项色谱条件依次进样测定,记录峰面积。以峰面积为纵坐标,溶液浓度为横坐标绘制标准曲线。求得洛伐他汀的线性回归方程为:Y=30.801 1X+5.332 1,r=1.000 0,线性范围1.628 8~122.160 0 μg/ml。

图1 脂必泰胶囊的HPLC图 A.溶剂;B.对照品溶液;C.供试品溶液;D.阴性对照溶液;1.洛伐他汀
2.5 精密度试验
精密吸取对照品溶液(含洛伐他汀40.72 μg/ml),按“2.1”项下色谱条件测定,连续进样6次,记录各色谱峰的峰面积。洛伐他汀平均峰面积为1 269.41,RSD为0.11%,表明精密度良好。
2.6 稳定性试验
精密吸取溶出度项下供试品溶液,按“2.1”项下色谱条件测定,分别于0、2、4、8、12 h进样,记录峰面积,其峰面积的RSD为0.87%,表明供试品溶液稳定性良好。
2.7 加样回收率试验
取脂必泰胶囊9粒,每3粒为一组,置溶出杯中,分别加洛伐他汀标准储备液(精密称取洛伐他汀对照品31.5 mg,置50 ml容量瓶中,加溶出介质溶解并稀释至刻度摇匀,备用)1.0、2.0、3.0 ml,参照溶出度第三法,以1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)200 ml为溶出介质,转速100 r/min,依法操作。经 45 min时,取溶液适量,冷却,用0.45 μm的微孔滤膜滤过,取续滤液,进行测定,计算,结果回收率分别为101.94%、100.94%、98.53%,平均回收率为100.5%,RSD为1.7%。
2.8 溶出度试验条件的选择
2.8.1测定波长的选择
取洛伐他汀对照品适量,先用适量甲醇溶解,再用1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)稀释成适宜的浓度,在200~400 nm波长范围内扫描,结果在238 nm波长处有最大吸收,因此,选择238 nm作为检测波长。
2.8.2溶出度方法的确定
取样品(批号:170206),以1.0%十二烷基硫酸钠的磷酸盐溶液(pH 7.0)200 ml为溶出介质,参考2015年版《中华人民共和国药典》四部要求,采用小杯法,转速为100 r/min进行试验,分别于5、10、20、30、45、60 min取样测定,结果见图2。
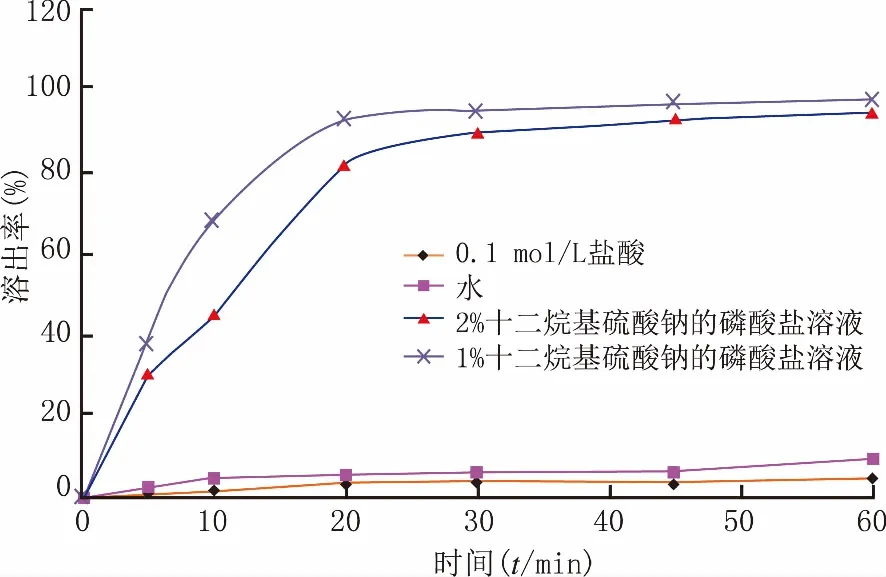
图2 不同溶出介质下脂必泰胶囊的溶出度曲线
2.8.3转速的确定
取样品(批号:170206),采用小杯法,1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)200 ml为溶出介质,转速为50、75、100、120 r/min进行实验,于45 min时取样测定,转速100、120 r/min时溶出度最大。根据2015年版《中华人民共和国药典》四部要求和洛伐他汀的溶出情况,确定转速为100 r/min。
2.8.4溶出介质的选择
取样品(批号:170206),分别以水、0.1 mol/L盐酸、1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)和2.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)为溶出介质。其中水和0.1 mol/L盐酸是常见的首选溶出介质,2.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)为2015年版《中华人民共和国药典》二部中“洛伐他汀胶囊”溶出度测定采用的溶出介质,而1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)是根据“若介质中加表面活性剂如十二烷基硫酸钠等,应尽量选用低浓度。”的原则。由于脂必泰胶囊中洛伐他汀含量较少,为保证高效液相色谱出现相对较大的色谱峰,故按照2015年版《中华人民共和国药典》四部的溶出度测定第三法,溶出介质为200 ml,转速为100 r/min,分别于5、10、20、30、45、60 min取样,测定溶出含量,结果详见图2,确定1.0%十二烷基硫酸钠的磷酸盐溶液(pH值为7.0)为溶出介质。
2.8.5取样时间的选择
取4个批号样品,采用小杯法,以1.0%十二烷基硫酸钠的磷酸盐溶液(pH 7.0)200 ml为溶出介质,转速为100 r/min进行实验,分别于5、10、20、30、45、60 min取样,测定溶出含量。由图3可见,20 min时已经达到85%以上,在30 min时溶出度都在90%以上,根据2015年版《中华人民共和国药典》四部要求和洛伐他汀的溶出情况,确定取样时间为45 min。

图3 不同取样时间下脂必泰胶囊的溶出度曲线
2.8.6样品溶出度的测定
取4批供试品,参照2015年版《中华人民共和国药典》四部附录0931的溶出度测定第三法小杯法,按“2.8.2”项下的方法进行测定,结果见表1。根据样品溶出度检查结果,限度均不得低于标示量的80%。
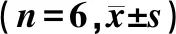
表1 样品溶出度测定结果
3 讨论
固体制剂要在人体内发挥其药效,首先要在人体内崩解、溶出后释放出药物,然后才能进一步产生作用。而预测在人体的释放吸收情况,作为体外评价样品质量、判断药物疗效的有效药学研究手段,
目前只有溶出度法最为适用。该法在当前药物的体外释放评定中应用最为广泛、便捷和准确。因此,在固体制剂的检验中溶出度检查应该成为一个必检项目。
脂必泰胶囊为复方中药制剂,国家药品标准规定其含量测定项仅为熊果酸。然而,脂必泰胶囊作为一种治疗高脂血症的药物,其主要成分是红曲,而红曲中降血脂的活性成分主要是洛伐他汀[5]。那么测定脂必泰胶囊中洛伐他汀这一成分的含量,及其在人体的释放程度就成了对其质量的一个必然考核。与脂必泰胶囊中红曲的有效成分洛伐他汀的含量测定的多篇文献相比较,本研究是采用HPLC法,测定脂必泰胶囊中红曲的有效成分洛伐他汀的溶出度,并对该溶出度的测定方法进行了方法学验证。该方法操作简便、重复性和稳定性好,结果准确,适用于测定脂必泰胶囊的溶出度。
