HPLC法测定人血浆中伏立康唑及其代谢物的浓度
2019-03-29王志君杨云云张文静王学彬宋洪杰
王志君,杨云云,张文静,王学彬,宋洪杰,王 卓
(海军军医大学附属长海医院药学部,上海 200433)
伏立康唑(voriconazole)为三唑类广谱抗真菌药,2004年被FDA批准为曲霉菌或念珠菌血症的首选药物。其抑制麦角甾醇的合成,导致细胞膜的通透性异常,促使真菌细胞死亡,从而发挥强大的抗真菌效应[1]。与其他三唑类抗真菌药相比,伏立康唑是一种耐受性良好的药物,但有肝毒性、神经毒性,同时伏立康唑的药动学个体间差异很大,主要原因是人体内的代谢酶CYP2C19具有遗传多态性,特别是亚洲人中弱代谢者的发生率高达15%~20%,同时患者自身的疾病状态或合并用药可能增加伏立康唑代谢的差异[2-7]。因此,对伏立康唑及其主要代谢物伏立康唑氮氧化物进行血药浓度监测具有临床意义。目前,用于伏立康唑血药浓度测定的方法主要包括微生物检测法、高效毛细管电泳(HPCE)法、高效液相色谱-荧光检测法和超高效液相色谱串联质谱法[8-11],考虑到临床应用的实用性和可行性,本研究建立了样品沉淀蛋白,并用HPLC-UV测定的方法,使其具有快速、灵敏、准确、稳定的特点,并可以同时测定伏立康唑及其氮氧化物,以便用于日常治疗药物监测(TDM)和个体化给药调整。
1 材料
1.1 仪器
LC-20A高效液相色谱仪(包括SPD-20A紫外检测器、SIL-20AC自动进样器、CTO-20A柱温箱日本岛津公司);C18-AR色谱柱(ACE 150 mm×4.6 mm,柱号:V12-6682);XW-80A涡旋混合器(上海琪特分析仪器有限公司);离心机(Eppendorf AG 22331 Hamburg 5452ZR858343);SQP电子天平(赛多利斯科学仪器北京有限公司);pH计(赛多利斯科学仪器北京有限公司);DL-180A超声波清洗器(上海之信仪器有限公司);1.5 ml微型离心管(EP管)。
1.2 药品与试剂
伏立康唑标准品(中国药品食品检定研究院,批号:100862-201402,含量 99.2%);罂粟碱(Cayman CHEMICAL 公司,批号:0476735-1,含量≥98%);伏立康唑氮氧化物(Toronto Research Chemicals公司,批号:7-dpm-64-3,含量97%);甲醇、乙腈(色谱纯)、氢氧化钠、磷酸二氢钠(分析纯,上海凌锋化学试剂有限公司);空白人血浆(长海医院血库)。
1.3 数据处理软件
LcSolution版本1.26 SP1(日本岛津公司)。
2 方法与结果
2.1 色谱条件
色谱柱ACE 5 C18-AR(150 mm×4.6 mm,柱号:V12-6682),以0.025 mol/L磷酸二氢钠(含三乙胺400 μl/L,用0.25 mol/L的氢氧化钠调至pH为7.0)-乙腈(67∶33)为流动相,检测波长:255、276 nm(双波长检测),流速:1.0 ml/min,自动进样器温度:4 ℃,柱温:40 ℃,进样量:20 μl。
2.2 溶液的制备
2.2.1对照品溶液
精密称取伏立康唑标准品、伏立康唑氮氧化物标准品适量,置50 ml棕色量瓶中,用乙腈溶解并定容至刻度,即得400 mg/L的标准品储备液,置2~8 ℃冰箱冷藏保存,备用。
2.2.2内标溶液
精密称取罂粟碱适量置100 ml棕色量瓶中,用乙腈溶解并稀释至刻度,得浓度为100 mg/L的内标储备液;取内标储备液5 ml置100 ml棕色量瓶中,用乙腈稀释至刻度,得浓度为5 mg/L的内标溶液,置2~8 ℃冰箱冷藏保存,备用。
2.3 血浆样品的预处理
取血浆0.3 ml于1.5 ml的EP管中,再加乙腈至1.2 ml,涡旋振荡0.5 min,13 000 r/min离心15 min,取上清液20 μl进样分析。
2.4 方法专属性试验
分别取空白血浆、加入内标溶液的空白血浆、加入伏立康唑和伏立康唑氮氧化物及内标溶液的空白血浆、使用伏立康唑的患者血浆样品,按“2.3”项下操作进行前处理,按“2.1”项下方法检测,结果发现伏立康唑氮氧化物、罂粟碱、伏立康唑保留时间分别为4.5、11.3、13.7 min,各峰分离度均大于2,理论塔板数均大于1 000,空白血浆和流动相中干扰组分的响应低于分析物定量下限响应的20%,并低于内标响应的5%,结果见图1。
2.5 线性关系考察
取空白血浆及伏立康唑和伏立康唑氮氧化物储备液以及罂粟碱储备液,将伏立康唑和伏立康唑氮氧化物浓度分别配制为0.5、1、2、5、10、15、20 μg/m1,内标罂粟碱浓度调为3.75 μg/m1的混合血浆样品。按“2.3”项下血浆样品预处理,按“2.1”项下色谱条件测定,以伏立康唑氮氧化物和罂粟碱面积的比值(F1)对血浆浓度(C1)进行线性回归(权重系数:1/C),得回归方程为:F1=0.111 1 C1+0.020 0,r=0.999 5;以伏立康唑和罂粟碱面积的比值(F2)对血浆浓度(C2)进行线性回归(权重系数:1/C),得回归方程为:F2=0.070 74C2-0.038 60,r=0.999 5。结果表明,伏立康唑和伏立康唑氮氧化物在0.5~20.0 μg/m1浓度范围内呈良好线性关系。定量限浓度为0.2 μg/ml(S/N>10)。
2.6 准确度与精密度试验
2.6.1批内回收率和精密度
分别配制定量下限及低、中、高浓度样品(0.5、1、5、15 μg/m1)的质控(QC)血浆样品,每个浓度取5个样本,按“2.3”项方法操作,测定。根据当日的标准曲线测定QC样品的相对回收率,伏立康唑:101.3%、103.8%、94.2%、91.7%(RSD分别为6.2%、4.4%、4.7%、1.4%,n=5),伏立康唑氮氧化物:106.8%、100.1%、94.3%、91.6%(RSD分别为6.2%、4.8%、4.7%、2.1%,n=5)。
2.6.2批间回收率和精密度
分别配制3批的定量下限及低、中、高浓度样品(0.5、1、5、15 μg/m1)的QC血浆样品,每个浓度取5个样本,按“2.3”项方法操作,分3 d进行测定,测定结果的峰面积代入相应的当日标准曲线,计算QC样品的回收率,伏立康唑:97.9%、99.6%、102.6%、101.6%(RSD分别为9.2%、5.9%、3.3%、3.6%),伏立康唑氮氧化物:100.9%、100.0%、97.3%、98.7%(RSD分别为9.3%、6.4%、5.9%、6.7%)。
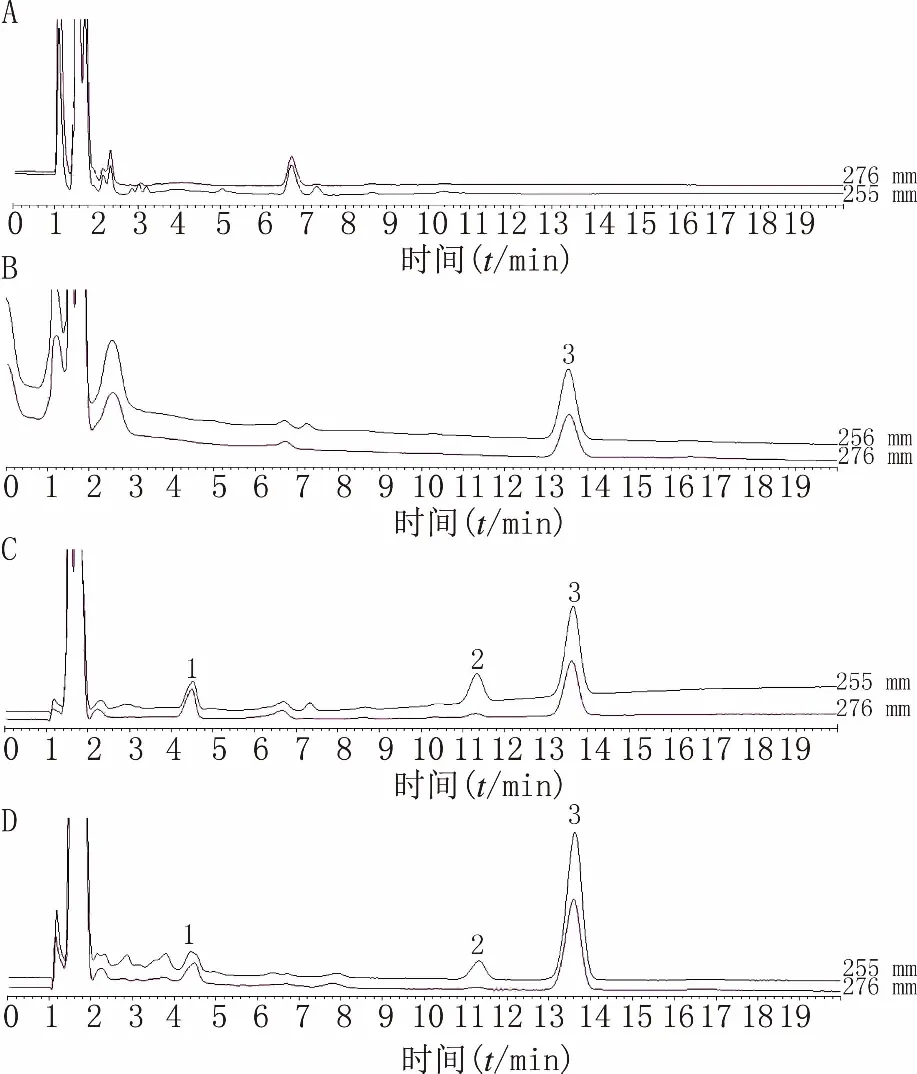
图1 伏立康唑和伏立康唑氮氧化物的专属性色谱图 A.空白血浆;B.空白血浆+内标;C.空白血浆+伏立康唑对照品+伏立康唑氮氧化物对照品+内标;D.患者血浆+内标 1.伏立康唑氮氧化物;2.伏立康唑;3.罂粟碱
2.7 稳定性试验
2.7.1工作溶液
取伏立康唑和伏立康唑氮氧化物乙腈溶液,配成0.5、2.0、15 μg/m1浓度系列,以及罂粟碱乙腈溶液1.0 μg/m1,按“2.1”项下方法处理进样,分别于日内和日间进样测定,计算日内和日间误差。结果显示,伏立康唑日内(0、2、4、6、8 h)和日间(3 d)测得浓度的RSD分别为1.6%和1.2%;伏立康唑氮氧化物日内(0、2、4、6、8 h)和日间(3 d)测得浓度RSD分别为1.5%和2.0%;罂粟碱测得浓度RSD为1.5%。伏立康唑、罂粟碱和伏立康唑氮氧化物的乙腈溶液3 d内稳定性良好。
2.7.2血浆样品
制备伏立康唑和伏立康唑氮氧化物低、高浓度(含伏立康唑氮氧化物和罂粟碱)的血浆样品,分别进行:①反复3次冻融 (-20~25℃)稳定性试验;②含药血浆样品(-20℃)放置1个月稳定性试验;③血浆样品处理后48 h稳定性试验;④血浆样品自动进样器中(4℃)放置24 h稳定性试验;⑤样品常温放置24 h稳定性试验。按“2.3”项方法操作,每个浓度取5个样本,测定结果的峰面积代入相应的当日标准曲线,计算准确度。结果由表1可见:血浆样品反复冻融3次后稳定性良好;血浆样品在-20℃条件下至少可以保存1个月;血浆样品处理后可在室温下保存48 h;处理后的血浆样品在自动进样器中(4℃)、室温中至少可保存48 h。
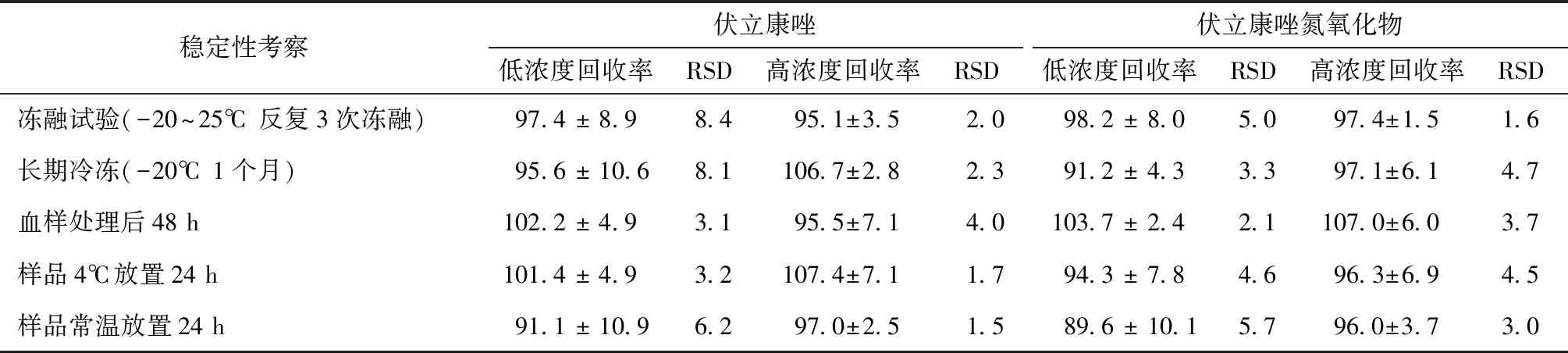
表1 稳定性试验结果(n=5,%)
2.8 临床标本测定应用
取血液科服用伏立康唑(同时服用环孢素A)的临床患者的血液样品(采用EDTA抗凝管,取血量2~3 m1),3 000 r/min离心5 min,取血浆300 μl,加5 mg/L的内标溶液至1 200 μl,涡旋振荡0.5 min,13 000 r/min离心15 min,取上清液20 μl进样分析,根据当日标准曲线定量。10例患者中,伏立康唑血药浓度在0.49~5.2 μg/m1;伏立康唑氮氧化物血药浓度在0.43~5.5 μg/m1;伏立康唑血药浓度/伏立康唑氮氧化物血药浓度的比值在0.63~20之间。在本研究过程中1名患者使用伏立康唑后,临床医生根据其血液样品监测结果对患者进行2次给药方案调整,最终使伏立康唑血药谷浓度在有效浓度范围内(1~5 μg/m1),具体监测结果见表2。在此过程中,通过TDM监测,临床医生及时调整给药方案,避免低效治疗并降低发生不良反应的风险。
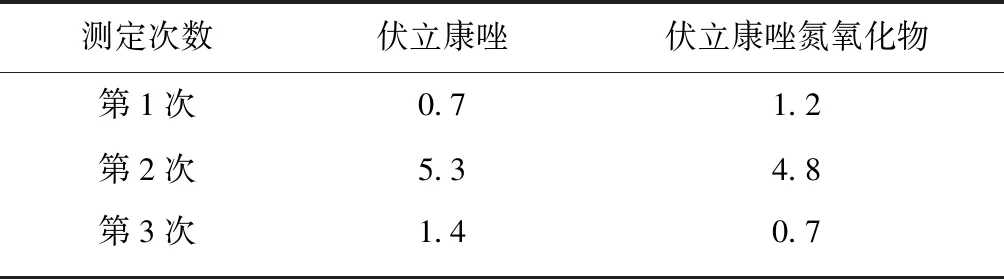
表2 患者血药浓度监测结果(ρB/μg·ml-1)
3 讨论
3.1 检测指标成分的选择
伏立康唑主要在肝脏通过CYP450的同工酶CYP2C19代谢,主要代谢产物为无抗菌活性的伏立康唑氮氧化物,血浆中约占72%。CYP2C19酶呈基因多态性,其在不同人种、不同基因型患者的伏立康唑代谢具有明显差异。在给予相同剂量伏立康唑后,因代谢的明显差异,导致体内血药浓度变化较为明显,从而引起治疗效果不佳或者不良反应增加。本研究拟考察伏立康唑和伏立康唑氮氧化物的浓度来提高治疗效果,从而达到精准治疗的目的。同时为下一步拟合CYP2C19酶多态性及伏立康唑、伏立康唑氮氧化物浓度的关系提供数据基础。
3.2 流动相的选择
伏立康唑是三唑类化合物,采用甲醇-乙腈溶剂系统流动相,干扰现象比较严重,在流动相中加入适量盐和三乙胺可抑制其拖尾,改善峰形。本研究曾分别考察了加入不同比例三乙胺、磷酸二氢钠、氢氧化钠调节pH值对峰形的影响。发现0.025 mol/L磷酸二氢钠(三乙胺400 μl/L,用0.25 mol/L氢氧化钠调至pH=7.0)-乙腈(67∶33)作为流动相时,峰形对称,分离效果较好,检测时间适宜,从而选择其作为流动相。
3.3 提取溶媒的选择
本研究采用以乙腈为沉淀剂的蛋白沉淀法处理血液样品。采用此方法时,干扰组分的响应低于分析物定量下限响应的20%,并低于内标响应的5%,按照《中国药典》四部通则9012生物样品定量分析方法验证指导原则,可作为提取方法。
3.4 检测波长的选择
255 nm、276 nm分别为伏立康唑和伏立康唑氮氧化物的最大吸收波长,在测定部分患者血液样品时发现:检测波长为276 nm时,伏立康唑氮氧化物的干扰小,测定准确性好;检测波长为255 nm时,伏立康唑的响应值高,精密性好,所以选择双波长检测。
3.5 临床标本的测定
由于血液科用药品种多,用药方案多变,本研究采用常见的环孢素A+伏立康唑的患者作为对象,文献报道[12]:环孢素A和伏立康唑具有相互作用,伏立康唑影响环孢素A的血药浓度,同时两者均有肝毒性,本研究拟通过监测患者(同时使用环孢素A药物)伏立康唑和伏立康唑氮氧化物的血药浓度,为个体化给药方案提供数据支持,为降低血液科患者这一特殊人群发生不良反应的风险做前期的研究准备工作。
