超声引导下竖脊肌平面阻滞用于骨质疏松椎体压缩性骨折的疼痛治疗效果
2019-03-23高巍巍王伍超葛衡江陈力勇
张 俊,高巍巍,王伍超,葛衡江,陈力勇
随着人口老龄化,骨质疏松症发病率呈明显上升趋势,骨质疏松性骨折是中老年最常见的骨骼疾病,其中以椎体压缩性骨折(OVCF)最为常见。疼痛是骨质疏松性压缩性骨折的主要临床表现。超声引导下竖脊肌平面阻滞(erector spinae plane block)是一种新兴的神经阻滞方法,由Forero等[1]于2016年首次报道用于胸部神经病理性疼痛治疗,随后被应用于多种胸腹部的术后镇痛及疼痛治疗。本研究以2017年4月—2018年4月陆军军医大学大坪医院疼痛科收治的OVCF住院患者作为研究对象,旨在探究超声引导下ESP阻滞用于OVCF患者的疼痛治疗的效果,并与传统非手术治疗进行比较。
临床资料
1一般资料
纳入笔者医院疼痛科门诊以“骨质疏松伴椎体压缩性骨折”收治入院的患者42例,均完善全脊柱MRI检查,提示椎体压缩程度在1/3~2/3。男性8例,女性34例;年龄59~86岁,平均75.1岁;BMI 14.5~30.1kg/m2。采用随机数字表法分为ESP组和对照组,每组各21例。入院时病程3~26d。骨折椎体1~4个。纳入标准:入院后影像学确诊为OVCF,且经3d口服镇痛药物治疗疼痛数字评分法(NRS)评分≥5分患者。排除标准:经3d药物治疗后NRS评分≤4分、凝血功能异常、穿刺部位感染、椎间盘突出、脊柱肿瘤、严重心脏和肺部疾病、严重糖尿病、肝肾功能不全或精神疾病患者。剔除研究过程中疼痛科住院时间<7d或出院后失访患者。
2治疗方案
对照组:仅进行基础治疗。住院期间除必要的日常活动外,均卧床休息。口服镇痛药物:氨酚曲马多(每片含:盐酸曲马多375mg,对乙酰氨基酚325mg)0.5片,口服3次/d。抗骨质疏松药物:碳酸钙颗粒3g,口服1次/d;阿发骨化醇软胶囊1μg,口服1次/d;阿仑磷酸钠片70mg,口服1次/周。疼痛部位局部物理治疗:微波炎症治疗20min,1次/d;双氯芬酸二乙胺乳胶剂超声药物离子导入30min,1次/d。支架固定:依据身高体重定制胸腰段固定支具,下床活动时佩戴。
ESP组:基础治疗部分采用与对照组相同的治疗方案,包括药物、物理治疗和支具固定的种类、剂量及频次。在基础治疗的基础上,于入院第4天及第6天行ESP阻滞治疗。ESP阻滞:在超声引导下行ESP阻滞。暴露腰背部皮肤,定位并标记骨折椎体,当影像学提示多个椎体骨折时,体格检查选择疼痛的责任椎体。常规消毒铺巾,行胸段ESP阻滞(图1):患者取俯卧位或坐位,使用超声(日本,柯尼卡美能达株式会社,SONIMAGE HS1)高频线阵探头(L18-4,4~18MHz)于正中横断面扫描骨折椎体。探头向一侧外移2~3cm,上下滑动或偏移调整探头,寻找责任椎体横突。图像上清晰显露斜方肌、菱形肌、竖脊肌、棘突、横突、胸膜。局麻后,以超声探头外侧1cm作为穿刺点,使用一次性麻醉穿刺针(驼人医疗器械,型号:AN-N,规格:0.7mm×90mm),采用平面内进针技术,避开血管,向横突表面缓慢进针,针尖到达横突表面后,回抽无血无气,间断回抽缓慢注射药液20mL,同时观察到药液在竖脊肌深面及横突表面扩散。行腰段ESP阻滞(图2):患者取侧卧位,选择凸阵探头(C5-2,2~5MHz),采用“三叶草”法,探头置于肋缘下方及髂嵴上方之间的腋中后线之间,横断面扫描椎体,超声图像上显露竖脊肌、腰方肌、腰大肌、横突、部分椎体。脊柱旁5~7cm作为穿刺点,平面内进针,针尖到达腰椎横突后以胸段同样方式注射药液。药液组成为1%盐酸罗哌卡因(AstraZenecaAB, 75mg/10mL) 6mL、复方倍他米松注射液(MSD Mercksharp&Dohme AG,1mL,二丙酸倍他米松5mg,倍他米松磷酸钠2mg)0.3mL、甲钴胺注射液(日本卫材株式会社,1mL:0.5mg)1mL、生理盐水12mL,注射前无菌混合制成。一侧ESP阻滞完成后,患者吸氧、冰盐水法测定阻滞范围,心电监护观察15min无明显不适后以同样方式完成对侧ESP阻滞。ESP组所有患者ESP阻滞均由同一位具有超声引导下神经阻滞资质和经验的操作者完成。
两组患者治疗过程中若出现较严重疼痛,且评估NRS≥5分时,均使用曲马多100mg臀大肌肌肉注射缓解疼痛,但进行NRS疼痛评分前2h内不进行曲马多肌注。两组患者出院后继续同前口服药物方案及支具固定。ESP患者出院后若出现较严重的疼痛,返回门诊经评估NRS评分≥5分时,可行同前双侧ESP阻滞。
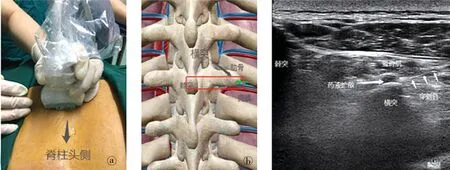
图1胸段ESP阻滞。a.横断面扫查探头位置;b.红色矩形示超声探头放置位置,绿色箭头示进针方向;c.胸段竖脊肌平面阻滞超声声像图
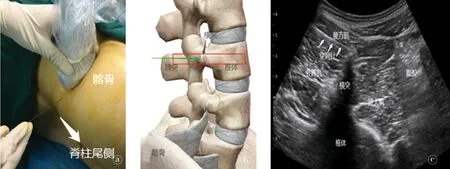
图2腰段ESP阻滞注。a.横断面扫查探头位置;b.红色矩形示超声探头放置位置,绿色箭头示进针方向;c.腰段竖脊肌平面阻滞超声声像图
3观察指标
采用NRS评分法[2]评估患者入院时(T1)、第4天ESP阻滞前(T2),阻滞后2h(T3)、8h(T4)、第5天(T5)、第6天ESP阻滞前(T6)、阻滞后8h(T7)、第7天(T8)、出院后21d(T9)疼痛程度,对照组于相同时间评估NRS评分;采用匹兹堡睡眠指数(Pittsburgh sleep quality index,PSQI)[3]评估患者第3天、出院后21d夜间睡眠指数;记录患者第4~7天肌注曲马多需求总次数。
4统计学分析

结 果
本研究初始纳入患者42例,ESP组1例因经济因素住院时间<7d退出本研究,对照组1例住院期间转入脊柱科行手术治疗退出本研究。最终纳入本研究患者40例进行数据分析。每组20例。两组患者各项一般资料比较(表1),差异无统计学意义(P>0.05),具有可比性。
ESP组患者中,行第一次ESP阻滞后2、8、24、48h(3.2±0.8~4.3±0.7)和第二次ESP阻滞后8、24h(4.0±0.6~4.3±0.8)及出院后21d(3.9±0.6)与入院时(6.8±0.6)和阻滞前(5.8±0.6)对比NRS显著降低(P<0.01),出院21d夜间睡眠质量指数(6.6±2.9)显著低于阻滞前(15.5±5.0)(P<0.01);与对照组对比,ESP组在ESP阻滞后(3.2±0.8~4.3±0.7)各时间点NRS评分显著低于对照组(3.9±0.6~5.3±0.6)(P<0.05)(见表2),夜间睡眠质量ESP组(6.6±2.9)显著低于对照组(9.8±3.0)(P<0.05)(见表3),肌注曲马多需求次数ESP组(0.6±0.6)显著低于对照组(3.6±1.2)(P<0.01)。ESP组所有患者行ESP阻滞均未见出血、血肿、感染、气胸、血气胸、局麻药毒性反应等不良反应。

表1 两组患者一般情况比较

表2 两组治疗前后NRS评分
ESP组内,第4天阻滞后各时间点评分显著低于阻滞前(*P<0.01);两组比较,ESP组阻滞后各时间点NRS评分低于对照组:#P<0.01,△P<0.05

表3 两组患者匹兹堡睡眠指数
ESP组内患者出院后21d睡眠指数显著低于第3天(*P<0.01);两组患者比较,出院后21d,ESP组睡眠指数低于对照组(#P<0.05)
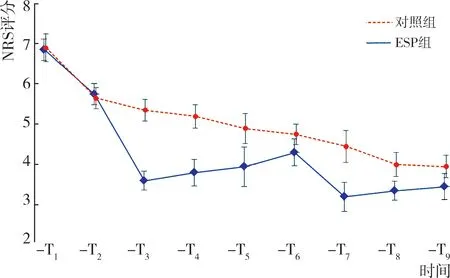
图3 两组患者平均NRS评分,误差线表示95%置信区间
讨 论
骨质疏松性骨折是老年最常见的骨骼疾病,也是骨质疏松症的严重阶段,其中以骨质疏松性椎体压缩性骨折(OVCF)最为常见。据计算我国每年大约有180万例新发与骨质疏松相关的椎体骨折,预计至2050年骨质疏松性椎体骨折患者数将高达4 850万[4]。
OVCF的主要临床表现有腰背部急慢性疼痛、相应神经分布区域的放射痛、后凸畸形、身高下降等,其中以腰背部疼痛为主要临床表现[5]。其疼痛产生的主要机制为:(1)骨骼因素:骨折直接刺激骨膜或邻近组织的感觉神经而引起疼痛,椎体内压力增加,压迫神经末梢引起疼痛[6];(2)神经因素:骨折导致椎间盘和椎体附件移位,如椎间孔等变形,脊神经根和窦椎神经受牵拉压迫、炎症反应、缺血和缺氧等刺激,引起局部疼痛和牵涉痛[7-8];(3)软组织因素:骨折椎体失去对周围组织的支撑和保护,前柱承重向后部转移,后方负荷增加,使椎间盘、关节突关节及邻近韧带和肌肉等受损[9-10];(4)骨质疏松性疼痛:破骨细胞溶骨、骨小梁微骨折等。椎体压缩性骨折所致疼痛较常发展为慢性疼痛,在椎体压缩性骨折的治疗中,对疼痛尽早的控制及管理尤为重要,可避免长时间卧床,有利于提高患者生活能力及生存质量、降低病死率、减少并发症,如肺部感染、压疮、肌肉力量丢失等。
目前压缩性骨折的治疗主要有非手术治疗和微创手术治疗。非手术治疗主要包括卧床休息、镇痛、抗骨质疏松治疗、支具外固定、物理治疗等。Venmans等[11]研究在发生压缩性骨折后6个月疼痛可显著缓解,但尽管使用高阶梯的镇痛药物,仍有40%接受非手术治疗的患者存在影响日常生活的疼痛,相当比例的患者即使使用最优的药物和支持治疗仍然无法控制。Klazen等[12]研究显示,1/3的患者在骨折发生后2年内持续存在需要药物和物理治疗的疼痛。微创手术治疗包括经皮椎体成形术(PVP)和经皮椎体后凸成形术(PKP),现已成为治疗急性椎体压缩性骨折疼痛方面疗效确切的流行术式[13],但其临床价值和适应证方面仍存在争议。美国介入放射学学会标准化委员会指南推荐椎体成形仅作为非手术治疗失败患者的治疗措施[14]。Xie等[15]对1 231例患者进行了2周~2年的13项随机对照研究的Meta分析指出,手术治疗与非手术治疗相比,患者的RDQ心理评估量表(Readiness for Discharge Questionnaire Scale)、健康相关生活质量(ED-5Q)量表评价及邻近椎体骨折发生率均无差异。Lee等[16]通过对259例骨质疏松压缩性骨折的研究分析,PVP及PKP手术治疗效果仅在术后1个月内优于非手术治疗,其效果1个月后与非手术治疗无显著差异。Firanescu等[17]研究表明PVP在缓解疼痛和改善生活质量方面并不优于假手术组。因此,无论是微创手术治疗或非手术治疗,在压缩性骨折患者的疼痛治疗方面都不够理想。在中国,由于医疗资源的分布、对疾病的认识程度及医疗费用等因素,非手术治疗仍为主要的治疗方式。
神经阻滞技术作为疼痛管理的常用方法,在多种神经病理性疼痛及创伤性疼痛方面有着独特的优势,相比微创手术治疗,创伤更小,更易于实施。目前国内外将神经阻滞用于OVCF疼痛治疗的报道主要有以下几种方式,腰椎背根内侧支神经阻滞和射频消融[18-19]、脊神经后支阻滞和射频治疗[20]、背根神经节阻滞[21]、选择性神经根阻滞[7]、关节突关节阻滞[22]等,均有较好疗效。但上述方法均为X线引导下完成,且尚缺乏大样本的临床研究证实其有效性。Forero等[1]在2016年首次报道将竖脊肌平面阻滞(erector spinae plane block)用于胸部神经病理性疼痛的治疗。随后,相继有报道ESP阻滞用于胸部手术、肋骨骨折等多种胸腹部创伤性疼痛的治疗。本研究在OVCF治疗上首次引入超声引导下的神经阻滞,且率先尝试将ESP阻滞用于治疗OVCF。
ESP阻滞在超声引导下穿刺并将药液注入竖脊肌深面及横突浅面,沿筋膜扩散至临近多节段的软组织、神经、和小关节等,发挥镇痛及消炎作用。胸段竖脊肌阻滞首先作用于脊神经后支,阻滞支配背部内侧肌肉及皮肤的神经;向内扩散可通过肋横突孔到达椎旁间隙,阻滞脊神经前支、后支、交通支及交感链,并有一定概率进入椎间孔到达硬膜外腔[23];向外侧沿肋间隙扩散阻滞脊神经前支(肋间神经),阻滞支配胸部侧面及前面的神经;沿脊柱方向,药物可扩散至多个椎体节段,使作用范围增加[1]。 Ivanusic 等[24]通过新鲜尸体研究进一步证实,ESP阻滞药物扩散具有很广的分布范围,从头侧向尾侧、由中线至外侧、竖脊肌浅面及深面都有扩散,对脊神经前支和后支都有很好的染色,对胸部背面及侧面有多层次阻滞的镇痛效果。腰段竖脊肌阻滞作用机制与应用报道较少,相关影像学研究表明,在L5水平行ESP阻滞时,药物可作用到不同节段的椎体后方、椎间孔、腰大肌间隙,对L4~5脊神经、股神经和闭孔神经都有明显效果,其用于髋关节和股骨近端的手术镇痛效果也被肯定[25],腰段ESP阻滞可对阻滞相应邻近多个节段的脊神经及其分支有良好的阻滞效果。
与其他神经阻滞比较,ESP阻滞穿刺针到达横突浅面注射药物,与椎旁相比穿刺层次更为表浅,路径更短,与胸膜及血管距离更远,故而安全性更高。与经椎板阻滞相比,药物可很好地向外侧扩散,对脊神经前支有更好的阻滞效果,药物进入椎旁间隙能力更强[23]。与前述各种神经根及分支阻滞相比,阻滞范围更广,在超声图像上具有更好的辨识度,不需辨认细小的神经组织,操作更加简易,且具有可实时观测药物扩散至目标层次的优点。
本研究行ESP阻滞术所注射的药物包含局麻药、皮质激素和维生素B12,对骨折及邻近部位具有镇痛、消炎、营养神经作用,罗哌卡因可阻断受累神经痛觉传导迅速止痛、扩张血管、改善局部循环,减少氧自由基的释放,减轻炎症反应和细胞损伤;甲钴胺可修复神经鞘膜,改善神经功能;复方倍他米松具有抗炎、抗免疫和镇痛作用,缓解神经根的炎性水肿及变性,同时降低因炎性刺激等因素所致痛觉敏感性增高,提高疼痛阈值,显著减轻疼痛[7,26]。
本研究中,ESP组患者在采用ESP阻滞后30min内疼痛即明显缓解,2h镇痛达到最大效应,8h后NRS评分逐渐上升,但阻滞后48h时NRS评分仍显著低于阻滞前(P<0.01)。第2次ESP阻滞后镇痛效果进一步加强,第2次阻滞后8h与第1次阻滞后8h相比具有更低的NRS评分(P≤0.05)。出院后21d NRS评分仍然维持在出院时水平,且与单纯非手术治疗相比,具有更好的疼痛治疗效果(P<0.05,P<0.01,表2、图2)。次要转归方面,睡眠质量改善显著(P<0.05)、阿片类药物使用明显更少(P<0.01)。
ESP组有2例患者在出院后21d内疼痛加重,返回门诊经评估NRS评分为5分和6分,该2例患者出院时NRS评分为2分和3分。由于疼痛程度明显缓解,患者出院后未加强卧床休息,1例出院后进行了常规的社区内活动,该患者疼痛从出院后第5天逐渐加重,于第8天停止社区内活动,但疼痛未缓解。另1例为出院后第6天站立打喷嚏时疼痛突然加重,休息6h后疼痛未缓解。回顾这2例患者病史,患者骨折后病程较短,第1次入院时为2d和4d。笔者推测,由于早期疼痛的治疗效果显著,但新鲜骨折仍然稳定性较差,患者活动能力提升,较多的活动可能增加骨折压缩程度和局部炎症反应,甚至可能导致新发的骨折,这可能是患者出院后疼痛加重的原因。因此,建议在良好的疼痛治疗基础上,新鲜骨折仍然需要更多时间的卧床休息,对于早期的功能锻炼,需以短时间低运动量为适,且可较长时间佩戴外支具,减少骨折椎体的应力与移位。该2例患者返回门诊后,均行如前ESP阻滞1次,嘱回家卧床休息,后期随访观察,2例患者疼痛显著缓解,未再明显加重。
对于影像学观察到存在椎体压缩的患者,根据压缩程度从轻度至重度,其存在临床症状患者仅占总体4.7%~28.4%[27],2/3的具有椎体压缩改变的患者为无症状性OVCF,或为轻度疼痛未达到需要临床干预的程度[28]。或许椎体压缩变形本身并非临床上OVCF患者疼痛的主要原因,特别是在慢性疼痛的形成方面,随着病程进展,骨折椎体逐渐稳定,其疼痛的主要原因可能为前所述来自于椎体后方的神经因素和软组织因素。一项针对椎体成形术后仍然存在疼痛患者的研究支持这一观点,大部分PVP术后仍存在疼痛的来源为腰骶部或关节突关节,该研究124例患者在进行了关节突关节阻滞之后疼痛均缓解[22]。 Firanescu等[15]将PVP术中注射骨水泥和局麻药对比研究显示两组患者疼痛均明显缓解,注射局麻药效果与骨水泥植入无明显差异。故笔者认为,ESP阻滞用于OVCF疼痛治疗效果是很有发掘潜力的,其意义在于针对疼痛发生机制,减轻神经根及周围水肿和炎症反应,缓解椎体后方软组织因素所致疼痛,打破炎症-疼痛恶性循环,使之转变为无症状性OVCF,阻止其发展为慢性疼痛,配合基础镇痛和抗骨质疏松治疗而发挥近远期的疗效。
由于试验设计的局限及其他因素限制,许多关于ESP阻滞和其用于OVCF的治疗上仍存在较多疑问,如药物的浓度与剂量选择、与其他神经阻滞方式的比较、病程对神经阻滞效果的影响、胸段与腰段ESP阻滞效果的比较等问题,期待有进一步的研究阐明。
