索磷布韦联合达拉他韦治疗慢性丙型病毒性肝炎
2019-03-22朱海超徐艳琴郭遂成甘建和
朱海超,徐艳琴,郭遂成,黄 普,甘建和
[作者单位]473007河南南阳,南阳医学高等专科学校第一附属医院消化内科(朱海超,徐艳琴,郭遂成,黄普);215006江苏苏州,苏州大学附属第一医院感染病科(甘建和)
2006年全国血清流行病学调查显示,我国HCV感染者约有1000万;随着医务工作者及公众对丙肝的认知度提高,近年来丙肝检出率的不断提高[1]。 在直接抗病毒药物 (direct-acting antiviral agents,DAAs)上市前,聚乙二醇干扰素+利巴韦林(PR)方案一直为丙型肝炎的标准治疗方案;由于PR方案疗程长,存在乏力、骨髓抑制、抑郁、失眠、溶血等诸多不良反应,这些导致丙肝患者抗病毒治疗的依从性差,故仅有部分患者接受抗病毒治疗[2]。随着DAAs类药物的研发成功及上市,丙肝治疗跨入了无干扰素的新时代[3]。由于国外原发研制的DAAs类药物价格昂贵、尚未在国内上市等诸多原因,在现实当中,我国很多患者通过各种途径获取国外仿制药物。由于对该类药物的使用缺乏经验,安全用药成为一个现实又迫切的问题;因此笔者所在课题组针对仿制药的疗效及安全性评价展开研究,以期为患者用药安全性提供指导。
1 资料与方法
1.1 研究对象 收集2016年1月—2017年1月在南阳医专一附院住院、并使用DAAs治疗的68例慢性丙型肝炎患者的临床资料,进行回顾性分析。其中男 30例,女 38例;年龄 30~70岁,平均(54±9.14)岁。肝功能正常者11例,慢性肝炎43例,肝硬化代偿期8例,肝硬化失代偿期6例;诊断标准参照丙型肝炎防治指南(2015更新版)[4]。其中初治患者63例,干扰素经治(停药复发/干扰素不耐受)患者5例。丙肝病毒基因分型:1b型41例(60.29%),2a型 27例 (39.71%);HCVRNA 载量为 5.60E+03~5.90E+07 IU/ml。
1.2 治疗方案 所有患者均口服索磷布韦片(Sofosbuvir SOF)联合达拉他韦片(Daclatasvir DCV)抗病毒治疗。药品来自印度NATCO公司,由患者自行代购方式获取。非肝硬化患者采用12 W方案,口服SOF 400 mg/d+DCV 60 mg/d,疗程12 W;肝硬化患者采用24 W方案,口服SOF 400 mg/d+DCV 60 mg/d,疗程24 W。治疗结束后随访12 W。
1.3 观察指标 (1)疗效观察指标:治疗过程中监测血清HCVRNA及肝功能,HCVRNA载量采用RT-PCR法,最低检测下限为15 U/ml。观察快速病毒学应答(rapid virological response,RVR):抗病毒治疗后4 W时血清HCVRNA低于检测下限;治疗结束时病毒学应答 (end treatment virological response,ETVR):抗病毒治疗结束时HCV RNA低于检测下限;持续病毒学应答 (sustained virologic response,SVR)抗病毒疗程结束后12 W时血清HCV RNA低于检测下限。(2)安全性指标:比较治疗前后的血常规、肾功能、心肌酶变化,及头痛、乏力、腹泻等不良反应发生率。
1.4 统计学处理 采用Excel 2003和SPSS 16.0软件进行统计分析。计量资料采用(±s)表示,治疗前后差异性比较采用自身配对t检验;计数资料用率(%)表示,两组率的比较采用χ2检验。P<0.05为差异具有统计学意义。
2 结果
2.1 病毒学应答 抗病毒治疗1 W,19例(27.94%)患者HCV RNA低于检测下限;4 W时64例(94.12%)患者获得RVR;抗病毒治疗结束时67例(98.53%)患者获得ETVR;抗病毒疗程结束后12 W,66例(97.06%)患者获得SVR。不同基因型之间病毒学应答差异无统计学意义(P>0.05),见表1;肝硬化与非肝硬化组的病毒学应答差异无统计学意义(P>0.05),见表 2。
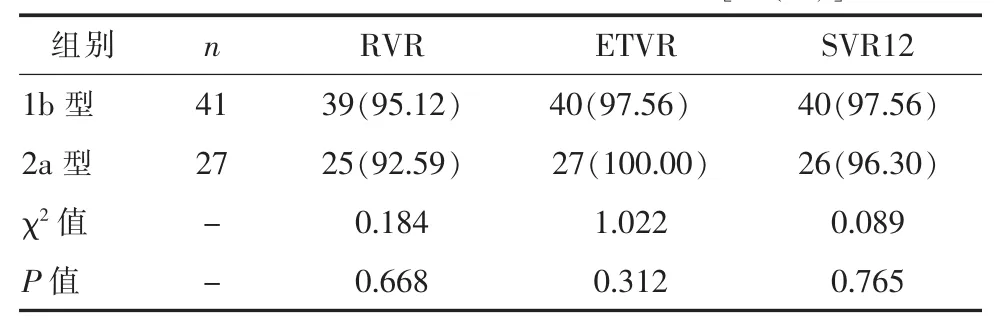
表1 不同基因型之间病毒学应答比较[例(%)]
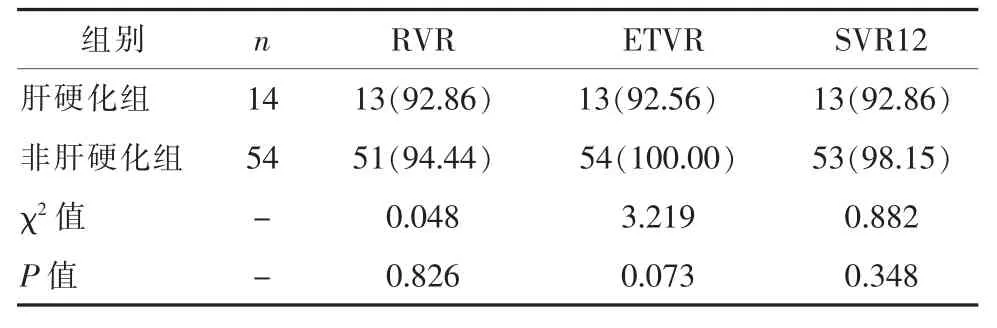
表2 肝硬化组和非肝硬化组病毒学应答比较[例(%)]
2.2 生化学应答 治疗结束后丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、胆红素均较治疗前明显下降,差异有统计学意义(P<0.05);慢性肝炎及肝硬化组,37例患者肝功能复常,复常率达86.05%。APRI指数也明显下降,差异有统计学意义(P<0.05)。见表 3。
表3 治疗前后肝功能及APRI指数的变化(±s)
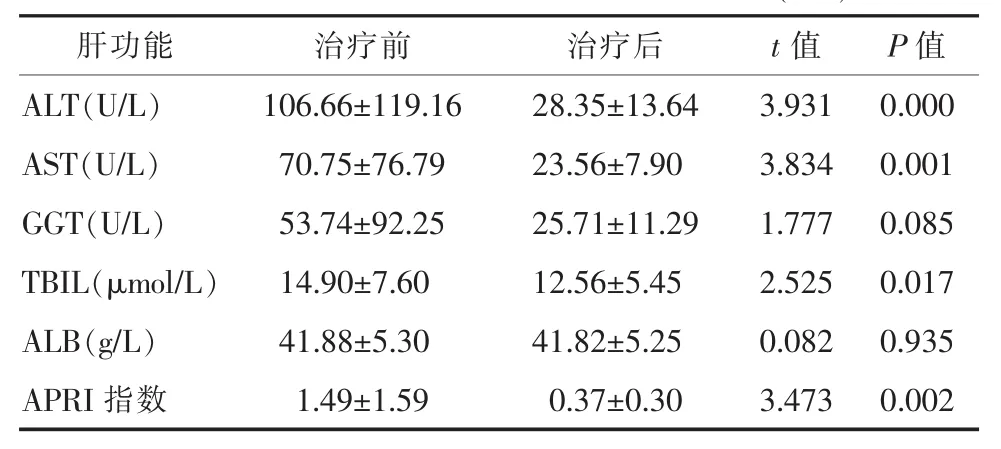
表3 治疗前后肝功能及APRI指数的变化(±s)
肝功能 治疗前 治疗后 t值 P值ALT(U/L) 106.66±119.16 28.35±13.64 3.931 0.000 AST(U/L) 70.75±76.79 23.56±7.90 3.834 0.001 GGT(U/L) 53.74±92.25 25.71±11.29 1.777 0.085 TBIL(μmol/L) 14.90±7.60 12.56±5.45 2.525 0.017 ALB(g/L) 41.88±5.30 41.82±5.25 0.082 0.935 APRI指数 1.49±1.59 0.37±0.30 3.473 0.002
2.3 安全性评价 监测治疗前后血常规、肾功能、心肌酶变化及患者不良反应。1例失代偿期肝硬化患者在治疗过程中因消化道出血中止治疗,其余患者均完成治疗,并停药随访12 W以上。仅15例患者(22.06%)出现轻微不良反应,表现为乏力7例、头晕3例、头痛2例、腹泻2例、皮疹1例,均可耐受,可自行缓解。其他指标见表4。
表4 治疗前后肾功能、心肌酶及血常规变化(±s)
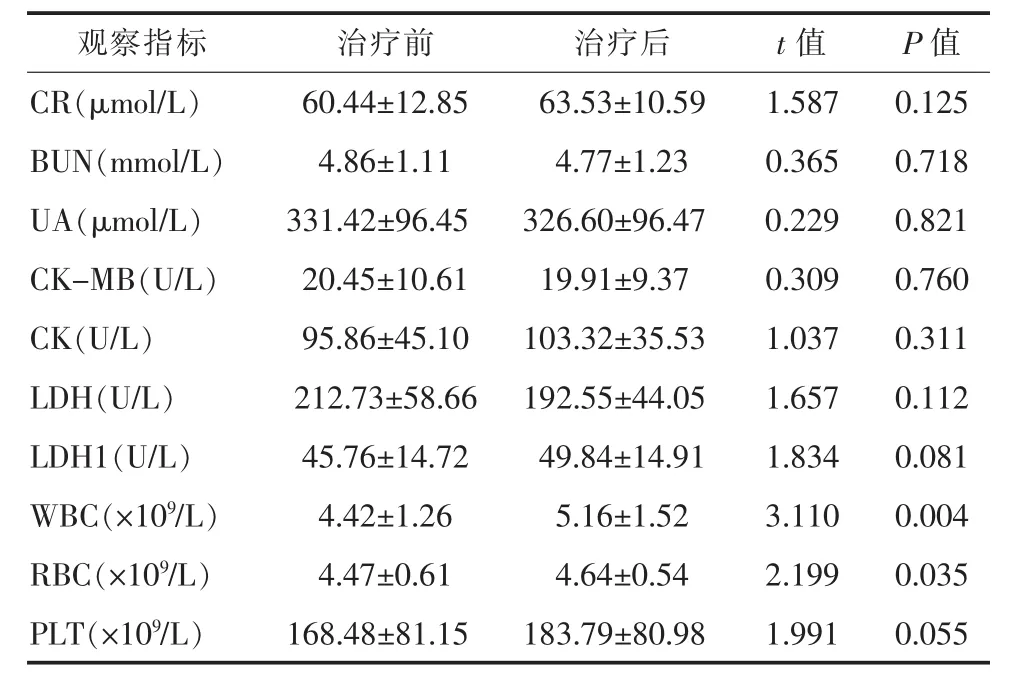
表4 治疗前后肾功能、心肌酶及血常规变化(±s)
观察指标 治疗前 治疗后 t值 P值CR(μmol/L) 60.44±12.85 63.53±10.59 1.587 0.125 BUN(mmol/L) 4.86±1.11 4.77±1.23 0.365 0.718 UA(μmol/L) 331.42±96.45 326.60±96.47 0.229 0.821 CK-MB(U/L) 20.45±10.61 19.91±9.37 0.309 0.760 CK(U/L) 95.86±45.10 103.32±35.53 1.037 0.311 LDH(U/L) 212.73±58.66 192.55±44.05 1.657 0.112 LDH1(U/L) 45.76±14.72 49.84±14.91 1.834 0.081 WBC(×109/L) 4.42±1.26 5.16±1.52 3.110 0.004 RBC(×109/L) 4.47±0.61 4.64±0.54 2.199 0.035 PLT(×109/L) 168.48±81.15 183.79±80.98 1.991 0.055
3 讨论
HCV基因组含有一个开放读码框,分为结构基因区和非结构基因区,分别编码结构蛋白和非结构(nonstructure,NS)蛋白。非结构蛋白主要是参与病毒复制的功能酶,NS3蛋白为病毒蛋白酶和HCVRNA螺旋酶,NS5蛋白为HCVRNA指导的RNA多聚酶,在病毒复制中起到非常重要的作用。DAAs类药物直接作用于非结构蛋白,从而抑制病毒复制。近年来,针对不同靶点的DAAs得到了迅速发展,其中NS5A和NS5B是主要作用靶位。国外诸多研究表明DAAS类药物治疗慢性丙型肝炎有效率高,可使超过90%的患者获得持续病毒学应答(SVR)[5,6]。
索磷布韦(sofosbuvir,SOF)是 HCVNS5B RNA依赖性RNA聚合酶抑制剂,该聚合酶对病毒复制有重要作用。SOF是一种核苷酸前体药物,在细胞内代谢为具有药理活性的尿苷类似物三磷酸盐,可被NS5B聚合酶嵌入HCVRNA中而终止病毒复制。大量临床研究证实,SOF治疗慢性丙型病毒性肝炎有良好疗效,安全性良好,该药耐药屏障高,抗病毒谱覆盖全部基因型[7,8]。达拉他韦(daclatasvir,DCV)是NS5A蛋白酶抑制剂,通过与NS5A蛋白结构域1的N-端相互作用,致使NS5A蛋白结构扭曲,从而干扰HCVRNA复制和装配,是强效抗HCV药物之一,抗病毒谱覆盖全部基因型[9-11]。研究表明索磷布韦和达拉他韦二者之间无交叉耐药,具有协同作用,国内外指南均推荐它用于治疗慢性丙型肝炎[4,12,13]。 该研究发现,索磷布韦联合达拉他韦(SOF+DCV)治疗慢性丙型肝炎,疗效显著,治疗1 W时即有27.94%的患者HCV RNA低于检测下限,94.12%的患者获得RVR,抗病毒治疗结束时98.53%患者获得ETVR,SVR12高达97.06%,与其他研究结果一致[14]。1b型和2a型病毒学应答无差异;肝硬化组和非肝硬化组的病毒学应答无差异。治疗结束后患者肝功能明显改善,ALT、AST及胆红素较治疗前均明显下降,ALB升高;提示SOF+DCV抗病毒治疗可以减轻肝脏炎症、改善肝功能。
国外研究表明,SOF+DCV治疗丙型肝炎不良反应小,依从性好[14]。该研究观察患者中,仅有1例失代偿期肝硬化患者在治疗过程中因消化道出血终止治疗;其余患者均完成治疗。22.06%的患者出现一过性乏力、头晕、头痛、腹泻、皮疹等轻微不良反应,均自行缓解。索磷布韦主要经肾脏排泄,轻至中度肾损伤患者不需要调整剂量[15]。曾有报道指出,在DAAS药物治疗过程中可见ALT及肌酸激酶一过性升高[16]。笔者在治疗过程中监测肾功能、心肌酶,发现治疗前后无明显变化,仅有LDH1较治疗前轻度升高,但差异无统计学意义。比较治疗前后血常规变化,发现白细胞、红细胞及血小板均较治疗前明显升高,这可能是抗病毒治疗后,肝功能改善,脾功能亢进缓解有关。同时还发现,抗病毒治疗后APRI指数较治疗前明显下降,提示SOF+DCV治疗可以减轻肝纤维化程度。针对肝硬化患者,在今后的随访中,将继续观察肝纤维化指标的变化。
