环状化合物-甲烷水合物稳定性的分子模拟
2019-03-22芦文浩梁海峰
芦文浩,梁海峰,王 帅,贾 菊
(太原理工大学 化学化工学院,山西 太原 030024)
天然气(NG)作为一种可提供高效热值、燃烧无污染和储量丰富的能源,被公认为未来重要的战略资源。以水合物形式存储天然气(主要成分为甲烷)的固化天然气技术 (Solidified natural gas,SNG),是最具有潜力、安全环保、高效解决能源供应问题的储运方式。
Ⅱ型水合物小笼晶穴可以容纳大量CH4,大晶穴填充热力学促进剂,稳定性提高,其中以环状化合物为主要的促进剂,可使水合物在温和条件下稳定存在。许多学者就实验探索已证明其可行性:胡亚飞等[1]构建环戊烷(CP)+CH4水合物实验体系,证明CP可提升水合物稳定存在温度;孙强等[2]添加环状醚类四氢呋喃(THF)提纯煤层气中的CH4,实验验证生成水合物压力明显降低;梁德青等[3]测定H2+CH4+环状醚类四氢吡喃(THP)+水(H2O)、H2+CH4+CP+H2O两种体系的水合物相平和数据,结果表明加入环状化合物,降低了生成压力;实验只能提供直观过程,无法洞悉微观结构改变和作用机理。水合物分子动力学模拟可为多组分体系中分析分子运动、作用和结构改变等微观角度的探究提供有效途径[4],对此研究也取得一些成果:梅东海等[5]首次采用分子动力学计算H型水合物,客体分子填充CH4和环辛烷,得出H型水合物3种笼形晶穴都需要有客体分子占据,水合物才能稳定存在;Wu[6]利用GROMACS模拟软件,计算CH4+THF混合客体分子水合物成核的分子动力学,结果说明体系形成的笼形簇团相对单组份更稳定;张庆东等[7-8]采用分子动力学模拟填充不同占有率的CH4和THF对水合物稳定性影响,结果表明水合物占有率决定水合物稳定性,随着温度降低,利于单组份CH4水合物稳定;殷开梁等[9]比较 Material studio(MS)软件中各分子力场对于氢键作用描述的适用性,结果表明该软件可以采用一般的非键作用近似反映氢键。耿春宇等[10]通过分子动力学模拟CH4对应Ⅰ型水合物,得出结论:因CH4占据晶穴,水合物晶穴的相互作用能降低,水分子间氢键作用加强,稳定性提高,且占据率高于87.5%水合物才能表现较好稳定性;丁丽颖等[11]模拟填充CH4的Ⅰ型水合物稳定性受晶穴占有率和温度的影响,结果表明较低占有率(<0.625)和较高温度(>320k)条件下,水合物基本瓦解。
综上所述,有关环状化合物-CH4水合物稳定性研究多数集中在实验,少有利用分子动力学探寻CP和THP对Ⅱ型天然气水合物的稳定作用,且高占有率利于水合物稳定性;本文采用Material Studio 8.0软件,搭建占有率100%分别添加CP、THF和THP的二元体系CH4水合物,从分子角度比较其稳定性和解释作用机理,为SNG技术实际应用提供参考。
1 模型搭建和模拟方法
1.1 笼形单元组成
水合物主体框架是以水分子氢键结合形成的一种空间点阵结构[12],Ⅱ型水合物原始单晶胞包含136个水分子,构成16个小笼晶穴(512)和8个大笼晶穴(51264)。小笼晶穴由CH4分子占据,大笼晶穴分别由CP、THF和THP占据。客体分子手动搭建,并进行能量几何优化,使其最接近真实状态。表1为依据胡盛志等[13]优化方法计算得到的客体分子范德华模型相关参数,笼形晶穴占据结构如图1所示。

表1 客体分子范德华模型参数

图1 客体分子占据笼形晶穴结构
1.2 模型搭建
在周期边界条件下,Ⅱ型水合物原始单晶胞在温度T=123K下,晶格参数a=b=c=1.7175nm。晶胞中心包含对称存在的四面体,与周边6个十二面体形成Ⅱ型水合物主体框架,其氧原子坐标来自X射线衍射实验[14],氢原子分布满足“冰规则”[15]。客体分子与主体框架间为范德华作用力(Van der Waals)[16],模拟体系构建2×2×2的Ⅱ型Super cell晶胞,该体系中1088个H2O构建128个小笼晶穴(512)和64个大笼晶穴(51264)的主体框架。小笼晶穴填充128个CH4,大笼晶穴分别填充64个CP、THF和THP,本文3种模拟体系分别命名为A、B、C,便于观察,将体系H原子隐藏,初始结构模型如图2所示。

图2 水合物模拟体系初始结构
1.3 模拟方法
先对模拟体系进行能量优化和几何优化,选用CVFF(一致性价力场)力场描述模拟体系,SPC(Simple point charge)模型[17]描述 H2O 分子,将其视作刚性分子,H-O-H平面夹角为104.52°,H-O键长为固定值0.09570nm,水分子和客体分子、客体分子间非键作用使用Lennard-Jones作用势描述,在MS中采用截断球近似代替,截断半径为1.5nm,Ewald加和法处理长程静电作用力,精度设置为4.1868×103J/mol。
对几何优化结束的体系进行结构松弛 ,选水分子中的O原子固定,控温方法使用Nose-Hoover,NVT(正则系综)模拟设定T分别为273K、283K、293K,分子初始速依据Maxwell-Boltzmann随机产生,模拟时间为 50ps(1ps=10-12s),步长为 1fs(1fs=10-15s),每5000步输出一帧结构图;解除O原子固定,在NPT(等温恒压)系综下进行动力学模拟,控温方式不变,采用Berendsen控压方式调整体系压力值,压力设为2MPa,模拟时间为400ps,模拟结束后分析二元体系水合物结构。
1.4 模拟最终结构
将软件输出的最终结构进行比较分析,如图3所示。

图3 水合物模拟体系最终结构
由图3水合物模拟体系最终结构看出:A、B可维系原有结构,氢键排序重叠度较高,客体分子仍能与笼形晶穴中心相对重合;压力不变,随着温度升高,出现部分晶穴的扭曲加深,B较A在293K下水合物结构破坏严重;C模型体系在273K时完整度与相同条件下的A、B相比较差,部分客体分子因晶穴的扭曲加重位移较大,氢键分布出现小范围的杂乱,随着温度的升高结构出现了不同程度的扭曲,283K温度下水合物结构基本破坏,残存的氢键不足以维系体系的稳定存在,客体分子位移较大,出现小范围的聚集,293K条件下氢键虽然存在,但晶穴有序结构不存在,客体分子逃逸,出现聚集现象,预判此时从固体转变为液体。
2 模拟结果分析
2.1 径向分布函数(Radial Distribution Function,RDF)
稳定的水合物主体框架水分子中的O原子RDF特征是:呈现多峰值曲线状态,其峰高随着O原子的增加逐渐降低。可依此判断其无序状态,也代表水合物区域密度和平均密度的比值;液态水分子中O原子go-o(r)在r值大于0.278nm时就趋向为1[18],即区域密度等于平均密度表现为液态流动,将A、B、C三种模型对应压力温度值下的go-o(r)值对比分析,如图4所示。

图4 水合物O原子RDF分布
由图4可知O原子RDF分布在r=0.278nm时出现第一峰高,代表相邻水分子最近的O原子间距离,第二特征峰高在r=0.452nm出现,满足晶体结构RDF特征;T=273K时,A、B、C呈现出稳定水合物晶体的特征峰,但都出现了峰高降低和峰谷升高的现象,说明有部分O原子发生位移,即部分笼形晶穴扭曲,但整体框架结构能够稳定存在,且第二峰高峰值ABC,则A稳定性要高于相同条件下的B,C模型峰谷升高,稳定性较差;T=283K时A同样略优于B,C模型在r=0.278nm出现峰值后,峰谷升高,第二特征峰消失,此时与液体特征峰相似[15];T=293K时,A和B模型RDF分布重合度相近,C模型RDF分布较T=283K对应分布:峰谷升高加剧,与液体特征峰分布更为接近,说明破坏程度更大,客体分子逃逸并发生聚集。
2.2 均方位移(MSD)
MSD表示指定分子位置与初始位置的偏离程度,依此可以判断体系是固态还是液态,MSD分布图像斜率K越大表示偏离初始程度越大。图5为A、B、C对应压力温度值下的MSD图像。
图5为模拟体系所有条件下的O原子MSD分布,为更清晰比较,去除C模型283K、293K条件,呈现图6。图6可分析出C模型在283K、293K条件下,MSD随着模拟时间增大,与液态水分子MSD斜率K相似,表明这两种状态下无序化程度严重,结构破坏变成了液态溶液;从图6、7综合比较,相同p值下,较稳定的模型体系MSD围绕在接近零值的地方波动,结果 KC(293K)KB(293K)KA(293K),KC(283K)KB(283K)KA(283K),KC(273K)KB(273K)KA(273K),说明对添加同种环状化合物促进剂,随着温度降低,有利于水合物的稳定性,且体系在对应模拟条件下呈现KAKBKC;

图5 水合物O原子均方位移
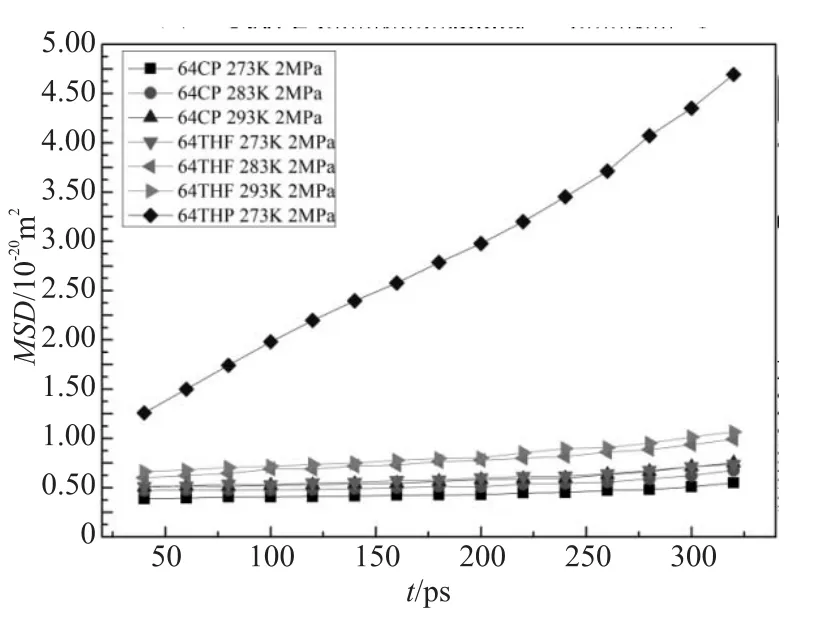
图6 水合物O原子均方位移局部放大图
2.3 相互作用能
分子动力学模拟结束后可得到模拟体系的总能量Etotal,主体框架能量Ecages以及填充的所有客体分子能量Eguests,从而得到主体框架和客体分子间的相互作用能Ebinding,满足公式:
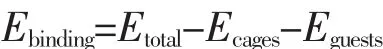
从能量角度分析,相互作用能越小,则体系最终结构越稳定,图7为A、B、C对应温度压力值下整个体系的相互作用能。
从图7可看出,A模型E(293K)E(283K)E(273K),B、C模型呈现相同规律即低温有利于水合物结构稳定;相互作用能越低,水合物结构越稳定,A模型整体稳定性较好,与MSD分析结果相一致;从分子角度分析3种促进剂对稳定性的影响,已知客体分子与晶穴直径比值在0.76~1之间[19],可维系稳定水合物结构,环状化合物的填充,起到支撑水合物框架的作用。从表1可看出Ⅱ型大晶穴,直径比值CP略高于THF,更接近1,稳定性得到提升,THP与晶穴比值优于CP和THF,理论上应相对更稳定,但模拟结果高温区稳定性较差,原因分析:THP分子过大,高温状态下分子活跃程度较大,其分子组成中的O原子会与周边水分子框架形成氢键作用,使得与周边其他水分子间范德华作用力不均衡,客体分子牵动晶穴单元发生位移(氢键作用强于范德华作用力),从而使得模拟体系稳定性下降。
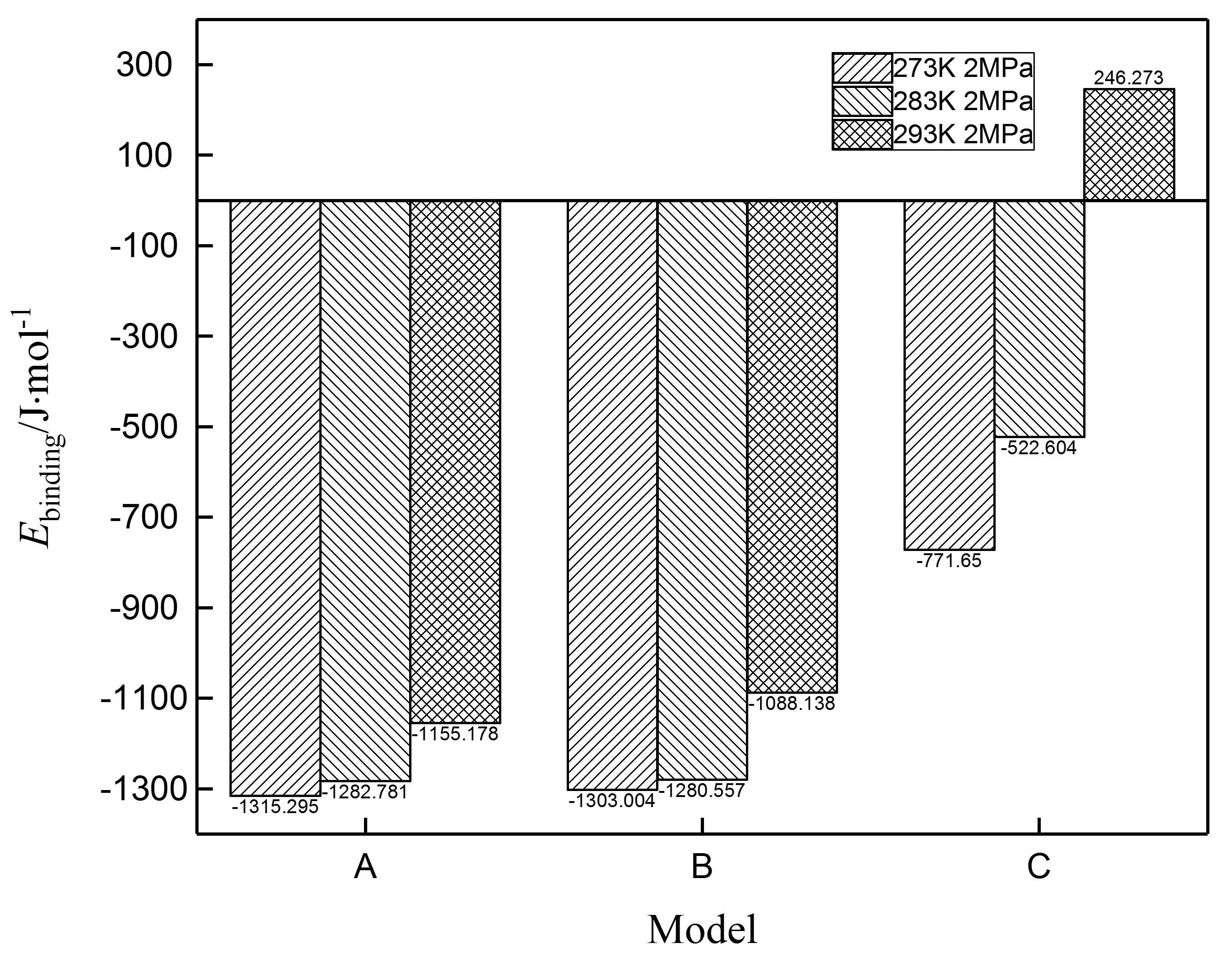
图7 模拟体系不同温度下相互作用能
3 结论
在NPT系综下分子动力学模拟,本文通过最终结构、RDF、MSD以及相互作用能对比分析,得出以下结论:
(1)环状化合物作为客体分子占据甲烷水合物大晶穴,能在温和条件下维系水合物稳定存在。随着温度升高,模拟体系稳定性下降;
(2)CP模拟体系稳定性优于THF模拟体系,说明环状化合物与Ⅱ型水合物大晶穴的直径比越接近1,水合物越稳定;
(3)THF模拟体系稳定性优于THP模拟体系,说明在高温条件下,当较大分子尺寸的环状化合物分子含有O原子时,环状化合物与水合物框架产生不平衡氢键作用,使水合物稳定性降低。
符号说明
a-晶格参数,nm;b-晶格参数,nm;c-晶格参数,nm;Ebinding-相互作用能,J/mol;Ecages-空晶穴能量,J/mol;Eguests-总客体分子能 J/mol;Etotal-模型总能量,J/mol;E(T)-对应温度下相互作用能,J/mol;K-MSD分布斜率,m2/s;MSD—O 原子均方位移,m2;N-分子总数, 个;p-压力,MPa;r-截断半径,nm;RDF-径向分布函数,量纲为1;T-温度,K。
