双香豆素衍生物的生物活性
2019-03-13杨丽君丁超编写高川冯连顺审校
杨丽君,丁超 编写,高川,冯连顺 审校
(湖北科技学院核技术与化学生物学院,咸宁 437100)
1 前言
与香豆素一样,双香豆素衍生物为苯并吡喃酮类化合物,广泛存在于天然产物中。双香豆素衍生物具有抗菌、抗炎、抗肿瘤、抗HCV、抗HIV、抗老年痴呆、抗疟疾、抗真菌、抗结核和抗精神病等多种生物活性,引起了科学家的普遍关注。其中,双香豆素等已在临床上作为抗凝血药物使用,提示这类化合物安全性较高。
本文将着重探讨双香豆素类化合物在抗菌、抗凝血、抗炎、抗病毒、抗寄生虫和抗肿瘤领域的研究进展,并讨论这类化合物的构-效关系(SAR),以期为进一步合理设计提供理论基础。
2 抗菌活性

图1 香豆素及基于香豆素的药物
细菌感染是院内感染的主要因素,严重威胁人类健康。主要的革兰阳性致病菌有金黄色葡萄球菌/金葡球菌、表皮葡萄球菌/表葡球菌、肺炎链球菌、粪肠球菌和屎肠球菌等,而典型的革兰氏阴性致病菌有肠杆菌科如大肠埃希菌、克雷伯菌属、铜绿假单胞菌、肺炎衣原体、肺炎支原体、嗜肺性军团病杆菌和不动杆菌属等。目前,临床上使用的抗生素大多发现于上世纪抗生素黄金时代。然而,长时间的使用,致病菌已对抗生素产生了耐药性,而且愈发严重。因此,有必要开发新型抗生素。
Li等研究了一系列单香豆素和双香豆素衍生物(图1)的体外抗野生型金葡球菌和3株临床分离耐甲氧西林金葡球菌(MRSA) XJ 75302、Mu50和USA 300LAC活性,结果发现双香豆素衍生物1的抗菌活性明显优于单香豆素衍生物。SAR显示,R位为烷基取代基的化合物1a,1b(图2)的抗菌活性高于相应的烷氧基衍生物1c,1d,而向此位置引入卤素(化合物1e,1f)则可提高这类化合物的抗菌活性;并环结构会导致抗菌活性的大幅下降,如化合物2(最小抑制浓度/MIC: 256μg/mL)活性极弱。值得一提的是,化合物1g(MIC: 2~4μg/mL)对3株所测临床分离MRSA的活性较高,是对照药头孢他啶、头孢曲松和哌拉西林的16~>128,而化合物1f对表葡球菌和耐甲氧西林表葡球菌(MRSE)的MIC均为8μg/mL。不幸的是,所有双香豆素衍生物对革兰阴性菌大肠埃希菌均为显示出任何活性,MIC>256μg/mL。有趣的是,某些衍生物具有潜在的抗肿瘤活性,值得进一步开发。
Muratović和Sompornpisut等评价了2个系列双香豆素衍生物3和4的体外抗金葡球菌和枯草芽孢杆菌活性,结果表明,大多数衍生物具有良好的活性,MIC为1.95~31.25μg/mL。SAR显示,向苯环的C-4位(3i)和C-5位(4b)引入-Br可提高此类化合物的抗金葡球菌活性,而引入至C-3位(4a)则对活性不利。其中,活性最强的4b对金葡球菌和枯草芽孢杆菌的MIC和最小杀菌浓度(MBC)分别为3.9和1.95μg/mL及7.8和7.8μg/mL,值得深入研究。
为优化两个香豆素母核之间的连接子,研究人员设计合成了一系列取代吡啶基、酰胺基和吡唑基为连接子的双香豆素衍生物。结果显示,这些衍生物的活性明显弱于相应的次甲基连接子衍生物,绝大多数衍生物5~8(MIC: ≥100μg/mL)未显示出任何抗菌活性。而以噻吩基(9)、噻唑-吡唑基(10)、亚胺(11)和氧原子(12)作为连接子时,衍生物则显示出潜在的抗菌活性,提示抗菌活性与连接子息息相关。
有趣的是,将2个或3个双香豆素揉合到一个分子中所得的化合物13和14也具有良好的抗菌活性,值得进一步研究。
3 抗凝血活性
香豆素类抗凝血药物如华法林和醋硝香豆醇等能抑制肝脏中的羧化酶,使维生素K依赖因子生成减少,在合成凝血酶原的酶系统中竞争性地置换维生素K,在临床上有着广泛的应用。
Manolov等研究了11个双香豆素衍生物在小鼠模型中的血凝固时间和急性毒性(腹腔注射或口服给药),结果显示,化合物15(图3)不仅具有良好的体内活性,而且毒性低,可作为先导物进一步优化。
天然产物具有结构和生物活性的多样性和独特性,在新药研发领域占据极为重要的地位。Qin等从紫花地丁中分离得到了双香豆素衍生物dimeresculetin(16)并研究了其抗凝血活性。与其它双香豆素相似,该化合物可竞争性抑制维生素K的环氧化物还原酶,阻止维生素K还原成氢醌,进而发挥抗凝血活性。
4 抗炎活性
炎症是十分常见的基本病理过程,是组织对损伤和异物的正常应答。细胞因子是急性和慢性炎症过程中不可或缺,而肿瘤坏死因子α(TNF-α)可刺激细胞因子分泌,是慢性炎症的介质,故TNF-α抑制剂可作为抗炎药物候选物。查耳酮具有潜在的抗炎活性,而香豆素和查耳酮又均是已知的TNF-α抑制剂,故将二者杂合可能会得到抗炎活性更高的杂合体。
Sashidhara等研究了10个双香豆素-查耳酮杂合体17(图4)在角叉菜胶致大鼠足肿胀模型中的体内抗炎活性,结果显示,其中的3个杂合体17a~17c在口服给药100mg/kg时可分别抑制29%、26%和33%的炎症,略弱于相同剂量的对照药布洛芬(59.5%);17a~17c对TNF-α的抑制活性呈剂量依赖性,且在400μg/mL时的抑制率分别为47%、43%和21%。不仅如此,这类杂合体在不同浓度时未显示出任何体内毒性,各项生理指标均正常且存活率高达80~90%。活性最强的杂合体17c还显示出潜在的抗氧化活性,提示这类杂合体的抗炎活性可能部分源于其自由基清除能力。显然,杂合体17c可作为先导物进一步研究。
5 抗病毒活性
病毒可在宿主细胞内复制,对人致命的病毒主要有人类免疫缺陷病毒(HIV)、乙肝病毒(HBV)、丙肝病毒(HCV)、冠状病毒和流感病毒等。在过去的30年间,香豆素作为口服非肽类抗病毒先导物,引起了研究人员的极大关注。众多香豆素衍生物对多个抗病毒药物作用靶点具有亲和活性,适当的修饰可明显的拓展此类化合物的抗病毒谱,值得深入研究。
5.1 抗HIV活性
绝大多数HIV感染患者最终会发展成为艾滋病(AIDS),并因免疫系统缺陷而死于机会感染和恶性肿瘤。据世界卫生组织(WHO)估计,全球约有4000万HIV患者,且每年新增200万,其中>100万患者因此丧命。高效抗逆转录病毒疗法对HIV患者具有良好的疗效,但耐药性的产生使得对新型抗HIV药物的研发迫在眉睫。香豆素衍生物可抑制HIV-1整合酶(HIV-1 IN),故有必要研究双香豆素衍生物的抗HIV活性。
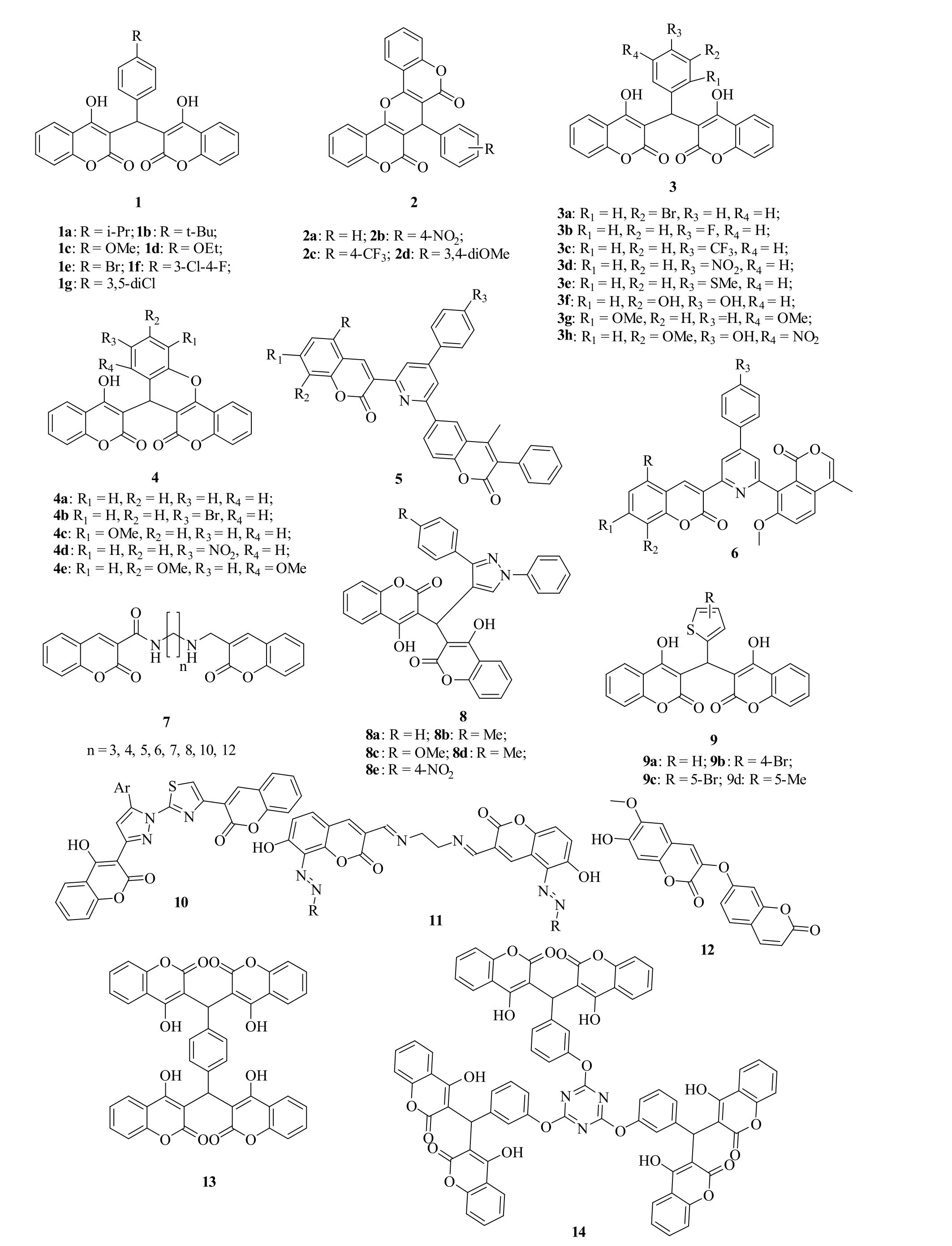
图2 具有抗菌活性的双香豆素衍生物1~14的化学结构

图3 具有抗凝血活性的双香豆素衍生物15和16的化学结构
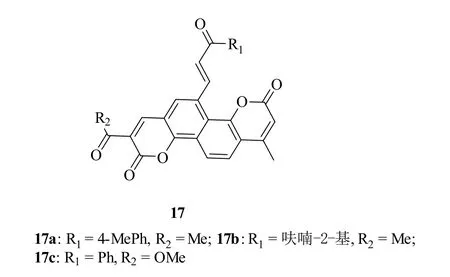
图4 具有抗炎活性的双香豆素-查耳酮杂合体17的化学结构
Pommier等研究了一系列双香豆素衍生物的抗病毒活性,其中双(双香豆素)衍生物NSC 158393(13)(IC50: 0.8~2.3μmol/L)对HIV-2、猫和猴免疫缺陷病毒整合酶具有良好的抑制活性,而对真核细胞DNA拓扑异构酶I的抑制活性较弱(IC50: 10μmol/L),提示该化合物逆转录病毒整合酶具有一定的选择性。SAR显示,该化合物中的-OH和羰基可能是其具有抗病毒活性所必需的基团。进一步研究表明,NSC 158393可同时抑制HIV蛋白酶和整合酶,可作为多靶点抗HIV药物候选物深入研究。
Zhao等对NSC 158393进行了进一步结构修饰得到了一系列次甲基上含有芳基的双香豆素衍生物18(图5),并评价了它们的抗HIV活性。SAR显示,R位的取代基为苯基时,对抗病毒活性不利;而用脂溶性更高的芳环取代基代替苯基时,抗病毒活性将有所改善。其中,抗HIV活性最高的双香豆素衍生物18a(IC50: 4.2μmol/L)的活性与母体NSC 158393(IC50:2μmol/L)相当,可作为先导物进一步优化。
Hsu等研究了2个含有苯胺结构单元的双香豆素衍生物19a,19b对HIV IN的抑制活性,而苯胺结构单元的引入或许会在香豆素-IN复合物结合位点附近形成共价键,进而提高抗HIV活性。然而,研究发现尽管19a,19b(IC50: 43.0和27.4μmol/L)显示出潜在的抑HIV-1 IN活性,但苯胺结构单元似乎并未在香豆素-IN复合物结合位点附近形成共价键,抗HIV活性并未显著提升,提示在香豆素-IN复合物结合位点附近可能存在一个非亲核性或疏水性区域。基于此,向此类化合物中引入疏水基团可能会提高抑HIV-1 IN活性。对母核含有磺酰氧基(20)和苯甲酰氧基(21)的双香豆素衍生物的抑HIV-1 IN活性测定结果显示,所有衍生物均显示出优秀的抑制活性,IC50为0.5~23.7μmol/L。其中,双香豆素衍生物21的活性优于化合物18,而与NSC 158393相当。SAR显示,含有芳基取代基的20b~20f和21a~21e(IC50:0.5~3.9μmol/L)优于相应的烷基取代基-Me衍生物20a(IC50: 23.7μmol/L);磺酰氧基和苯甲酰氧基为高抑制活性所必需。代表物21d抑HIV-1 IN的IC50为0.5μmol/L,是NSC 158393 (IC50: 1.1μmol/L)和18(IC50: 43μmol/L)的2.2和86倍,值得深入评价。而双(双香豆素)衍生物22(IC50: 0.49μmol/L)活性优于相应的双香豆素衍生物,可作为先导物进一步开发。
5.2 抗牛病毒性腹泻病毒活性
牛病毒性腹泻病毒(BVDV)属于黄病毒科瘟病毒属,可引起严重的家畜疾病。香豆素衍生物可作用于BVDV RNA-依赖性RNA聚合酶,对BVDV显示出良好的活性。因此,从香豆素衍生物中寻找新型抗BVDV候选物引起了研究人员的普遍关注。

Loddo等评价了C-8位通过不同连接子连接的双香豆素衍生物23(图6)的抗BVDV活性,初步活性测试结果显示,所有衍生物均具有明显的活性,EC50为0.3~30μmol/L。值得一提的是,代表物23a(EC50:0.3μmol/L)抗BVDV活性是所有对照药的7~>333 倍,且对各种细胞系未显示出毒性(CC50: >100μmol/L),值得进一步研究。
6 抗寄生虫活性
植物寄生线虫是臭名昭著的植物病原体,每年导致数十亿美元损失。某些香豆素衍生物如呋喃香豆素类和双香豆素类显示出良好的杀线虫活性,故对这类化合物进一步优化有可能得到新型杀线虫剂。
Qin等研究了6个双香豆素衍生物24a~24c(图7)和25a~25c的杀线虫活性,SAR显示连接子的长度对活性有显著影响:对24a~24c而言,长连接子有利于活性,而对25a~25c而言,则恰好相反,短连接子更有利。活性最强的25a对根结线虫、马铃薯块茎腐烂线虫、拟松材线虫、松材线虫和水稻干尖线虫等具有广谱活性,LC50为35.8~190.9μmol/L,但弱于对照药阿维菌素(LC50: 0.26~0.62μmol/L)。
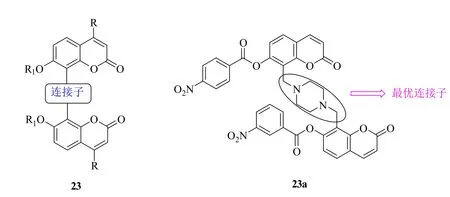
图6 具有抗BVDV活性的双香豆素衍生物23的化学结构
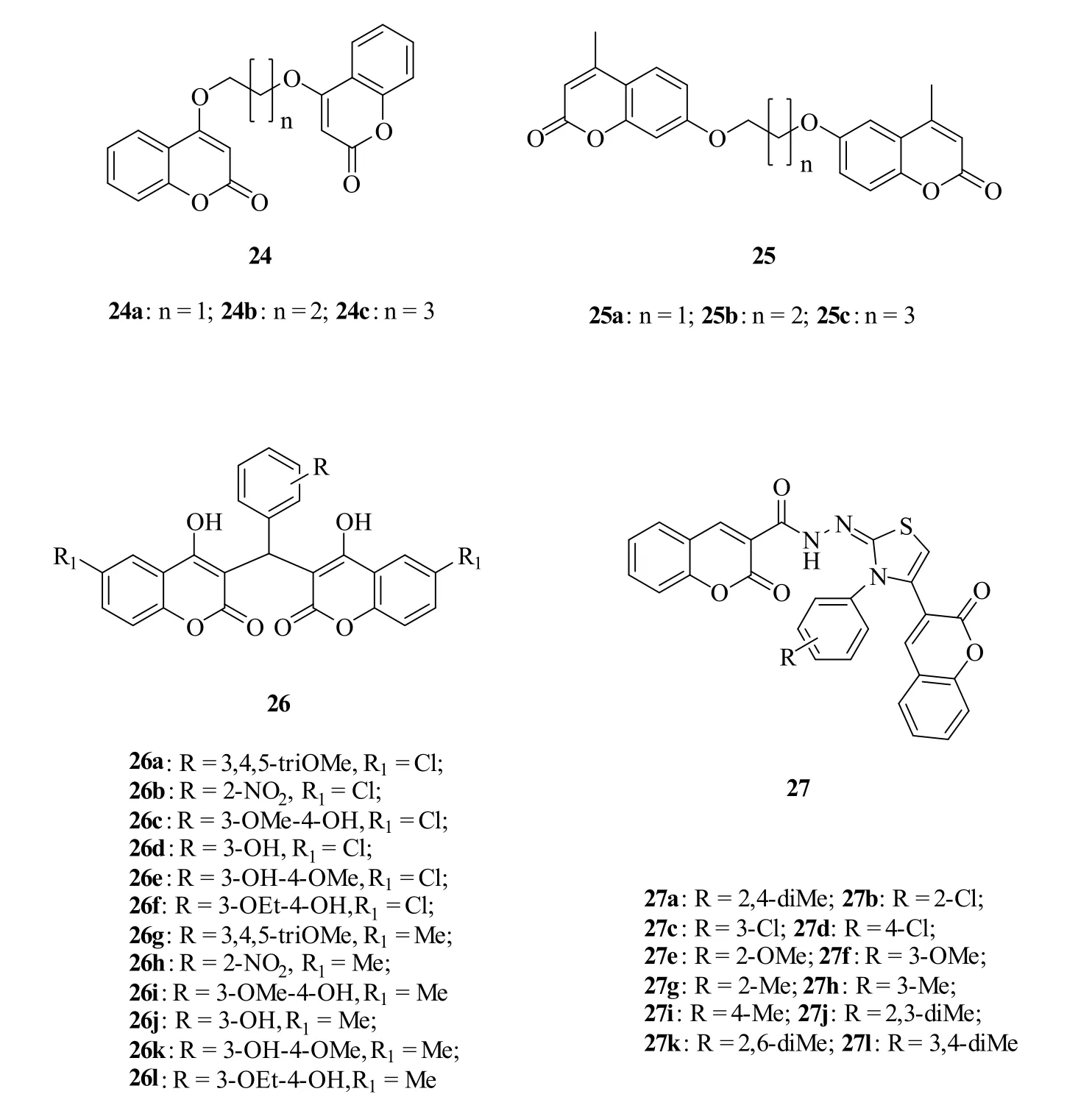
图7 具有抗寄生虫活性的双香豆素衍生物24~27的化学结构
利什曼病是由利什曼原虫引起的慢性病变,目前已知寄生于人体的利什曼原虫共3种,即杜氏利什曼原虫(主要寄生于内脏)、热带利什曼原虫和巴西利什曼原虫(只侵犯皮肤黏膜)。据估计,全球每年约新增50万杜氏利什曼原虫和150万巴西利什曼原虫患者。香豆素类化合物具有潜在的抗利什曼虫活性,值得深入研究。
Rahim等研究了一系列双香豆素衍生物26的抗利什曼虫活性,然而约一半左右的衍生物未显示出任何活性,剩余化合物仅显示出弱到中等强度的活性,IC50为35.62~82.36μmol/L。SAR研究结果表明,苯环上含有供电子基如-OMe和R1位为-Cl对活性有利。尽管活性最强的双香豆素衍生物26a(IC50:35.62μmol/L)弱于对照药喷他脒(IC50: 5.09μmol/L),但该研究丰富了SAR。
Saeed 等测定了一系列双香豆素-腙噻唑杂合体27的抗利什曼虫活性,发现所有杂合体具有潜在的活性(在100μmol/L时,抑制率为40.6~70.4%)。其中,代表物27a在100μmol/L时,抑制率为70.4%,与对照药两性霉素B(79.8%的抑制率)相当。SAR显示,当衍生物苯环含有2个甲基时,无论甲基在任何位置均对活性不利;在苯环间位含有1个甲基时对活性有利;当含有1个强供电子基如-OMe或1个吸电子基如-Cl时,衍生物显示出中等强度的活性。总之,活性最强的27a可作为先导物进一步优化。
7 抗肿瘤活性
癌症仍是发达国家排在首位、发展中国家排在第二位的致死性疾病,仅2012年一年全球就约有1400万人罹患癌症,其中820万人死于癌症相关性疾病。更为严峻的是,如果防控不利,在未来的20年中,新发癌症病例可能增长高达70%。因此,亟需新型抗肿瘤药物。香豆素类化合物是潜在的抗肿瘤候选物,研究人员设计合成了众多此类化合物并筛选了它们的抗肿瘤活性。
Zhai等对一系列单香豆素和双香豆素衍生物的体外抗肿瘤细胞活性研究结果表明,双香豆素衍生物28(IC50: 15~93.5μg/mL)对所测HUTU80、4T1和PANC1肿瘤细胞系的活性优于相应的单香豆素衍生物(IC50: 97~>300μg/mL)。对双香豆素衍生物28(图8)而言,苯环上含有吸电子基如二氟(28d)或-CN(28c)时对活性有利,而供电子基如-OMe则不利于活性。活性最强的双香豆素衍生物28d对所测所有肿瘤细胞系的IC50为15~82.5μg/mL,对HUTU80的活性是卡铂(IC50: 54.3μg/mL)的3.6倍,对4T1和PANC1肿瘤细胞系的活性则与卡铂(IC50: 52.5和70.1μg/mL)相当。初步的作用机制研究结果显示,双香豆素衍生物28d可阻滞HUTU80细胞的S期,诱导细胞凋亡。所有双香豆素衍生物均显示出良好的选择性指数(SI:3.1~7.5),优于卡铂(SI: 1.6~1.8)。不仅如此,在小鼠模型中这类化合物未显示出明显的急性毒性,在给药14天时各项生理指标均未发生明显变化。显然,此类化合物尤其是28d可作为先导物进一步研究。
基于芳香化酶抑制剂(AI)的内分泌疗法对乳腺癌具有潜在的疗效,而香豆素衍生物具有潜在的抑制芳香化酶活性,故可用于内分泌疗法。Oda等评价了一系列包括双香豆素衍生物29a,29b在内的香豆素衍生物的抑芳香化酶活性,结果显示,二者(IC50: 0.0287和7.0μmol/L)尤其是29a显示出极为优秀的活性,其活性略优于CYP19抑制剂依西美坦(IC50:0.0425μmol/L),值得进一步开发。
甾族硫酸酯酶是潜在的乳腺癌药物作用靶点,对12个双香豆素硫代磷酸盐30的体外抗甾族硫酸酯酶活性研究结果显示,这类化合物对源与人胎盘的甾族硫酸酯酶具有良好的活性,IC50为0.86~109.97μmol/L。SAR显示,R基对活性有显著影响,且贡献顺序为:-OH > -Cl > -OMe > -NH2。其中,活性最强的30a的IC50为0.86μmol/L,略优于对照药665-COUMATE(IC50: 1.01μmol/L)。
Perumalsamy等测定了双香豆素31的抗MDAMB-231、MDA-MB-453和MCF-7细胞系活性,发现该化合物可通过内在的线粒体途径诱导肿瘤细胞凋亡。该化合物对所测3株肿瘤细胞的IC50分别为5.63、7.30和10.84μg/mL,值得进一步研究。Silva等的研究结果显示,双(4-羟基香豆素)32对TNF-α具有良好的抑制活性,IC50为17.5和19.0μmol/L,值得研究。
3个双香豆素衍生物33对HepG2、HCT-116、MCF-7和Hep-2肿瘤细胞系显示出优秀的抑制活性,IC50为2.41~8.31μg/mL。SAR显示,第二个苯基的引入如化合物33b,33c对活性不利。活性最强的33a(IC50: 2.41~6.72μg/mL)可与5-氟尿嘧啶(IC50:2.35~6.56μg/mL)媲美,极具深入研究潜质。
此外,其它一些通过各种连接子连接的双香豆素衍生物及双香豆素金属螯合物也显示出一定的抗肿瘤活性,尽管绝大多数活性较弱,但丰富了SAR。
8 其它生物活性
除上述活性外,双香豆素衍生物还具有一些其它生物活性,本部分将进行简单介绍。
脲酶(又称尿素酶)不仅为各种微生物的生长提供氮源,在植物萌发过程对氮代谢具有举足轻重的作用。但土壤脲酶降解尿素肥料太快,导致富营养和氮的流失,故亟需新型脲酶抑制剂。Khan等评价了21个双香豆素衍生物34(图9)的抑脲酶活性,结果显示所有衍生物均显示出良好的活性,IC50为15.06~91.35μmol/L。SAR显示,双香豆素衍生物上的2个-OH可与酶活性位点相结合,负责抑脲酶活性;向C-11位引入任何取代基均对活性不利,故该位点不适合修饰。其中,代表物34a抑脲酶的IC50为15.06μmol/L,略优于标准药物硫脲(IC50:21.00μmol/L),可作为先导物进一步研究。
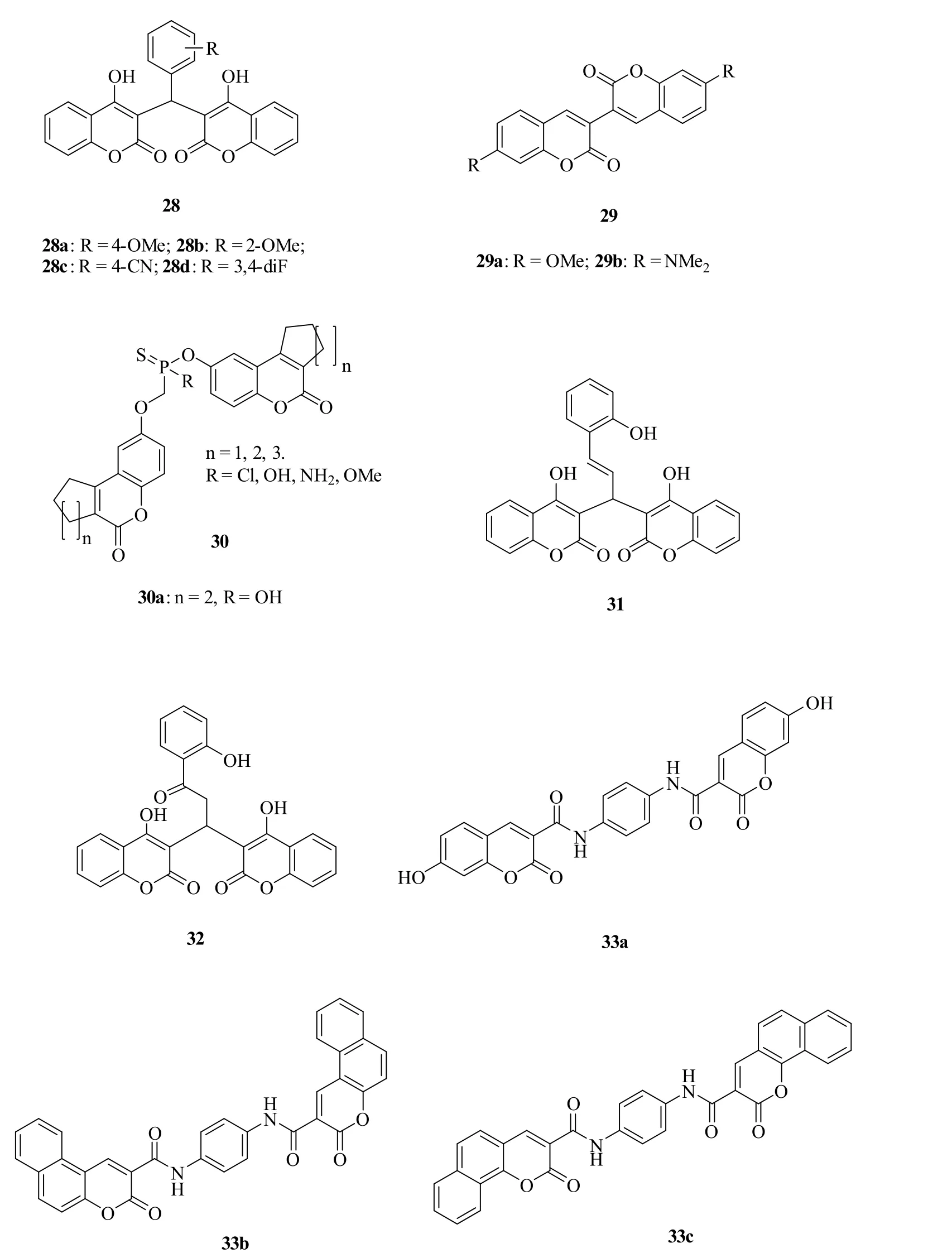
图8 具有抗肿瘤活性的双香豆素衍生物28~33的化学结构
双香豆素衍生物还具有抗氧化活性,某些化合物的活性甚至优于对照药,如化合物35(IC50:53.33μg/mL)消除自由基的能力高于对照药丁基羟基甲苯(IC50: 71.00μg/mL),值得深入研究。
NAD(P)H:醌氧化还原酶1(NQO1)被认为是一种解毒酶,可抑制活性氧的生成,是潜在的抗肿瘤药物作用靶点。Bryce等研究发现,双香豆素衍生物36对NQO1具有极为优秀的抑制活性,其中,代表物36a(IC50: 5nmol/L)的活性可与双香豆素(IC50: 5nmol/L)媲美,值得进一步优化。
Yang等研究发现,从川白芷根部分离得到的(±)-川白芷双香豆素37可抑制脂多糖活化的RAW264.7巨噬细胞产生一氧化氮,且呈浓度依赖性,IC50为49.6μmol/L,优于吲哚美辛(IC50:61.6.6μmol/L)。进一步研究显示,该化合物对诱导型一氧化氮合成酶mRNA具有极强的抑制活性,且呈浓度依赖性。

图9 双香豆素衍生物34~37的化学结构
此外,某些双香豆素衍生物还具有控制肥胖、抗补体活性、抑酶活性和作为CB2激动剂的潜力,深入研究仍在进行中。
9 结束语
近年来,研究人员分离和合成了众多双香豆素衍生物,并评价了它们的生物活性。本文将着重探讨双香豆素类化合物在抗菌、抗凝血、抗炎、抗病毒、抗寄生虫和抗肿瘤等领域的研究进展,并讨论这类化合物的SAR。
某些双香豆素衍生物尽管具有潜在的生物活性,但在临床上使用的这类药物并不多见,这可能归结于这类衍生物价格较高、制备较为复杂和生物活性谱较窄所致。有理由相信,通过科学家的不懈努力以上缺点可能会在不久的将来得以解决,使这类化合物为人类健康服务。
