高钙油田卤水富锂工艺研究
2019-02-19李龙涛唐耀春
潘 磊,李龙涛,唐耀春
(1.浙江煤炭地质局勘探一队,浙江 湖州 313004;2.青海省第七地质矿产勘查院)
油田卤水也称油田水,广义的油田水包括油田区域内的油层水和非油层水在内的地下水,狭义的油田水是指油田区域内的和油层直接联通的地下水[1]。长期以来,中国有众多学者从油田卤水的形成与演化、分类和成分及油田水资源利用等方面做了研究[2-4]。 中国油田卤水资源丰富,油田水中除含有大量的Na+、K+、Ca2+、Mg2+等无机盐离子外,往往还富集有多种微量元素,如Li+、Rb+、Cs+等[1]。
目前,以碳酸锂(Li2CO3)为原料制备的高新技术产品的开发及应用正渐渐深入到各个领域。 随着世界锂盐产品在新能源、医学、航空航天等领域需求量逐年攀升,针对Li2CO3的需求量也在不断增加[5]。油田卤水中含有丰富的Li+,具有很好的经济效益和社会效益,将油田卤水中富含的锂资源实现产业化生产利用同样具有重要的战略意义。然而,在矿化度较低的油田卤水中Ca2+和Mg2+的含量较高[1],高镁锂比和钙锂比对提取油田卤水中的锂资源非常不利。为此,中国一些学者对卤水除钙和提锂方法做了研究。 李青林[6]采用芒硝和生石灰分别去除卤水中的Ca2+和Mg2+,制备得到碳酸锂产品主含量(质量分数,下同)达98.34%。 高文远等[7]采用芒硝兑卤的方法去除高钙盐田老卤中的Ca2+。 李冰等[8]将油田卤水蒸发浓缩后, 通过低温冷冻的方法分离出油田卤水中的钙。
笔者以某油田卤水为实验原料, 研究了兑卤除钙和冷冻结晶/兑卤复合除钙2 种工艺的分离效果,再采用纯碱沉锂的方法制备了Li2CO3并做了相关探讨。
1 实验
1.1 原料与试剂
实验所用原料为某油田卤水,其各主要离子含量、pH 及密度见表1。 Na2SO4·10H2O,分析纯,天津市化学试剂厂提供。

表1 油田卤水各主要离子含量、pH 及密度
1.2 仪器
ICAP6300 型电感耦合等离子光谱仪、78-1 型磁力加热搅拌器、AL104-IC 型电子天平、HH-8 型电热恒温水锅、WSB-3C 型荧光白度计、HYL-1001型粉体物理特性测试仪、烧杯、量筒等。
2 实验结果
2.1 有机相去除
油田卤水中含有部分水溶性有机物杂质,会对最终的产品指标产生影响。 本实验以CCl4为萃取剂,采用萃取分离的方法除去这部分有机物杂质[9]。油田卤水中除了含有部分有机物外, 剩余的为大量无机盐离子。 因此,化学需氧量(COD)作为有机物含量的一项综合性指标同样适用于表示油田卤水中有机物的含量。本实验采用分光光度法测量萃取前后油田卤水中有机物含量,结果如图1 所示。 由图1 可以看出,萃取前后油田卤水中有机物含量明显减少。
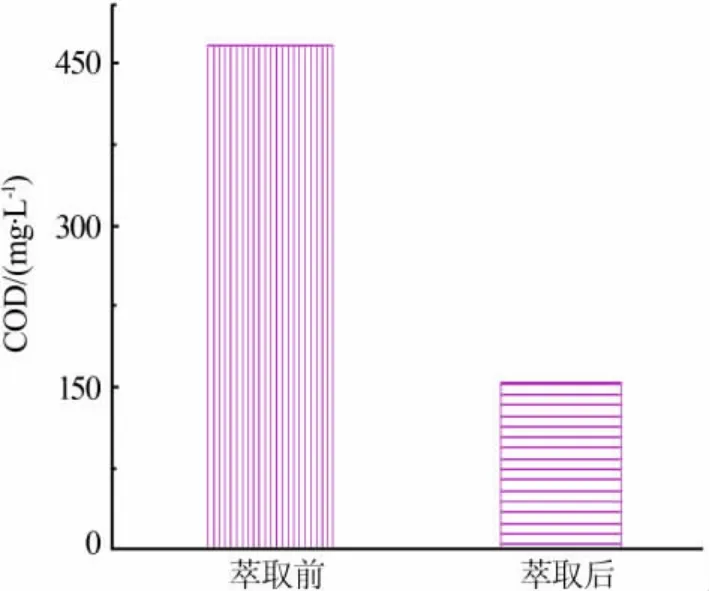
图1 萃取前后油田卤水COD 值
2.2 卤水蒸发浓缩
将油田卤水摊晒至小型盐田中,在自然条件下蒸发浓缩20 d,如图2 所示。
蒸发过程结束后, 采用抽滤方式分离其中的固相并测量卤水中各主要离子含量、pH 及其密度,结果如表2 所示。

图2 油田卤水及其自然蒸发照片

表2 油田卤水各主要离子含量、pH 及密度
2.3 芒硝兑卤除钙-纯碱沉锂工艺
2.3.1 芒硝兑卤除钙
兑卤结束后,采用抽滤方式除去其中的固相。将过滤后的卤水在自然条件下蒸发20 d, 经固液分离测得液相卤水中各主要离子含量,结果见表3。由表3可知,卤水中剩余Ca2+的质量浓度只有0.17g/L。

表3 除Ca2+后油田卤水各主要离子含量、pH 及密度
2.3.2 纯碱沉锂
温度为85 ℃条件下, 在2.3.1 节制得的原料卤水中按过量20%加入质量分数为25%的纯碱溶液,搅拌转速设定为120 r/min,反应时间为45 min。
反应完成后,采用离心分离方式进行固液分离,将所得固相(湿相)与90 ℃去离子水按质量比1∶3混合,在恒温条件下搅拌浆洗5 min,搅拌转速设定为120 r/min,浆洗过程结束后采用离心分离制得固相产品。将所得样品在120 ℃下干燥,研磨后做检测分析,结果见表4。 从表4 分析结果可以看出,采用芒硝兑卤工艺除去油田水中的Ca2+, 再采用纯碱沉淀卤水中的锂制备得到的碳酸锂产品主含量为95.65%,其中Ca2+质量分数较高,主要是因为采用芒硝兑卤方法去除卤水中的Ca2+后, 仍然有少量Ca2+残存于卤水中,加入纯碱后以CaCO3形式存在于产品中,造成Li2CO3主含量降低。

表4 Li2CO3 成品检测分析结果
2.4 冷冻结晶/芒硝兑卤除钙-纯碱沉锂工艺
2.4.1 冷冻结晶/芒硝兑卤除钙
取2.2 节浓缩制备的卤水5 L 置于冰箱内,在-5 ℃下冷冻6 d, 待冷冻过程结束后即刻采用抽滤的方法进行固液分离, 检测液相卤水中各主要离子含量,结果见表5。 从表5 可以看出,冷冻结晶后卤水中Ca2+质量浓度为37.4 g/L,说明该方法只能去除卤水中的大部分Ca2+。
对于上述冷冻结晶除钙后的卤水, 继续采用芒硝兑卤的方法除去其中剩余的Ca2+, 将芒硝溶液和卤水按与Ca2+物质的量比为1.3∶1 兑卤,再在室温下静置12 h,使其充分反应。
兑卤过程结束后进行固液分离, 将所得液相卤水在自然条件下蒸发浓缩5 d,除去其中固相后对液相卤水中各主要离子含量及密度进行检测, 结果见表6。

表6 除Ca2+后油田卤水各主要离子含量、pH 及密度
2.4.2 纯碱沉锂
温度为85 ℃条件下,在上述卤水中按过量20%加入质量分数为25%纯碱溶液, 搅拌转速设定为120 r/min,反应时间为45 min。
反应完成后采用离心分离方式进行固液分离,将所得固相(湿相)与90 ℃去离子水按质量比为1∶3混合, 在恒温条件下搅拌浆洗5 min, 搅拌转速为120 r/min, 浆洗过程结束后采用离心分离得固相产品。将所得样品在120 ℃下干燥,经研磨后再对其进行检测分析,结果见表7。 从表7 可以看出,该工艺制备的Li2CO3产品中杂质含量相对较少, 白度较高,堆积密度有所降低,因此采用复合工艺对于去除卤水中杂质离子效果更好。

表7 Li2CO3 成品检测分析结果
3 结论和展望
综合以上实验结果可以看出, 直接冷冻结晶去除卤水中Ca2+的工艺可以将卤水中大部分Ca2+分离,然而分离后的卤水无法直接用于碳酸锂制备;相比较而言,采用冷冻结晶/芒硝兑卤复合的工艺去除卤水中Ca2+的效果更佳,制得Li2CO3主含量可达到96.73%(质量分数)。 采用上述工艺制备的Li2CO3中杂质含量较高,为了进一步提高产品质量,可以借助目前兴起的膜分离、 吸附及电渗析等技术进一步除去卤水中的杂质离子,对于其中的可溶性杂质离子可以采用多次浆洗或淋洗的工艺去除。
