基质固相分散-乙腈/盐双水相萃取结合高效液相色谱法检测蔬菜中的苯脲类农药残留
2019-02-18徐尉力马铭扬李守志王志兵
徐尉力,马铭扬,李守志,赵 洋,付 壮,王志兵
(长春工业大学化学与生命科学学院,吉林长春 130012)
苯脲类除草剂(Phenylurea herbicides,Pus)是脲类除草剂中主要的一类,广泛用于一年生宽叶杂草的芽前和芽后阶段,主要通过抑制光合作用中的希尔反应以减弱叶绿体的活性,从而达到控制杂草的目的[1-2]。由于其在环境水[3-5]、土壤[6-8]中降解较慢,可通过生物富集作用残存于水果[9]、蔬菜[10-12]、茶叶[13]、稻谷[14]以及奶制品[15-17]中,继而对人体健康产生不利影响。相关研究[18-19]表明:灭草隆和利谷隆对野生动物和人类具有潜在的致癌作用,而其它苯脲类衍生物也具有一定的生态和遗传毒性。目前,欧盟、日本等发达国家和地区已对食品中苯脲类农药残留做出了相关规定,我国规定绿麦隆在麦类、玉米和大豆中的最高残留限量为0.1 mg/kg[2,20-21]。因此,建立一种检测食品中苯脲类农药残留的方法显得尤为重要。

图1 基质固相分散盐析诱导乙腈/盐双水相萃取流程图Fig.1 Schematic procedure of matrix solid phase dispersion followed by acetonitrile-salt based aqueous two-phase extraction
目前,常见的农残检测方法有毛细管电泳法[22]、气相色谱法[23]、酶联免疫法[24]、高效液相色谱-串联质谱法[25]以及高效液相色谱法[17]等,其中高效液相色谱法具有检测灵敏度高,选择性强,分析时间短等优点,已被广泛应用。基质固相分散是在固相萃取的基础上发展起来的一种新型样品处理方法,可用于固体、半固体及高粘性样品的制备[26]。它集样品分散、提取、净化于一体,有效提高了目标物的提取性能[27-28],但基质固相分散法仍使用较多的萃取溶剂,当处理复杂的基质样品时,会造成目标分析物在后续的旋蒸、浓缩、回溶等环节大量损失,从而使萃取回收率大大降低。双水相(Aqueous two phase systems,ATPs)是一种简单、高效的液-液分离萃取技术[29],在临界浓度下将两种溶液混合,当加入一种成相物质时,组分因疏水作用、范德华力以及表面张力等作用而发生相分离,逐渐形成稳定且互不相容的两相[30],由于目标物在两相中具有不同的分配系数,因此可以起到富集目标物的作用[31]。双水相萃取凭借作用条件温和,分离效果明显,环境友好无污染等优势在萃取、浓缩、分离过程中发挥着重要作用。
因此,本法选用乙腈水溶液为洗脱剂,采用基质固相分散法对蔬菜样品进行前处理,随后向洗脱剂中加入K2HPO4,使之发生盐析效应,形成稳定的乙腈/盐双水相体系,实现目标物的进一步萃取、净化与富集。本研究首次将基质固相分散与乙腈/盐双水相萃取相结合,用于蔬菜中苯脲类化合物的提取、分离和富集,并通过高效液相色谱对目标物进行定性、定量分析。
1 材料与方法
1.1 材料与仪器
黄瓜、西红柿、马铃薯、辣椒、西兰花(分别编号1~5) 购于当地超市;绿麦隆、灭草隆、利谷隆、敌草隆标准品 纯度均>99%,阿拉丁试剂公司;硅胶(200~300目)、硅藻土(200~300目)、弗罗里硅土(60~100目)、酸性氧化铝(100~200目,pH4.0~5.0)、中性氧化铝(200~300目,pH6.5~7.5)和碱性氧化铝(200~300目,pH9.0~10.0) 中国药品生物制品检定所。
Agilent LC-1100高效液相色谱仪(配有四元泵、真空脱气机以及二极管阵列检测器)、Zorbax SB-C18色谱柱(3.5 μm,4.6 mm×150 mm)、C18预柱(5 μm,7.5 mm×2.1 mm) 美国安捷伦科技公司;KQ-100DE超声波清洗器 江苏昆山超声仪器公司;Allegra 64R高速离心机 美国贝克曼库尔特公司。
1.2 实验方法
1.2.1 标准溶液配制 分别准确称取绿麦隆、灭草隆、利谷隆和敌草隆标准品各5 mg置于10 mL棕色容量瓶中,用乙腈定容至10 mL,混匀后得到500 μg/mL的标准储备液,于4 ℃环境中避光保存。后续实验所用工作溶液均由标准储备液经乙腈稀释得到。
1.2.2 样品预处理 将所有新鲜蔬菜样品洗净后沥干,用搅拌机切碎后保存于-20 ℃冰箱中备用。加标样品通过向样品中加入一定量的工作溶液搅拌均匀后得到。在后续实验中,除回收率和实际样品分析外,其余实验结果均由样品1(黄瓜)获得。
1.2.3 基质固相分散-乙腈/盐双水相萃取 如图1所示,首先向玛瑙研钵中准确加入0.3 g加标样品和0.9 g硅胶,充分研磨5 min,使样品与硅胶完全混匀,将混合物转移到底层铺有脱脂棉的萃取柱中,在混合物上方再放置一层脱脂棉,并用玻璃棒轻轻压实。随后,用20%的乙腈水溶液(自然pH)作洗脱剂,在重力作用下对目标物进行洗脱,随后用10 mL离心管收集洗脱液。收集3 mL后,向离心管中加入0.9 g K2HPO4,并在200 W下超声10 min,然后在8000 r/min下离心5 min,则乙腈/盐双水相体系形成,上层溶液为富集有目标物的乙腈相。最后取100 μL上相,用100 μL乙腈稀释后,过0.22 μm滤膜,进行色谱分析。
1.2.4 色谱条件 流动相由水(A)和乙腈(B)组成,梯度洗脱条件为:0 min,30%(B);0~10 min,30%~40%(B);10~18 min,40%~50%(B);18~25 min,50%~65%(B),25~27 min,65%~30%(B);27~30 min,30%(B)。流动相流速:0.5 mL/min;进样体积:10 μL;柱温:35 ℃;检测波长:245 nm。
1.2.5 加标回收率、萃取率和相比计算


萃取率(%)=[上相体积(mL)×上相中目标物浓度(μg/mL)]/[加标体积(mL)×加标浓度(μg/mL)]×100
1.3 数据处理
萃取条件优化与方法学的数据均通过Excel进行统计分析,并通过Origin 8.0.6软件进行作图和数据拟合。
2 结果与分析
2.1 萃取条件优化
2.1.1 分散剂的影响 不同的分散剂对样品组织的破碎能力以及对目标物的吸附能力有所不同。当使用酸性氧化铝、中性氧化铝和碱性氧化铝作分散剂时。一方面,由于它们对目标分析物的吸附能力较强[28],使目标分析物不易从萃取柱中被洗脱出来,从而使各目标分析物的回收率相对较低(见图2A)。另一方面,由于它们的吸水性差,易粘结,不利于高水分含量蔬菜样品的研磨。当使用硅胶和硅藻土做分散剂时,由于其具有较大的网状孔隙结构,对目标物具有较大的接触面积,其吸水性好,从而使蔬菜样品的分散效果较好,回收率较高。但使用硅藻土作分散剂时,由于粘性较大,使后续洗脱时间较长。而弗罗里硅土略有吸水性,无沙性,不利于样品的分散。因此,本研究选用硅胶作为分散剂。
此外,本研究还考察了样品与分散剂的质量比(1∶1、1∶2、1∶3、1∶4和1∶5)对目标物回收率的影响。实验结果如图2B所示,当样品与硅胶的质量比为1∶3时,目标分析物的回收率最高。所以,本研究将样品与硅胶的质量比定为1∶3。

图2 分散剂种类(A)和样品与分散剂的 质量比(B)对回收率的影响Fig.2 Effect of type of dispersant(A)and mass rotio of sample to dispersant(B)on recovery
2.1.2 乙腈浓度的影响 在本研究中,通过向10 mL水溶液中加入不同体积的乙腈溶液配制出不同体积比(20%、22%、24%、26%、28%、30%、32%,v/v)的乙腈水溶液,乙腈水溶液作为基质固相分散的洗脱剂和乙腈/盐双水相体系的成相溶剂,乙腈浓度决定了上相体积和富集效果,对萃取率和回收率均产生影响。一方面,乙腈作为基质固相分散的洗脱剂,其浓度越高,从萃取柱中提取和分离的目标物分子越多,萃取率越高,如图3A所示,当乙腈浓度达到28%时,各目标物的萃取率达到最大值。另一方面,乙腈作为双水相体系的成相溶剂,不仅影响后续双水相体系的形成,也影响目标分析物的富集效果。当乙腈浓度低于20%时,萃取体系无法观察到明显的浊点现象,双水相体系不能形成,当乙腈浓度高于20%时,浊点现象产生,静置后双水相体系形成,且随着乙腈浓度的增加,相比显著升高。从图3B可以看出,当乙腈浓度为20%时,各目标分析物的回收率达到最大值。此时,目标物的萃取率尽管只有50%左右,但相比最小(见图3A),上相溶液(即乙腈相)体积仅为200 μL,富集效果最佳。综合考虑,本研究选用浓度为20%的乙腈水溶液作为洗脱剂。

图3 乙腈浓度对萃取率、相比(A)和回收率(B)的影响Fig.3 Effect of acetonitrile concentration on extraction yield,phase ratio(A)and recovery(B)
2.1.3 洗脱剂pH的影响 通过向水溶液加入pH=1的HCl溶液和pH=14的NaOH溶液以调节洗脱剂的pH,改变了目标分析物的解离状态和双水相体系的电荷分布,继而影响目标分析物的回收率。因此,本研究考察了不同pH的洗脱溶剂对各目标物回收率的影响,由于乙腈浓度和体积均固定,双水相中上相体积不会发生变化,因而并未考察不同pH的洗脱剂对各目标物萃取率的影响。实验结果如图4所示,当洗脱剂pH由1逐渐增加到12时,各目标物回收率基本不变,这说明pH对回收率没有明显的影响,这与文献报道的相一致[32]。因此,为了简化实验操作,本研究选择不调节洗脱剂的pH。

图4 洗脱剂pH对回收率的影响Fig.4 Effect of pH value of elution solution on recovery
2.1.4 洗脱液体积的影响 本研究考察了不同洗脱液体积(1、2、3、4、5、6、7和8 mL)对目标物回收率及萃取率的影响。由于样品中目标物含量一定,乙腈水溶液用量越大,相比越大,目标物萃取率随洗脱液体积的增加而增大,当收集的洗脱液达到3 mL时萃取率趋于平衡,实验结果如图5A所示。但实验既考虑上相体积增大对目标物的提取效果的影响也要考虑对富集效果的影响,通过分析上相中各目标物的回收率,发现当洗脱液体积由 1 mL 增加到 3 mL时,各目标物回收率明显提升且达到最大值,实验结果如图5B所示。这说明3 mL左右的洗脱液足以将目标物从基质固相分散萃取柱中洗脱出来,但随着收集的洗脱液体积的继续增加,目标物回收率反而大幅度下降,造成这种现象的原因是当收集的洗脱液体积体积达到3 mL时目标物萃取率趋于稳定,但上相体积增大,起到一定的稀释作用,目标物回收率逐渐下降,富集效果变差。因此,本研究选择收集3 mL洗脱液用于后续实验。

图5 洗出液体积对萃取率、相比(A)和回收率(B)的影响Fig.5 Effect of volume of elution solvent on extraction yield,phase ratio(A)and recovery(B)
2.1.5 成相盐种类的影响 当样品用基质固相分散法处理后,获得了由乙腈水溶液组成的样品洗脱液,向其中加入成相盐后,盐离子与水分子间产生较强的离子水合作用,使乙腈溶液不断失去水分子,当乙腈聚集到一定程度时与盐水相发生分离,双水相体系形成,目标分析物则通过疏水作用、氢键和范德华力等分配到上相溶液(乙腈相)中,从而达到分离富集的目的[33]。由于不同种类的盐溶于水后会产生不同的盐析效果,因此本研究考察了K2HPO4、Na2CO3、(NH4)2SO4、K2CO3、KH2PO4、Na2SO4、NaCl(添加量均为0.9 g)等7种成相盐对回收率的影响,由图6A中可以较为直观的看出,KH2PO4、Na2SO4无法诱导乙腈/盐双水相体系的形成,NaCl上相体积过少,无法定量取出,而K2HPO4、Na2CO3、(NH4)2SO4、K2CO3这四种盐则可形成稳定的乙腈/盐双水相体系。因此,

图6 盐的种类对相比(A)和回收率(B)的影响Fig.6 Effect of salt type on phase ratio(A)and recovery(B)

表1 线性关系、检出限和定量限Table 1 Linear regressions,LODs and LOQs for the analytes

表2 日内和日间精密度(n=6)Table 2 Intra-day and inter-day precision for the analytes(n=6)
本研究又选取了K2HPO4、Na2CO3、(NH4)2SO4、K2CO3等四种盐进行了回收率实验。实验结果如图6B所示,当乙腈浓度为20%,洗脱液体积为3 mL,成相盐用量为0.9 g时,选用K2HPO4作为成相盐所获得的目标分析物的回收率最高。因此,本研究选用K2HPO4作为成相盐。
2.1.6 盐用量的影响 成相盐的用量会影响目标物解离状态以及离子强度,进而影响双水相体系的上相/下相体积比和对目标分析物的富集效果。实验结果如图7所示,当盐的用量少于0.8 g时,不能形成双水相体系;当盐用量由0.8 g增加到0.9 g时,双水相体系形成,目标分析物被乙腈富集到上相溶液中,其回收率逐渐增加,且达到最大值;当继续增加盐的用量时,目标物回收率先略有下降,后逐渐趋于稳定。这可能是因为盐的用量不断增加,使得盐离子与乙腈竞争水分子的能力不断增强,从而导致更多的乙腈被聚集,上相体积略有增加,进而对目标物产生一定的稀释作用。所以,本研究选择成相盐的质量为0.9 g。
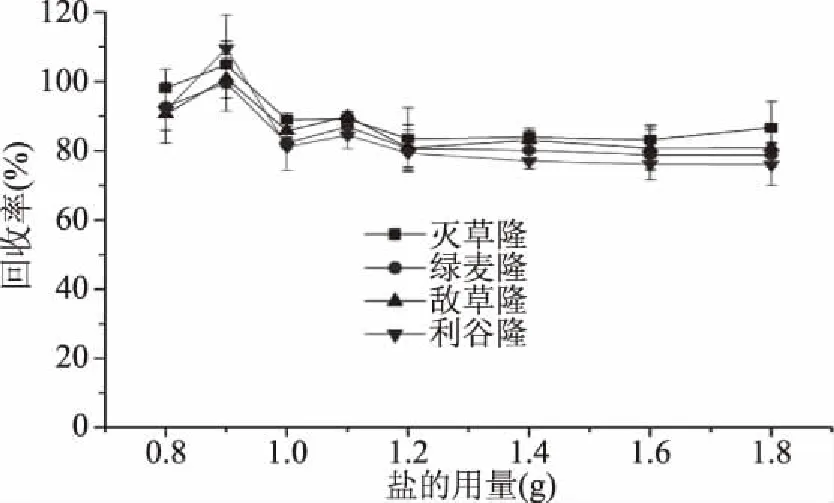
图7 成相盐用量对回收率的影响Fig.7 Effect of salt amount on recovery
2.2 方法评价
2.2.1 线性关系、检出限和定量限 配制含有4种目标物的混合标准溶液,经乙腈梯度稀释后加入到样品1中,得到含有系列浓度的加标样品,在最优条件下对加标样品进行提取分析。以加标浓度(c)为横坐标,以峰面积(A)为纵坐标绘制工作曲线,得到线性回归方程。通过分析11组低浓度空白加标样品,计算方法检出限和定量限。实验结果表明,各目标物线性关系良好(r>0.9988),检出限和定量限分别为0.9~1.5和2.9~4.9 μg/kg。实验结果如表1所示。
2.2.2 精密度 本研究测定了样品加标浓度分别为5.0、50.0和150.0 μg/kg时的方法精密度,并用重复分析测定所得回收率的相对标准偏差(RSD)表示日内和日间精密度。日内精密度指1 d内对加标样品连续分析6次所得回收率的相对标准偏差;日间精密度指每天分析2次,连续分析3 d所得回收率的相对标准偏差。结果如表2所示,日内和日间精密度分别为1.7%~8.6%和4.0%~9.8%。
2.2.3 回收率 为了检验本法的准确度,本研究分析了加标浓度为5.0和50.0 μg/kg的5种蔬菜样品,各目标物的回收率在84.3%~118.8%之间,其相对标准偏差为1.3%~10.1%,实验结果表明,本法具有良好的准确度,可用于蔬菜中苯脲类化合物的检测。结果如表3所示。

表3 实际样品分析(n=3)Table 3 Analysis of real samples(n=3)
注:“-”表示空白样品;“ND”表示未检出。

表4 化合物的稳定性(n=5)Table 4 Stability analysis of spiked samples(n=5)
2.2.4 稳定性 为了考察蔬菜样品中苯脲类化合物的稳定性,将加标浓度为5.0和50.0 μg/kg的蔬菜样品每隔1周分析一次。结果如表4所示,各目标物回收率在95.3%~110.8%之间,相对标准偏差为1.2%~8.6%。结果表明,苯脲类化合物在28 d内是相对稳定的,样品基质对目标物影响不大。
2.3 实际样品分析
为了考察本法的适用性,本研究分析了5种蔬菜样品,实验结果如表3所示,所有实际样品中均未检出苯脲类除草剂。色谱图如图8所示,各目标物保留时间内无明显杂质干扰峰。因此,本法可用于检测不同种类蔬菜中的苯脲类除草剂残留。
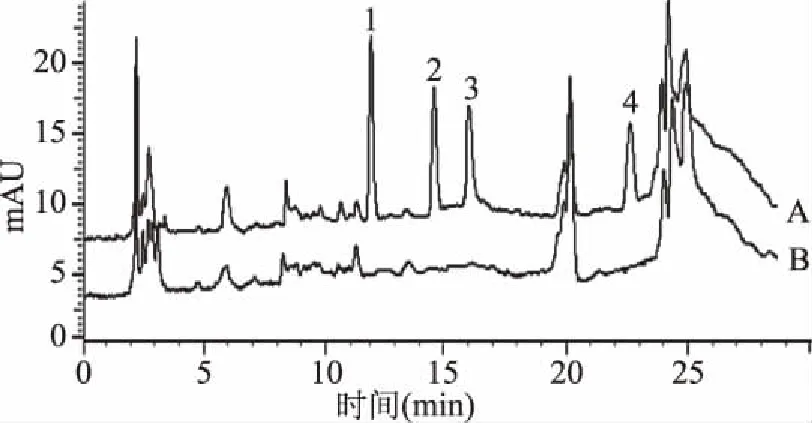
图8 加标样品(A)和空白样品(B)的色谱图Fig.8 Chromatograms of spiked sample(A) and blank sample(B)注:1:灭草隆;2:绿麦隆;3:敌草隆;4:利谷隆。
2.4 方法比较
本研究构建了一种新的基质固相分散-乙腈/盐双水相萃取体系,用于蔬菜中苯脲类农药残留的提取、净化、浓缩与富集,如表5所示。与基质固相分散法和固相萃取法相比,本法有机试剂用量少(仅为1 mL),不需旋蒸、离心等操作,可直接用于色谱分析,简化了实验步骤,并且在检出限和回收率等方面也表现出优良的性能。

表5 本方法与其它方法比较Table 5 Comparison between the proposed method and other methods
3 结论
本研究将基质固相分散与乙腈/盐双水相萃取法相结合,通过高效液相色谱同时测定蔬菜中的4种苯脲类化合物,建立了一种简单、高效的农残分析方法。本研究采用基质固相分散法对蔬菜样品进行前处理,并通过乙腈/盐双水相体系对目标物进一步提取、净化与富集,减少了样品基质的干扰,使得提取过程变得更加简单、高效。各目标化合物在线性范围内具有良好的线性关系(r>0.9988),检出限与定量限分别为0.9~1.5 μg/kg 和 2.9~4.9 μg/kg。日内和日间精密度分别为1.7%~8.6%和4.0%~9.8%,加标回收率在84.3%~118.8%之间。与其他方法相比,该法具有试剂用量少,净化效果好,提取过程简单、高效等优势,可用于蔬菜中苯脲类化合物的提取与分析。
