三维可视化技术辅助解剖性肝切除术的应用体会
2019-02-14李留峥王峻峰徐雷升俸家伟王志萍高学昌龚国茶于杰
李留峥,王峻峰,徐雷升,俸家伟,王志萍,高学昌,龚国茶,于杰
(1.临沧市人民医院 肝胆外科,云南 临沧 677000;2.云南省第一人民医院 肝胆外科,云南 昆明650032)
随着肝脏外科技术的提高,解剖性肝切除术已在临床广泛应用[1-2],但术前评估不足,手术操作不当仍可导致胆管、血管损伤及术后肝功能衰竭等不良后果。随着数字医学的发展,三维可视化技术能显示肝脏脉管系统与病灶的三维立体关系,准确测量残肝体积,对指导解剖性肝切除手术规划,减少手术并发症具有重要作用。临沧市人民医院2016年1月至2017年12月共对78例肝肿瘤及复杂肝胆管结石患者行三维可视化技术辅助解剖性肝切除术,取得了满意效果,现报道如下。
1 资料和方法
1.1 一般资料
纳入标准:(1)患者本人有手术愿望,肝脏肿瘤未做过介入、栓塞等治疗;(2)大肝癌及特殊解剖部位的肿瘤或复杂肝内胆管结石;(3)术前肝功能Child-Pugh分级为A级;(4)一般情况好,能耐受肝叶及肝段切除者。排除标准:(1)小肝癌、较小直径的肝脏良性肿瘤等手术操作相对容易者;(2)多叶、多段的多发性肝癌;(3)肝外远处转移或者晚期肿瘤恶液质;(4)肝功能Child-Pugh C级难以耐受手术者。
全组纳入78例,其中男47例,女31例,年龄32~70岁,平均(44.1±11.2)岁。其中原发性肝癌59例,胆管细胞癌5例,肝门部胆管癌2例,胆囊癌5例,巨大肝血管瘤4例,复杂肝内胆管结石3例。并发HBV 54例,HCV 1例。肿瘤最大直径27.0 cm,平均(10.4±2.7)cm。术前肝功能Child-pugh分级78例均为A级,54例合并不同程度的肝硬化,术前行PTCD引流2例。患者均签署知情同意书,经医院伦理委员会批准。
1.2 术前三维可视化分析
肝脏CT数据的采集:78例均行肝脏CT增强扫描,采集患者平扫以及动脉、静脉、门脉期三期检査的图像数据,获取亚毫米DICOM格式的CT数据,将上述数据导入Slicer三维重建软件,进行分割、配准和三维重建,构建肝脏三维可视化图像模型,计算肿瘤的大小、数目,肝内血管走行及解剖分型,肿瘤与血管的三维空间比邻。拟行肝切除术,则于Slicer系统中进行虚拟肝切除术,计算肝脏的全肝体积、肿瘤体积、拟切除标本体积、残肝体积、功能性肝体积、残肝体积比,进行手术安全评估。
1.3 手术规划
78例患者术前均行肝肾功能、凝血功能、肿瘤标志物、HBV-DNA及肝脏CTA等资料进行综合分析,术前应用三维可视化技术精确评估,明确肝脏储备功能、病灶与血管的毗邻关系,术前分析肝脏解剖及变异,判断病灶及切除平面与门静脉、肝静脉各级分支距离及所属关系,设计虚拟切除平面,从残肝体积方面评估患者肝脏储备功能,准确进行手术风险评估,在三维可视化模型指导下制定手术规划及解剖性肝切除方案。精确量化评估肝脏储备功能,半肝以上切除时依据体质量(kg)×0.8%的公式计算残肝体积。本组78例满足患者所需最小残肝容积。伴有乙型肝炎肝硬化者常规行吲哚菁绿15 min滞留率(ICG-R15)测定,全组检测ICG-R15结果,符合《肝切除术前肝脏储备功能评估的专家共识》肝脏切除安全限量的要求。
1.4 辅助治疗
术前常规给予极化液、VitK、新鲜血浆、人血白蛋白等保肝对症支持治疗,所有患者术前肝功能恢复到Child A级。术后严格控制液体摄入量,防止大量腹水形成,注意纠正水盐电解质平衡等。
1.5 手术方法
78例均采用解剖性肝切除术:常规全麻,采用反“L”切口,充分离断肝周韧带暴露肝脏,按Glisson蒂横断式肝切除法行解剖性肝切除[3]。解剖第一、第二肝门,切断相应肝段的Glisson系统分支,预置肝静脉阻断带。按肝脏缺血范围、段间解剖平面,采用钳夹法切断肝实质,对肝静脉属支及肝内Glisson蒂结扎切断,结合术中B超显露保护肝静脉主干,完整切除病变的肝叶或肝段。图1是典型肝癌患者的三维可视化辅助解剖性肝切除手术。图2是典型复杂肝内胆管结石患者的三维可视化辅助解剖性肝切除手术。
1.6 观察指标
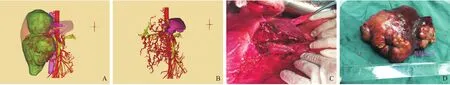
图1 巨大肝癌病例术前规划和手术图片
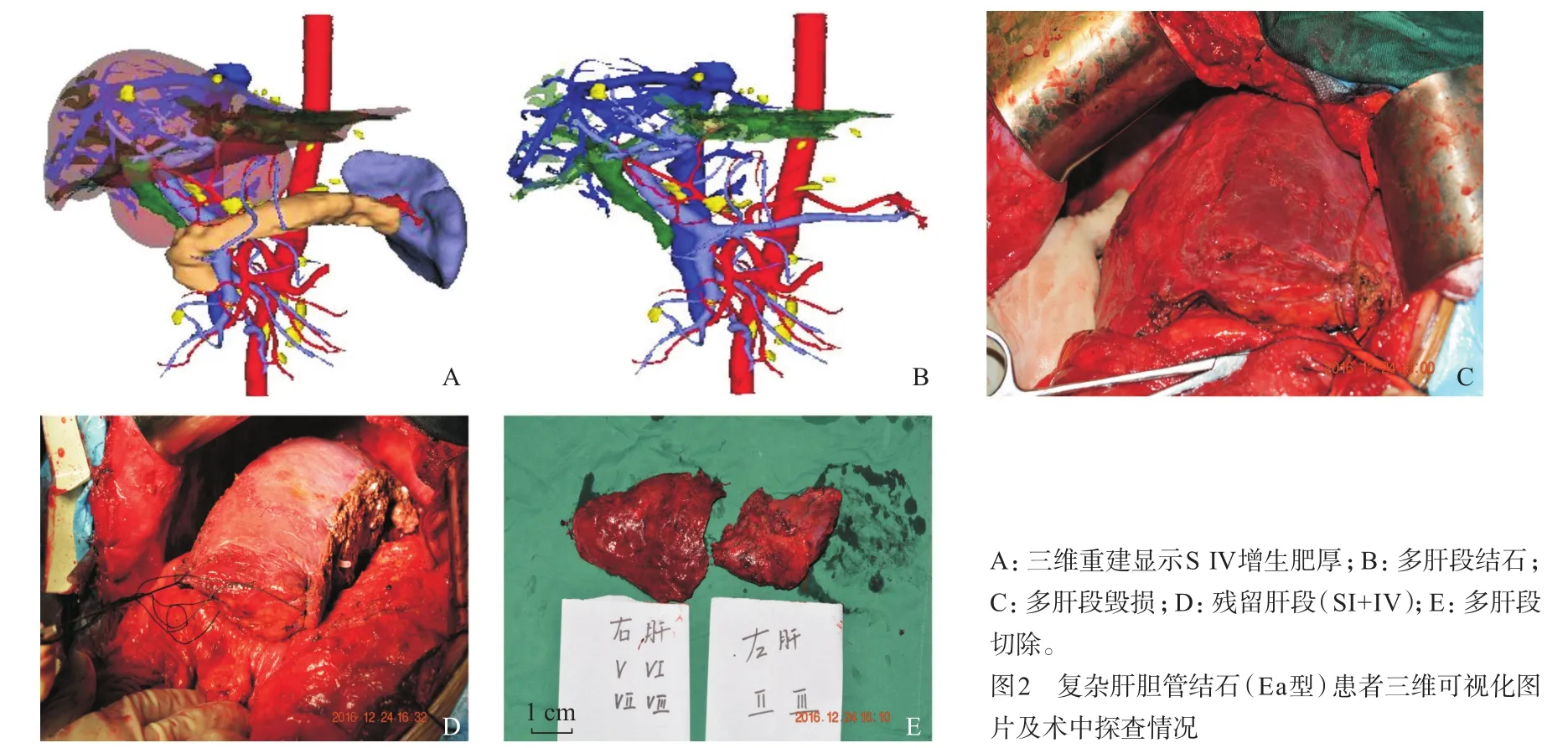
图2 复杂肝胆管结石(Ea型)患者三维可视化图片及术中探查情况
(1)手术时间:从切开皮肤开始至完成肝切除术及关腹所用的时间;(2)术中出血量:手术中吸引出血液体量(mL)及血垫称重(1g相当于1 mL)出血量的总和;(3)实际切除肝体积:切除的功能肝体积和肝肿瘤的体积,以量杯排水法按mL计量;(4)术后住院时间:患者手术当日至出院时的天数。
1.7 统计学分析
采用SPSS 20.0统计软件进行分析,计量资料数据均符合正态分布,以(±s)表示;采用率表示分类资料。采用配对t检验比较虚拟切除肝体积和实际切除肝体积。P< 0.05为差异具有统计学意义。
2 结果
78例患者均通过Slicer软件获得了完整解剖结构的三维可视化图像,清楚显示肝病变部位、大小、形态,与胆管、血管的关系。借助三维可视化分析系统对肝脏进行三维重建和三维可视化分析,计算功能肝体积、肝肿瘤体积、虚拟切除体积、和残肝体积比等,分析肝脏解剖、制定手术规划。
全组均采用三维可视化技术辅助完成了解剖性肝切除术,虚拟切除肝体积为(1 020±264)mL,实际切除肝体积(1 125±267)mL,二者无统计学差异(P>0.05)。功能肝体积(1 471±194)mL,残肝体积(733±130)mL,残肝体积比(0.49±0.09),实际切除肝体积(1 028±258)mL。
按照三维可视化模型和手术方案完成手术69例(88.5%),9例因术中判断病灶与手术规划有偏差,而缩小或扩大切除范围,其中6例病灶较大,侵犯肝中或肝右静脉,手术规划方案需要行肝三叶切除,术中充分考虑到患者肝硬化重,残肝体积及功能残肝的代偿能力不足,完整切除肿瘤的前提下,改为半肝切除;3例患者计划肝段切除,术中发现病灶切除不彻底或切缘阳性,改为多段或半肝切除。
本组I段切除3例,I+II+III+IV段切除3例,I+II+III+IV+V+VIII段切除1例,I+IVb+V段切除3例,左半肝(II+III+IV段)切除16例,II+III+IV+VIII段切除1例,II+III+V+VI+VII+VIII段切除1例,左三叶(II+III+IV+V+VIII段)切除3例,IVb+V段切除5例,IV+V+VIII段切除3例,右三叶切除(IV+V+VI+VII+VIII段)3例,右半肝切除(V+VI+VII+VIII段)23例,右前叶(V+VIII段)切除5例,右后叶切除术(VI+VII段)4例,VIII段切除4例。其中2例肝门部胆管癌I+IVb+V段切除同时行肝管空肠Roux-en-Y吻合术。手术时间(210±54)min,术中出血量(671±231)mL,术后住院时间(18.5±3.2)d。术后并发症率15.4%(12/78),1例术后15 d肝衰竭死亡,其余均对症治疗痊愈,详见表1。
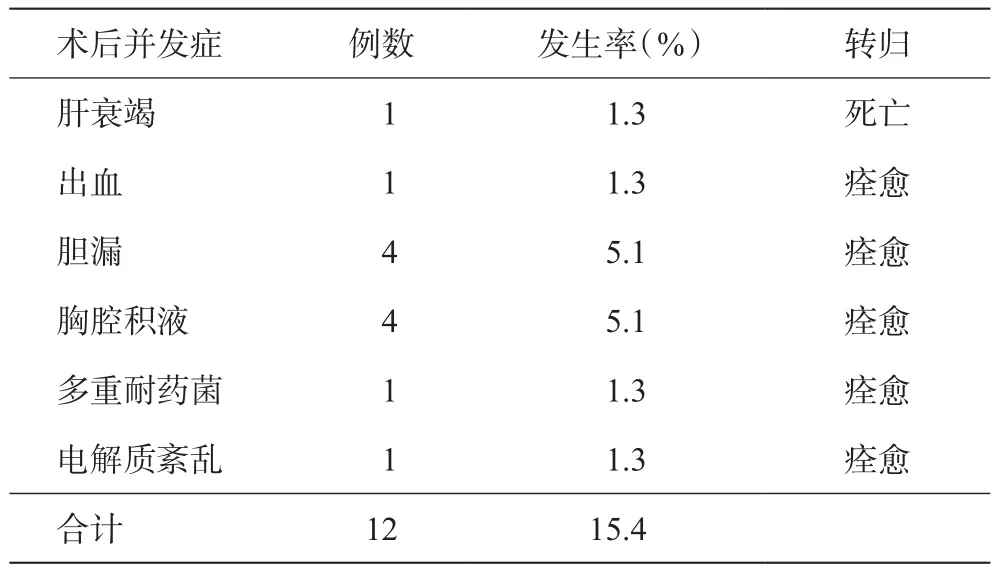
表1 术后并发症情况
术后获随访61例,其中肝恶性肿瘤患者术后1、2年存活率为79.6%(43/54)、64.8%(35/54),7例肝血管瘤和肝内胆管结石患者术后无复发。
3 讨论
手术切除是目前公认的治疗肝细胞癌最有效的方法[4]。解剖性肝切除使肿瘤的切除更为彻底,但较非规则性肝切除术,损失了更多的功能性肝脏组织,尤其是慢性肝炎肝硬化患者面临更大的术后肝衰竭的风险[5]。传统的CT、MRI等影像学技术,术者多凭二维图像以及临床经验来评估病灶的形态、大小,难以准确计算残肝体积及残肝体积比,尤其容易忽略存在的血管及胆管的变异,经验不足者术前读片往往难以全面掌握肿瘤与周围血管的空间关系及相关结构,可能导致术前制定不合理的手术方案,增加了手术的盲目性和风险,降低了精准肝切除的可靠性,并会对患者造成血管、胆管等损伤,出现严重并发症[6-7]。三维可视化技术辅助解剖性肝切除术可术前虚拟切除体积、准确计算残肝体积和残肝体积比等数值,从肝储备功能方面评估肿瘤的可切除性及术后患者肝衰竭的几率,评估手术风险,有效提高手术安全性及精准肝切除术的可靠性。同时能让患者直观了解手术方案及手术风险,促进医患沟通,减少不必要的医疗纠纷[8-9]。
结合文献[10-11]及本组78例治疗体会,笔者认为三维可视化技术辅助解剖性肝切除术有以下优势:(1)三维可视化技术可提供精密的肝脏三维定量分析及模拟手术规划方案,是实现解剖性肝脏精准手术操作的基础。最大限度切除病灶,避免副损伤,提高手术的有效性;(2)对肝脏的解剖和变异进行个体化分析,准确测算残肝体积和残肝体积比等数值,计算安全的肝切除量,术前制定优化比对不同的手术方案,科学评估手术风险,在保证安全切缘的同时,减少对功能性肝组织的损伤和过多切除,帮助术者确定最佳手术路径,降低肝衰竭及其他术后风险,确保手术的安全性;(3)三维重建的立体结构,让术者更直观地分析病灶的位置与血管的毗邻关系,划定预切除的肝脏范围和界限,完整切除肿瘤的同时,保护残肝的胆管及血管受损,保证手术的合理性;(4)通过三维重建系统,术者从不同角度阅读肝脏肿瘤的确切位置、大小、数目,及脉管侵犯情况,掌握肝脏离断层面的解剖变异,确定残余肝脏的供血及引流路径,预判术中可能造成的副损伤以及必要的脉管重建,提高手术的精准性;(5)三维可视化技术对肝脏亚段肿瘤的定位以及肝段/亚段的肝脏体积测量较二维方法更加精确,能够测算门静脉分支和肝静脉的支配和引流区域,实现二维方法难以完成的肝段/亚段的肝脏体积测量,使术前手术规划更为精密;同时三维模拟手术设计对增加年轻医师的信心和外科手术操作具有较大帮助。有学者认为,应用三维可视化技术有助于提高手术安全性,降低术后并发症和残石率[12]。尤其对复杂肝内胆管结石施行多肝段切除时,如果缺乏清晰的肝脏三维可视化技术重建,将难以做到精准的肝段血管阻断和毁损肝段的彻底清除,必然导致结石残留或复发[12-13]。
鉴于目前的影像学技术尚不能完全显露肝内的管道结构,尤其是胆道结构,临床中往往难以获得理想的肝内胆管图像,尤其在伴门静脉癌栓或病灶压迫静脉时,导致血管充盈不足,三维重建效果不佳。故三维可视化技术仍存在局限性和不足,盲目依赖三维重建数据和手术规划有时会出现判断和手术偏差,造成不良后果。获得清晰、高质量的可靠CT影像数据,具备扎实的肝脏解剖和阅片能力,准确识别管道系统的解剖变异,才可能最大限度发挥三维可视化技术的临床价值优势,也是解剖性肝切除术的基础和安全保障。
术后肝衰竭和肿瘤早期复发是肝癌术后患者死亡的主要原因,手术及肝门阻断时间、大量出血及输血等是肝衰竭的主要因素。三维可视化技术对巨大肝脏肿瘤,肿瘤子病灶,血管微侵犯情况进行精确术前评估,对肿瘤的规范切除有较大帮助,并能明显缩短平均手术时间、住院时间,降低并发症发生率,术后肝功能较快得到恢复[14]。对肝切除术临床上较为粗糙的评估是术后残余肝体积在30%以上为安全范围,肝硬化患者则需要50%以上,才能有效地防止术后肝衰竭。虽然肝脏具备较强的再生和代偿能力,但由于术者对功能性肝脏体积、残余肝脏体积及残余肝脏体积比计算的重要性缺乏认识,术后肝衰竭仍时有发生。特别是对于复杂的巨大肝脏肿瘤手术,如果术前对肿瘤侵犯区域不明确,术中极容易损伤血管、胆管,术中、术后大出血和术后肝功能障碍等并发症的发生率较高。三维可视化技术可有效测量计算功能性肝体积,准确评估肝储备功能,对肝硬化患者的残余肝体积的计算有较大价值,大大提高了手术安全性,明显降低术后肝功能衰竭发生率。
本组78例患者进行了术前三维重建、手术规划及手术风险评估。其中69例按手术计划完成解剖性肝切除;6例病灶较大,侵犯肝中或肝右静脉,手术规划方案需要行肝三叶切除,术中充分考虑到患者肝硬化重,剩余肝体积及功能残肝的代偿能力不足,完整切除肿瘤的前提下,改为半肝切除,精准切除病灶的同时最大限度保护剩余肝;另3例计划肝段切除,术中发现病灶切除不彻底或切缘阳性,改为多段或半肝切除。78例患者均完整切除肿瘤及结石所涉及的肝叶肝段,达到解剖性肝切除的目的,但1例仍于术后15 d因肝功能衰竭死亡。笔者体会,三维可视化技术能多角度全方位地立体观察和术前模拟手术计划,术前能及时发现肝脏解剖变异,选择合理的手术方案,为解剖性肝切除提供依据,尤其对大肝癌的手术风险评估具有较大的价值;但对小肝癌及左外叶等切除则作用较小,况且增加患者的医疗成本。有报道三维可视化技术在无胆管、血管变异的标准肝切除术中并未体现出较多的优势[15]。故目前尚无依据把三维可视化技术作为术前常规检查,临床中应根据患者肝脏病灶的复杂程度选择性应用,方能凸显其价值。
