万古霉素在超重、肥胖患儿中的给药方案及药物监测的Meta分析
2019-01-30吕萌马姝丽
吕萌 马姝丽
(郑州大学附属儿童医院,河南省儿童医院,郑州儿童医院,药学部,郑州 450000)
近年来,超重和肥胖发生率在全世界不断攀升。2017年《中国儿童肥胖报告》指出,目前我国主要大城市0到7岁儿童肥胖率约为4.3%,7岁以上学龄儿童肥胖率约为7.3%[1]。超重、肥胖已经是危害儿童健康的一大问题。超重、肥胖还影响药物的体内药动学过程,例如药物的分布[2-3],引起血药浓度不达标,导致治疗失败。
万古霉素(vancomycin)属于糖肽类抗生素,可通过抑制细菌细胞壁的合成而发挥抗菌作用,用于治疗严重的革兰阳性菌感染,尤其是耐甲氧西林金黄色葡萄球菌、表皮葡萄球菌和肠球菌等所致严重感染。然而万古霉素说明书中并未提及此类患儿的给药方案。如何确定万古霉素在超重、肥胖患儿中的给药方案,使其血药浓度更加准确迅速达到有效浓度,是困扰临床诊疗的难题。本文通过文献检索和Meta分析,系统评价万古霉素在超重、肥胖患儿中的给药方案、血药浓度达标率及药动学特征,为临床万古霉素个体化治疗提供依据。
1 材料、对象与方法
1.1 检索策略
计算机检索英文数据库PubMed、Embase、Cochrane library、ClinicalTrials.gov。数据库PubMed及Embase检索策略见表1;Cochrane library以“vancomycin”为自由词搜索;Clinicaltrials.gov以“vancomycin”为自由词检索;检索中文数据库为中国知网(China National Knowledge Internet,CNKI)、万方医学网,检索词为“万古霉素”、“儿科”、“儿童”、“小儿”、“婴儿”、“新生儿”。检索时间均为建库至2017年12月31日。并通过追溯相关综述或研究的参考文献以寻找有效的研究。
1.2 文献纳入和排除标准
1.2.1 入选标准
文献有明确的分组,明确的给药剂量,研究对象≤18岁。
1.2.2 排除标准
非中文、英文文献个例报道,数据为重复文献,动物或者体外实验。
1.3 质量评价
由两名研究者独立评价文献质量。意见不一致时,通过讨论或咨询第三位研究者解决。观察性研究采用Newcastle-Ottawa Scale(NOS)评分(表2)。
1.4 统计学处理
对纳入的研究数据进行系统性评价,用相对危险度(risk ration, RR)表示二分类变量差异,用均值差(mean deviation, MD)表示连续型变量差异。必要的时候则用Cochrane协作网提供的Revman 5. 3软件进行荟萃分析。

表1 PubMed及Embase数据库检索策略Tab. 1 The search strategies of PubMed and Embase databases
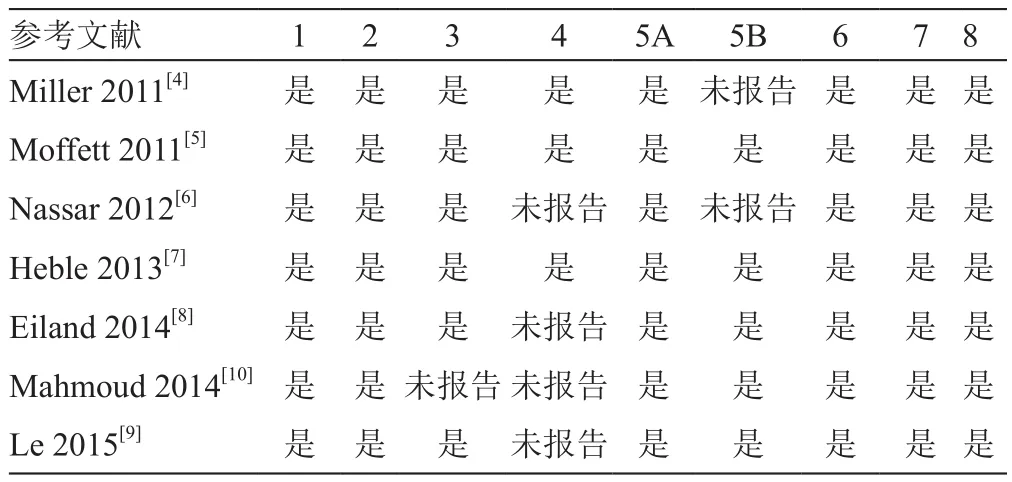
表2 纳入文献的质量评价Tab. 2 Quality evaluation of included studies
2 结果
2.1 检索结果及文献一般情况
最终纳入系统评价的文献共7篇[4-10],具体筛选过程如图1所示。其中5篇研究为回顾性研究,2篇研究为前瞻性研究。样本量为42~187人,5篇研究[4-5,7-8,10]纳入的对象是2~18岁患儿,2篇研究[5,8]纳入对象是2月~18岁患儿。3篇研究对象[5-6,10]主要是肿瘤患者;3篇研究[4,7-8]对象主要是感染患者;1篇研究[9]对象主要是感染和肿瘤患者,但是具体在超重、肥胖患儿中比例不详。对于超重、肥胖患儿的定义,7篇研究[4-10]以美国疾病预防控制中心(centers for disease control and prevention, CDC)的身体质量指数(body mass index,BMI)和儿童生长曲线为标准,其中1篇研究[10]仅指出超重、肥胖以BMI生长曲线定义,但未对BMI生长曲线的具体百分位数值进行说明。纳入系统评价的文献基本信息如表3~4所示。
2.2 结果分析
2.2.1 给药方案
7篇研究的给药间隔为6、8、12h及一日两次的给药方案(表4)。所有研究均未采用负荷剂量给药。维持剂量均基于实际体重(total body weight, TBW),在10~20mg/(kg·dose)范围之内。Miller等[4]研究表明,对于超重、肥胖及正常体重患儿,给药剂量无显著性差异的情况下[超重、肥胖组:(16.6±3.9)mg/(kg·dose);正常体重组:(17.2±4.1)mg/(kg·dose),P>0.05],给药间隔为8h更容易使患儿血药浓度达到5~15mg/L;血药浓度达到10~20mg/L需进一步缩短给药间隔。Moffett等[5]研究表明,在正常体重组患儿给药剂量更高的情况下[肥胖组:(14.1±1.5)mg/(kg·dose);正常体重组:(14.9±0.9)mg/(kg·dose),P=0.03],以q8h给药(87.5%),肥胖组患儿与正常体重组患儿血药浓度相比没有显著性差异[肥胖组:(6.9±4.3)mg/L;正常体重组:(4.8±3.1)mg/L,P>0.05]。Nassar等[6]研究表明,在肿瘤患者中(81.3%),给药剂量为20mg/(kg·dose),一天两次给药时,超重、肥胖组患儿血药浓度与体重正常组患儿血药浓度相比无显著性差异[超重、肥胖组:(3.06±1.86)mg/L;正常体重组:(3.53±2.53)mg/L,P>0.05],血药浓度达标率分别为0和3.2%,差异无统计学意义(P>0.05)。Eiland等[8]研究表明,给药总量没有显著性差异情况下[超重、肥胖患儿组:(44.40±14.14)mg(kg·dose);正常体重组:(48.86±10.50)mg/(kg·dose),P=0.08],q6h及q8h给药方案使所有患儿血药浓度达标率显著高于q12h给药方案。
2.2.2 稳态谷浓度
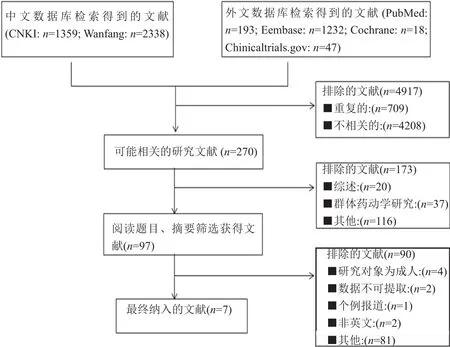
图1 文献检索、筛选流程及结果Fig.1 Process of selecting studies and the results
6篇研究报道了稳态血药谷浓度(表5),由于不同研究给药剂量差异较大,未进行数据合并,进行描述性分析。Miller等[4]研究发现,超重、肥胖患儿的的稳态谷浓度较正常体重患儿显著性升高[超重、肥胖组:(9.6±8.9)mg/L;正常体重组:(7.4±5.7)mg/L,P=0.03]。Herbe等[7]研究表明,超重、肥胖患儿谷浓度中位数较正常体重患儿显著性增高[肥胖组:15.2mg/L;超重组:13.5mg/L;正常组:10.5mg/L,P<0.001]。Madigan等[11]研究表明,同样的给药方案[q6h, 10mg/(kg·dose)或15mg/(kg·dose)],超重、肥胖患儿血药浓度较正常体重患儿显著性增高(P<0.05)。Mahmoud等[10]研究出现了相反的结果,同样的给药方案(q6h, 15mg/(kg·dose)),肥胖患儿血药浓度较正常体重患儿显著性降低[肥胖组:(4.34±2.9)mg/L;正常组:(6.14±1.87)mg/L,P<0.05]。另外2篇研究[5-6]差异无统计学意义。
分析稳态谷浓度>20mg/L的人群分布。Hebl等[7]研究表明,超重、肥胖组患儿血药浓>20mg/L发生率明显高于正常体重组(P=0.011)。Madigan等[11]将患儿按照体重划分(>50kg, 25~50kg, ≤25kg),结果表明体重>50kg组中,患儿血药浓度>20mg/L发生率显著性升高。
2.2.3 血药浓度达标率
5篇研究报告了血药浓度达标率(表5),达标的标准均定义为稳态谷浓度为10~20mg/L。根据文献对超重、肥胖的定义进行亚组分析。BMI>85th作为超重、肥胖的标准,患儿年龄在2~18岁之间的共3篇研究[4,7-8],各研究间同质性好(P=0.93,I2=0),采用固定效应模型,进行Meta分析。结果表明,超重、肥胖组患儿血药浓度达标率高于正常体重组,差异有统计学意义(RR=1.32, 95%CI: 1.01~1.72,P=0.04)。Nassar等[6]纳入年龄在2月~2岁的患儿,超重、肥胖的定义为≥98th身长体重曲线,超重、肥胖组患儿血药浓度达标率与正常体重组患儿血药浓度达标率没有统计学差异(P>0.05)。Moffett等[5]研究了BMI>95th患儿血药浓度达标率与正常体重组(25th
2.2.4 肾毒性
1篇研究[4]报告了超重、肥胖组患儿与正常体重组患儿肾毒性的发生率。肾毒性的定义是血清肌酐(serum creatinine, SCr)变化超过了0.5mg/dL或者相比于基线增加了30%。结果表明,超重、肥胖组患儿与正常体重组患儿肾毒性发生率无统计学差异(P=0.093)。
2.2.5 药动学参数
纳入的药动学参数主要为半衰期(half life,T1/2)、清除率(clearance, CL)及表观分布容积(volume of distribution,Vd)。3篇研究[6,9-10]均采用了一室模型计算获得超重、肥胖组患儿和正常体重患儿的药动学参数(表6)。但由于纳入的标准不一致,故进行描述分析。Nassar等[6]研究表明,与正常体重组患儿相比,超重、肥胖组患儿药动学参数无显著性差异。Le等[9]研究表明,超重、肥胖患儿T1/2、CL相比于正常体重组患儿均显著增加,Vd无显著性差异。Mahmoud等[10]研究表明,肥胖组患儿CL较正常体重组患儿显著性增加,T1/2、Vd相比于正常体重组患儿无显著性差异。
3 讨论
目前儿童给药方案可以分为两类:1)基于体重给药,例如基于调整体重、理想体重、实际体重、体表面积等给药方案;2)基于清除率的给药方案[12]。目前,美国感染病学会(infectious diseases society of America, IDSA)推荐无论是否为肥胖患者,万古霉素均基于实际体重给药[13]。本研究显示,目前万古霉素在超重、肥胖儿童中的给药方案比较统一,均基于实际体重给药。给药间隔为6h或8h更容易使血药浓度达到10~20mg/L,缩短给药间隔可以进一步升高患儿万古霉素血药浓度,这与万古霉素的药物代谢动力学特点相一致。
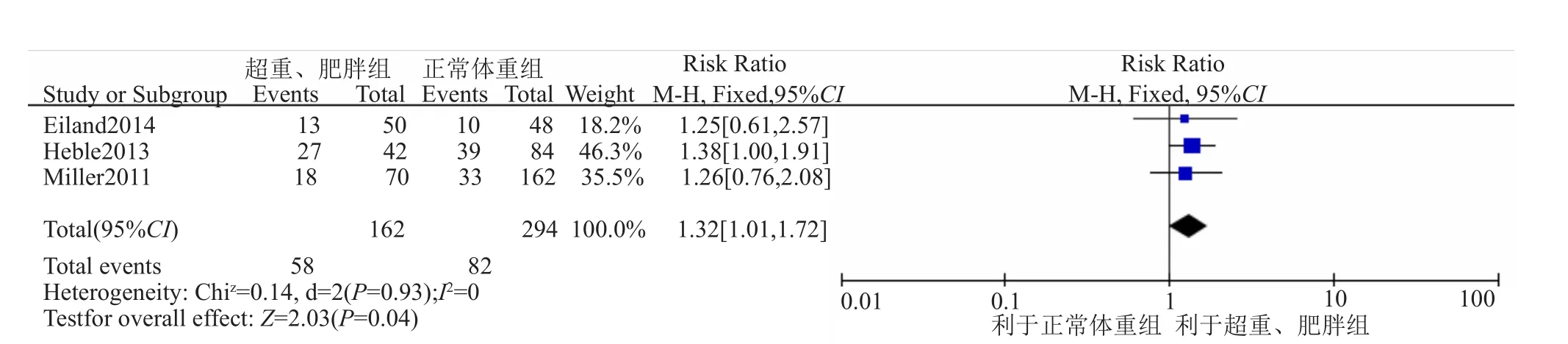
图2 超重、肥胖组患儿与正常体重组患儿血药浓度达标率Meta分析森林图Fig.2 Forest plot showing target concentration rate of vancomycin in overweight and obese versus normal weight pediatric patients
中国药理学会推荐成人患者应用万古霉素治疗时,谷浓度常规推荐10~15mg/L,若患者为重症感染等,可将谷浓度适当提升至15~20mg/L[14]。纳入6篇研究关于稳态血药浓度研究结果不一致。3篇研究[4,7,11]结果表明超重、肥胖患儿稳态谷浓度高于正常体重患儿,2篇研究[5-6]结果无统计学差异,1篇研究[10]结果表明正常体重患儿稳态谷浓度高于超重、肥胖患儿。分析原因可能由于纳入研究对象差异导致,Miller[4]、Heble[7]、Madigan等[11]研究纳入对象主要为非肿瘤患儿,Moffett[5]、Nassar[6]、Mahmoud等[10]研究对象主要为肿瘤患儿。此外,Moffett等[5]研究中50%数量的稳态谷浓度未能检测出来(<5mg/L),可能是未能检出统计学差异的原因。

表3 纳入研究的基本信息Tab. 3 Basic informationof selected studies

表4 纳入研究给药方案Tab. 4 Dosing regimes of selected studies

表5 纳入研究稳态谷浓度和血药浓度达标率Tab. 5Steady-state trough concentration andtarget concentration rate of selected studies
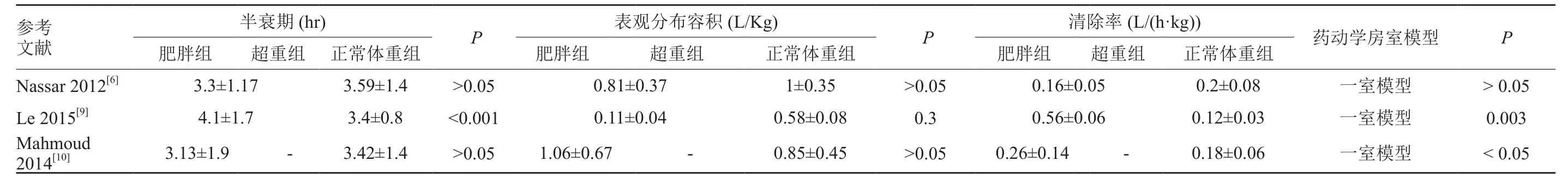
表6 纳入研究药动学参数Tab. 6 Vancomycin pharmacokinetic parameters of selected studies
Meta分析结果表明,超重、肥胖患儿的血药浓度达标率较普通体重患儿血药浓度达标率显著性增高。且超重、肥胖患儿万古霉素谷浓度>20mg/L发生率较正常体重患儿显著增高[7,11]。而更高的万古霉素谷浓度与肾毒性发生率有关[15]。因此,在超重、肥胖患儿使用万古霉素时,更应该进行血药浓度监测指导用药。此外,万古霉素稳态谷浓度作为药动学指标受儿童生长发育影响较大,研究表明以24h药时曲线下面积/最小抑菌浓度(area-under-the-curve of the serum concentrations vs. time over 24 hours/minimum inhibitory concentration,AUC/MIC)作为药效学指标更加精确[16-17],临床应严格将AUC/MIC作为超重、肥胖儿童的药效学评价指标。万古霉素CL在超重、肥胖患儿显著性增加,T1/2有增加的趋势,说明在以体质量为基础的给药方案时,要缩短给药间隔,这与给药方案的研究结果一致,给药间隔为6或8h给药更容易达到目标血药浓度。
本文的局限性主要为纳入的原始研究质量较低,纳入研究的数量较少,样本量较少。其次,纳入研究的人群种族各异、基础疾病复杂及肝肾功能存在一定差异。这些因素导致了研究之间存在一定的异质性。为了更加准确的了解超重、肥胖患儿万古霉素的给药剂量、药动学特点,尚需要进一步设计质量高、规模大的前瞻性临床研究。
4 结论
目前超重、肥胖患儿的万古霉素给药方案尚需进一步研究。基于实际体重的给药方案,给药间隔为6或8h,更容易达到血药浓度10~20mg/L。万古霉素在超重、肥胖患儿体内过程存在较大的个体差异,需要进行治疗药物监测指导给药。开展中国超重、肥胖患儿的万古霉素的给药方案及药动学参数临床研究亟待进行。
