不同提取方法对牡丹籽油品质与抗氧化性的影响
2019-01-26赵优萍张沙沙孙卢狄肖金妮蔡成岗肖竹钱沙如意毛建卫
赵优萍,张沙沙,张 婷,孙卢狄,肖金妮,蔡成岗,2,3,方 晟,肖竹钱,2,3,沙如意,2,3,毛建卫,2,3,*
(1.浙江科技学院生物与化学工程学院,浙江杭州310023;2.浙江省农业生物资源生化制造协同创新中心,浙江杭州310023;3.浙江省农产品化学与生物加工技术重点实验室,浙江杭州310023;4.绍兴文理学院元培学院,浙江绍兴312000)
牡丹(Paeonia suffruticosa)别称木芍药,有“花中之王”称号,是我国特有的木本花卉。牡丹为毛莨科芍药属落叶灌木,可分为观赏牡丹和药用牡丹。观赏牡丹主要在河南洛阳和山东菏泽广泛种植,而药用牡丹以安徽铜陵的“凤丹”最为著名[1]。牡丹籽是牡丹植株的精华结晶,其提取物含有大量人体需要的氨基酸、维生素和不饱和脂肪酸等活性成分,但是目前牡丹籽作为牡丹花和丹皮的副产物,一直未得到合理的开发和利用[2]。牡丹籽油是卫生部公布的一种木本食用油,富含油酸、亚油酸、亚麻酸等不饱和脂肪酸,特别是α-亚麻酸,是人体必需的脂肪酸,在体内可代谢生成二十二碳六烯酸(DHA)和二十碳五烯酸(EPA),还具有降血脂、预防心脑血管等疾病的重要生理功能[3-6]。牡丹籽油除含有大量不饱和脂肪酸外,还含有β-谷甾醇和角鲨烯等活性成分[7],开发利用前景广阔。
目前,用于植物油提取的主要方法包括机械压榨法、超临界CO2萃取法、亚临界流体萃取法、超声波辅助提取法和有机溶剂浸提法等[8]。易军鹏等[9]、史国安等[10]对牡丹籽油的超临界CO2萃取工艺进行了优化,牡丹籽油得率分别为24.22%和28.86%。超临界CO2萃取法的提取效率高,且能有效保留活性成分,但生产成本较高。机械压榨法分为热榨法和冷榨法,热榨法至今仍普遍使用,尤其是民间作坊,提取率高,但高温导致生物活性物质大量损失,所得油脂基本属于低档食用油[11]。冷榨法是在低温下物理压榨制取油脂,营养成分保留较完整,但提取率相对较低。白章振等[12]分析了超临界CO2萃取法、冷榨法和有机溶剂浸提法提取的牡丹籽油,发现有机溶剂浸提法的出油率最高,可达28.61%,超临界CO2萃取法次之,冷榨法最低,为19.14%,表明提取方式对牡丹籽油的理化特性存在较大影响,但对脂肪酸组成及相对含量无显著影响。目前在工业生产中主要应用有机溶剂浸提法,但有机溶剂浸提法存在溶剂残留等问题;机械压榨法通过物理机械作用制油,操作简单、无溶剂污染,且制得的油品质好。本实验以‘凤丹’牡丹籽为试材,应用两种机械压榨法——瞬时压榨法和液压法提取牡丹籽油,与传统的有机溶剂浸提法进行比较,分析三种不同提取方式对牡丹籽油提取率及品质特性的影响;同时对牡丹籽油的抗氧化性进行研究,以期为牡丹籽油及其他功能油脂的深入开发和利用提供一定的参考。
1 材料与方法
1.1 材料与仪器
‘凤丹’牡丹籽,颗粒饱满均匀,水分含量4.10%
由河北保定太行山油用牡丹基地提供;中级初榨橄榄油 由北京市品利食品有限公司提供;双(三甲基硅烷基)三氟乙酰胺(BSTFA)-三甲基氯硅烷(TMCS)(体积比99∶1) 为色谱纯,上海阿拉丁生化科技股份有限公司;其他化学试剂 均为国产分析纯。
RE-2000A型旋转蒸发仪 上海亚荣生化仪器厂;UV-5500PC型紫外分光光度仪 上海元析仪器有限公司;DFT-100型药用粉碎机 温岭市林大机械有限公司;DSH-50A-1型水分测定仪 上海佑科仪器仪表有限公司;DD85G型瞬时压榨机 德国KOMET公司;QYZ-550型液压榨油机 泰安市良君益友机械有限公司;Allegin X-12R台式大容量冷冻离心机 杭州合众生物科技有限公司;7890A-5975C型气相-质谱联用仪(GC-MS) 郑州中谱仪器设备有限公司。
1.2 实验方法
1.2.1 牡丹籽油的提取
1.2.1.1 正己烷浸提法 参考刘建华等[13]的方法,取20 g牡丹籽于高速粉碎机中粉碎3 min,并置于80℃烘箱中干燥1 h。以正己烷为溶剂,将粉碎烘干后的牡丹籽置于索氏提取器中回流提取6 h,料液比为1∶18 g/mL,旋转蒸发回收溶剂得到牡丹籽油,计算出油率。
1.2.1.2 瞬时压榨法 参考陈玉宏等[11]的方法,安装瞬时压榨机加热套,设定温度为90℃,预热15 min后取下加热套并关闭加热开关,加入80℃烘干1 h的粉碎牡丹籽进行压榨,将压榨所得毛油经过滤离心,得到粗牡丹籽油,储存于4℃冰箱中待用,并计算出油率。
1.2.1.3 液压压榨法 参考郭刚军等[14]的方法,将牡丹籽粉碎,80℃下烘干1 h。将处理过的牡丹籽置于液压榨油机中压榨3 h,压榨温度为70℃,压力为50~60 MPa。收集牡丹籽油储存于4℃冰箱中待用,并计算出油率。
1.2.1.4 出油率与残油率计算 出油率和残油率的计算公式如下:

式中:m1为残留牡丹籽油质量(g);m2为试样质量(g)。

1.2.2 牡丹籽油理化特性检测 酸值测定参考GB 5009.229-2016《食品中酸价的测定》[15];过氧化值测定参考 GB 5009.227-2016《食品中过氧化值的测定》[16];碘值测定参考 GB/T 5532-2008《动植物油脂碘值的测定》[17];皂化值测定参考 GB/T 5534-2008《动植物油脂皂化值的测定》[18];水分及挥发物含量测定参考GB 5009.236-2016《动植物油脂水分及挥发物的测定》[19];透明度、气味、滋味测定参考 GB/T 5525-2008《植物油脂透明度、气味、滋味鉴定法》[20]。1.2.3 牡丹籽油脂肪酸含量检测 硅烷化:称取样品油脂0.2~0.3 g于50 mL离心管中,加入2 mol/L氢氧化钾-甲醇溶液6 mL混匀,室温下超声提取10 min,后于60℃烘箱中皂化1 h。取出漩涡混合2 min,冷却至室温。加入4 mL水和6 mL正己烷,漩涡混合提取5 min,4500 r/min离心10 min,转移上层有机相至玻璃试管中,加入1.5 g无水硫酸钠,静置至澄清透明。转移全部上清液于15 mL具塞玻璃离心管中,25℃下氮气吹干。加入200μL硅烷化试剂BSTFA-TMCS(体积比为99∶1),密封后于70℃烘箱中反应30 min,再加入1 mL正己烷溶解,用0.45μm微孔滤膜过滤,滤液作为待测溶液。
色谱条件:HP-5MS(30 m×0.25μm)毛细管柱;升温程序:柱子初始温度100℃,保持1 min;以5℃/min升至200℃,保持2 min;再以3℃/min升
式中:m1为牡丹籽油质量(g);m2为试样质量(g)。至280℃,保持3 min;载气为高纯氦;进样方式为分流进样,分流比1∶25;进样量为1μL。
质谱条件:电离方式为电子轰击离子源(EI源);电子能量70 eV;传输线温度280℃;离子源温度230℃;四极杆温度150℃;溶剂延迟2.6 min;全扫描模式(SCAN),扫描范围 50~1000 u;NIST 谱库[21-22]。
1.2.4 牡丹籽油抗氧化性检测
1.2.4.1 DPPH自由基清除能力 参考Larrauri等[23]和 Cheng 等[24]的方法加以改进。取一定体积牡丹籽油于10 mL离心管中,加乙酸乙酯至1 mL,加120μmol/L DPPH-乙酸乙酯溶液4 mL。混匀静置30 min后用乙酸乙酯做参照,在517 nm下测定其吸光度Ai,同时测定DPPH-乙酸乙酯溶液与1 mL乙酸乙酯混合液的吸光度A0以及一定牡丹籽油加乙酸乙酯至5 mL的混合液吸光度B。以橄榄油为对照,根据式(3)计算清除率(%):

式中:Ai为加牡丹籽油反应后DPPH溶液的吸光度;A0为不加牡丹籽油,只加DPPH溶液的吸光度;B为不加DPPH溶液时,牡丹籽油在517 nm波长下的吸光度。
1.2.4.2 羟基自由基 配制不同浓度的样品液,取一定体积梯度的牡丹籽油溶于1 mL无水乙醇中,混匀,充分溶解,10000 r/min离心10 min,取上清液100μL于10 mL试管中,加入5 mL无水乙醇,充分混匀,待测。
在10 mL试管中依次加入PBS缓冲液(pH=7.4)、邻菲罗啉乙醇溶液、去离子水、FeSO4溶液(0.75 mmol/L),加入双氧水(0.01%)和牡丹籽油样品液启动 Fenton反应。按表1顺序加入各溶液[25-27]。
反应体系置于37℃恒温水浴中,反应3 h,反应完全后立即取出并测定其在536 nm处的吸光度,以去离子水为参比。以橄榄油为对照,按式(4)计算羟基自由基的清除率:
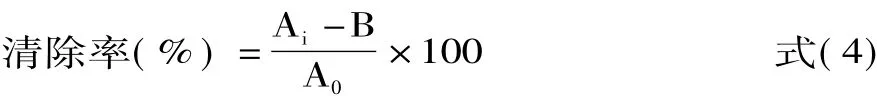
式中:Ai为牡丹籽油样品液的吸光度;A0为不含样品液和双氧水的吸光度;B为只含双氧水的吸光度。
1.2.4.3 牡丹籽油防晒性能检测 取牡丹籽油1 mL,加入10 mL环己烷,混匀。采用紫外分光光度计法,以环己烷为参比,测定样品在波长为200~800 nm处的吸光度,对照组为橄榄油[28-30]。
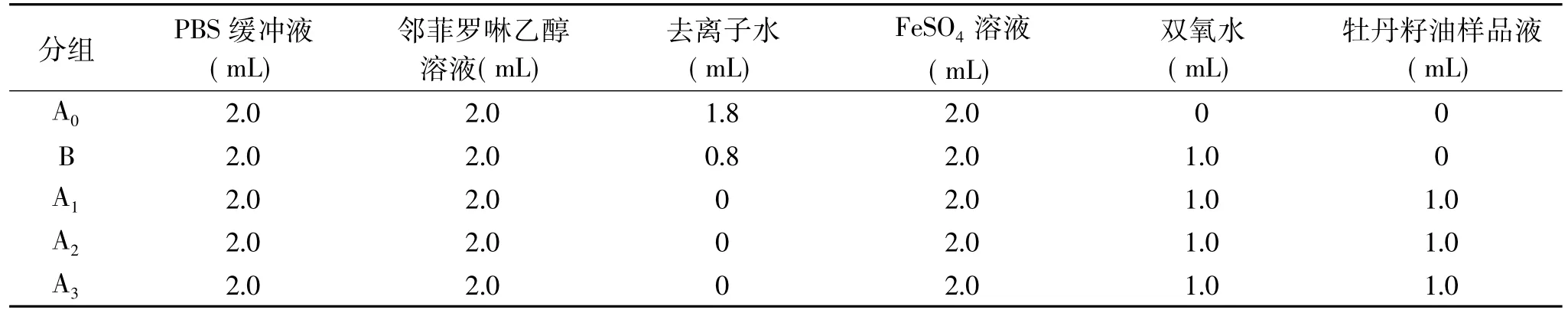
表1 加入溶液的种类和体积Table 1 Type and volume of the reagents added
1.3 数据分析
实验数据表示为Mean±SD,采用SPSS 17.0数据统计软件和Origin 8.6软件对实验数据进行数据处理和分析,并采用Duncan’s multiple rang test进行组间显著性分析。
2 结果与分析
2.1 不同方法提取牡丹籽油的出油率比较
正己烷浸提法、瞬时压榨法和液压法提取牡丹籽油的出油率分别为31.26% ±1.74%、14.27% ±0.72%和7.81% ±0.15%,如表2所示,与正己烷浸提法相比,液压法和瞬时压榨法的出油率均显著性低于浸提法,且液压法也显著低于瞬时压榨法(p<0.05)。液压法为目前生产中应用较为广泛的方法,本次结果表明该法出油率最低,主要是因为牡丹籽较为坚硬,装入物料袋后压榨接触面积较大,之后通过外加60 MPa压力不断榨取油脂,提取率为7.81%±0.15%,且物料的粉碎程度也可能影响出油率,需要后续进一步分析,实验结果表明该法的残油率约20%,显著高于瞬时压榨法和正己烷提取法,与出油率结果成反比。瞬时压榨法为本实验探索的新方法,是通过螺旋推动物料至固定位置,瞬时挤压将油脂分子从牡丹籽细胞中分离出来,残留率接近10%。这两种方法均为物理压榨,无法将油脂彻底提取出来。正己烷浸提法作为传统有机溶剂提取法,提取时间久,提取比较完全,其出油率可近似看作牡丹籽的含油量,文献报道该方法提取率在29%~34%之间,其差异主要与牡丹籽品种和含水量不同有关。

表2 不同提取方法对牡丹籽出油率的影响(%)Table 2 Effects of different methods on Paeonia suffruticosa seed oil extraction rate(%)
2.2 不同方法提取牡丹籽油理化特性比较
三种不同提取方法制取的牡丹籽油的主要理化特性指标如表3所示。
由表3可知,3种不同方法提取的牡丹籽油的理化特性略有不同。正己烷浸提法得到的牡丹籽油水分及挥发物含量最大,为8.43%,主要为正己烷残留;液压法提取的牡丹籽油水分及挥发性物质含量为6.61%,液压法为纯物理压榨,压榨过程全封闭,水分和油脂同时提取出来,因此水分及挥发性物质含量较高;瞬时压榨牡丹籽油由螺旋压榨所得,压榨温度为80℃,在提取过程中,水分及挥发性物质不断减少,仅0.05%。瞬时压榨法和液压法制得的牡丹籽油酸值均较小,符合食用植物油卫生标准(植物原油酸值<4.0 mgKOH/g),正己烷浸提法用时久,长时间暴露在空气中,活性成分易被破坏,酸败程度较高。三种提取方法所得牡丹籽油的过氧化值均符合标准,其中碘值无显著性差异,皂化值各组间差异显著,如表3所示。瞬时压榨法所得牡丹籽油略有混浊,是由于压榨过程中混入细微物料过滤不彻底造成。两种压榨牡丹籽油均具有牡丹籽油特有气味,而正己烷浸提法所得牡丹籽油香味较淡,可能是由于索氏提取过程中挥发性物质的损失所致。

表3 不同提取方法制取的牡丹籽油理化指标Table 3 Physical and chemical characteristics of Paeonia suffruticosa seed oil extracted by different extraction methods
2.3 不同方法提取牡丹籽油的成分分析

图1 瞬时压榨牡丹籽油成分硅烷总离子流图谱Fig.1 Total ion current chromatogram of fatty acids in Paeonia suffruticosa seed oil by instant press method
分别将3种牡丹籽油用气相色谱-质谱联用仪进行分析鉴定,得到其总离子流图谱,进一步利用NIST98标准谱库检索,并结合有关文献进行人工谱图解析,确定了3种牡丹籽油的主要成分组成,并采用峰面积归一化法计算得到各组分的相对含量。由表4可知,3种方法提取的牡丹籽油主要成分为脂肪酸、角鲨烯和β-谷甾醇,其中脂肪酸占70%以上。据GC-MS结果分析,3种牡丹籽油中脂肪酸以不饱和脂肪酸为主,其相对含量为72.30%~87.47%,其中瞬时压榨牡丹籽油亚麻酸含量最高,占总脂肪酸的30.98%,其次是液压牡丹籽油(23.22%),正己烷浸提牡丹籽油最低,仅15.98%;油酸和亚油酸含量则是正己烷浸提牡丹籽(43.04%,14.00%)>液压牡丹籽油(28.49%,15.62%)>瞬时压榨牡丹籽油(30.33%,8.21%)。正己烷浸提牡丹籽油所含β-谷甾醇远小于其他两种牡丹籽油,主要是因为索式提取时间长导致的β-谷甾醇损失。同时,3种方法对角鲨烯含量并无显著影响(p>0.05)。
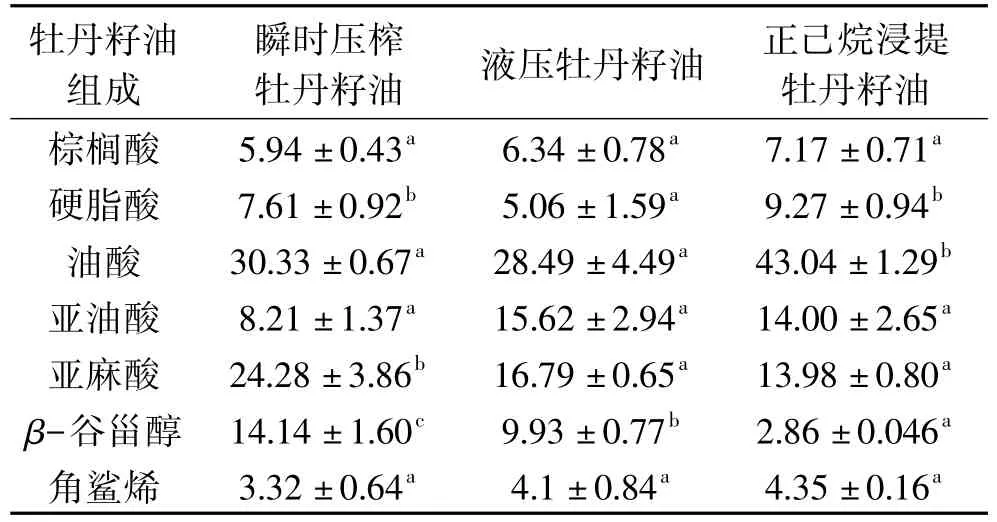
表4 不同提取方式制得牡丹籽油主要组成质量分数(%)Table 4 Composition quantity percentage of Paeonia suffruticosa seed oil extracted by different methods(%)
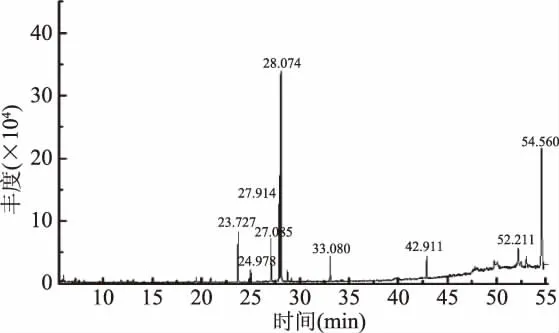
图2 液压牡丹籽油成分硅烷总离子流图谱Fig.2 Total ion current chromatogram of fatty acids in Paeonia suffruticosa seed oil by hydraulic press method
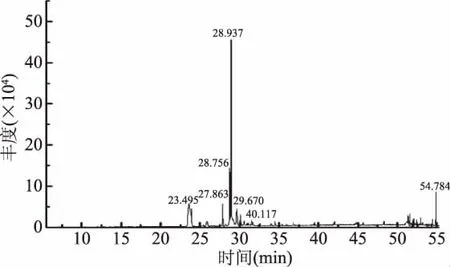
图3 正己烷浸提牡丹籽油成分硅烷总离子流图谱Fig.3 Total ion current chromatogram of fatty acids in Paeonia suffruticosa seed oil by n-hexane extraction method
2.4 不同方法提取牡丹籽油抗氧化性分析
2.4.1 DPPH自由基清除能力 不同提取方法制得的牡丹籽油对DPPH自由基的清除能力如图4所示,随着牡丹籽油体积浓度的升高,DPPH自由基清除能力也随之提高。当牡丹籽油体积浓度为40μL/mL时,三种牡丹籽油的清除率均达到最大值,其中瞬时压榨法与正己烷浸提法所得牡丹籽油的清除率高于对照组橄榄油,可达99%,而液压法低于对照组,且与其他两种方法有极显著性差异(p<0.01)。同时以图4中差异较大的12μL/mL和36μL/mL油脂用量进行差异显著性分析,结果表明在12μL/mL时正己烷浸提法与其他两种方法有极显著性差异((p<0.01);在36μL/mL时液压法与其他两种方法有极显著性差异(p<0.01)。
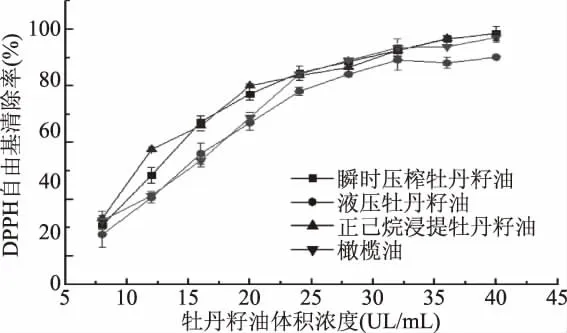
图4 牡丹籽油对DPPH自由基清除作用的体积浓度-效应关系Fig.4 Volume concentration effect relationship of DPPH free radical scavenging effect of Paeonia suffruticosa seed oil
2.4.2 羟基自由基清除能力 羟基自由基是多数氧自由基的母体,可衍生出多种自由基。氧自由基均具有较强的细胞毒性,可损伤细胞膜及细胞DNA[32]。羟基自由基清除率是反映油脂抗氧化作用的重要指标。不同牡丹籽油对羟基自由基的清除能力如图5所示,随着牡丹籽油体积浓度的增加,其对羟基自由基的清除能力逐渐提高,浸提牡丹籽油和液压牡丹籽油的清除率在2.4和3.0μL/mL时达到最大,分别为38.46%和36.82%,瞬时压榨油对羟基自由基最高清除率仅20.56%。在体积浓度达一定值后,清除率反而下降,是由于油脂浓度过大,反应体系不稳定,形成乳浊液所致。但与对照组橄榄油相比,在相同体积浓度下,如以1.0和2.4μL/mL两组为例,牡丹籽油的羟基自由基清除率显著高于橄榄油(p<0.01)。

图5 牡丹籽油对羟基自由基清除作用的体积浓度-效应关系Fig.5 Volume concentration effect relationship of Paeonia suffruticosa seed oil on hydroxyl radical scavenging effects
2.4.3 防晒性能分析 由图6可知,在200~270 nm的波长区间,三种牡丹籽油的吸光度基本一致,而从270~450 nm区间,液压牡丹籽油的吸光度明显高于其他两种牡丹籽油。UVB紫外线(275~320 nm)可透射到人体皮肤的表皮层,能促进人体矿物质代谢和维生素D的形成,但长期或过量照射会导致皮肤红斑、红肿脱皮等。UVA紫外线(320~400 nm)具有很强的穿透力,可直达皮肤真皮层,破坏弹性纤维和胶原蛋白纤维,造成皮肤黑化、皱化、老化等,甚至出现癌变[31]。由结果可知,液压牡丹籽油在270~450 nm 范围内吸光度值高于其他两种方法,表明了良好的防晒效果;在450 nm之后,液压牡丹籽油和正己烷浸提牡丹籽油的吸光度值略高于瞬时压榨牡丹籽油,综合防晒效果以液压法最佳。

图6 不同方法制得牡丹籽油防晒性能比较Fig.6 Comparison of sunscreen performance of Paeonia suffruticosa seed oil by different methods
3 结论
牡丹籽作为新型油料,在功能油脂方面具有较高的开发价值。采用瞬时压榨法、液压法和正己烷浸提法提取牡丹籽油,结果表明,正己烷浸提法(31.26%)可以获得较高的出油率,但瞬时压榨法(14.27%)和液压法(7.81%)更加绿色安全,无溶剂残留。在理化性质方面,瞬时压榨法和液压法所得牡丹籽油相差不大,正己烷浸提法因氧化而导致酸值过高,油脂品质较差。由于3种提取方法的原理不同,造成油脂主要成分的组成含量差异显著,瞬时压榨牡丹籽油和液压牡丹籽油亚麻酸和β-谷甾醇含量较高。在体外抗氧化方面,3种牡丹籽油对DPPH自由基的清除率相近,液压牡丹籽油较低;液压法和正己烷浸提所得牡丹籽油对羟基自由基的清除率表现出显著优势;液压牡丹籽油较其他两种牡丹籽油在防晒性能方面较好。通过上述指标的显著性分析以及综合不同方法的优缺点分析可知,瞬时压榨法和液压法作为冷榨法,可用于提取绿色高品质的牡丹籽油,在实际生产中可先采用瞬时压榨法或液压法进行高活性成分牡丹籽油的提取,其油饼可进一步利用正己烷浸提,以提高综合提取率,提高牡丹籽油的利用率。
