主动脉缩窄和主动脉弓离断术后婴儿短期随访发生左室流出道梗阻的影响因素分析
2019-01-25黄景思许伟滨孔娟娟孙善权
邹 鹏 李 虹 黄景思 许伟滨 饶 姣 刘 琴 孔娟娟 孙善权
主动脉缩窄(CoA)和主动脉弓离断(IAA)分别占先天性心脏病的5%~7%和1.5%,多在婴儿期甚至新生儿期出现急性心力衰竭和酸中毒,诊断明确后即须行手术治疗[1]。近年来,CoA和IAA的手术效果及术后生存率有了很大提高,据报道,部分CoA和IAA患儿在术后出现左室流出道梗阻(LVOTO)[2-4]。本研究回顾性纳入行手术治疗的CoA和IAA婴儿,分析术后短期随访中发生LVOTO的危险因素,并评价再次手术的效果。
1 方法
1.1 病例纳入标准 ①2012年3月28日至2017年12月15日在广东省妇幼保健院(我院)心脏中心年龄<6月、接受CoA或IAA外科治疗并存活的婴儿;②手术后随访时间≥12个月。
1.2 CoA、IAA的手术指征 CoA患儿诊断明确后,如出现心力衰竭、酸中毒等临床表现,即行手术治疗;IAA患儿诊断明确后,即行手术治疗。
1.3 CoA、IAA手术方式和随访 在全身麻醉体外循环下进行手术,CoA患儿根据具体情况进行扩大的端-端吻合术或降主动脉移植术;IAA患儿行IAA矫治术。出院后1、3、6和12个月各随访1次,之后每年随访1~2次。门诊随访,包括体格检查和超声心动图检查(采用美国PHILIPS公司的iE33超声心动图诊断仪)。随访中,如出现中、重度主动脉瓣狭窄(AS)达到LVOTO,并出现左室心肌肥厚,二期进行主动脉瓣成形术和/或主动脉瓣下隔膜(SubAM)切除术。本文病例随访至2018年12月15日。
1.4 LVOTO诊断标准及主动脉瓣环(AV)-Z值的评估 AS的诊断根据美国心脏病协会2014年关于瓣膜性心脏病的指南[5],轻度AS:主动脉瓣最大血流速度(AV-Vmax):2.0~2.9 m·s-1,平均跨瓣压差(PG)<20 mmHg;中度AS:AV-Vmax:~3.9 m·s-1,PG ~39 mmHg;重度AS:AV-Vmax ~4.9 m·s-1,PG ~59 mmHg;极重度AS:AV-Vmax >5.0 m·s-1,PG>60 mmHg[4]。
AV-Z值的评估采用Petterson等[6]的方法,根据患儿的体表面积对AV内径进行标准化的评估。
1.5 资料截取 单人提取如下数据:①患儿年龄、性别等;②术前的超声心动图和心脏CT报告,包括CoA和IAA分型、AV-Z值、是否伴有室间隔缺损等;③手术年龄、手术方式;④随访中的超声心动图检查,AV-Vmax,2.0~3.0 m·s-1为AS,>3.0 m·s-1为LVOTO。
1.6 统计学方法 采用SPSS 20.0软件包进行统计学分析。计量资料以均数±标准差表示,计数资料以百分数表示。计量资料的比较行独立样本的t检验,双侧检验P<0.05为差异有统计学意义。Logistic回归分析CoA和IAA患儿术后出现LVOTO的危险因素,AS患儿中未发生LVOTO的发生率采用Kaplan-Meier曲线描述。
2 结果
2.1 一般情况 符合本文纳入标准的118例患儿进入本文分析,男75例,手术年龄的中位数为19(4~150)d,在新生儿期接受手术的患儿有75例(63.6%),术前平均体重(3.3±0.8)kg,术前平均AV-Z值-0.5±1.2。
CoA 95例,其中73例合并室间隔缺损(VSD),手术方式为扩大的端-端吻合术93例、降主动脉移植术2例。IAA 23例,A型15例,B型6例,C型1例,其他类型1例,手术方式均为IAA矫治术。
二叶式主动脉瓣(BAV)23例(19.4%),术前平均AV-Z值-1.19±1.24;三叶式主动脉瓣(TAV)95例,术前平均AV-Z值-0.41±1.19,差异有统计学意义(t=-2.773,P=0.006)。
2.2 随访中LVOTO的发生情况 118例CoA和IAA患儿中位随访时间18(12~81)个月。18例(15.3%)在主动脉弓术后出现AS(AV-Vmax>2.0 m·s-1),术前的平均AV-Vmax(1.2±0.5)m·s-1,再次手术前或最后一次随访时,平均AV-Vmax(3.1±0.9)m·s-1。
18例AS患儿的术前AV-Z值为-0.98±1.38,100例未出现AS患儿的术前AV-Z值为-0.44±1.18,差异无统计学意义(t=-1.723,P=0.088)。①在随访中,10例轻度AS进展为LVOTO(临床资料见表1),再次手术前或最后一次随访时,平均AV-Vmax:(3.7±0.6) m·s-1。②至随访终点,在10例LVOTO患儿,中度AS 8例,重度AS 2例。随着术后随访时间的延长,AS的程度呈进展性变化。③10例LVOTO患儿中,术前AV-Z值:-0.58±1.17,与108例非LVOTO患儿的术前AV-Z值(-0.53±1.23)比较,差异无统计学意义(t=-0.135,P=0.893)。其中,TAV患儿有5例,BAV有5例。至再次手术前或最后一次随访时,TAV和BAV两组患儿的AV-Z值分别为:1.02±1.53和1.25±1.10,差异无统计学意义(t=0.412,P=0.788)。
5例TAV患儿中,LVOTO狭窄的部位3例为主动脉瓣下,2例为主动脉瓣及瓣下(表1中例1和2);在5例BAV患儿中,LVOTO狭窄的部位3例为主动脉瓣,2例为主动脉瓣及瓣下。7例主动脉瓣下LVOTO的患儿的诊断时间为(22.2±14.4)个月,均为隔膜型的主动脉瓣下狭窄,其隔膜是在主动脉弓术后出现,再次手术前或末次随访AV-Z为-4.35±0.99。有6例行SubAM切除术,再次手术后的中位随访时间为8(2~36)个月。表1中例1、2分别在随访24个月和36个月后,AV-Vmax均达到2.9m·s-1;余4例患儿随访2~8个月,AV-Vmax均<2.0m·s-1。单纯主动脉瓣狭窄的LVOTO患儿的诊断时间是(24.0±14.7)个月,均为BAV,且是中度的AS,仍在随访并等待手术。
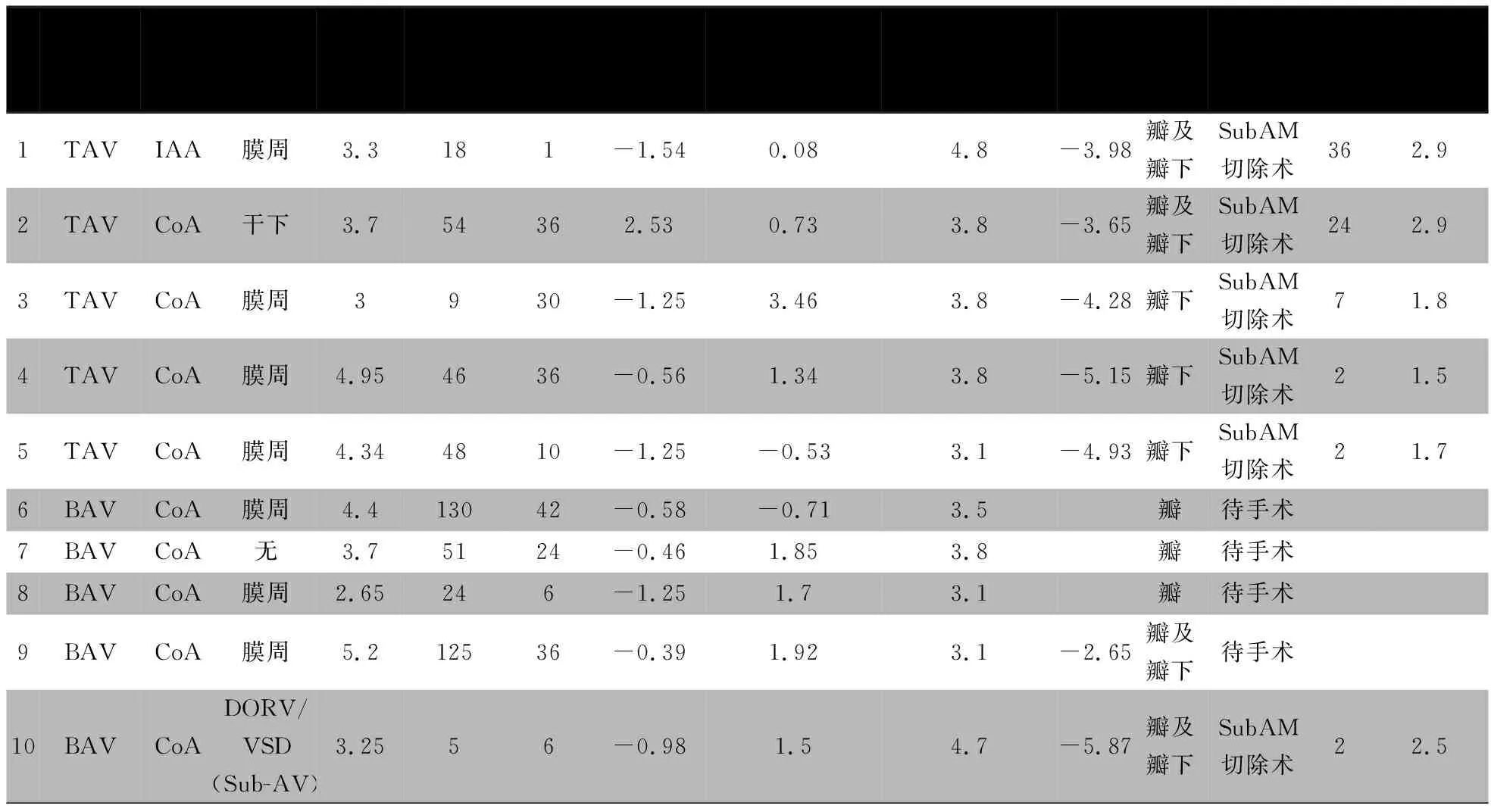
表1 10例在主动脉弓术后由轻度AS进展为LVOTO的临床资料
注 CoA:主动脉缩窄 IAA:主动脉弓中断 VSD:室间隔缺损 BAV :二叶式主动脉瓣,TAV:三叶式主动脉瓣 LVOTO:左室流出道梗阻;DORV/VSD(Sub-AV):右室双出口/室间隔缺损(主动脉瓣下)
2.3 CoA和IAA患儿术后出现LVOTO的危险因素分析 以患儿的年龄、性别、手术时体重、是否伴有VSD,AV-Z值、BAV和主动脉弓病变的类型(CoA或IAA)为自变量,行多因素Logistic回归分析,表2显示,BAV(OR=8.994)是CoA和IAA患儿在手术后出现LVOTO的危险因素。

表2 CoA和IAA患儿主动脉弓手术后出现LVOTO危险因素的Logistic回归分析
2.3 SubAM的情况 有15例婴儿(12.7%)在主动脉弓手术后检出SubAM,14例合并VSD。超声心动图检出SubAM的时间中位数18(1.5~36)个月,11例SubAM患儿出现AS,其中有7例进展为LVOTO,6例行SubAM切除术,另1例随访观察中。
3 讨论
对于CoA和IAA的小婴儿术后发生LVOTO的预测,一些研究主要关注AV内径的大小及其Z值和左室流出道的截面积等指标[7-10]。Junya等[4]的研究表明,较小的AV-Z值(<-3.0)是CoA和IAA的患儿发现LVOTO的危险因素之一,行Ross或者Konno手术等相关治疗可以解决较小的AV问题。本研究患儿术前平均AV-Z值-0.5±1.2,Logistic回归分析显示其不是术后发生LVOTO的危险因素。
本研究中,BAV占研究患儿的19.4%,且是术后出现LVOTO的危险因素。 文献报道,相比正常的人群,BAV在CoA和IAA的患者中更为常见,是一种瓣膜相关的伴发畸形,发生率20%~85%[11-13]。多项研究对CoA或IAA患儿手术后随访至成年,有33%~51%的病例需要行主动脉瓣的外科治疗[12,14,15]。本研究患儿中,有5例BAV患儿出现LVOTO。尽管BAV患儿的术前AV-Z值较TAV患儿小,但是在LVOTO的患儿中,BAV所引起AS的主要原因是瓣膜开放受限所导致的瓣口截面积变小。其中有2例合并SubAM而行隔膜切除术,另有3例单纯的BAV引起的LVOTO患儿,仍需随访观察。
发生LVOTO的另一部位是在主动脉瓣下。在
本研究中,有15例患儿在术后1.5~30个月出现SubAM。在10例LVOTO患儿中,有7例是因出现SubAM,造成主动脉瓣下的梗阻(AV-Z值-4.35±0.99)。SubAM限制了主动脉瓣的活动,导致了明显的AS。当前的一些研究认为,SubAM是因圆锥间隔的向后移位,某些机制刺激纤维组织的增生而导致的。由于SubAM的存在,使得局部的射流会引起主动脉瓣的纤维化,同时,SubAM可能会逐渐累积主动脉瓣和二尖瓣,因此,具有进展性的特点[4,16,17]。
有6例患儿因SubAM造成中或重度的AS,行SubAM切除术,这是对于LVOTO患儿主要的再次手术方式,有2例患儿在再次手术后24月至36月,仍达到轻度的AS,间接提示SubAM对主动脉瓣的功能造成影响。对于再次手术的患儿,仍需进行长期的随访。
本研究的局限性:①单中心、样本量较小的的短期随访研究;②关于BAV患儿的再次手术的时机及术后中远期的随访经验,也有待在今后实践中进一步积累。
