西红花HPLC 指纹图谱建立及成分分析
2019-01-25邢越阳司睿蓉吴佩颖
邢越阳, 高 崎, 张 雪, 司睿蓉, 吴佩颖,∗
(1. 上海中医药大学, 上海201203; 2. 上海上药杏灵科技药业股份有限公司, 上海201203; 3. 上海市药材有限公司, 上海200002)
西红花为鸢尾科植物番红花Crocus sativus L.的干燥柱头, 有活血化瘀、 凉血解毒、 解郁安神之功效, 《本草纲目》[1]对其功效表述为“心忧郁积,气闷不散, 活血。 久服令人心喜。 又治惊悸”, 西红花苷是西红花主要活性成分, 在抗肿瘤、 治疗心脑血管疾病和中枢神经系统疾病方面有一定疗效。现代药理研究表明, 西红花具有降血脂、 调节胆固醇[2-4]、 抗炎[5-6]、 抗氧化[7-8]、 改善记忆[9-10]、 抗肿瘤[11]等作用。
西红花在食品、 医药、 美容等领域有重大应用价值, 但其需求量巨大, 无法完全满足市场需求。目前, 2015 版《中国药典》 仅规定西红花苷-I 和西红花苷-II 总含有量不低于10.0%, 但中药成分复杂, 单靠1、 2 种成分含有量来评价其质量并不全面。 曾水云等[12]通过建立HPLC 指纹图谱对不同产地西红花进行比较, 共标定12 个共有峰, 通过分析各峰面积相对比值的差异来区别其来源; 本实验采用该方法, 以期对该药材进行更全面的质量评价。
1 仪器与试药
1.1 仪器 Waters Acquity ARC UHPLC 高效液相色谱仪、 Waters ACQUITY UPLCTMI-CLASS 超高效液相色谱仪、 Waters XevoG2-XS Q-TOF·ESI 液质联用仪(美国沃特世公司); KQ5200DE 型数控超声波清洗器 (昆山市超声仪器有限公司);Sartorius Quintx65-1CN 分析天平[十万分之一, 赛多利斯科学仪器(北京) 有限公司]。
1.2 试药 甲酸(分析纯, 批号20141223, 上海豪申化学试剂有限公司); 甲醇(色谱纯, 批号175159, 德国Merck 公司); 乙腈(色谱纯, 批号175157, 德国Merck 公司); 水为纯净水(杭州娃哈哈集团有限公司, 批号201801053210BL06683)。西 红 花 苷-Ⅰ ( 批 号 111588-201303, 含 有 量92.6%)、 西红花苷-Ⅱ(批号111589-201304, 含有量92.4%) 对照品购自中国食品药品检定研究院。
建立对照指纹图谱所需西红花由上海市药材有限公司西红花事业部提供; 市售样品经网络购物平台按销量排序, 选购排名前二十者, 经上海市药材有限公司裴卫忠药师鉴定为正品。 具体见表1。
2 方法与结果
2.1 分析条件
2.1.1 色谱条件 Agilent Poroshell 120 EC-C18色谱柱 (4.6 mm × 100 mm, 2.7 μm); 流 动 相[0.2%乙酸-乙腈(87 ∶13) ] (A) -甲醇(B),梯度洗脱 (0 ~12 min, 0 ~35% B; 12 ~18 min,35% ~50% B; 18 ~26 min, 50% ~100% B; 26 ~28 min, 100%B); 体积流量1.0 mL/min; 检测波长254 nm; 柱温35 ℃; 进样量10 μL。
UPLC 液相方法同上, 洗脱梯度调整为0 ~30 min, 0~35%B; 30~45 min, 35% ~50%B; 45 ~65 min, 50% ~100%B; 65~70 min, 100%B, 进样量2 μL。
2.1.2 质谱条件 电喷雾离子源(ESI); 正离子检测模式; 毛细管电压3.0 kV; 锥孔电压30 V;离子源温度120 ℃; 去溶剂化温度500 ℃; 去溶剂化气体积流量800 L/h; 锥孔气体积流量50 L/h;碰撞气氩气; 低碰撞能量通道5 eV; 高碰撞能量通道20 eV。
2.2 供试品溶液制备 精密称取药材粉末50.0 mg, 置棕色样品瓶中, 精密加入50.0 mL 稀乙醇, 称定质量, 冰水浴超声(200 W、 40 kHz)30 min, 取出, 放置室温, 溶剂补足减失的质量,摇匀, 过0.22 μm 微孔滤膜, 即得。
2.3 方法学考察
2.3.1 重复性试验 称取同一药材粉末5 份, 按“2.2” 项下方法制备供试品溶液, 在“2.1.1” 项色谱条件下进样, 测得各共有峰相对峰面积RSD均小于2.87%, 表明该方法重复性良好。
2.3.2 精密度试验 取药材粉末, 按“2.2” 项下方法制备供试品溶液, 在“2.1.1” 项色谱条件下连续进样5 次, 测得各共有峰相对峰面积RSD均小于2.72%, 表明仪器精密度良好。
2.3.3 稳定性试验 取药材粉末, 按“2.2” 项下方法制备供试品溶液, 在“2.1.1” 项色谱条件下于0、 2、 4、 8、 12 h 进样, 测得各共有峰相对峰面积和相对保留时间RSD 均小于2.85%, 表明溶液在12 h 内稳定性良好。
2.4 HPLC 指纹图谱建立 取“1.2” 项下10 批样品, 按“2.2” 项下方法制备供试品溶液, 在“2.1.1” 项色谱条件下进样, 色谱图见图1。 采用中药色谱指纹图谱相似度评价软件2012.130723 版进行分析, 在生成对照状态下通过多点校正, 时间窗0.1 min, 平均数模式, 全谱峰匹配, 生成对照图谱。 西红花苷-I 作为西红花中主要成分, 易于得到对照品, 含有量较高, 在指纹图谱中的分离度良好, 因此选择其作为参比峰, 共标定20 个共有峰,计算10 批药材共有峰与参比峰的相对保留时间和相对峰面积, 结果见表2~3。
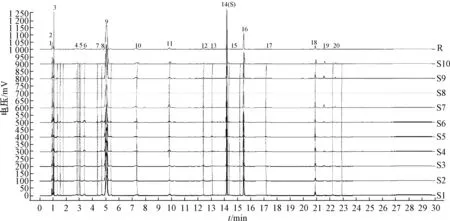
图1 10 批样品HPLC 指纹图谱Fig.1 HPLC fingerprints of ten batches of samples

表2 10 批样品共有峰相对保留时间Tab.2 Relative retention time of common peaks of ten batches of samples

表3 10 批样品共有峰相对峰面积Tab.3 Relative peak areas of common peaks of ten batches of samples
2.5 相似度评价 20 种药材按“2.2” 项下方法制备供试品溶液, 在“2.1.1” 项色谱条件下进样, 将结果与对照指纹图谱比对, 采用中药色谱指纹图谱相似度评价系统2012.130723 版系统评价软件计算相似度。结果, S1 ~S10 的相似度分别为0.997、 0.998、 0.998、 0.999、 0.996、 0.956、0.995、 0.999、 0.990、 0.988, A~T 的相似度分别 为 0.998、 0.998、 0.993、 0.996、 0.996、0.999、 0.998、 0.996、 0.998、 0.998、 0.995、0.997、 0.999、 0.995、 0.998、 0.995、 0.993、0.999、 0.996、 0.995, 均在0.9 以上, 表明药材中各成分整体比例相近, 相似度较高, 差异较小。
2.6 成分标定 在“2.1” 项条件下进样, 得色谱图和正、 负离子模式下的总离子流图, 分别记录各色谱峰在HPLC、 UPLC 条件下的出峰时间, 以及以峰14 为参照的相对保留时间。结果见表4、图2~3。
2.7 质谱分析 根据正离子模式下各色谱峰的母离子及二级碎片信息, 通过与对照品比对指认了HPLC 指纹图谱中的10 个主要色谱峰。
西红花苷是一类由西红花酸与不同数量葡萄糖形成的酯类化合物, 而糖苷键不稳定, 易发生断裂。 通 过 总 结 分 析 Carmona[13]、 Verma[14]、Lech[15]等对西红花的研究, 发现在质谱信号中常会出现西红花酸与Na+或H+结合的分子离子峰m/z351.2 或329.2, 或不同数量葡萄糖基团与西红花酸结合的质谱碎片, 如m/z 513.2 为与单糖结合的分子离子峰、 m/z 675.2 为与双糖结合的分子离子峰等, 由此推断峰2~10 为西红花苷类成分, 其中峰19、 20 在330 nm 波长处有较强吸收, 推测其可能为质谱图顺式结构。

表4 色谱峰相对保留时间Tab.4 Relative retention time of chromatographic peaks
峰14、 19 质谱图见图4 ~5, 其准分子离子峰m/z 999.36, 为西红花酸结合4 分子葡萄糖的西红花苷类成分, 峰14 正离子模式下碎片离子峰m/z有511.180 8 [M +2Na]2+, 675.264 0 [M-Gnt +Na]+, 837.315 7 [M-Glc +Na]+, 329.174 9 [M-2∗Gnt +H]+, 351.158 2 [M-2 ∗Gnt +Na]+,347.094 8 [Gnt+Na]+, 311.164 0 [M-2∗Gnt+HH2O]+; 峰19 在正离子模式下碎片离子峰m/z 与其类似, 两者质谱裂解规律也大致相同。 结合碎片离子峰, 推断峰14 为西红花苷-I (C44H64O24), 根据对照品证实西红花苷-I; 峰19 的保留时间较峰14 晚, 同时在330 nm 波长处有较强吸收, 根据文献推断为西红花苷-I 的顺式结构cis-4-GG。

图2 样品UPLC-UV 色谱图Fig.2 UPLC-UV chromatogram of samples

图3 样品总离子流色谱图Fig.3 Total ion current chromatograms of samples
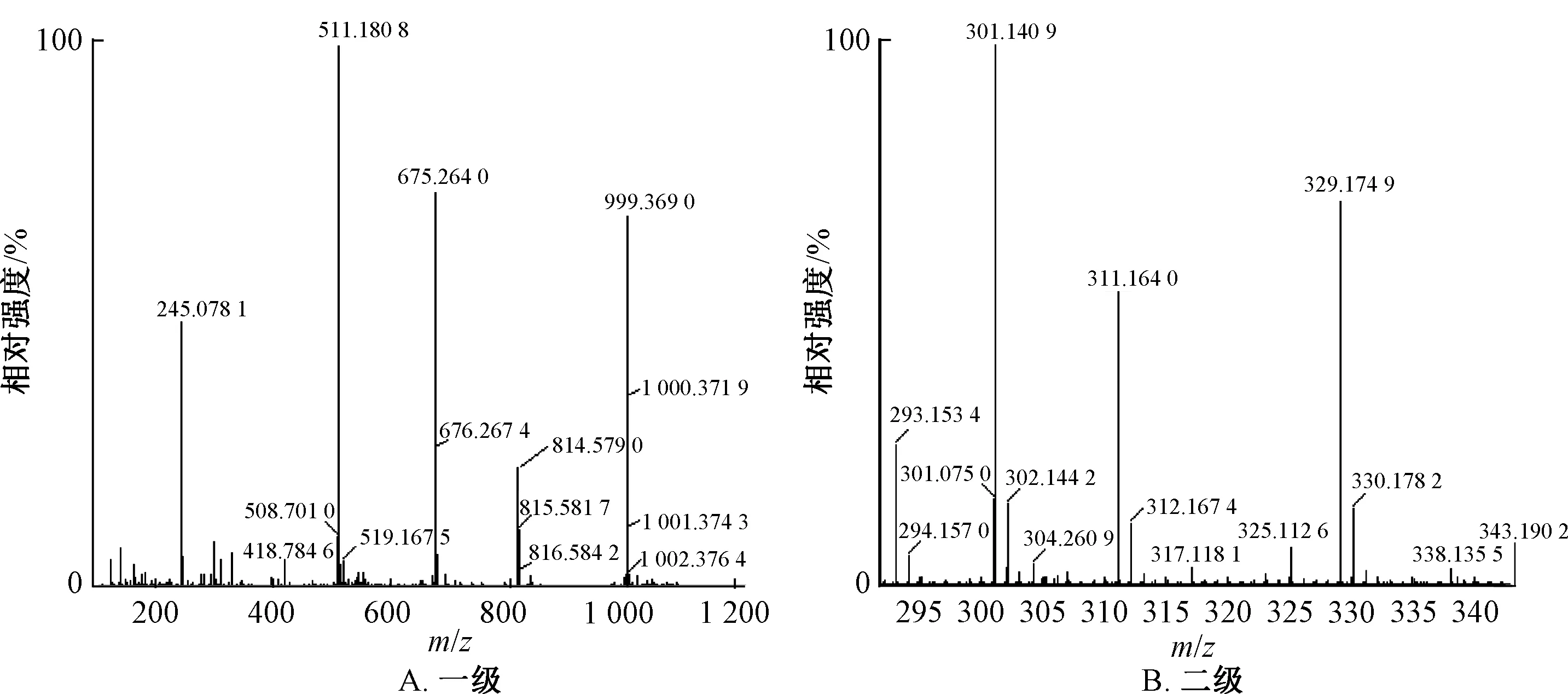
图4 峰14 化合物质谱图Fig.4 Mass spectra of peak 14 compounds

图5 峰19 化合物质谱图Fig.5 Mass spectra of peak 19 compounds
图5 表明, 该化合物在254 nm 波长处有较强吸收, 结合其保留时间及文献推断为西红花苦苷(C16H26O7), m/z 353.156 8 [M+Na]+是其母离子与一分子Na+结合的分子离子峰, 质谱碎片m/z 151.110 4 推断为母离子脱掉葡萄糖基团的分子离子峰。 西红花苷类成分裂解规律大致相同, 西红花酸结合不同数目糖基团所形成苷类成分的准分子离子峰及碎片离子峰信息见表5。

表5 各成分LC-MS 分析Tab.5 LC-MS analysis of various constituents
3 讨论
本实验建立了稳定、 可靠、 重复性好的西红花HPLC 指纹图谱, 选取指标性成分作为特征峰, 并通过计算其与参比峰之间的比例关系为药材质量控制提供依据, 比以某一种或几种成分含有量作为鉴别标准全面得多。
指纹图谱共有模式为根据不同检测目的, 通过软件拟合不同批次样品得到的对照图谱。 本实验收集了不同年份和产地的西红花, 用所建立的对照指纹图谱进行质量检测, 适用于大部分样品, 还可根据不同检测目的生成特定年份或产地的指纹图谱。
应用LC-MS 法对西红花中特征性成分的离子碎片信息进行采集分析, 结合文献及数据分析, 指认了其指纹图谱中10 种成分。 西红花中主要成分的对照品较难获得, 通过质谱技术所得化合物的碎片离子峰推测共有峰成分, 明确各成分比例关系,比仅标定若干共有峰的指纹图谱更能全面评价药材质量。 本实验指认的10 种成分中西红花苷-I 和西红花苷-II 区分了其顺式及反式结构, 目前对西红花苷的药理研究主要集中在其反式结构上[16-18],而一般认为化合物反式结构的活性较顺式结构强,因此可通过比较不同西红花中顺、 反式西红花苷-I和西红花苷-II 的含有量加以区别。 同时, 2 种成分也是栀子主要化合物, 部分西红花掺伪就是添加两者所致, 而应用指纹图谱对西红花进行质量评价时, 可通过分析不同成分间的比例关系来发现这种行为。
对成分的简单指认并不是指纹图谱建立的最终目的, 仍需进行相关药理实验, 明确具体药效成分, 在化学成分与药理活性之间建立更明确的关系, 通过指纹图谱直观了解某种药物的品质。
