基于UPLC-Q-Extractive Orbitrap MS鉴定姜黄提取物在大鼠体内的代谢产物
2022-03-16刘美娟王宏进殷光玲张旭光孙立新
王 媛,刘美娟,王宏进,殷光玲,李 妍,张旭光,孙立新
(1.沈阳药科大学,辽宁 本溪 110016;2.汤臣倍健股份有限公司,广东 广州 300146)
姜黄提取物主要包括姜黄素(CUR)、去甲氧基姜黄素(DMC)、双去甲氧基姜黄素(BDMC)等姜黄素类化合物[1],具有降脂、抗炎、抗氧化、抗肿瘤、抗阿尔茨海默病、抗病毒等多种药理活性[2]。有研究表明,姜黄素氢化代谢物四氢姜黄素表现出多种优于姜黄素的生物活性[3],二氢姜黄素可抑制细胞凋亡[4]、对油酸诱导的HepG2细胞的脂堆积、氧化应激损伤、胰岛素抵抗具有一定的预防作用[5]。筛选出活性、稳定性、生物利用度高于CUR、DMC、BDMC的代谢产物,在一定程度上能够解决CUR、DMC、BDMC稳定性差、生物利用度低的问题。
目前,与CUR相关的代谢产物研究较多[6-9],而DMC和BDMC的研究较少,且仅报道了其在大鼠粪便、尿液中的一相代谢物[10-11]及其纳米制剂[8]在大鼠粪便、尿液、血浆中的二相代谢物。对于姜黄提取物,仅报道了3种姜黄素类化合物在大鼠粪便、尿液中的一相代谢物[11]和人血浆[12]中的代谢产物,且分离出的代谢物较少[10-11]、质谱数据不完善[12]。因此,本研究拟采用超高效液相色谱-四极杆-静电场轨道阱高分辨质谱(UPLC-Q-Extrative Orbitrap MS)技术鉴定姜黄提取物中3种姜黄素类化合物的代谢产物,以期对姜黄素类化合物的代谢产物进行补充,为后期筛选活性代谢物研究提供理论依据。
1 实验部分
1.1 主要仪器与装置
Vanquish Flex超高效液相色谱仪、Q-ExactiveTM四极杆-静电场轨道阱高分辨质谱仪:美国Thermo公司产品,配有电喷雾离子源(HESI)、TraceFinder 4.1工作站及TraceFinder 4.1 General Quan数据处理系统;CPA225D型电子分析天平(1/10万):德国赛多利斯科学仪器有限公司产品;TGL-16型高速冷冻离心机:湖南湘仪实验室仪器开发有限公司产品。
1.2 主要材料与试剂
姜黄素对照品(纯度≥98%):中国药品生物制品检定所产品;去甲氧基姜黄素、双去甲氧基姜黄素、二氢姜黄素、四氢姜黄素、六氢姜黄素、八氢姜黄素对照品(纯度≥98%):上海源叶生物有限公司产品;姜黄素-β-O-葡萄糖醛酸钠、姜黄素硫酸四叔丁基铵对照品(纯度≥98%):多伦多研究化学公司产品;甲醇、甲酸、乙腈(色谱纯):美国Sigma公司产品;纯净水:杭州娃哈哈集团有限公司产品。
姜黄提取物:汤臣倍健股份有限公司产品,主要由姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素3种化学成分组成,经工作曲线法测定,其含量分别为192.5±1.6、44.99±0.56、44.29±0.7 mg/g(平均值±标准差,n=3)。
1.3 实验动物
SPF级SD(Sprague-Dawley)大鼠(雄性,体质量220~250 g,动物生产合格证号:SCXK(辽) 2020-0001):由沈阳药科大学动物实验中心提供。
1.4 实验方法
1.4.1对照品溶液的制备 取适量的姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素、二氢姜黄素、四氢姜黄素、六氢姜黄素、八氢姜黄素、姜黄素-β-O-葡萄糖醛酸钠、姜黄素硫酸四丁基铵对照品,分别置于10 mL棕色容量瓶中,除姜黄素-β-O-葡萄糖醛酸钠对照品用20%甲醇-水溶液溶解外,其他对照品均用甲醇溶解并稀释至刻度,摇匀,制成浓度分别为87.0、72.0、102.0、61.0、80.0、109.0、99.0、89.0、107.0 mg/L对照品储备液,于4 ℃储存,待用。
混合对照品溶液的制备:精密量取各0.2 mL姜黄素、双去甲氧基姜黄素、六氢姜黄素、八氢姜黄素、姜黄素-β-O-葡萄糖醛酸钠、姜黄素硫酸四丁基铵对照品储备液,各0.3 mL去甲氧基姜黄素、四氢姜黄素,0.4 mL二氢姜黄素,置于100 mL棕色量瓶中,用甲醇稀释至刻度,摇匀,制成浓度分别为0.174、0.204、0.218、0.198、0.178、0.214、0.216、0.240、0.244 mg/L混合对照品溶液,于4 ℃储存,待用。
1.4.2灌胃溶液的制备 精密称取适量的姜黄提取物,用0.5%羧甲基纤维素钠溶液(取约0.5 g羧甲基纤维素钠,加入100 mL纯净水中,80 ℃加热使其溶解,制成质量分数约为0.5%羧甲基纤维素钠溶液)混悬,配制成约142 g/L混悬液。
1.4.3动物分组和给药 取18只健康雄性SD大鼠,随机分成6组(n=3),依次编号为K1、K2、K3、Y1、Y2、Y3。K1、K2、K3组分别用于收集空白粪便和尿液、空白血浆、空白胆汁;Y1、Y2、Y3组分别用于收集给药粪便和尿液、给药血浆、给药胆汁。
实验前所有动物于SPF级动物房中适应性饲养7天,给药前禁食12 h,可自由饮水。禁食12 h后,Y1、Y2、Y3组大鼠灌胃给予姜黄提取物-0.5%羧甲基纤维素钠溶液,给药剂量1 703 mg/kg(姜黄素327.8 mg/kg、去甲氧基姜黄素76.6 mg/kg、双去甲氧基姜黄素75.4 mg/kg)。K1、K2、K3组大鼠灌胃给予等体积0.5%羧甲基纤维素钠溶液。
1.4.4生物样品采集 将K1和Y1组大鼠置于代谢笼中,分别收集0~12 h时空白粪便和尿液、给药粪便和尿液,并将收集的粪便样品置于室温下避光风干,所有样品于-20 ℃储存,待用。
K2和Y2组大鼠分别于灌胃后0.25、1、2、3、4、6、8、12、24 h时从眼眶后静脉丛取0.5 mL血,置于经肝素钠处理的EP管中,以3 000 r/min离心10 min,取上清液,得到空白血浆和给药血浆样品,于-20 ℃储存,待用。
K3和Y3组大鼠经麻醉后做胆汁插管手术,分别收集0~12 h时空白胆汁和给药胆汁样品,于-20 ℃储存,待用。
1.4.5样品处理 血浆样品:避光操作。分别取100 μL 9个不同时间点的血浆样品,置于同一棕色EP管中,加入3 mL甲醇,涡旋2 min,4 ℃下以12 000 r/min离心10 min,上清液转移至另一棕色EP管中,室温下氮气吹干;残渣用200 μL 75%甲醇复溶,4 ℃下以12 000 r/min离心10 min,离心2次,取上清液,备用。
粪便样品:避光操作。将风干后的粪便置于研钵中研碎,混合均匀。取约1 g混合均匀的粪便样品,置于25 mL烧杯中,加入5 mL甲醇,超声提取30 min,4 ℃下以12 000 r/min离心10 min,取上清液,室温下氮气吹干;残渣用2 mL甲醇复溶,4 ℃下以12 000 r/min离心10 min,离心2次,取上清液,备用。
尿液、胆汁样品:避光操作。精密量取各1 mL尿液、胆汁样品,分别置于25 mL烧杯中,加入5 mL甲醇,超声提取30 min,4 ℃下以12 000 r/min离心10 min,取上清液,室温下氮气吹干;尿液残渣用200 μL甲醇复溶,胆汁残渣用2 mL甲醇复溶,4 ℃下以12 000 r/min离心10 min, 离心2次,取上清液,备用。
1.5 实验条件
1.5.1色谱条件 色谱柱:Acquity UPLC®BEH C18柱(2.1 mm×100 mm×1.7 μm);流动相:A相为0.1%甲酸水溶液,B相为乙腈;梯度洗脱程序:0~6 min(10%~30%B),6~14 min(30%~65%B),14~17 min(65%~95%B),17~20 min(95%B),20~20.1 min(95%~10%B),20.1~23.1 min(10%B);流速0.2 mL/min;柱温35 ℃;进样量2 μL。
1.5.2质谱条件 电喷雾离子源(HESI源),负离子模式检测,鞘气流速9 L/min,辅助气流速3 L/min,喷雾电压3.8 kV,毛细管温度320 ℃,辅助气温度310 ℃。采用自动触发二级(Full scan-ddMS2(TopN))数据采集模式;一级质谱质量扫描范围m/z150.0~2 000.0,分辨率70 000;二级质谱质量扫描范围m/z50~1 500,分辨率17 500;碰撞气为高纯氮气;碰撞能20、30、40 eV;Top(N):10,自动选择质谱产生的前10个最强离子峰作为二级质谱的母离子进行碎裂。
2 结果与讨论
2.1 对照品质谱裂解行为
在负离子模式下,对照品CUR、DMC、BDMC、二氢姜黄素、四氢姜黄素、六氢姜黄素、八氢姜黄素、姜黄素-β-O-葡萄糖醛酸钠、姜黄素硫酸四叔丁基铵的色谱保留时间及准分子离子峰[M-H]-分别为13.68、13.43、12.95、13.42、13.17、9.59、8.95、10.38、11.19 min和m/z367.116 5、337.104 9、307.097 4、369.130 5、371.147 6、373.166 4、375.178 2、565.132 8、447.073 5。同时发现对照品二氢姜黄素与四氢姜黄素分别在10.65、10.84 min处有1个色谱峰,其各自的质谱数据(一级及二级质谱碎片)分别与二氢姜黄素、四氢姜黄素的质谱数据相同。研究表明,姜黄素类为庚二酮类化合物,在溶液中同时存在酮式和烯醇式结构[13-16],推测保留时间10.65、10.84 min处分别为二氢姜黄素、四氢姜黄素烯醇式结构的色谱峰。各对照品提取离子流色谱图示于图1。负离子模式下,姜黄素类化合物主要从碳碳单键处发生裂解,各对照品的具体裂解规律示于附图1(请登录《质谱学报》网站http:∥www.jcmss.com.cn下载)。
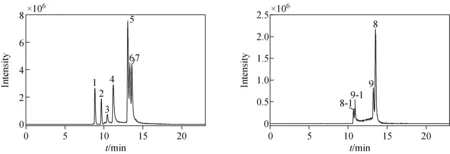
注:1.八氢姜黄素;2.六氢姜黄素;3.姜黄素-β-O-葡萄糖醛酸钠;4.姜黄素四叔丁基铵;5.双去甲氧基姜黄素;6.去甲氧基姜黄素;7.姜黄素;8.二氢姜黄素(酮式);8-1.二氢姜黄素(烯醇式);9.四氢姜黄素(酮式);9-1.四氢姜黄素(烯醇式)图1 各对照品提取离子流色谱图Fig.1 Extracted ion chromatograms of references
2.2 代谢产物分析
首先,根据原型药物结构推测可能的代谢产物,检索姜黄素类化合物代谢产物文献,建立包括化合物名称、分子式、精确分子质量、一级和二级质谱碎片的代谢物数据库;其次,利用TraceFinder 4.1 General Quan数据处理软件,同时在空白样品和给药样品的总离子流图中提取数据库中代谢产物的相对分子质量,得到仅在给药样品中色谱峰的保留时间、质谱碎片信息,并结合文献、对照品质谱数据及姜黄素类化合物的裂解规律[13-14],鉴定代谢产物,对照品质谱数据列于表1。姜黄提取物在大鼠体内代谢产物扣除空白后的总离子流色谱图示于图2。

表1 负离子模式下,各对照品一级和二级质谱数据Table 1 MS1 and MS2 data of references in negitive ion mode

注:a.血浆;b.粪便;c.胆汁;d.尿液图2 姜黄提取物在大鼠体内代谢产物扣除空白后的总离子流图Fig.2 Total ion chromatograms of metabolites subtracted background of turmeric extract in rats
2.3 姜黄提取物在大鼠体内代谢产物鉴定
本研究共鉴定出59个代谢产物,包括16个双去甲氧基姜黄素代谢产物(B1~B16)、15个去甲氧基姜黄素代谢产物(D1~D15)、16个姜黄素代谢产物(C1~C16)、12个无法归属的代谢产物(W1~W12)。代谢产物的质谱数据列于附表1。B3、B7、B8、B11~B13、C3、D3、D5、D8、D10、W1~W5、W7、W10、W12代谢产物的鉴定如下(其他代谢物二级质谱数据均与文献[8,10,17-23]数据一致)。
B3保留时间为6.14 min,其准分子离子峰[M-H]-m/z565.099 9,推测分子式可能为C25H25O13S,比对照品BDMC准分子离子峰大258 u(176+80+2),表明B3可能为BDMC硫酸酯化葡萄糖醛酸化氢化代谢产物。B3的二级碎片离子m/z485.145 0、389.067 9分别比准分子离子峰少80 u、176 u,证实B3中含有硫酸和葡萄糖醛酸;碎片离子m/z309.111 6比BDMC准分子离子峰多2 u,表明BDMC双键处发生还原,其母核结构可能为二氢双去甲氧基姜黄素。进一步裂解发现,m/z199.006 2由m/z565.099 9从C2、C3处裂解得到,m/z199.006 2失去1分子硫酸后得m/z119.049 7,因此,推测B3为二氢双去甲氧基姜黄素葡萄糖醛酸硫酸酯。由碎片离子m/z199.006 2可知,硫酸与双键左侧的羟基结合。
B7保留时间为7.05 min,其准分子离子峰[M-H]-m/z491.191 3,推测分子式可能为C25H32O10,比对照品BDMC准分子离子峰大184 u(176+8),表明可能为BDMC葡萄糖醛酸化氢化代谢物。B7的二级碎片离子m/z315.158 3比准分子离子峰多176 u,比对照品BDMC准分子离子峰多8 u,表明B7可能为八氢双去甲氧基姜黄素葡萄糖醛酸代谢物。进一步比较B7与B1(八氢双去甲氧基姜黄素葡萄糖醛酸硫酸)的质谱碎片,发现B7的二级质谱数据m/z491.191 3、315.158 3与B1的碎片离子m/z491.191 0[M-H-SO3]-、315.159 7[M-H-SO3-GluA]-相同,且B1中m/z315.159 7同样未进一步发生裂解,二者裂解方式相同。在保留时间6.29 min处,其准分子离子峰、碎片离子均与B7相同,因此推测6.29 min处为B7烯醇式结构色谱峰。
同理,可分别鉴定B8、B11为二氢双去甲氧基姜黄素葡萄糖醛酸、四氢双去甲氧基姜黄素葡萄糖醛酸。保留时间7.91 min处为B11烯醇式结构色谱峰。B8碎片离子m/z203.070 5、119.049 8由B8准分子离子峰[M-H]-m/z487.159 1失去1分子葡萄糖醛酸后,分别从C6、C7及C2、C3处发生断裂得到;B11碎片离子m/z205.086 1、163.075 7由B11准分子离子峰[M-H]-m/z487.159 1失去1分子葡萄糖醛酸后,分别从C6、C7及C4、C5处发生断裂得到。
B12保留时间为10.49 min,其准分子离子峰[M-H]-m/z389.067 7,推测分子式可能为C19H17O7S,比对照品BDMC准分子离子峰多82 u(80+2),表明可能为BDMC硫酸酯化氢化代谢物。B12碎片离子m/z309.112 1比其准分子离子峰少80 u,比对照品BDMC准分子离子峰多2u,比对照品BDMC准分子离子峰多2 u,推测可能为二氢双去甲氧基姜黄素硫酸酯代谢物。碎片离子m/z269.011 9为准分子离子峰m/z389.067 7从C5、C6处断裂得到,且可知硫酸与双键一侧羟基结合;m/z203.070 6为准分子离子峰m/z389.067 7从双键处发生断裂得到,因此推测B12可能为二氢双去甲氧基姜黄素硫酸酯,其二级碎片离子m/z189.055 1由m/z269.011 9失去1分子硫酸得到。同理,B13为四氢双去甲氧基姜黄素硫酸酯,保留时间8.38 min处为B13烯醇式结构色谱峰。
C3准分子离子峰[M-H]-m/z625.120 7,推测分子式可能为C27H29O15S,与对照品CUR准分子离子峰相比多258 u(176+80+2),推测为CUR硫酸酯化葡萄糖醛酸化氢化代谢物。C3的碎片离子m/z545.165 6、449.091 0与准分子离子峰分别相差80 u、176 u,证实C3中含有葡萄糖醛酸和硫酸酯结构。二级碎片离子m/z369.131 3、219.065 5、149.060 2、113.024 1与二氢姜黄素对照品的二级质谱碎片相同,因此推测C3为二氢姜黄素葡萄糖醛酸硫酸酯。m/z229.016 5表明葡萄糖醛酸与双键左侧羟基结合。
D3准分子离子峰[M-H]-m/z595.112 5,推测分子式可能为C26H27O14,与对照品DMC准分子离子峰相比多258 u(176+80+2),推测为DMC葡萄糖醛酸硫酸酯化氢化代谢物。m/z419.078 7[M-H-GluA]-、339.120 2[M-H-GluA-SO3]-证实结构中含有葡萄糖醛酸和硫酸,且其碎片离子m/z339.120 2比去甲氧基姜黄素准分子离子峰多2 u,因此推测D3为二氢去甲氧基姜黄葡萄糖醛酸硫酸酯。m/z229.016 5表明葡萄糖醛酸与双键左侧羟基结合、甲氧基位于双键左侧,由准分子离子峰从C2、C3处裂解得到。
D5准分子离子峰[M-H]-m/z519.183 5,推测分子式为C26H31O11,利用TraceFinder 4.1 General Quan数据处理软件对m/z519.183 5进行元素成分分析,发现D5与六氢去甲氧基姜黄素葡萄糖醛酸的分子质量误差小于5×10-6,初步推测为六氢去甲氧基姜黄素葡萄糖醛酸。用ChemDraw软件绘制六氢去甲氧基姜黄素葡萄糖醛酸结构,并进行碎片裂解,发现D5碎片离子m/z179.070 7为m/z519.183 5失去1分子葡萄糖醛酸后,从C3、C4处发生断裂得到,m/z179.070 7进一步失去1分子OCH3后,得到碎片离子m/z149.060 7,因此推测D5为六氢去甲氧基姜黄素葡萄糖醛酸。
D8保留时间为9.85 min,准分子离子峰[M-H]-m/z421.095 6,推测分子式为C20H21O8S,比对照品DMC准分子离子峰多84 u(80+4),表明其可能为DMC氢化硫酸酯化代谢物。碎片离子m/z341.136 5[M-H-SO3]-证实存在硫酸酯,碎片离子m/z341.136 5比DMC准分子离子峰多4 u,因此推测D8为四氢去甲氧基姜黄素硫酸酯。其二级碎片离子m/z235.097 6由准分子离子峰失去1分子硫酸后,从C6、C7处发生断裂得到;m/z219.101 1由准分子离子峰失去1分子硫酸后,从C5、C6处发生断裂,同时C5上羰基失去1分子氢与C3环合成丁烯内酯结构得到。同理,保留时间7.13 min处为D8烯醇式结构色谱峰,m/z259.027 6表明硫酸与甲氧基一侧的羟基结合,由m/z421.095 6从C3、C4处裂解得到。
D10与D8拥有相同的碎片离子m/z341.137 4、235.096 7,推测D8与D10具有相同的母核结构,且其准分子离子峰[M-H]-m/z517.171 8比碎片离子m/z341.137 4多176 u,表明D10为葡萄糖醛酸代谢物,因此推测其为四氢去甲氧基姜黄素葡萄糖醛酸。
W1~W5:W5保留时间为4.92 min,准分子离子峰[M-H]-m/z273.043 8,推测分子式为C11H13O6S。W5准分子离子峰与C8特征碎片离子m/z273.043 0相同,表明该化合物结构可能与C8特征碎片离子结构相同。碎片离子m/z193.086 2[M-H-SO3]-证实存在硫酸,m/z178.063 0为m/z273.043 8失去1分子硫酸后,再失去1分子CH3得到,因此推测W5为4-(4-羟基-3-甲氧基苯基)-丁-2-酮硫酸酯,其二级质谱图及可能的裂解规律示于图3。W3保留时间为4.66 min,准分子离子峰m/z369.117 0,推测分子式为C17H21O9。二级碎片离子m/z193.086 7[M-H-GluA]-表明W3为葡萄糖醛酸代谢物,且其碎片离子m/z193.086 7、178.063 6与W5相同,因此推测W3为4-(4-羟基-3-甲氧基苯基)-丁-2-酮葡萄糖醛酸。
W1准分子离子峰[M-H]-m/z371.132 0,推测分子式为C17H23O9,比W3准分子离子峰多2 u,推测W1为W3氢化代谢物。W1的二级质谱碎片m/z195.101 9[M-H-GluA]-证实存在葡萄糖醛酸,且W1准分子离子峰、碎片离子m/z195.101 9、180.078 3比W3准分子离子峰、碎片离子m/z193.086 7、178.063 6均多2 u,表明W1发生了氢化,因此推测W1为4-(3-羟丁基)-2-甲氧基苯酚葡萄糖醛酸。W2准分子离子峰[M-H]-m/z275.059 6,推测分子式为C11H15O6S,比W5准分子离子峰多2 u,推测W2为W5氢化代谢物,其二级碎片离子m/z195.101 9[M-H-SO3]-证实结构中含有硫酸,碎片离子m/z195.101 9、180.078 6与W1相同,因此推测W2为4-(3-羟丁基)-2-甲氧基苯酚硫酸酯。
W4准分子离子峰[M-H]-m/z243.032 7,推测分子式为C10H11O5S,比W5准分子离子峰少30 u,表明W4在结构上比W5少1个甲氧基。m/z243.032 7比碎片离子m/z163.076 0多80 u,证实W4中含有硫酸结构,而m/z119.048 9为m/z243.032 7失去1分子硫酸后,再失去1分子CO得到,因此推测该化合物为4-(4-羟苯基)-丁-2-酮硫酸酯。
W7保留时间为7.12 min,其准分子离子峰[M-H]-m/z409.094 2,推测分子式为C19H21O8S,与对照品BDMC相比多102 u(80+16+6),推测W7可能为BDMC羟基化氢化硫酸酯化代谢物。碎片离子m/z329.137 5证实存在硫酸。碎片离子m/z149.060 1为m/z329.137 5从C4、C5处裂解后失去1分子羟基得到,表明W7中含有羟基,因此推测W7为羟基化六氢双去甲氧基姜黄素硫酸酯。碎片离子m/z245.011 6、259.027 7表明羟基与硫酸化均位于羰基碳一侧,m/z179.070 7为m/z259.027 7失去1分子硫酸得到。保留时间5.12 min处为W7烯醇式结构色谱峰。
W10准分子离子峰[M-H]-m/z291.102 6,推测分子式为C19H15O3,与对照品BDMC准分子离子峰相比少16 u,推测W10为BDMC去羟基化代谢物。利用ChemDraw软件绘制BDMC去掉1分子羟基的结构,并根据姜黄素类化合物裂解规律[7-8]进行碎片裂解,发现得到的碎片离子与实际得到的碎片离子不符,推测W10为BDMC去羟基化的同分异构体。尝试将C3、C4位置的双键结构换成三键,并去掉C1、C2位置的双键,再次进行裂解发现,准分子离子峰m/z291.102 6分别从C1和C2、C2和C4、C4和C5处断裂得到m/z185.060 0、171.044 6、145.056 2。其中,m/z249.091 1为m/z291.102 6失去1分子CO后重排得到,因此推测W10为1,7-双(4-羟基苯基)庚-1-烯-4-炔-3-酮,其质谱裂解规律示于图4。

图3 W5二级质谱图及可能的裂解规律Fig.3 MS2 spectrum and proposed fragmention pathways of W5
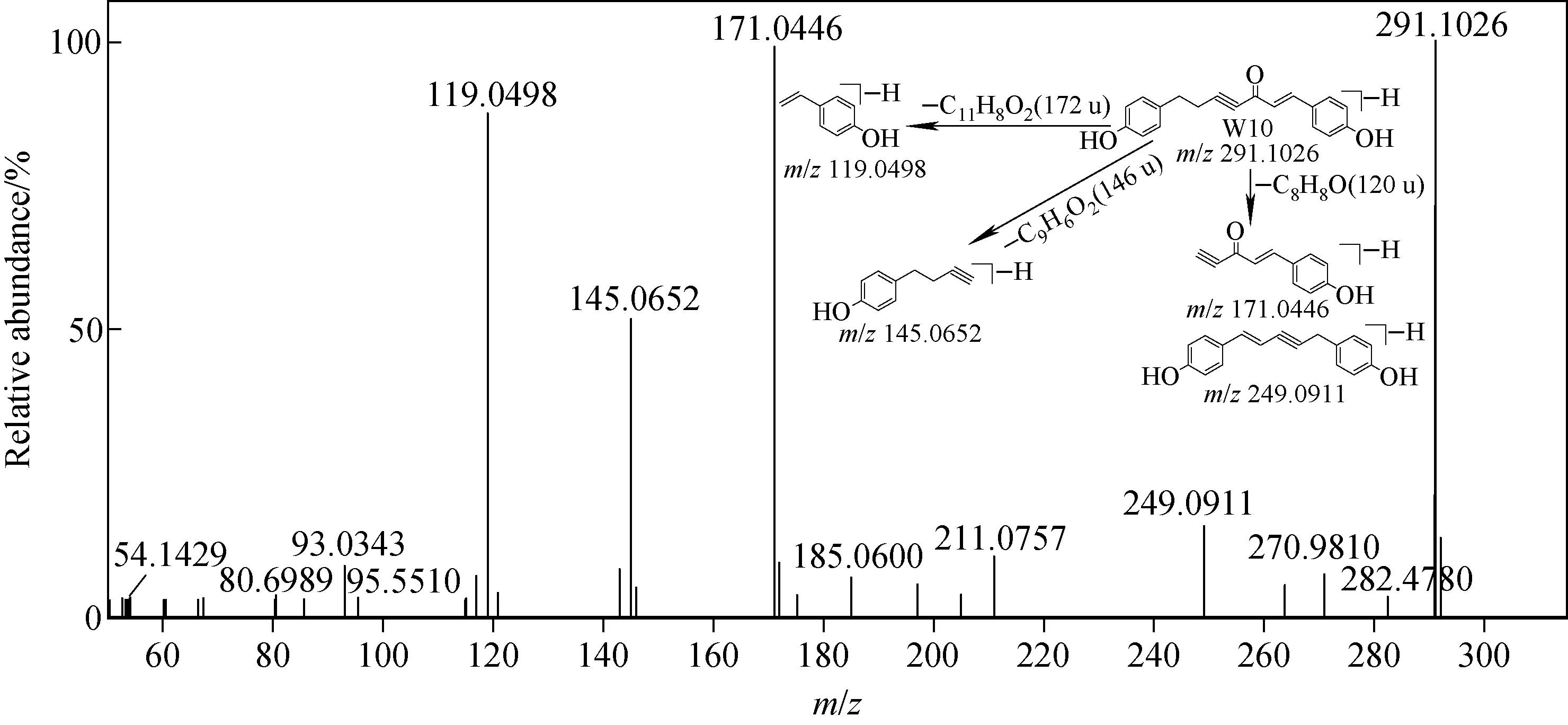
图4 W10二级质谱图及可能的裂解规律Fig.4 MS2 spectrum and proposed fragmental pathways of W10
同理,W12准分子离子峰[M-H]-m/z295.133 2,推测分子式为C19H19O3,与对照品BDMC准分子离子峰相比少12 u(16-4),推测由BDMC失去1分子双键氧和1分子双键得到。利用ChemDraw软件绘制BDMC去掉1分子双键氧和1分子双键的结构,并根据姜黄素类化合物的裂解规律[13-14]进行碎片裂解,推测W12为四氢双去甲氧基姜黄素去羟基化代谢物,其质谱裂解规律示于图5。
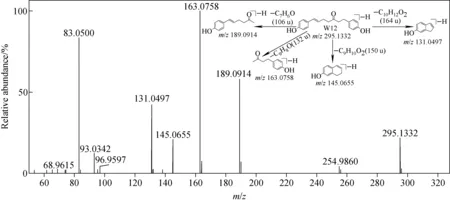
图5 W12二级质谱图及可能的裂解规律Fig.5 MS2 spectrum and proposed fragmental pathways of W12
2.4 CUR、DMC、BDMC在大鼠体内的代谢途径
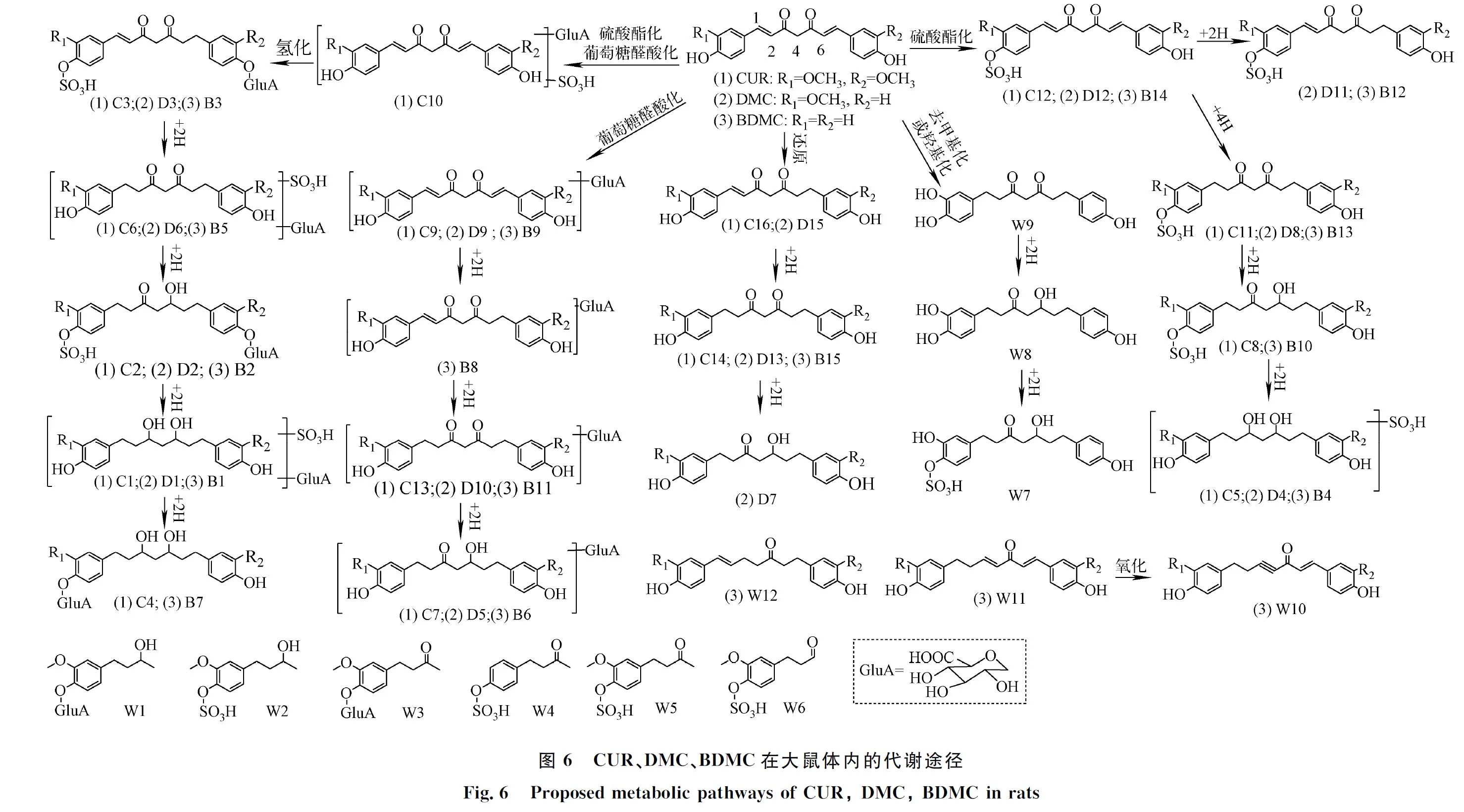
姜黄提取物中3种姜黄素类化合物在大鼠血浆、胆汁中的代谢途径以母体药物还原氢化后与葡萄糖醛酸和硫酸结合为主;粪便中以母体药物还原氢化、还原氢化后与硫酸结合为主;尿液中以母体药物还原氢化、还原氢化后与葡萄糖醛酸和硫酸结合为主。姜黄提取物中3种姜黄素类化合物在大鼠体内可能的代谢途径示于图6。
2.5 讨论
本研究在姜黄提取物中共鉴定出59个代谢产物,粪便中18个、尿液中39个、血浆中33个、胆汁中36个。其中,姜黄素代谢产物16个(血浆中8个、粪便中5个、尿液中11个、胆汁中8个);去甲氧基姜黄素代谢产物15个(血浆中8个、粪便中3个、尿液中10个、胆汁中9个);双去甲氧基姜黄素代谢产物16个(血浆中11个、粪便中4个、尿液中12个、胆汁中13个);无法归属的代谢产物12个(血浆、粪便、尿液、胆汁各6个)。
不同生物样品中,姜黄提取物各代谢产物在种类和数量上存在交叉。研究发现,同时存在于血浆、尿液、胆汁3种生物样品中的代谢物最多,有14个(B1、B2、B6、B8、B9、B14、C2、C5、D2、D5、D8、W2、W4、W5),为六氢或八氢原型药物的葡萄糖醛酸或硫酸结合物、六氢或八氢原型药物的葡萄醛酸和硫酸共同结合物;同时存在于粪便、尿液和胆汁生物样品中的代谢物有3个,分别为C11(四氢双去甲氧基姜黄素硫酸)、D14(去甲氧基姜黄素)、W7(六氢羟基化双去甲氧基姜黄素硫酸酯)。粪便与尿液共同代谢产物有8个(B15、B16、C14、C15、C16、D13、W10、W12),为一相代谢物和原型药物;血浆与尿液共同代谢产物有4个(B11、C9、C12、D12),主要为原型药物葡萄糖醛酸或硫酸酯结合物;血浆与胆汁共同代谢产物有4个(B5、B13、C6、D6),主要为四氢原型药物的葡萄糖醛酸和硫酸共同结合物;尿液与胆汁生物样品中共同代谢产物有3个(B7、C4、D1),为八氢原型药物的葡萄糖醛酸结合物或葡萄糖醛酸和硫酸共同结合物;4种生物样品中均可发现代谢物B4、B10、C8、D4,为八氢或六氢原型药物的硫酸酯结合物。此外,D3、D11、C3、B3、B12等二氢化原型药物的葡萄糖醛酸结合物或葡萄糖醛酸和硫酸共同结合物仅在胆汁中发现。
本研究未对W1~W12进行归属,是因为W1~W5化合物结构较小,无法判断是姜黄提取物中哪种成分的代谢产物;而W8、W9既可能是去甲氧基姜黄素去甲基化代谢产物,也可能是双去甲氧基姜黄素羟基化代谢物;W10~W12既可能是双去甲氧基姜黄素代谢物,也可能是姜黄提取物中其他姜黄素类化合物以原型形式排出体外;W7作为W8硫酸酯化代谢物同样无法进行归属。另外,由于3种姜黄素类化合物均可能产生W6,因此本研究并未将W6归属为姜黄素代谢产物[19]。
与文献[6,8-11]对比,本研究在大鼠体内发现了16个新的代谢产物(B3、B7、B8、B11~B13、C3、D3、D5、D8、D10、W1、W2、W4、W5、W7、W10)、4个已知代谢物(B6、W3、W11、W12)。但未鉴定出文献[11](大鼠灌胃给予姜黄素类化合物)在大鼠粪便和尿液中分离出的六氢姜黄素、六氢双去甲氧基姜黄素、八氢姜黄素、八氢双去甲氧基姜黄素、1,5-环氧-3-羰基-1,7-双(4-羟基苯基)-4,6-庚二烯、八氢姜黄素二去甲基化二去羟基化代谢物、八氢双去甲氧基姜黄素去羟基化代谢物;未鉴定出文献[10](大鼠灌胃给予去甲氧基姜黄素单体)在大鼠粪便和尿液中分离出的5-去羟基二氢去甲氧基姜黄素、六氢去甲氧基姜黄素甲基化代谢物、六氢去甲氧基姜黄素去羟基化代谢物、八氢去甲氧基姜黄素去羟基化代谢物,这可能是因为上述代谢产物排出体外需要的时间较长(收集粪便和尿液时间为48 h),而本研究仅收集了0~12 h的粪便和尿液;未鉴定出文献[6,9](大鼠灌胃给予姜黄素单体)在大鼠血浆中分离出的六氢姜黄素[6,9]、八氢姜黄素[6]、4-(3-羟丙基-1-烯基)-2甲氧基苯酚[6]、4-(3-羟丙基)-2-甲氧基苯酚[6]、1-羟基-4-(4-羟基-3-甲基苯基)-3-烯-2-酮[6]、二氢姜黄素葡萄糖醛酸[9],这可能是因为姜黄提取物中的其他成分会促进姜黄素在大鼠体内的代谢,加快了一相代谢物向二相代谢物的转变;未鉴定出文献[8](大鼠分别灌胃给予姜黄素纳米制剂、去甲氧基姜黄素纳米制剂、双去甲氧基姜黄素纳米制剂)在大鼠体内分离出的去甲氧基姜黄素葡萄糖醛酸硫酸酯、双去甲氧基姜黄素葡萄糖醛酸硫酸酯、六氢去甲氧基姜黄素硫酸酯、二氢双去甲氧基姜黄素,这可能是因为本研究中去甲氧基姜黄素和双去甲氧基姜黄素的给药剂量比文献低。
3 结论
本研究共鉴定出59个大鼠血浆、粪便、尿液、胆汁中的姜黄提取物代谢产物,其中16个新的代谢产物,粪便、血浆中新发现的代谢产物各2个,尿液中新发现1个代谢产物。研究表明,姜黄素类化合物原型成分及一相代谢产物主要存在于粪便、尿液中,二相代谢产物主要存在于血浆、胆汁中。本研究对去甲氧基姜黄素、双去甲氧基姜黄素代谢产物进行了补充,可为后续活性代谢物的筛选提供依据。
