HPLC 法同时测定涤痰丸中7 种成分
2019-01-25单柏宇徐伟男鲍慧玮
徐 阳, 单柏宇, 徐伟男, 鲍慧玮
(1. 长春医学高等专科学校药品食品学院, 吉林 长春130031; 2. 白城市食品药品检验所, 吉林 白城137000; 3. 呼伦贝尔北方药业有限公司, 内蒙古 呼伦贝尔022150; 4. 长春中医药大学药学院, 吉林长春130117)
涤痰丸收载于《中华人民共和国卫生部药品标准(中药成方制剂) 》 第二册(标准编号WS3-B-0386-90), 是由牵牛子(炒)、 大黄、 黄芩3 味药材与百草霜、 煅金礞石粉末、 桃胶一起配研、 熔化制成的褐黄色水丸, 具有清热化痰、 开郁化痞的功效, 临床上用于痰火郁结、 气急疯痫、 湿热咳嗽、 胸满作喘、 痰涎壅盛、 大便燥结[1-2]。 其中,大黄素、 大黄酸、 儿茶素、 没食子酸、 阿魏酸是大黄主要药效成分, 具有泻下攻积、 清热泻火、 逐瘀通经、 抗病原微生物、 抗炎、 止血等作用[3-4]; 黄芩苷是黄芩主要药效成分, 具有清热燥湿、 泻火解毒、 止血、 抗炎等作用[5-6]; 大黄素、 咖啡酸是牵牛子(炒) 的主要药效成分, 具有治疗水肿胀满、二便不通、 痰饮积聚、 气逆喘咳等作用[7]。 然而,目前涤痰丸质量标准不完善, 尚无针对其含有量测定的方法, 故本实验建立HPLC 法同时测定其中没食子酸、 儿茶素、 咖啡酸、 大黄酸、 大黄素、 阿魏酸、 黄芩苷的含有量, 为该制剂质量评价和控制提供依据。
1 材料
1.1 仪器 Agilent 1260 高效液相色谱仪, 配置DAD 检测器(美国Agilent 公司); AB135-S 型电子分析天平[梅特勒-托利多国际贸易(上海) 有限公司]; DK-98-Ⅱ型电热恒温水浴锅(天津市泰斯特仪器有限公司); R 系列旋转蒸发器(上海申生科技有限公司); KQ-250 型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 涤痰丸(按照标准处方及制备工艺自制)。 没食子酸 (批号110831-201204)、 儿茶素(批 号 877-200001)、 咖 啡 酸 ( 批 号 110885-200102)、 大黄酸(批号110757-2000206)、 大黄素(批号110756-200110)、 阿魏酸(批号110773-200611)、 黄芩苷(批号110715-201318) 对照品(中国食品药品检定研究院)。 甲醇为色谱纯; 其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 Agilent ZORBAX SB-C18色谱柱(4.6 mm×250 mm, 5 μm); 流动相甲醇(A) -0.1%磷酸(B), 梯度洗脱, 程序见表1; 体积流量1.0 mL/min; 柱温30 ℃; 检测波长254、 278、320 nm; 进样量10 μL。
2.2 溶液制备
2.2.1 对照品溶液 取没食子酸、 儿茶素、 咖啡酸、 大黄酸、 大黄素、 阿魏酸、 黄芩苷对照品适量, 置于10 mL 量瓶中, 甲醇溶解并定容至刻度,制得每1 mL 分别含没食子酸349.3 μg、 儿茶素584.3 μg、 咖啡酸0.943 5 μg、 大黄酸134.4 μg、大黄 素53.32 μg、 阿 魏 酸1.636 μg、 黄 芩 苷863.8 μg的溶液, 即得。

表1 梯度洗脱程序Tab.1 Gradient elution programs
2.2.2 供试品溶液 本品研细, 精密称取约0.5 g粉末, 置于具塞锥形瓶中, 加入10 mL 甲醇, 密塞, 称定质量, 超声60 min, 放冷, 甲醇补足减失的质量, 摇匀, 滤过, 取续滤液, 即得。
2.2.3 阴性样品溶液 按处方和工艺分别制备缺大黄、 缺牵牛子和大黄、 缺黄芩和大黄的阴性样品, 按“2.2.2” 项下方法制备相应溶液, 即得。
2.3 方法学考察
2.3.1 专属性试验 取对照品、 供试品、 阴性样品溶液, 在“2.1” 项色谱条件下进样测定, 结果见图1~3。 由图可知, 各成分在相应位置均无干扰, 表明该方法专属性良好, 而且其色谱峰理论塔板数均大于3 000, 分离度均大于1.5。
2.3.2 线性关系考察 精密称取没食子酸、 儿茶素、 咖啡酸、 大黄酸、 大黄素、 阿魏酸、 黄芩苷对照品适量, 甲醇制成2 794.4、 4 674.4、 7.548、1 075.2、 426.56、 13.088、 6 910.4 μg/mL 贮 备液, 依次稀释1/2、 1/4、 1/8、 1/16、 1/32、 1/64倍, 在“2.1” 项色谱条件下进样测定。 以待测成分峰面积为纵坐标(Y), 对照品质量浓度为横坐标(X) 进行回归, 结果见表2, 可知各成分在各自范围内线性关系良好。
2.3.3 精密度试验 取“2.2.1” 项下对照品溶液6 份, 在“2.1” 项色谱条件下进样测定, 测得没食子酸、 儿茶素、 咖啡酸、 大黄酸、 大黄素、 阿魏酸、 黄芩苷峰面积RSD 分别为0.98%、 0.68%、1.78%、 1.84%、 1.77%、 0.59%、 1.98%, 表 明仪器精密度良好。

图1 各成分HPLC 色谱图(278 nm)Fig.1 HPLC chromatograms of various constituents (278 nm)
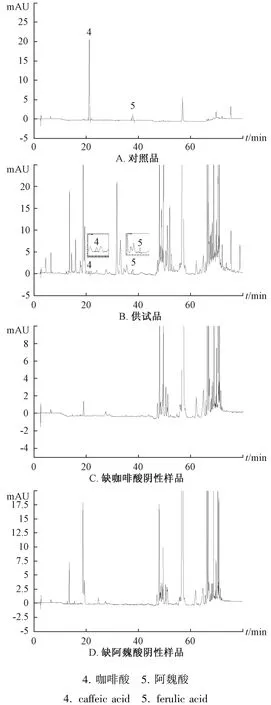
图2 各成分HPLC 色谱图(320 nm)Fig.2 HPLC chromatograms of various constituents (320 nm)

表2 各成分线性关系Tab.2 Linear relationships of various constituents

图3 各成分HPLC 色谱图(254 nm)Fig.3 HPLC chromatograms of various constituents(254 nm)
2.3.4 重复性试验 称取本品粉末适量, 共6 份,按“2.2.2” 项下方法制备供试品溶液, 在“2.1”项色谱条件下进样测定, 测得没食子酸、 儿茶素、咖啡酸、 大黄酸、 大黄素、 阿魏酸、 黄芩苷含有量RSD 分 别 为 1.98%、 1.90%、 1.96%、 1.77%、1.93%、 1.59%、 1.44%, 表明该方法重复性良好。
2.3.5 稳定性试验 取“2.2.2” 项下供试品溶液, 于0、 2、 4、 8、 12、 24 h 在“2.1” 项色谱条件下进样测定, 测得没食子酸、 儿茶素、 咖啡酸、大黄酸、 大黄素、 阿魏酸、 黄芩苷峰面积RSD 分别为0.75%、 1.80%、 1.98%、 1.96%、 1.82%、0.62%、 1.32%, 表明溶液在24 h 内稳定性良好。
2.3.6 加样回收率试验 精密称取含有量已知的本品(批号20170501) 6 份, 每份约0.25 g, 精密加入对照品溶液, 按“2.2.2” 项下方法制备供试品溶液, 在“2.1” 项色谱条件下进样测定, 计算回收率。结果, 没食子酸、 儿茶素、 咖啡酸、 大黄酸、 大黄素、 阿魏酸、 黄芩苷平均加样回收率分别为99.77%、 99.84%、 100.55%、 98.74%、 99.67%、100.95%、 100.74%, RSD 分别为1.60%、 1.25%、1.84%、 1.77%、 1.08%、 1.58%、 0.86%。
2.4 样品含有量测定 取3 批本品, 按“2.1.2”项下方法制备供试品溶液, 在“2.1” 项色谱条件下进样测定, 计算含有量, 结果见表3。
3 讨论
3.1 流动相选择 本实验考察甲醇-水、 乙腈-水,甲醇-磷酸-水, 乙腈-磷酸-水体系, 发现在甲醇-水、 乙腈-水体系下没食子酸和儿茶素有拖尾现象,而在甲醇-磷酸-水体系下各待测成分色谱峰峰形和分离度均良好。 另外, 由于待测成分多, 极性差异明显, 流动相极性跨度也较大, 故梯度变化不宜过快。 最终, 确定 “2.1” 项下流动相进行梯度洗脱。

表3 各成分含有量测定结果(mg/g, n=3)Tab.3 Results of content determination of various constituents (mg/g, n=3)
3.2 检测波长选择 本实验通过HPLC-DAD 检测器, 在200~400 nm 波长范围内进行考察, 同时比较供试品中各待测成分色谱峰, 以物质吸收大小和与其他色谱峰分离度作为指标。 最终确定, 检测波长为254 nm (大黄酸、 大黄素)[8-10]、 278 nm (没食子酸、 儿茶素、 黄芩苷)[11-13]、 320 nm (咖啡酸、 阿魏酸)。
3.3 供试品制备方法选择 本实验比较了超声提取法、 热回流提取法、 索氏提取法、 浸渍法的提取效果, 最终选择超声提取法, 该方法具有较高的提取率, 而且可保护一些热敏性物质不被破坏。 然后, 比较了乙醇、 甲醇、 三氯甲烷、 石油醚的提取效果, 最终选择甲醇作为提取溶剂。
