咖啡酸苯乙酯固体分散体的制备
2019-01-25张德辉庞赞明
王 兰, 张德辉, 沈 文, 龚 频, 庞赞明, 孙 蕊, 敖 芬
(陕西科技大学, 陕西 西安710021)
咖啡酸苯乙酯作为蜂胶提取物的主要成分之一[1-2], 在抗肿瘤、 保肝、 抗缺血再灌注损伤、 抑菌、 降血糖等方面有不同程度的作用[3-8], 而且迄今尚未发现它对正常细胞的有害影响[1], 故在食品、 医学等领域具有广阔的应用前景。 但咖啡酸苯乙酯溶解度很低, 从而影响其生物利用度[1,9], 限制了在治疗和预防上的应用, 同时对该成分的研究目前主要集中在提取工艺、 药理活性等方面, 鲜有制剂方面的报道。
研究表明, 固体分散体可提高水溶性差的药物的溶 解 度[10]。 因 此, 本实 验 以PVP K30 为 载体[11], 采用溶剂法制备咖啡酸苯乙酯固体分散体,并对其溶解度及体外溶出特性进行研究, 然后通过扫描电镜、 X-射线粉末衍射法、 差示扫描量热法对其进行物相鉴别。
1 材料
1.1 试药 咖啡酸苯乙酯原料药(湖北远成赛创科技有限公司); 咖啡酸苯乙酯对照品(中国食品药品检定研究院); 聚乙烯吡咯烷酮K30 (PVP K30, 上海蓝季生物有限公司)。
1.2 仪器 TA2603B 电子天平(上海天美天平仪器有限公司); ZRS-8GD 智能溶出试验仪(天津市天大天发科技有限公司); UV-5100 紫外可见分光光度计(上海元析仪器有限公司); RE52CS 旋转蒸发仪(上海亚荣生化仪器厂); X-射线粉末衍射仪; 飞纳Phenom Pro 台式扫描电镜; STA409PC 同步综合热分析仪(德国耐驰公司)。
2 方法与结果
2.1 检测波长选择 无水乙醇配制质量浓度适宜的咖啡酸苯乙酯溶液, 再配制空白辅料, 过0.45 μm微孔滤膜, 在200 ~400 nm 波长范围内进行紫外扫描。结果, 咖啡酸苯乙酯在330 nm 波长处有最大吸收, 空白辅料无干扰, 故选择其作为检测波长。
2.2 线性关系考察 精密称取咖啡酸苯乙酯对照品1 mg, 无水乙醇定容于50 mL 量瓶中, 得到20 μg/mL贮备液, 分别精密量取2、 3、 4、 5、 6、7、 8、 9 mL 于10 mL 量瓶中, 定容至刻度。 以吸光度为纵坐标(Y), 咖啡酸苯乙酯质量浓度为横坐标(X) 进行回归, 得到回归方程为Y =0.056 9X +0.071 8 (R2=0.999 7), 在4~18 μg/mL 范围内线性关系良好。
2.3 精密度、 准确度试验 配制低、 中、 高(4、10、 15 μg/mL) 质量浓度的咖啡酸苯乙酯溶液,同1 d 内平行测定5 次, 考察日内精密度; 每天测定1 次, 连续5 d, 考察日间精密度。结果, 低、中、 高质量浓度溶液的日内、 日间精密度RSD 分别为1.12%、 1.42%, 1.23%、 1.89%, 0.97%、1.51%, 准确度分别为97%、 103%、 96%, 表明该方法精密度、 准确度良好。
2.4 样品制备
2.4.1 固体分散体 按处方比例(1 ∶4、 1 ∶6、1 ∶8、 1 ∶10、 1 ∶12) 分别称取适量咖啡酸苯乙酯、 PVP K30, 溶于适量无水乙醇中, 混合均匀后置于旋转蒸发仪上, 60 ℃下水浴旋蒸至黏稠状态,转移至烘箱中烘干, 粉碎, 过80 目筛, 即得, 置于干燥器中保存备用。
2.4.2 物理混合物 按“2.4.1” 项下处方比例分别称取适量咖啡酸苯乙酯、 PVP K30, 研细后等量递加法混合均匀, 过80 目筛, 即得, 置于干燥器中保存备用。
2.5 溶解度测定 取适量咖啡酸苯乙酯、 固体分散体, 置于100 mL 烧杯中, 加50 mL 水, 在(25±1)℃下磁力搅拌4 h (吸光度不再变化时达到平衡), 使其成为过饱和溶液, 0.45 μm 微孔滤膜过滤, 取续滤液, 计算两者在水中的平衡溶解度。
2.6 溶出度测定 按照2015 年版《中国药典》四部通则0931 “溶出度与释放度测定法” 第二法(桨法) 测定[12], 以900 mL 脱气水为溶出介质,满足漏槽条件。 投入15 mg 咖啡酸苯乙酯及各待测处方载药量均为15 mg 的固体分散体, 在温度(37.0±0.5)℃、 转速100 r/min 条件下于10、 20、30、 40、 50、 60 min 取样5 mL, 同时补充等温同体积溶出介质, 样品过0.45 μm 微孔滤膜后测定吸光度, 并代入“2.2” 项下回归方程, 测得各时间点质量浓度, 计算累积溶出度, 绘制溶出曲线。
2.7 载体材料选择 在预实验中选择PEG6000、PVP K30 作为载体材料制备固体分散体, 发现采用熔融法时, PEG6000 制备的固体分散体材质偏软, 不易干燥粉碎, 难以取用; 采用溶剂法时,PVP K30 制备的固体分散体易干燥粉碎, 便于取用。 因此, 选择PVP K30 作为载体进行下一步实验, 并通过溶剂法制备固体分散体。
2.8 载体比例选择
2.8.1 溶出度 图1 显示, 相同比例下固体分散体的溶出速率明显大于原料药和物理混合物, 而且在10 min 时的累积溶出度最高可达到80% 左右,而物理混合物仅为6%左右, 原料药更是只有1%,表明PVP K30 对咖啡酸苯乙酯溶出具有一定促进作用。 同时, 咖啡酸苯乙酯与PVP K30 的最佳比例为1 ∶10。

图1 固体分散体溶出曲线Fig.1 Dissolution curves for solid dispersions
2.8.2 溶解度 图2 显示, 25 ℃时咖啡酸苯乙酯的溶解度为(23.374±1.572) μg/mL, 物理混合物略有增加, 而固体分散体显著提高, 以咖啡酸苯乙酯与PVP K30 比例1 ∶10 时最佳, 比原料药提高了56%, 但与其他比例相比提升不明显, 而且随着其增加载药量反而降低。 因此, 选择两者比例为1 ∶10。

图2 固体分散体溶解度Fig.2 Solubilities of solid dispersions
2.9 扫描电镜(SEM) 条件为真空镀金60 s,高压5 kV, 采用SEM 观察样品形态和晶体结构,结果见图3。 由图可知, 咖啡酸苯乙酯以大小不一的矩形片状晶体形式存在; PVP K30 为球形或类球形, 物理混合物中仍可观察到咖啡酸苯乙酯结构和PVP K30 存在, 而且两者互无影响; 固体分散体中已无明显咖啡酸苯乙酯晶体结构存在, 表明该成分以非结晶态均匀分散在PVP K30 中, 并可能已形成固体分散体。

图3 样品SEM 图Fig.3 SEM images for samples
2.10 差示扫描量热(DSC) 以空白铝坩埚为参比物, N2为保护气, 温度40 ~150 ℃, 升温速度5 ℃/min, 采用DSC 对样品进行分析, 结果见图4。 由图可知, 咖啡酸苯乙酯在128 ℃处有1 个熔融吸热峰, 为其熔点, 与前期报道[1]一致; PVP K30 在128 ℃处未出现明显吸收峰; 物理混合物在128 ℃处仍存在较小的熔融吸热峰, 为咖啡酸苯乙酯熔点, 表明PVP K30 与其未发生相互作用, 该成分仍以晶体形式存在; 固体分散体在128 ℃处吸收峰消失, 表明咖啡酸苯乙酯与PVP K30 可能形成低共熔物或共沉淀物, 即以无定形态分散在载体中。
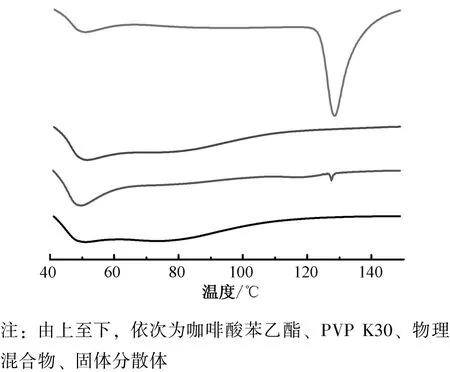
图4 样品DSC 曲线Fig.4 DSC curves for samples
2.11 X 射线衍射(XRD) 采用XRD 对样品进行分析, 结果见图5。 由图可知, 咖啡酸苯乙酯在6.24°处有较强的吸收峰, 表明它以结晶态存在;PVP K30 在0°~10°处无特征衍射峰, 表明它是无定型材料; 物理混合物在6.24°处的峰强度减弱,表明咖啡酸苯乙酯仍以晶体形式存在, 但占总成分比例降低, 故其峰强度低于咖啡酸苯乙酯; 固体分散体衍射峰消失, 表明咖啡酸苯乙酯以无定形状态存在于PVP K30 中。

图5 样品XRD 图Fig.5 XRD patterns for samples
3 讨论
本实验制备了咖啡酸苯乙酯固体分散体, 发现其溶解度及溶出速率与原料药相比得到了显著提高。 结合SEM、 XRD、 DSC 分析可知, 载体与药物共蒸发溶剂时, 药物分子以无定形状态分散于载体中, 两者之间存在氢键等相互作用, 导致在固化时形成了具有较高能量的非结晶无定形物, 从而增加咖啡酸苯乙酯在溶出介质中的释放速率。 另外,咖啡酸苯乙酯与PVP K30 比例为1 ∶10 时, 所得固体分散体中前者溶解度、 溶出度最大。
综上所述, 本实验提供了一种简单有效的咖啡酸苯乙酯固体分散体制备方法, 它作为一种药物中间体, 可为片剂、 颗粒剂等剂型的研制奠定基础。
