Peg-IFNα-2b联合利巴韦林治疗基因1/6型慢性丙型肝炎患者临床研究*
2019-01-23侯春阳马玉梅李方治
侯春阳,马玉梅,李方治
全世界感染丙型肝炎病毒(hepatitis C virus,HCV)大概为1.8亿人,我国一般人群抗HCV阳性率仅为3.2%,大约有5000万慢性丙型肝炎(chronic hepatitis C,CHC)患者,不同地区其感染率也不太一样[1]。聚乙二醇化干扰素(pegylated interferon,peg-IFN)α-2a联合利巴韦林(ribavirin,RBV)治疗 CHC患者,持续病毒学应答率(sustained virological response,SVR)高达 75%[2]。研究发现,抗病毒效果会受到如基线HCV载量、病毒基因型、年龄、性别、使用的药物及其剂量、肝纤维化或脂肪变程度及有无乙型肝炎病毒(hepatitis B virus,HBV)、丁型肝炎病毒(hepatitis D virus,HDV)或人类免疫缺陷病毒(human immunodeficiency virus,HIV)合并感染等因素的影响[3]。我们应用peg-IFNα-2a联合RBV治疗了基因1/6型CHC患者,观察了临床疗效情况,现报道如下。
1 资料与方法
1.1 一般资料 2012年10月~2017年10月在我院就诊的CHC患者246例,年龄为18~65岁。血清抗-HCV或HCV RNA阳性超过6个月,HCV基因分型为1/6型。排除标准:6个月内接受过干扰素治疗者或既往对干扰素治疗无应答者,疑似肝硬化或肝细胞癌、合并其他系统疾病、神经精神疾病病史或家族史和HCV混合基因型感染者。采用随机数字表法将患者分为观察组123例和对照组123例,两组年龄、性别和病情比较无统计学差异(P<0.05),具有可比性。本研究已获得我院医学伦理委员会审核,患者签署知情同意书。
1.2 治疗方法 给予观察组Peg-IFNα-2b 80 μg皮下注射,1次/w;给予对照组Peg-IFNα-2a 180 μg皮下注射,1次/w。给予两组患者利巴韦林l 000 mg·d-1(体质量<75 kg)或l 200 mg·d-1(体质量≥75 kg),分早、晚2次口服,疗程均为48 w。随访24 w。
1.3 检测 采用罗氏公司COBAS Taqman HCV实时定量PCR试剂检测血清HCV RNA;采用Abbott RealTime HCV Genotype II试剂检测HCV基因型。
1.4 统计学方法 应用SPSS 20.0统计学软件,计量资料以±s表示,采用t检验,计数资料采用x2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组基线资料比较 两组基因型、血清HCV RNA水平、白细胞计数、血小板计数和血清ALT水平差异无统计学意义(P>0.05,表1、表2)。
表1 两组基线资料[%,(±s)]比较
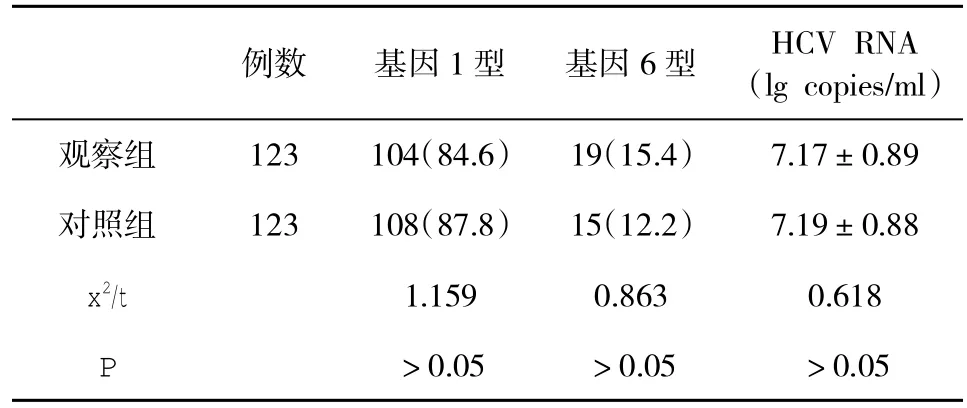
表1 两组基线资料[%,(±s)]比较
例数 基因1型 基因6型 HCV RNA(lg copies/ml)观察组 123 104(84.6) 19(15.4) 7.17±0.89对照组 123 108(87.8) 15(12.2) 7.19±0.88 x2/t 1.159 0.863 0.618 P>0.05 >0.05 >0.05
表2 两组基线资料(±s)比较
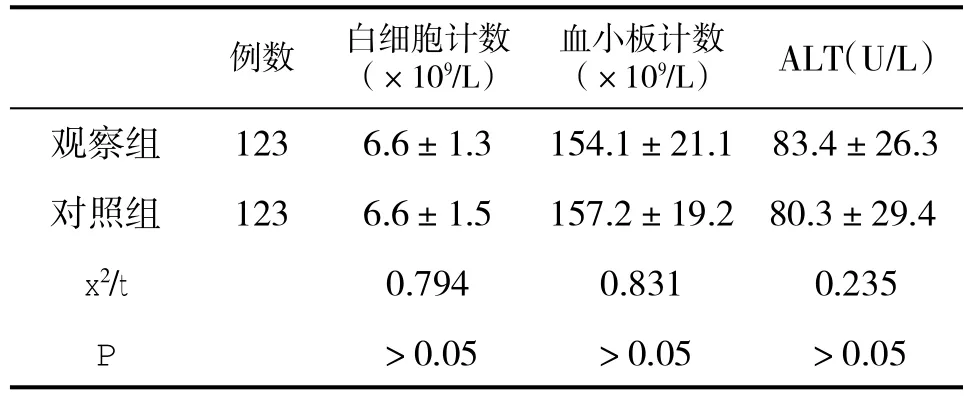
表2 两组基线资料(±s)比较
血小板计数(×109/L)观察组 123 6.6±1.3 154.1±21.1 ALT(U/L)83.4±26.3对照组 123 6.6±1.5 157.2±19.2 80.3±29.4 x2/t 0.794 0.831 0.235 P>0.05 >0.05 >0.05例数 白细胞计数(×109/L)
2.2 两组病毒学应答率比较 两组快速病毒学应答率(RVR)、早期病毒学应答率(EVR)、治疗结束时病毒学应答率(ETVR)、SVR和复发率比较,差异无统计学意义(P>0.05,表3)。
2.3 两组不良反应发生率比较 在治疗过程中,两组发热、肌肉酸痛、乏力、头痛、厌食、脱发、失眠、白细胞下降、红细胞下降、血小板下降和血清T3/T4/TSH异常等不良反应发生率比较,差异无统计学意义(P>0.05,资料未列出)。

表3 两组病毒学应答率(%)比较
3 讨论
根据异质性的不同,可将HCV基因分为la、lb、2a、2b、3a、4a、4b、4c、4d、5a 和 6a 等不同的亚型,其中全世界都有的基因型有la、lb、2a、2b,欧美比较流行的为la、lb、2a、2b和3a型,以1a型占比比较高,中国和日本的大部分地区常见基因型以lb、2a和2b型为主,其中有65%~75%为lb型[4]。Péres et al认为不同HCV基因型因致病性不同可能导致不同的疾病类型和不同的治疗效果,致病性较强的是基因1型,其治疗效果较差[5]。Cox-North et al提出治疗HCV感染患者,应该根据基因型的不同来进行个性化的有针对性的治疗,因为有记载显示标准的聚乙二醇化干扰素联合利巴韦林治疗对除了HCV 1型感染患者外,SVR可以到达82%,而在1型患者只有43%[6]。Telaprevir是一种HCV NS3/4A蛋白酶抑制剂,具有可逆性,能够直接攻击HCV基因组,控制其复制[7]。研究显示,加入Telaprevir对PEG-IFNα-2a联合利巴韦林的标准治疗方案治疗CHC患者,基因1型患者RVR有所提高[8]。研究认为这类蛋白酶抑制剂如VX-950,能够快速降低CHC患者血清HCV RNA负荷[9]。联合应用PEGIFNα-2a、Telaprevir和RBV治疗CHC患者持续24周,原本对标准治疗无应答和停药后复发的基因1型患者出现了很好的疗效[10]。直接抗病毒药物(DAA)能够使基因1型CHC患者血清HCV RNA载量下降3 log10IU/ml,作用还是很明显的[11]。有学者在468例先前对标准治疗无应答的基因1型患者,给予boceprevir 800 mg,3次/d,持续治疗后发现SVR大幅提高,特别是在第一次治疗虽然无效但是血清HCV RNA下降超过2 1ogl0IU/ml的患者,其效果更为明显[12]。
研究表明,HCV基因型不同、准种的基因突变率不同、基因亚型不同,宿主肝损伤程度不同,同样治疗方案的疗效也不同。
Al-Busafi et al研究发现,抗病毒治疗能够持续使血清HCV RNA在一定的水平以下保持的时间长短会影响到SVR以及患者复发率[13]。Hansen et al研究发现CHC患者血清病毒RNA水平转阴得越早,即RVR越高,其获得SVR的机会越大[14]。在抗病毒治疗4周内血清HCV RNA水平就能够转阴的患者,94%以上能够获得SVR,而需要24周才能够实现血清HCV RNA转阴的患者,只有40%获得SVR[15]。Mangia et al在75例CHC患者,联合应用PEGIFNα-2a和利巴韦林持续治疗48周,对获得SVR者进行随访观察比较发现,获得RVR的患者,其SVR要比完全早期病毒学应答(cEVR)或部分早期病毒学应答(pEVR)患者要高,而且病情不容易复发[16]。还有临床研究结果表明不管HCV什么基因型感染者,在治疗过程中获得RVR或cEVR的患者获得SVR者要比早期获得部分早期病毒学应答(pEVR)或未获得EVR患者要高。这些结果说明,在应用聚乙二醇化干扰素-α治疗CHC患者后,越早获得病毒学应答,其最终的疗效就越好。Lawson et al研究报道认为,PEG-IFNα-2a比普通IFN-α能更敏感地诱导HCV特异性CD4+Thl细胞活性,这种反应持续的时间越长,细胞内病毒的清除就越彻底,这可能是出现治疗后血清学应答第二相的原因[17]。换句话说,对于应用聚乙二醇化干扰素-α治疗的CHC患者,在未获得早期病毒学应答者,应考虑延长疗程或转换治疗方法,以免延误了治疗。
不断增多的临床试验研究发现,48周固定疗程的抗病毒治疗对于CHC患者,特别是基因1型感染患者,可能无法获得令人满意的疗效[18]。Kumada et al观察了应用聚乙二醇化干扰素-α治疗基因1型CHC患者48周和72周的治疗效果,结果发现在获得相同RVR或EVR人群,治疗72周患者比仅治疗48周患者SVR明显提高[19]。Mogahed et al建议,对于应用聚乙二醇化干扰素-α治疗的CHC患者,在4周治疗后没有出现HCV RNA转阴的患者,应延长疗程至72周,以提高SVR,因为他们的结果表明,治疗48周和72周获得的SVR分别为26%和41%[20]。所以,对于没有获得快速病毒学应答或早期病毒学应答者,可以考虑延长治疗时间以提高SVR。
有研究认为CHC患者可能存在维生素D缺乏,而趋化因子5受体(chemokine receptor 5)可能并没有参与CHC患者肝损害作用[21,22]。因此,进一步研究CHC的发病机制,将有助于对CHC患者制定个体化的治疗方案。相信,随着DAA药物不断在我国上市应用,将使大批CHC患者最终获得最大的治疗获益[22,23]。