妊娠中晚期应用替比夫定阻断HBsAg阳性孕妇HBV母婴传播效果及对婴儿接种乙肝疫苗应答的影响*
2019-01-23叶晓林
谭 静,叶晓林,王 慧
2012年欧洲肝病学会发布的指南指出,对于血清HBsAg阳性和HBV DNA>1×106IU/ml的孕妇,可于妊娠后期服用替比夫定(LDT)、拉米夫定(LAM)和替诺夫韦(TDF)阻断围生期和宫内HBV感染。同时,2012年亚太肝病学会(APSAL)有关指南也指出,为了防止HBV母婴传播,对于血清HBV DNA>2×106IU/ml的妊娠妇女,在妊娠后期可以用LDT治疗,TDF也可作为选择之一。已知LDT和LAM同属左旋类核苷类似物(NUCs),在病毒学和组织学应答方面,LDT优于LAM[1]。同时,LDT为明确的妊娠B级药物,比LAM耐药发生率更低。本研究选择LDT治疗妊娠中晚期血清HBsAg阳性的孕妇,观察了其阻断HBV传播的效果及其对婴儿接种乙肝疫苗应答的影响,现将研究结果报道如下。
1 资料与方法
1.1 一般资料 2013年7月~2015年12月我院诊治的血清HBsAg阳性的妊娠中晚期孕妇及其新生儿各100例,纳入孕妇在妊娠期未使用过其他C级以上药物,排除妊娠期合并丙型肝炎或其他感染性疾病、妊娠期合并高血压、流产或分娩死胎人群。孕妇知情本研究的所有内容并签署知情同意书。
1.2 治疗与免疫接种 在41例孕妇,自妊娠28周开始给予替比夫定(北京诺华制药有限公司,批准文号:H20070029)600 mg口服,1 次 /d,直至分娩后停止服药;另59例未接受抗病毒治疗。按我国“0-1-6”方案给予所有新生儿重组酵母乙肝疫苗10 μg全程接种,同时在出生24 h内注射人乙型肝炎免疫球蛋白(哈尔滨派斯菲科生物制药有限公司,国药准字S19983012)200 IU。
1.3 检测指标 采用电化学发光法(ECLIA)定量检测血清HBsAg和HBeAg水平;采用FQ-PCR法检测血清HBV DNA载量。血清HBV DNA载量<1×103copies/ml为阴性,1×103copies/ml≤HBV DNA载量<1×106copies/ml为低载量组,血清HBV DNA载量≥1×106copies/ml为高载量组。采用ELISA法检测血清IFN-γ和和IL-10水平(试剂购自合肥锐捷生物科技股份有限公司)。
1.4 判定标准 HBV宫内传播:新生儿出生24 h内,即在主、被动免疫接种前,静脉血HBsAg阳性和/或HBV DNA>1×103copies/ml者诊断为HBV宫内传播;乙肝疫苗无或弱应答:按标准全程接种乙肝疫苗后,血清抗-HBs达不到保护水平,即<10 mIU/ml为无应答,抗体水平在10~100 mIU/ml者为弱应答,≥100 mIU/ml者为强应答。
1.5 统计学分析 应用SAS 92软件和SPSS 20.0软件进行数据分析,对正态分布的计量资料以±s表示,采用t检验,计数资料的比较采用x2检验,采用非条件Logtistic回归模型分析影响应答的因素,P<0.05表示差异有统计学意义。
2 结果
2.1 两组生化、血清和病毒学指标变化的比较 抗病毒组分娩后血清HBV DNA载量水平显著降低(P<0.05),而未抗病毒组未见明显变化(P>0.05,表1。
表1 两组病毒、血清和生化学指标(±s)比较

表1 两组病毒、血清和生化学指标(±s)比较
与未抗病毒组比,①P<0.05
例数 HBV DNA(lg IU/ml) HBeAg(s/co) HBsAg(lgIU/ml) ALT(U/L)抗病毒组 抗病毒前 41 7.6±0.3 1268.7±248.6 4.3±0.4 37.2±3.1分娩后 41 2.0±1.3① 1268.9±121.5 4.3±0.5 38.2±2.9未抗病毒组 入组时 59 7.5±0.4 1289.1±329.7 4.3±0.5 37.1±4.5分娩后 59 7.1±1.6 1256.9±267.5 4.2±1.0 37.6±4.1
2.2 两组围生期指标的比较 两组剖宫产、早产、产后出血和新生儿窒息发生率比较无统计学差异(P>0.05)。在出生后随访1年,在41例抗病毒组孕妇分娩的婴儿中无一例血清HBsAg呈阳性,而在59例未抗病毒组婴儿中6例(10.2%)血清HBsAg阳性,组间差异有统计学意义(x2=4.436,P=0.035)。
2.3 影响婴儿对乙肝疫苗接种应答的因素分析 在婴儿(12.3±1.0)月龄随访,发现对乙肝疫苗强应答者80例,无/弱应答者20例。是否抗病毒、血清HbeAg是否阳性和是否发生HBV宫内感染孕妇分娩的婴儿对乙肝疫苗接种应答强弱有显著差异(P<0.05,表2);进一步地调整混杂因素,经Logistic多因素分析发现,孕妇是否抗病毒治疗为婴儿对乙肝疫苗接种应答的独立影响因素(RR为0.121,95%CI为0.018~0.894,P<0.05)。

表2 影响婴儿对疫苗接种应答的单因素分析(%)
2.4 血清不同IFN-γ和IL-10水平幼儿对乙肝疫苗接种应答的差异比较 以血清IFN-γ水平为60.25 pg/ml和IL-10为88.24 pg/ml为界,发现高水平组婴儿对乙肝疫苗强应答发生率高(P<0.05,表3);以婴儿对乙肝疫苗免疫应答为因变量,在调整混杂因素后发现,新生儿血清IFN-γ和IL-10高水平是婴儿对乙肝疫苗接种强应答的保护因素;80例强应答组血清IFN-γ和IL-10水平分别为(68.5±6.2)pg/ml和(98.2±7.8)pg/ml,显著高于弱应答组【分别为(54.2±4.0)pg/ml和(75.2±6.9)pg/ml,P<0.05】。
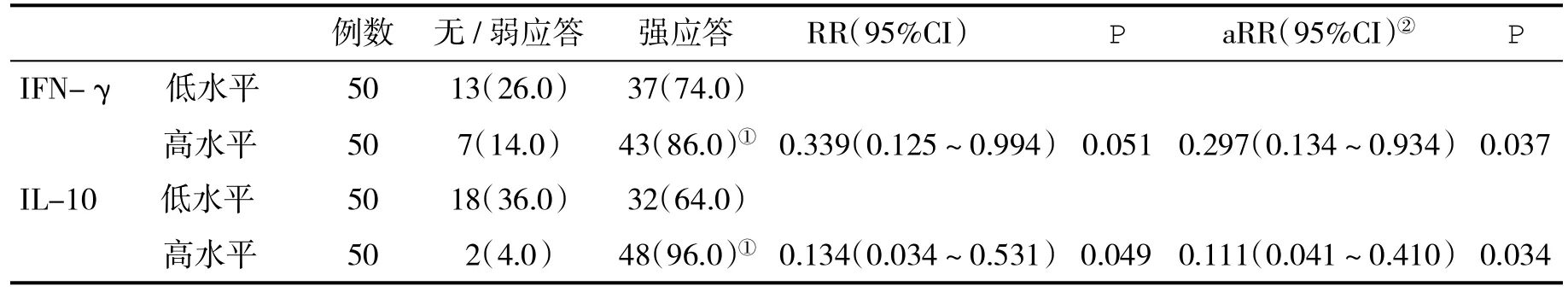
表3 不同血清IFN-γ和IL-10水平婴儿对乙肝疫苗应答强度(%)比较
3 讨论
针对HBV抗原透过胎盘的研究发现,还存在一些有效性和安全性的问题[2~5]。有研究发现,孕妇血清HbeAg水平显著高于HBsAg[6~8],即血清HbsAg水平可能较低,可能系孕妇处于妊娠这样一个特殊的生理期,机体会自动趋向于更强的免疫耐受来保护体内的胎儿免受病毒的感染。同时HBeAg的分子量显著低于HbsAg,也提示抗原颗粒大小也会影响胎盘透过率[9~11]。另一研究证明,因为HBV cccDNA是HBV复制的原始模板,尽管服用抗病毒药物,孕妇体内HBV cccDNA下降也很慢,由于其未被彻底地清除[12~14],所以导致血清HBsAg和HBeAg持续合成,水平居高不下。HBeAg可以与血清蛋白结合而进入血液[15]。考虑到HBV通过胎盘屏障的机制本身与特异性受体、受体种类、数量和易感性以及免疫复合物形成等多重因素有关,阻断HBV母婴传播的研究还需深入。同时,由于本研究用药时间短,孕妇的免疫状态可能不同,并且本研究纳入样本量有限,因此仅借此结果推断母婴传播的发生机制还较难。
研究发现,T细胞免疫反应弱是导致HBV持续复制的原因之一。因此,本研究通过检测血清Th1和Th2型细胞因子水平来探讨婴儿对乙肝疫苗接种应答的问题,因为IFN-γ由Th1细胞产生,可以促进NK细胞和单核巨噬细胞吞噬病毒颗粒。IL-10由Th2细胞产生,可以促进B细胞增殖,分化并产生lgG2a抗体,从而限制和终止炎症反应。本研究结果提示,母亲在妊娠中晚期服用替比夫定及新生儿血清IFN-γ和IL-10高水平是婴儿对乙肝疫苗接种应答的保护性因素。由于新生儿和婴儿期,进行多次血清学检测的困难,可能导致观察研究难以按计划进行。研究新生儿对免疫接种应答的影响因素,将有助于早期发现可能应答差的婴儿而给予相应的干预和补种措施,是非常重要的课题。
本研究结果表明,在妊娠中晚期服用替比夫定,在分娩时检测发现,血清病毒载量确实已经阴转,提示孕妇通过服用替比夫定可以通过抑制病毒复制,而降低传播病毒的风险。有学者提出,服用替比夫定会导致HBsAg阳性孕妇心肌酶升高,这也是一个应该注意和密切随访的问题。