肺鳞状细胞癌合并相邻支气管肺空洞1例及文献回顾
2019-01-23孔田田岳小山秦玉娇
孔田田,岳小山,秦玉娇,盛 辉
(吉林大学第一医院二部 呼吸科,吉林 长春130031)
肺癌占所有新癌症病例的12.4%[1],是全球癌症死亡的主要原因。肺空洞一般定义为肺实变、肿块或结节内的含气空腔[2]。癌性空洞为肺空洞性疾病的常见病因,肺空洞的形成在肺鳞状细胞癌(SCC)中最为常见,并且多提示预后不佳[3]。在一项对244例肺部恶性疾病患者的调查中,27例患者(11%)为空洞性肺癌。 其中26例为原发性肺癌,21例为SCC[4]。引起肺空洞的其他原因包括结核分枝杆菌感染、曲霉菌病和肺脓肿以及较罕见的疾病等。
1 临床资料
患者男性,77岁,因咳嗽、咳痰伴右侧胸痛、呼吸困难2个月,发热伴咯血3天入院。查体:T 36.6℃,P 86次/分,R 18次/分,BP 120 mmHg/75 mmHg,无颈静脉怒张;胸廓对称,双肺呼吸音粗,未闻及干湿啰音。既往糖尿病史(未治疗)和吸烟史30余年(未戒),否认结核病史或药物使用史,否认癌症家族史。在3个月内体重下降约5 kg。
实验室检查:血常规:白细胞(WBC)计数为12×109/L,
中性粒细胞百分比(NE%)为76%,C反应蛋白(CRP)水平为232 mg/L,肺癌标志物:细胞角蛋白19片段(CYPRA)21-1 6.44 ng/L(正常范围0-3.3 ng/ ml)。痰培养和血培养病原微生物均为阴性的。胸部计算机断层扫描(CT)显示右肺上叶、中叶支气管壁厚,右肺中间段及下叶支气管改变;双肺炎症,右肺下叶显著,考虑合并肺脓肿;右肺门及纵隔淋巴结肿大;双侧胸腔积液(图 1)。支气管镜检查显示右肺中叶支气管壁显著增厚,右中肺叶支气管起源处明显狭窄。另外,右肺下叶支气管的开口尚通畅,可见坏死肉芽组织,其内可见一巨大空腔,有明显的坏死性肺组织且周围环绕褐色坏死物质(图2)。支气管镜下于右肺中叶及下叶开口处取活检,同时对右肺下叶行支气管肺泡灌洗。支气管肺泡灌洗液的培养和细胞学检查均为阴性。活检标本的组织学分析提示右肺中叶支气管鳞状细胞癌(SCC)和右肺下叶支气管炎性反应(图3和4)。 头部CT扫描和腹部超声检查未见明显异常。根据这些发现,患者被诊断为肺鳞状细胞癌(T2N2Mx),气管镜下肺空洞表现较罕见,肺空洞病因无法确定。
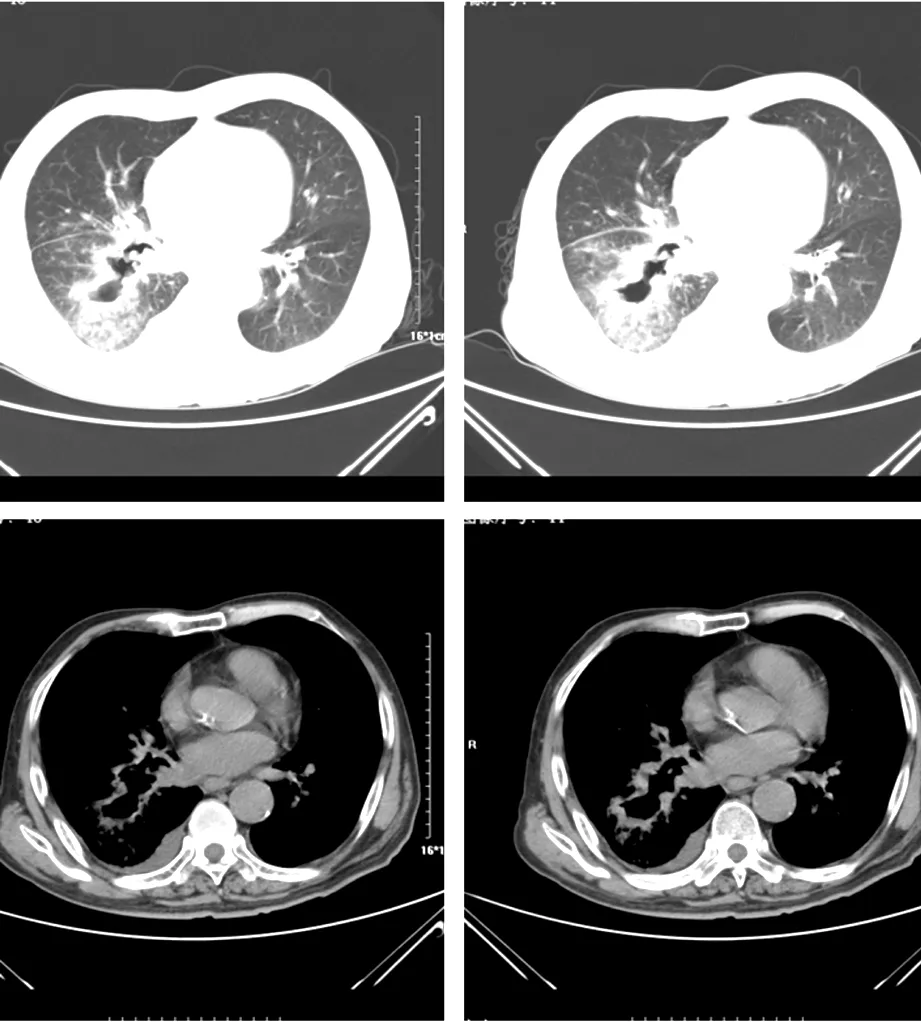
图1 肺CT影像
肺部CT显示右肺上叶、中叶支气管壁厚,右肺中间段及下叶支气管改变;双肺炎症,右肺下叶显著,考虑合并肺脓肿;右肺门及纵隔淋巴结肿大;双侧胸腔积液。

图2 支气管镜下表现
支气管镜检查显示右肺下叶支气管的开口尚通畅,可见坏死肉芽组织,其内可见一巨大空腔,有明显的坏死性肺组织且周围环绕褐色坏死物质。
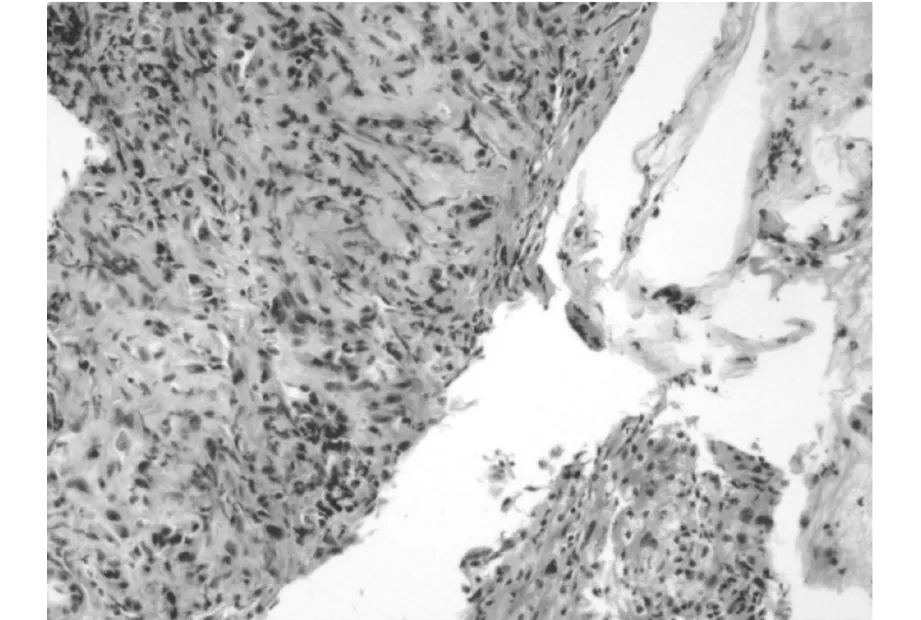
图3 HE染色×100
右肺下叶急慢性炎症,局部纤维血管组织增生,炎症渗出及坏死。
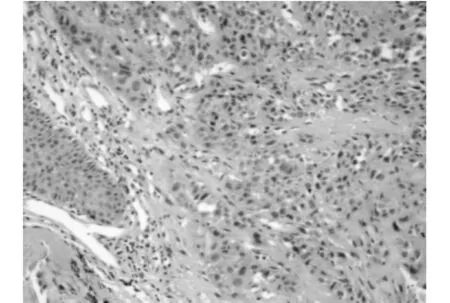
图4 HE染色×100
右肺中叶中分化鳞状细胞癌。 免疫组化染色:CK5/6(+),P63(+),TTF-1(-),NapsinA(-),Syn(-)。
2 讨论
引起肺空洞性疾病的病理机制包括化脓性坏死,干酪性坏死,缺血性坏死,肺结构囊性扩张或由囊性结构引起的肺组织移位等,它们由多种病因造成,包括肿瘤,感染性疾病(例如结核分枝杆菌、肺脓肿、曲霉病),风湿性疾病(如韦格纳肉芽肿病),肺栓塞和闭塞性细支气管炎等[5]。因此,对于肺空洞病理过程和病因的鉴别诊断对指导治疗决策至关重要。
本文中,我们介绍一个以胸痛、咯血和发热为主诉入院并最初被诊断为肺脓肿的案例。 而在随后的支气管镜检查证实,右肺中叶为鳞状细胞癌,右下叶有空洞病变。据了解,公布的肺癌并发的独特非恶性支气管内肺腔的报道很少。 该病例的诊断具有挑战性,肺空腔的确切病因无法确定。 虽然没有证实,但我们认为最可能的病因是恶性肿瘤或结核分枝杆菌,曲霉病或细菌感染。
通常伴有恶性病因的肺空腔以三种方式进展:①由于肿瘤破裂可能引起空洞性坏死。②肿瘤远端的肺实质感染或破裂。③由携带微生物的支气管栓塞产生而继发性癌性脓肿。 有证据表明,大部分空洞肺癌是鳞状细胞来源。由于空洞型肺癌症状与其他慢性呼吸道病症类似,导致早期对于原发性肺癌诊断困难[6]。 伴有空洞型鳞状细胞癌(cSLC)的患者可能最初的临床表现仅仅提示感染,从而易导致误诊,因此我们建议在患有肺空洞的患者中需警惕恶性可能。
结核分枝杆菌感染更容易形成空洞,因为它提供了生物体繁殖的机会,而恶性肿瘤患者发生活动性结核的风险大大增加[7]。最近对接受非小细胞肺癌切除术的患者进行的一项研究显示17例(1.3%)患者并发结核;其中11例患有肺鳞状细胞癌(SCC),6例患有腺癌[8]。肺癌合并活动性结核的患者通常会出现特征性临床症状,包括发热、中毒现象、呼吸困难和咯血等。本文患者痰和支气管肺泡灌洗液的细菌学分析提示结核分枝杆菌阴性,但由于结核分枝杆菌培养的生长速度缓慢,因此我们不能完全排除结核分枝杆菌病感染的而未被我们发现的可能。
肺癌患者往往合并免疫缺陷,因此会增加真菌感染的风险。曲霉病是一种少见的肺部疾病,包括侵入性肺曲霉病(IPA),慢性坏死性曲霉病(CNA)和过敏性支气管肺曲霉病(ABPA)。 一些研究报道,在接受高剂量化疗的免疫缺陷患者的肺腔中,曲霉病和肺癌共存[9,10]。 区分恶性空洞和曲霉菌较困难,因为这两种情况在胸部CT表现上存在重叠。 本文中,痰、支气管肺泡灌洗液和组织活检的细菌学分析对曲霉病为阴性。
肿瘤患者更容易增加细菌感染的风险,原因包括肿瘤阻塞(最常见),破坏自然解剖屏障(皮肤或黏膜)以及与治疗相关因素(化疗、放疗、侵入性检查、手术)等。阻塞性肺炎在肺癌患者中最常见,约40-50%肺癌患者最初表现为阻塞性肺炎,而大约10%-15%的阻塞性肺炎可发展为肺脓肿等严重并发症[11]。CT检查一般难以区分伴有恶性病因的肺脓肿和肺空洞,临床中极易将肺脓肿误诊为腺癌。在目前的情况下,痰液和支气管肺泡灌洗液的细菌学分析对于细菌感染是阴性的。 然而,从组织学分析的活检标本中下叶支气管提示为炎性反应。 因此,该患者的肺空洞可能是由肺脓肿引起的。
空洞性肺疾病的临床表现是非特异性的,主要包括呼吸困难、咳嗽、咯血、胸痛和发热。在肿瘤早期准确的诊断病变对于患者预后至关重要。 胸部X线和CT常用于检测肺部疾病。CT对于诊断肺空洞性病变是一种具有重要价值,空洞的形态、位置、分布和其他影像学表现可提示潜在的疾病[12]。具体而言,恶性和非恶性病因之间的区别是诊断空洞性肺病的重要因素。 一些证据表明,CT下,肺癌相关肺腔通常壁厚≥4 mm,而囊肿等良性病变的壁厚可能≤4 mm[13]。 然而,应该谨慎使用壁厚来区分肺腔的病因,因为恶性肺空洞和曲霉菌及感染性病因之间的壁厚是重叠的。 因此推荐对患者全面的病理和微生物分析来诊断与肺空洞相关的病变并指导治疗。
由于空洞性肺癌的临床表现缺乏特异性以及CT扫描判断的主观性,可能导致早期对空洞性肺癌的误诊。鉴别肺空洞病因很重要,因为这可以指导治疗和预后。在本文案例中,患者右肺中叶被诊断为肺鳞状细胞癌,而右肺下叶为空洞性改变。患者痰液和支气管肺泡灌洗液培养以及脱落细胞均为阴性,且未检出结核分枝杆菌,结合患者症状及辅助检查考虑该病例肺部空洞与炎症相关。肿瘤生长相邻气管的空洞改变较少见,这种少见病例应该提高临床医生对非恶性空洞性肺部病变合并的肺恶性疾病的认识,以避免误诊而延误治疗。
