HPLC同时测定生地黄汤颗粒中11种指标性成分的含量△
2019-01-16刘基李佳程江雪邹俊波郭东艳
刘基,李佳,程江雪,2,邹俊波,2,郭东艳,2*
(1.陕西中医药大学 药学院,陕西 咸阳 712046;2.陕西省中药基础与新药研究重点实验室,陕西 咸阳 712046)
生地黄汤为唐代孙思邈《千金方》中收载方,由生地黄、大黄组成,具有滋阴凉血、化瘀止血的功能,主要用于肾阴亏虚、瘀血阻滞引起的吐、衄血百治不愈及崩漏。生地黄汤颗粒为生地黄汤经提取浓缩后制成的颗粒剂。方中生地黄为主药,味甘,寒,入心、肝、肾经,具有清热凉血、养阴生津之功能。《药性论》曰其“通血脉,破血,通利月水闭绝……捣敷心腹,能消瘀血。”《开宝本草》云生地黄“破恶血……通血脉,主妇人崩中血不止及产后血上薄心闷绝,伤身胎动下血,瘀血,留血,衄血,吐血。”《本草经疏》称地黄为“补肾家之要药,益阴血之上品”,是中药复方用药频率较高的药味之一[1]。生地黄主要含有苷类、糖类及氨基酸类等成分,其中环烯醚萜苷类成分和苯乙醇苷类成分是地黄中的主要成分,同时也是地黄发挥药效的主要物质基础。目前已分离出的环烯醚萜苷类化合物中,梓醇含量最高,此外尚含有桃叶珊瑚苷、地黄苷A、地黄苷D等[2-6]。苯乙醇苷类成分主要以毛蕊花糖苷为主[7]。大黄主要含有蒽醌、鞣质等成分[8],其中蒽醌苷元是大黄活血化瘀主要物质基础[9]。目前关于生地黄、大黄单味药的含量测定方法较多[10-13],但是有关生地黄汤或生地黄大黄配伍的中药复方中相关指标性成分的含量测定未见报道。本实验拟采用HPLC法对生地黄汤颗粒中的主要成分进行含量测定方法学考察,以期建立同时测定11种主要指标性成分含量的方法,为生地黄汤颗粒的质量评价与控制提供依据,同时也为中药复方中含有生地黄大黄药对的制剂质量评价提供参考。
1 仪器与材料
1.1 仪器
Agilent 1260 Infinity高效液相色谱仪(G1311C型四元泵、G1329B型进样器、G4212B型二极管阵列检测器、Open LAB工作站);电子天平[万分之一,梅特勒-托利多仪器(上海)有限公司];SartoriusMC 电子天平(十万分之一)。
1.2 试药
生地黄饮片购买于宝鸡汉方国药饮片有限责任公司,经陕西中医药大学高级实验师王继涛鉴定为玄参科(Scrophulariaceae)植物地黄RehmanniaglutinosaLibosch.的块根;大黄饮片购于兰州旭康药业有限公司,经陕西中医药大学高级实验师王继涛鉴定为廖科(Polygonaceae)植物掌叶大黄RheumpalmatumL.的干燥根及根茎;生地黄汤颗粒实验室自制(批号分别为20171001、20171201、20180301)。
梓醇(批号:110808-200508)、没食子酸(批号:110831-200302)、芦荟大黄素(批号:110795-200806)、大黄酸(批号:110757-200716)、大黄素(批号:110756-201010)、大黄酚(批号:110796-200310)、大黄素甲醚(批号:110758-200611)对照品购于中国食品药品检定研究院;桃叶珊瑚苷(批号:1512102)、地黄苷A(批号:16051725)、地黄苷D(批号:150401)、毛蕊花糖苷(批号:150402)对照品,购于成都普菲德生物技术有限公司;水为娃哈哈纯净水;乙腈为fisher色谱纯;其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Accurasil-C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈(C)-0.1%磷酸水(D)梯度洗脱(洗脱程序见表1),检测波长:210 nm;柱温:30 ℃;流速:1 mL·min-1;进样量:10 μL。理论塔板数以梓醇计不低于3000。对照品及供试品的色谱图见图1。
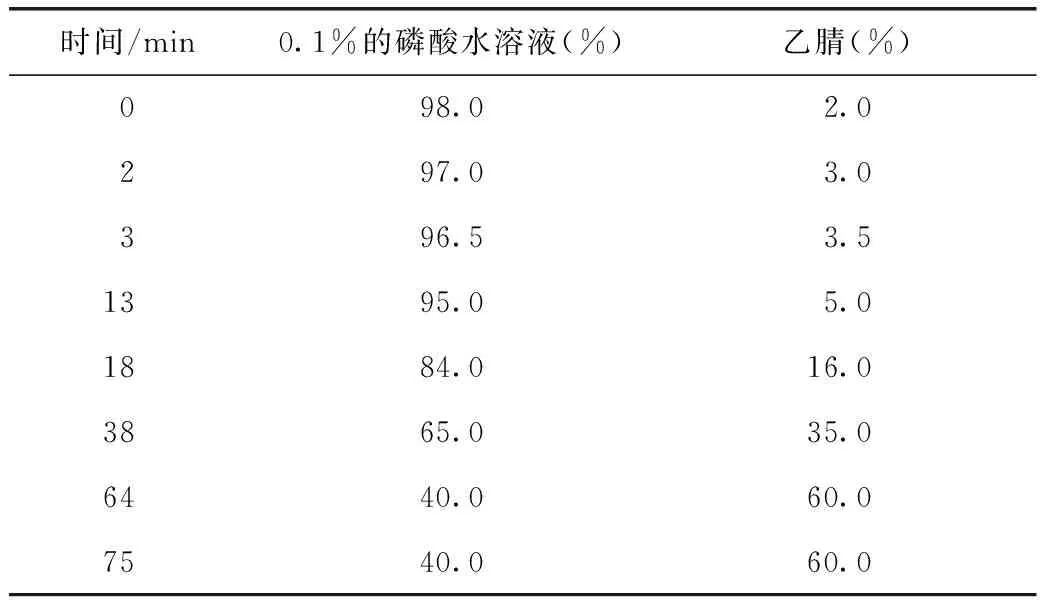
表1 梯度洗脱程序
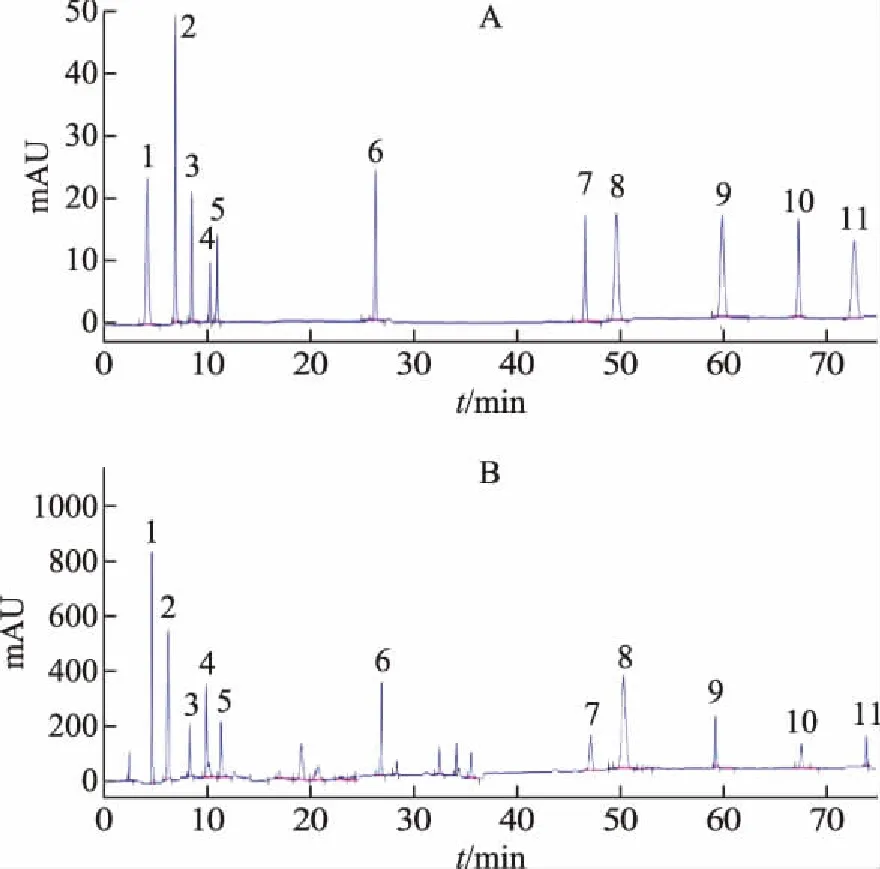
注:A.混合对照品;B.供试品;1.梓醇;2.没食子酸;3.桃叶珊瑚苷;4.地黄苷D;5.地黄苷A;6.毛蕊花糖苷;7.芦荟大黄素;8.大黄酸;9.大黄素;10.大黄酚;11.大黄素甲醚。图1 对照品及样品HPLC图
2.2 溶液及样品的制备
2.2.1 对照品溶液 精密称取梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚适量,色谱甲醇溶解,分别制成质量浓度分别为110、55、198、132、220、176、99、99、98、98、99 μg·mL-1的储备液。
2.2.2 混合对照品溶液 分别精密移取梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚各0.1 mL至量瓶中,制成质量浓度分别为10.0、5.0、18、12.0、20.0、16.0、9.0、9.0、8.9、8.9、9.0 μg·mL-1大黄素甲醚的混合对照品溶液。
2.2.3 生地黄汤颗粒 按照处方比例称取生地黄600 g,大黄20 g,加10倍量20%乙醇浸渍提取36 h,滤过,滤液减压浓缩、干燥(60 ℃),粉碎,80%乙醇制粒,即得生地黄汤颗粒剂[14],批号分别为:20171001、20171201、20180301。
2.2.4 供试品溶液 称取生地黄汤颗粒约2.0 g,研细,精密称定,置25 mL容量瓶中,加入色谱甲醇20 mL,精密称重,超声30 min,放至室温,用色谱甲醇补足重量,摇匀并滤过,取续滤液,0.22 μm微孔滤膜滤过,即得。
2.3 方法学考察
2.3.1 线性关系考察 用移液器分别精密吸取2.2.2项下混合对照品溶液0.063、0.125、0.25、0.50、1.00、2.00 mL,置于2 mL量瓶中,色谱甲醇稀释至刻度,摇匀,得6个系列浓度的混合对照品溶液。在2.1色谱条件下分别进样10 μL,以各成分的质量浓度X(μg·mL-1)分别对相应峰面积Y进行线性回归,得相应的回归方程和相关系数(见表2),结果表明,在一定质量浓度范围内,各成分均有良好的线性关系。
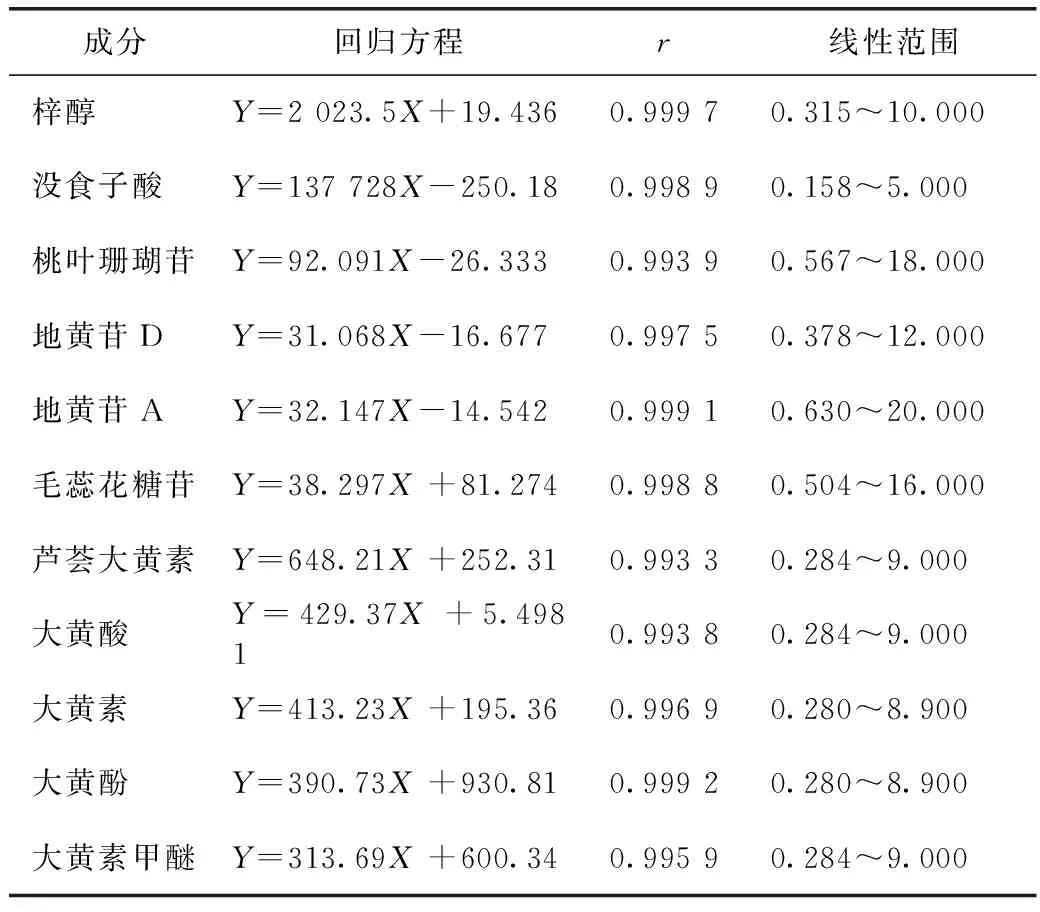
表2 11种成分的线性回归方程及线性范围 μg·mL-1
2.3.2 精密度试验 分别精密移取2.2.2项下的混合对照品溶液适量,按照2.1项下色谱条件重复进样6次,每次进样10 μL,记录峰面积。梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积积分值的RSD分别为1.37%、0.98%、1.16%、1.21%、1.05%、0.99%、1.16%、1.15%、1.02%、1.00%、1.03%,均符合要求,表明该仪器的精密度良好。
2.3.3 稳定性试验 取2.2.4项下供试溶液,分别于0、2、4、8、12、24 h按2.1项下色谱条件进样10 μL,记录峰面积。梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰峰面积积分值的RSD分别为1.64%、1.24%、1.31%、1.00%、1.05%、0.98%、1.20%、1.09%、0.98%、1.06%、1.12%,均符合要求,表明供试品溶液在24 h内稳定性良好。
2.3.4 重复性试验 取2.2.3项下生地黄汤颗粒6份(批号:20171001),分别按照2.2.4项下供试品溶液制备方法制备,依照2.1项下色谱条件进样10 μL,记录峰面积,外标两点法计算各成分含量及RSD。结果生地黄汤中梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的平均含量分别为4.346 3、1.742 0×10-2、0.102 1、1.487 2、0.585 5、0.423 1、0.342 6×10-2、1.113 8×10-2、0.414 8×10-2、0.241 5×10-2、0.050 8×10-2mg·g-1;含量的RSD分别为1.69%、1.34%、2.15%、1.00%、1.21%、1.56%、2.27%、1.74%、1.35%、1.65%、1.16%,表明重复性良好。
2.3.5 加样回收率试验 精密称取已知含量的同一批生地黄汤颗粒6份(批号:20171001),分别加入适量梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚及大黄素甲醚对照品。按照2.2.4项下方法制备供试液,依照2.1项下的色谱条件,分别进样10 μL,记录峰面积,外标两点法计算含量及加样回收率。结果梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的平均回收率分别为98.73%、97.09%、96.43%、97.36%、97.87%、96.34%、96.67%、96.17%、97.04%、97.97%、97.11%;RSD分别为0.97%、1.35%、0.72%、1.47%、0.98%、0.64%、1.29%、1.78%、1.41%、0.77%、1.04%。说明该方法准确度良好。结果见表3。
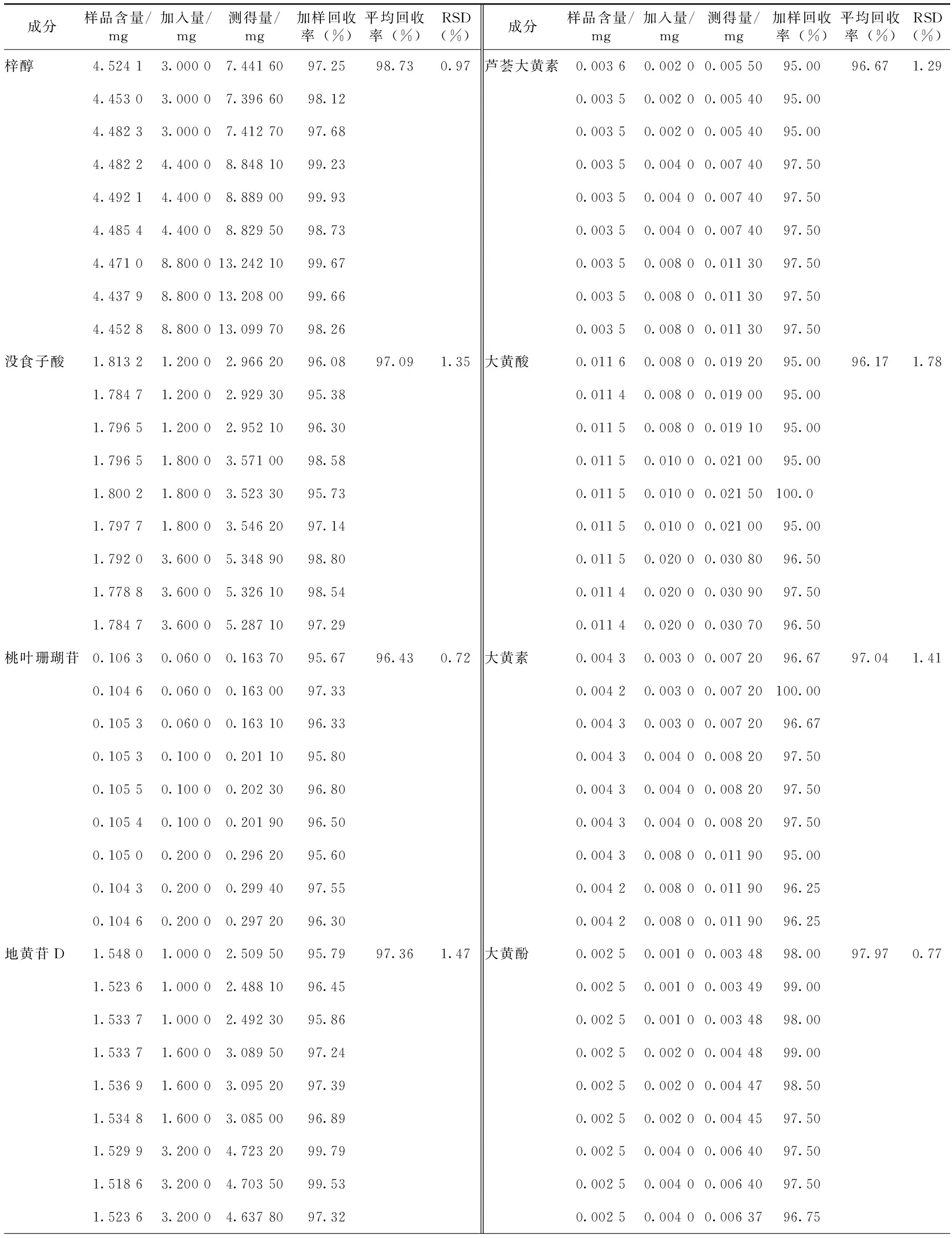
表3 加样回收率试验结果(n=9)
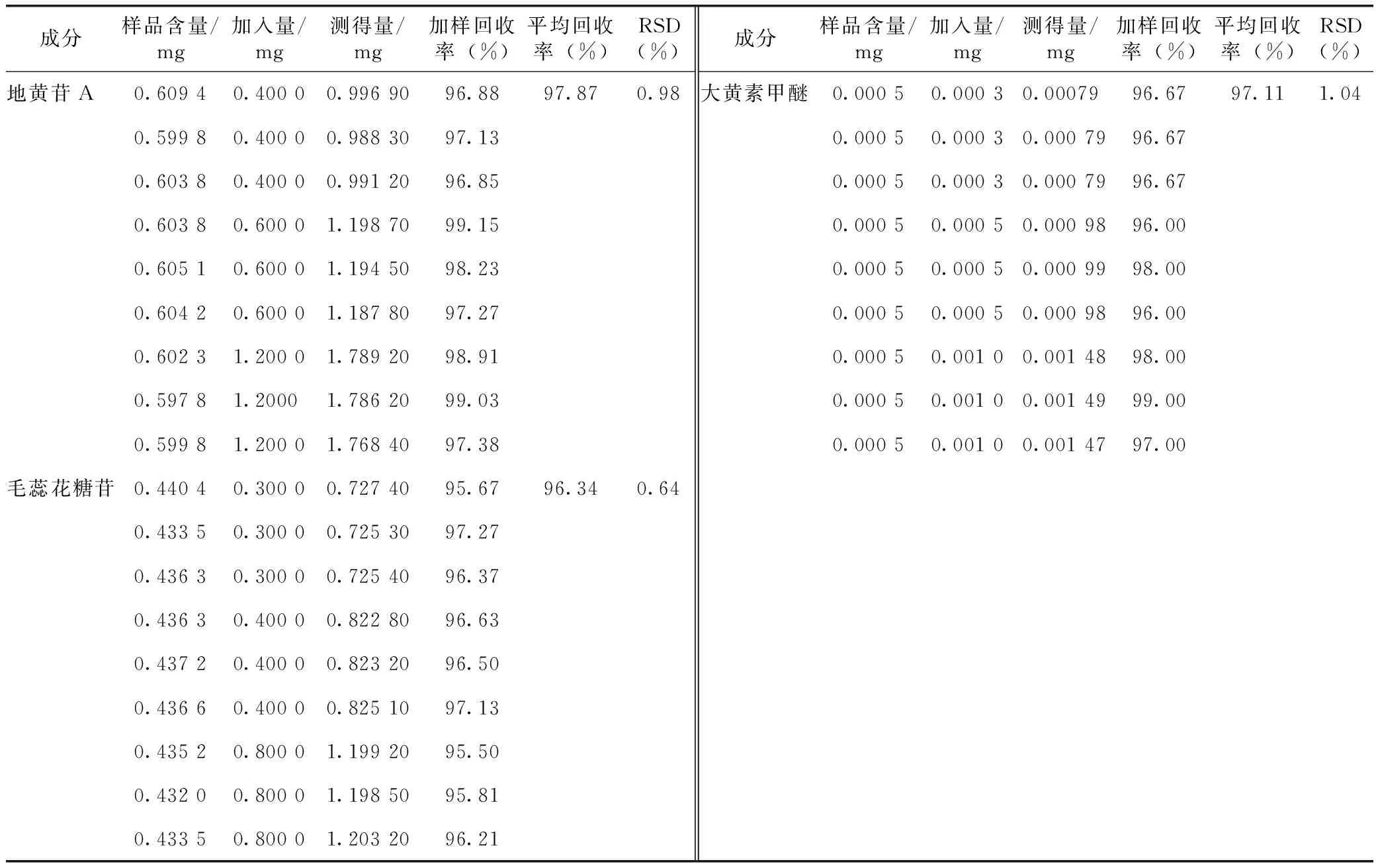
续表3
2.3.6 样品含量测定 取3批生地黄汤颗粒,按2.2.4项下方法制成供试品溶液,依2.1项下色谱条件进样10 μL,记录峰面积。按外标两点法计算样品中梓醇、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、没食子酸、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的含量,结果见表4。
3 讨论
《中华人民共和国药典》2015年版(一部)中地黄项下仅对梓醇和毛蕊花糖苷进行测定[15],而且采用了两种测定方法,较为繁琐。地黄中主要含有环烯醚萜苷及苯乙醇苷,而且这两大类成分也是其主要活性成分,中华人民共和国药典中仅对梓醇及毛蕊花糖苷进行含量测定,难以全面反映该饮片的质量。因此对主要活性成分进行含量测定方法学考察,确定含量测定方法,对于全面有效控制制剂的质量具有重要的意义。
波长的选择:在进行含量测定方法学考察时,发现梓醇、桃叶珊瑚苷、地黄苷A、地黄苷D在203 nm处有末端吸收,毛蕊花糖苷最大吸收在334 nm处,大黄中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚在252 nm处有强吸收峰[16-18]。经过在不同波长下及转换波长多次实验,结果发现,梓醇在252 nm及334 nm响应值均较小,毛蕊花糖苷及大黄各成分在210 nm处有较高响应值。而采用转化波长进行测定时基线波动较大。综合考虑各成分在210 nm波长下,均能得到较好的响应值,灵敏度较好,杂质峰干扰较小,同时也避免了更换检测波长引起的基线漂移,最终确定210 nm作为检测波长。

表4 生地黄汤颗粒中11种成分含量测定结果(n=3)mg·g-1
流动相的确定:依据待测11种成分的理化性质及色谱行为,实验过程对不同比例的甲醇-0.1%磷酸溶液及乙腈-0.1%磷酸溶液进行了考察,结果表明,以甲醇-0.1%磷酸溶液进行梯度洗脱,系统压力较高,以乙腈-0.1%磷酸水进行梯度洗脱,检测波长为210 nm,柱温30 ℃,流速1 mL·min-1时,样品中各成分分离度良好,峰形尖锐对称,色谱图基线平稳,因此最终确定以乙腈-0.1%磷酸水溶液系统作为流动相,进行梯度洗脱。
本实验建立了生地黄汤颗粒中11种指标成分梓醇、没食子酸、桃叶珊瑚苷、地黄苷D、地黄苷A、毛蕊花糖苷、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的含量测定方法,方法学考察结果表明,该方法的精密度、稳定性、重复性、加样回收率均符合要求。而且操作简单、对仪器设备要求不高,重复性好,能够同时进行11种成分的含量测定,简化了样品制备方法,节约分析时间,可用于生地黄汤颗粒的质量控制,同时也为其他含地黄大黄药对的中药复方制剂质量控制提供了参考。
