药用植物丹参中丹参酮IIA的提取分离工艺研究
2019-01-14邓昌平曹建国开国银
张 毅, 邓昌平, 时 敏, 付 蓉, 王 瑶, 曹建国, 开国银,*
(1.上海师范大学 生命科学学院 植物种质资源开发协同创新中心,上海 200234;2.浙江中医药大学 药学院,浙江 杭州 311402)
0 引 言
丹参(Salviamiltiorrhiza)为唇形科(Labiatae)鼠尾草属(Salvia)多年生草本植物,因其根色红,形状似参而得名“丹参”[1].丹参有效成分主要包括水溶性的酚酸类化合物和脂溶性的丹参酮类化合物[1].丹参酮类化合物包括丹参酮I、丹参酮IIA、丹参酮IIB、隐丹参酮、二氢丹参酮等[2].丹酚酸类化合物主要包括丹酚酸A、丹酚酸B 、丹酚酸C、咖啡酸、迷迭香酸、紫草酸等[3].丹参酮IIA是丹参中含量较多且具有广泛药理活性的化合物.近年来研究表明,丹参酮IIA可以抑制包括乳腺癌、肺癌、肝癌等多种肿瘤细胞株的生长[4-7],对提高心肌耐缺氧的能力,保护红细胞膜,修复心肌等有重要作用[8-10].此外它还可有效改善微循环障碍,降低冠心病、脑缺血中风及心肌梗塞病人的全血和血浆黏度[11-12],是临床上广泛应用于治疗心血管病的中成药制剂[13-15],同时也应用到保健品及化妆品行业[16-17].
聚酰胺是由酰胺聚合而成的一类高分子物质,作为一种高性能的塑料,被广泛应用于各类工程中[18],近年来也被大量应用于天然产物的分离中.聚酰胺吸附层析法主要原理为“氢键吸附”,即由于聚酰胺分子内有很多酰胺键可与酚羟基(黄酮体、蒽醌等) 形成氢键,能对酚类化合物产生吸附作用.其中,王怡红等[19]首先使用聚酰胺层析的方法分离出了银杏叶中的黄酮类物质.林春梅等[20]使用聚酰胺层析柱纯化出牛蒡的总黄酮.张伟丰等[21]使用聚酰胺层析柱对阿魏酸多糖进行脱色.根据形成氢键的基团(羟基、羧基等)数目,含羟基越多的物质,越容易被吸附.
丹参酮IIA在丹参中的含量较低[22],目前已有的研究中采用超临界CO2萃取法[23]、硅胶柱层析法[24]、高速逆流法[25]、大孔树脂分离技术[26]等方法来提取分离出丹参酮IIA单体.但是采用上述常规方法提取分离丹参酮IIA效率低,成本较高,并且提取纯度也有待提高.本研究采用乙醇作为提取溶剂,配合聚酰胺柱层析的方法,并采用不同浓度的乙醇作为洗脱剂分离丹参酮IIA.所分离的丹参酮IIA纯度达93%以上,具有提取率和提取纯度高,安全可靠,且溶剂可以重复利用,避免浪费等优点,是一种高效的丹参酮IIA分离提纯方法.
1 材料与方法
1.1 实验材料
丹参根部粗品(市售);石油醚(分析纯)、乙醇(分析纯)、乙酸乙酯(分析纯)、二氯甲烷(分析纯)、甲醇(分析纯),上海润捷化学有限公司;磷钼酸(分析纯),国药集团化学试剂有限公司;乙腈(色谱纯)、聚酰胺凝胶,上海阿拉丁生化科技股份有限公司;氘代氯仿,美国CIL公司;薄层层析硅胶板,烟台江友硅胶开发有限公司.
仪器设备:落地式连续粉碎机(DFY-500),上海鼎广仪器有限公司;循环水式多用真空泵[SHZ-D(Ⅲ)],上海科升仪器有限公司;旋转蒸发仪(RE52-99),上海亚荣生化仪器厂;低温冷却水循环泵(CCA-20),巩义市予华仪器有限责任公司;电热恒温鼓风干燥箱(DHG-9140A),上海海向仪器设备厂;纯水仪(Master-S30),上海和泰仪器有限公司;紫外分析仪(ZF-1),上海骥辉科学分析仪器有限公司;电子天平(FA1204B),上海天美天平仪器有限公司;高效液相色谱仪(1260 Infinity I),Agilent Technologies;核磁共振谱仪(Bruker AVANCE III 500 MHz),德国Bruker公司;吹风机(HP8220),飞利浦(中国)投资有限公司;玻璃毛细点样管(直径0.3 mm,长度100 mm),上海积裕实验室设备有限公司.
1.2 实验方法
1.2.1 丹参有效成分的提取
将10 kg丹参干燥根部原料洗净后自然晾干,粉碎;加入2~3倍体积的95%(体积分数)乙醇浸泡7 d,期间每间隔12 h搅拌一次;将提取液通过砂芯漏斗过滤,取滤液用旋转蒸发仪蒸出溶剂,得到浸膏;将溶剂再次倒回材料中进行浸泡提取,重复3次.最后合并得到丹参提取总浸膏,备用.
1.2.2 丹参酮类物质的粗提取
将提取所得的乙醇提取浸膏倒入分液漏斗中,加入15倍浸膏体积的纯水,后加入10倍体积的石油醚进行充分振荡萃取,待静置分层后取上层石油醚相,减压浓缩,得到石油醚相浸膏.重复该操作3次,得到总的石油醚相浸膏;再向石油醚萃取后的水相中加入10倍体积的乙酸乙酯再次进行萃取,减压浓缩,得到乙酸乙酯相浸膏.重复该操作3次,得到乙酸乙酯相总浸膏64 g.
1.2.3 乙酸乙酯相浸膏的聚酰胺凝胶柱层析分离
1.2.3.1 装柱处理
用体积分数为10%的乙醇溶解聚酰胺胶粉并装入相应规格(长度为45 cm,直径为7 cm)的层析柱中,胶粉体积约为柱体积的三分之二,用10%(体积分数)的乙醇冲洗柱子,直至层析柱内壁无杂质且胶粉紧实填充.
1.2.3.2 样品处理
加入总体积约为40 mL的二氯甲烷和甲醇混合溶剂(体积比为1∶1)来溶解样品,再加入1.5倍浸膏体积的聚酰胺胶粉充分搅拌混匀,旋转蒸发,将混有样品的干燥粉末取出,干法上样.
1.2.3.3 梯度洗脱
用不同质量分数(10%,20%,…,100%)的乙醇溶剂进行梯度淋洗,每种质量分数的乙醇溶剂洗脱3~5 L,控制流速为13~20 mL·min-1,每1 L接瓶,通过薄层色谱(TLC)检视、观察洗脱情况,分段合并收集洗脱液.将含有丹参酮IIA的洗脱液合并,减压浓缩,得到丹参酮IIA粗品.
1.2.4 重结晶洗脱液
将上步所得的丹参酮IIA粗品用二氯甲烷和甲醇溶剂溶解,将粗品溶液置于试管中,待其结晶;再用石油醚洗涤至颜色成均一的棕红色结晶,干燥.
2 结果与分析
2.1 不良溶剂洗脱结晶
将得到的结晶置于砂芯漏斗中,加入适量石油醚抽滤、洗涤,洗涤至颜色均一无其他杂质,为深红色晶体(图1),取出并称量质量为2.00 g.

图1 丹参根及丹参酮IIA结晶
2.2 薄层色谱条件及结果分析
用毛细点样管吸取二氯甲烷溶解获得的结晶溶液少许,与丹参酮IIA标品溶液点于同一硅胶板上,以二氯甲烷-甲醇(体积比为10∶1)为展开剂,前沿线约至硅胶板的3/4 长度处取出、晾干,置于紫外分析仪254 nm紫外波长下观察,显示具单一荧光(图2),再加入显色剂磷钼酸溶液,用吹风机吹干,观察到无其他荧光物质干扰(图3).

图2 丹参酮IIA标品与样品TLC分析

图3 磷钼酸染色后丹参酮IIA标品与样品分析
2.3 核磁共振氢谱(1H NMR)分析
条件:(500 MHz,氘代氯仿),δ 7.63(d,J(偶合常数) = 8.1 Hz,1H),7.55(d,J= 8.2 Hz,1H),7.24~7.20(m,1H),3.18(t,J= 6.4 Hz,2H),2.286(s,3H),1.83~1.75(m,2H),1.68~1.62(m,2H),1.31(s,6H),如图4所示.δ 7.63(d,J= 8.1 Hz,1H),7.55(d,J= 8.2 Hz,1H)根据其化学位移及耦合常数可以确定其为邻位耦合的芳香氢,即6位和7位的苯环上的氢;7.24~7.20(m,1H)为15位呋喃上的氢;3.18(t,J= 6.4 Hz,2H)为三重峰,说明其为1号氢信号;2.28~2.24(m,3H)为17位甲基氢;1.83~1.75(m,2H),1.68~1.62(m,2H)为2、3号位的亚甲基氢;1.31(s,6H)为18、19位6个甲基氢(表1).
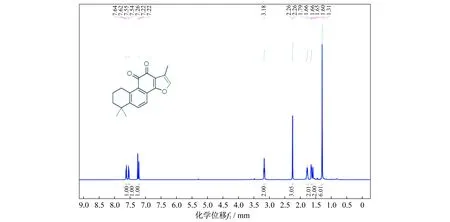
图4 1H NMR核磁分析结果
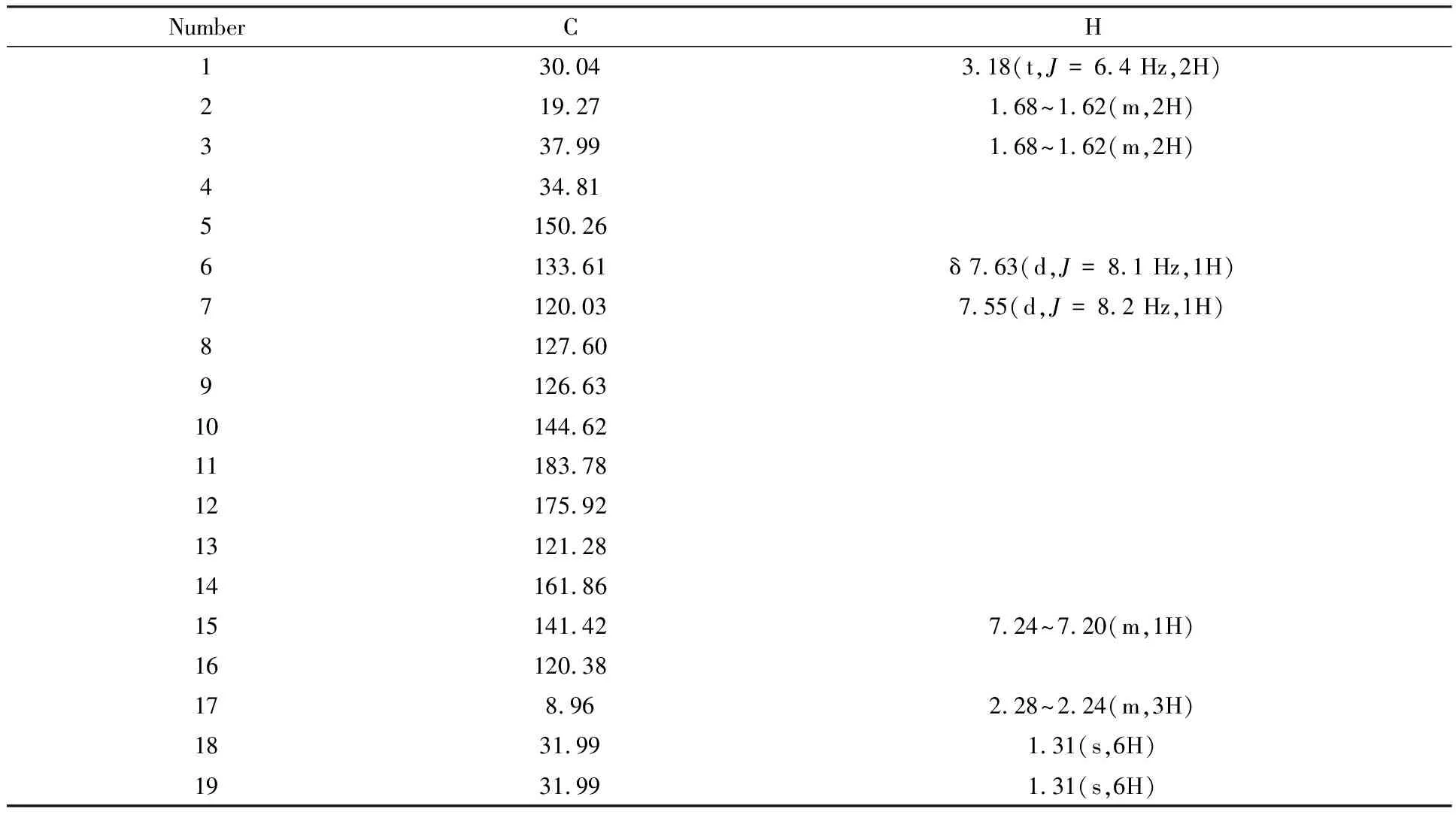
表1 丹参酮IIA的1H NMR、核磁共振碳谱(13C NMR)分析结果
2.4 核磁共振碳谱分析
条件:(125 MHz,氘代氯仿),δ 183.78(C-11),175.92(C-12),161.86(C-14),150.26(C-5),144.62(C-10),141.42(C-15),133.61(C-6),127.60(C-8),126.63(C-9),121.28(C-13),120.38(C-16),120.03(C-7),76.91(CDCl3),37.99(C-3),34.81(C-4),31.99(C-18),30.04(C-1),19.27(C-2),8.96(C-17),如图5所示.以上波谱数据与文献[26-28]报道的丹参酮IIA数据一致,故鉴定此化合物为丹参酮IIA.

图5 13C NMR核磁分析结果
2.5 高效液相色谱(HPLC)分析
取10 μL样品进行高效液相色谱分析,色谱条件为:C-18 反相硅胶柱(Symmetry Shield TM C18,5 μm,250 mm× 4.6 mm,waters);乙腈-超纯水(体积比为65∶35)为流动相;柱温为30 ℃;流速为1 mL·min-1;检测波长为220 nm.分析结果表明在23 min左右出现均一单峰,与丹参酮IIA标准品出峰时间吻合,可以确定样品为丹参酮IIA(图6).

图6 丹参酮IIA (a) 标品、(b) 样品以及 (c) 混合品(标品和样品体积比为1∶1)的HPLC分析结果
3 结 论
采用聚酰胺柱层析、乙醇梯度洗脱,合理有效地控制柱层析流速为13~20 mL·min-1,分离出了丹参酮IIA单体,纯度为93%,是一种高效的丹参酮IIA分离提纯方法,适合产业化生产.应用无毒或低毒的有机溶剂,并减少有机溶剂种类及使用量,达到了降耗节能,减少人员危害和环境污染的效果,且成本低、安全可靠,可为其他植物中相关产物的分离、提取提供参考.同时,本研究过程中还获得了其他极性的混合组分,下一步可以通过其他的分离方法(如硅胶层析、凝胶层析、大孔树脂分离技术等)进一步将其分离.
