重组人生长激素治疗儿童生长激素缺乏症和特发性矮小症的临床观察
2019-01-08谢雯胡红庆
谢雯, 胡红庆
儿童生长激素缺乏症(growth hormone deficiency,GHD)是因为下丘脑或垂体功能障碍造成生长激素合成或分泌不足,或因为生长激素结构或受体异常等造成生长发育障碍,临床表现为身材矮小、代谢紊乱、神经系统及心肾功能异常等[1]。目前,治疗GHD的主要方法是重组人生长激素(recombinant human growth hormone,rhGH),临床证实rhGH在改善GHD患儿身高方面具有显著疗效。同时在rhGH治疗期间需定期监测血清中IGF-1的水平,确保其保持在年龄、性别的正常范围,评估患儿是否有潜在肿瘤风险,保证rhGH治疗过程中的安全性和依从性。本研究对采用rhGH治疗达6个月的12例GHD、7例特发性矮小(idiopathic short stature,ISS)患儿的临床资料进行回顾性分析,分析胰岛素样生长因子1(insulin-like growth factor-1,IGF-1)标准差积分与身高生长速度的关系,旨在评估rhGH治疗中的剂量调整及安全性。
1 资料与方法
1.1 临床资料 选择2016年1月至2017年12月宜兴市人民医院收治的GHD患儿12例、ISS患儿7例为研究对象,按诊断分为GHD组和ISS组。GHD组中男7例,女5例;年龄4~9岁,平均年龄(7.0±1.9)岁。ISS组中男3例,女4例;年龄5~10岁,平均年龄(6.6±1.7)岁。两组患儿在性别、年龄方面比较差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准 参照2013版《基因重组人生长激素儿科临床规范应用的建议》中GHD、ISS的诊断标准[2]。生长激素药物激发试验采用精氨酸+左旋多巴联合激发,少数患儿因左旋多巴断货改用精氨酸+可乐定联合激发。生长激素峰值<10 μg/L为生长激素缺乏。
1.3 纳入标准 (1)符合GHD、ISS的诊断标准;(2)年龄4~10岁;(3)应用rhGH治疗且治疗时间6个月以上;(4)患儿家属知情同意。
1.4 治疗方法 予rhGH水剂(长春金赛药业有限责任公司)治疗,每周6~7 d,每晚睡前30 min予0.1~0.2 U/(kg·d)皮下注射。
1.5 观察指标 每3个月测体质量、身高,计算身高生长速度。每3个月查甲状腺功能3项、IGF-1、IGF结合蛋白3、空腹血糖、血脂、胰岛素。IGF-1标准差积分=(测量值-同种族同年龄同性别平均值)/(同种族同年龄同性别人群IGF-1标准差);生长速度=[2次身高测量差值(cm)]/间隔时间(m)×12。
2 结果
2.1 两组患儿身高增值、生长速度比较 见表1。
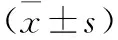
表1 rhGH治疗后身高增值及生长速度的变化
注:与GHD组比较,at=2.285,4.914,2.534,4.348,P<0.05。
表1结果表明,GHD组身高增值、身高增长速率均显著高于ISS组,差异有统计学意义(P<0.05)。
2.2 rhGH治疗前后IGF-1标准差积分的改变 见表2。
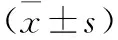
表2 rhGH治疗前后IGF-1标准差积分的改变
注:与治疗前比较,aP<0.05;与GHD组比较,bt=-3.208,P<0.05。
表2结果表明,GHD组中治疗3个月后IGF-1有明显升高,IGF-1标准差积分高于基线值(P<0.05),治疗6个月后IGF-1升高,IGF-1标准差积分较治疗前比较差异有统计学意义(P<0.05)。但其中有1例患儿在治疗过程中IGF-1无明显增高。ISS组中治疗3个月后IGF-1有升高,IGF-1标准差积分比较差异无统计学意义(P>0.05),治疗6个月后IGF-1升高,IGF-1标准差积分高于基线值,差异有统计学意义(P<0.05)。同时有1例患儿在治疗6个月查IGF-1高于2.5SD,后予停药。两组进行IGF-1标准差积分比较,治疗前两组比较差异有统计学意义(P<0.05),治疗后3个月、6个月比较差异均无统计学意义(P>0.05),考虑与GHD组升高幅度较ISS组明显有关。
2.3 不良反应 19例患儿在治疗过程中,1例空腹血糖升高,未予处理自行缓解,3例局部皮肤出现注射反应,主要是局部皮肤红肿和皮疹,均未影响治疗。1例因在治疗6个月后检查IGF-1超过2.5SD后予停药。治疗过程中未发现颅内高压、糖耐量异常、甲状腺功能减退、全身过敏、脊柱侧弯等严重不良反应。
3 讨论
生长激素是脑垂体千叶分泌的一种非糖基化蛋白质激素,由191个氨基酸组成,是人体内最重要的促生长的激素之一,而它是通过IGF-1直接或间接的作用,诱导维生素D活化,进而增加骨体积、骨矿物质密度及骨矿物含量,从而使长骨不断生长[3-4]。人体多个组织均可分泌IGF-1,以肝脏为主,它是一种促细胞生长多肽,与胰岛素结构和功能相似,其合成受生长激素调节和营养状况的影响[5-6]。研究显示IGF-1与短期身高增加相关,但IGF-1能不能作为判定生长激素治疗效果的指标尚不能证实。
在药品说明使用范围内rhGH治疗存在剂量依赖,但剂量并非越大越好。有研究发现,长疗程低剂量的治疗可更好的改善终身高,且剂量与矮小原因、青春期状态等有关[7]。在本研究中rhGH采用个体化治疗,确定病因后,根据个体情况从小剂量开始,GHD组剂量在0.1~0.15 U/(kg·d),ISS组剂量在0.15~0.2 U/(kg·d),发现GHD组中rhGH剂量较ISS组低,但其身高增值、身高增长速率均高于ISS组,说明GHD患儿用rhGH治疗疗效最明显,最有治疗价值。其中ISS组中在治疗后身高增值及身高增长速度较正常同龄儿童有明显升高,说明对于ISS患儿rhGH短期治疗效果满意,长期治疗效果需等待进一步研究。同时在研究中发现两组患儿随治疗时间的延长,身高增值及身高增长速率均呈下降趋势,治疗最开始的3个月内的身高增值及身高增长速率均最大。考虑这可能与随着治疗时间延长,一方面儿童生长板软骨细胞的增殖能力逐渐耗尽,一方面可能存在生长激素抵抗有关[8]。
IGF-1是生长激素的效应激素,其水平与短期身高增加有相关,临床通过测定IGF-1的水平来判定是否有GH分泌的异常[9]。在本研究中通过rhGH治疗后,IGF-1均增长明显,从而影响GH分泌,促进身高增加。但IGF-1的合成受生长激素及营养情况的影响,有1例IGF-1增值不明显,考虑与患儿平素有明显热量摄入偏低相关,故在治疗中不能盲目的由于IGF-1水平不增而不断加大rhGH用量。研究表明在rhGH治疗过程中,IGF-1标准差积分的升高可能导致胰岛素抵抗,出现胰岛素水平差异,而且这些变化在可能潜在有中枢神经系统肿瘤、急性淋巴细胞白血病、骨髓移植、代谢综合症等疾病的患儿中表现尤其明显[10]。所以在接受 rhGH治疗过程中IGF-1可作为其安全性监测的重要指标之一。在rhGH治疗过程的2年中,若血清IGF-1水平持续超过正常范围,特别是持续高于正常值2.5SD,需考虑减量或停药[11]。在本研究中有1例患儿在治疗6个月后IGF-1高于2.5SD,已予停用。这也体现出rhGH治疗患儿需长期管理的重要意义,突出了对IGF-1标准差积分进行仔细、适当监测的必要性,以防止潜在疾病对患儿产生不必要的影响,优化潜在风险和儿童终身高之间的平衡。
综上所述,rhGH治疗儿童矮小症有明显的促生长效果,尤其是GHD患儿疗效明显。但在rhGH治疗中一定要进行跟踪管理,定期、连续监测多种激素水平,尤其IGF-1水平,一方面有助于评估疗效,调整rhGH剂量,提高治疗效率,另一方面对rhGH治疗安全性进行更好的评估,并及时采取有效的干预措施。
