紫胶色酸A的荧光性质及其在检测中的应用
2019-01-07伊冠东刘兰香雷福厚张加研孙彦琳
伊冠东,刘兰香,雷福厚,张加研,李 凯,郑 华,张 弘,孙彦琳,*
(1.昆明理工大学化学工程学院,云南 昆明 650500;2.中国林业科学研究院资源昆虫研究所,云南 昆明 650224;3.广西民族大学 广西林产化学与工程重点实验室,广西 南宁 530006;4.西南林业大学化学工程学院,云南 昆明 650224)
紫胶红色素来源于紫胶虫的新陈代谢产物[1-2],是一种被多个国家允许用于食品添加的天然色素[3],同时被广泛运用在棉、羊毛、纺织品等的染色[4-5]。紫胶红色素的主要染色成分是紫胶色酸混合物,主要含有A、B、C、D、E 5 种组分,其中紫胶色酸A占总质量的85%左右,它们均属于蒽醌类化合物[6-8](图1)。蒽醌及其衍生物由于具有较好的平面及共轭结构,大多可发射荧光,被广泛用来识别不同体系中多种金属离子或其他阴离子[9-10]。紫胶红色素已被证明具有荧光性[6],然而,化学结构确定的单一成分紫胶色酸的荧光性质还鲜见有关报道。另外,目前检测食品、化妆品等样品中天然色素的常用方法有毛细管电泳法、高效液相色谱法、高效液相色谱-质谱联用法等,而检测食品中紫胶红色素方法的相关报道很少见[11-12]。因此,为满足食品安全发展的需要,开发快速、灵敏、准确检测食品中紫胶红色素的方法具有现实意义。
另一方面,金属元素广泛存在于自然界中,它们与生命体的生理活动有着密不可分的联系,当人体中摄入的某种元素过少或过多时都会影响身体健康[13-16]。因此,开发快速、便捷的检测金属离子方法,在食品[17-18]、环境[19]、化学、生命科学[8]等领域具有重要意义。荧光探针法[20-22]具有灵敏度高、特异性强、及时性及简便快捷等优点,在金属离子检测研究中受到了密切关注[23]。
本实验考察紫胶色酸A的荧光及吸收光谱的基本性质和影响因素,探索紫胶色酸A对金属离子的识别作用,期望将紫胶色酸A开发为检测某种特定金属离子的荧光分子探针,同时开发一种快速、准确检测紫胶色酸A的方法,为紫胶红色素的综合开发利用提供理论基础,预期了紫胶红色素更加广泛的应用特性和市场前景。
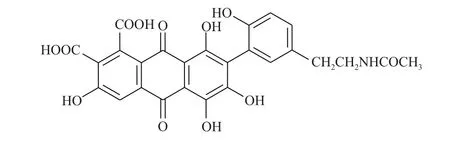
图1 紫胶色酸A的分子结构图Fig. 1 Molecular structure of laccaic acid A
1 材料与方法
1.1 材料与试剂
海之言果味饮料。紫胶红色素及紫胶色酸A(≥95%)由中国林业科学研究院资源昆虫研究所提供;盐酸、氢氧化钠、甲醇、乙醇、正丁醇、N,N-二甲基甲酰胺(N,N-dimethylformamide,DMF)、二甲基亚砜(dimethyl sulfoxide,DMSO)、硝酸银及其他金属无机盐(氯化盐)(均为分析纯) 广东光华科技股份有限公司;实验室用水为去离子水。
1.2 仪器与设备
F-4600荧光光谱仪 日本Hitachi公司;Cary Series紫外-可见吸收光谱仪 美国Agilent Technologies公司;WD-9403C紫外仪 北京六一生物科技有限公司;AB204-型精密电子天平 梅特勒-托利多(中国)有限公司;CPC-505台式pH计 欧洲Elmetron公司;TY742X2A型纯水机 美国Barnstead公司。
1.3 方法
1.3.1 一般光谱测定方法
荧光光谱测定时设置激发波长为380 nm,狭缝宽度为10 nm,扫描速率为12 000 nm/min,光电倍增管电压为950 V。紫外-可见吸收光谱全波长扫描过程中扫描速率为600 nm/min。
1.3.2 溶剂的影响
将2.7 mg紫胶色酸A分别溶于体积为25.0 mL的水、甲醇、乙醇、正丁醇、DMF、DMSO溶剂中,配成浓度为2×10-4mol/L的紫胶色酸A溶液,室温超声10 min后分别进行光谱测定。
1.3.3 紫胶色酸A浓度的影响
称取107.5 mg的紫胶色酸A溶于50.0 mL体积分数为75%的乙醇溶液,配成浓度为4.0×10-3mol/L的紫胶色酸A储备液,然后逐级稀释至不同浓度(2.0×10-3~2×10-6mol/L)作为待测样品溶液备用,考察紫胶色酸A浓度对其光谱性质的影响。
1.3.4 pH值的影响
分别制备0.1 mol/L的HCl和0.1 mol/L的NaOH储备溶液,然后将溶液适当稀释至所需pH值并用pH计校正。称取2.7 mg的紫胶色酸A溶于25.0 mL上述不同pH值的稀释液中,配成浓度为2.0×10-4mol/L的紫胶色酸A溶液,室温超声10 min,考察pH值不同的HCl和NaOH溶液对紫胶色酸A光谱性质的影响。
1.3.5 紫胶色酸A对金属离子的选择性识别
称取紫胶色酸A溶于75%乙醇溶液中,配成浓度为2.0×10-4mol/L的标准溶液,然后分别取5.0 mL紫胶色酸A乙醇溶液与1.0 mL金属离子(4.0×10-3mol/L)溶液混合于离心管中,混合均匀后静置20 min,然后测定荧光强度,考察金属离子对紫胶色酸A的荧光影响。
1.3.6 抗干扰性实验
将紫胶色酸A溶于75%乙醇溶液,配成浓度为2.0×10-4mol/L的样品溶液,将5.0 mL紫胶色酸A溶液和1.0 mL Al3+(4×10-3mol/L)溶液混合于离心管中,然后再分别加入1.0 mL浓度为4.0×10-3mol/L的其他金属离子溶液,混合均匀后测定其荧光强度。
1.3.7 Zn2+或 Al3+浓度与紫胶色酸A荧光强度的关系
配制浓度为0.1 mol/L的Zn2+或Al3+储备液,并将其逐级稀释至不同浓度(8.0×10-2~1.0×10-4mol/L)待用,然后将5.0 mL浓度为2.0×10-4mol/L的紫胶色酸A的75%乙醇溶液和1.0 mL不同浓度的Zn2+或Al3+混合均匀后检测荧光,考察Zn2+或 Al3+浓度与紫胶色酸A的荧光强度的关系。
1.3.8 Al3+存在下紫胶色酸A浓度与其荧光强度的关系
将紫胶色酸A溶于75%的乙醇溶液中,配成浓度为4.0×10-3mol/L的储备液,逐级稀释至不同浓度(2.0×10-3~1.0×10-6mol/L)作为待测样品备用。配制浓度为0.04 mol/L的Al3+溶液备用。取5.0 mL不同浓度的紫胶色酸A溶液于离心管中,分别加入1.0 mL Al3+溶液,混合均匀后测定溶液的荧光强度并绘制工作曲线。
1.3.9 实际应用实验
配制浓度为0.04 mol/L 的AlCl3标准液;紫胶色酸A加入至饮料中配制成3.7×10-3mol/L的储备液,然后用75%乙醇溶液稀释至不同浓度作为待测样品。取5.0 mL待测样品于离心管中,分别加入1.0 mL Al3+标准液,混合均匀后测定溶液的荧光强度,将所得数据代入标准方程,计算得到待测样品中紫胶色酸A的浓度。
1.4 数据处理
实验数据均平行处理3 次,结果以 ±s表示。各因素对紫胶色酸A荧光性质的影响采用Origin 9.1数据分析软件绘制。
2 结果与分析
2.1 溶剂对紫胶色酸A光谱的影响
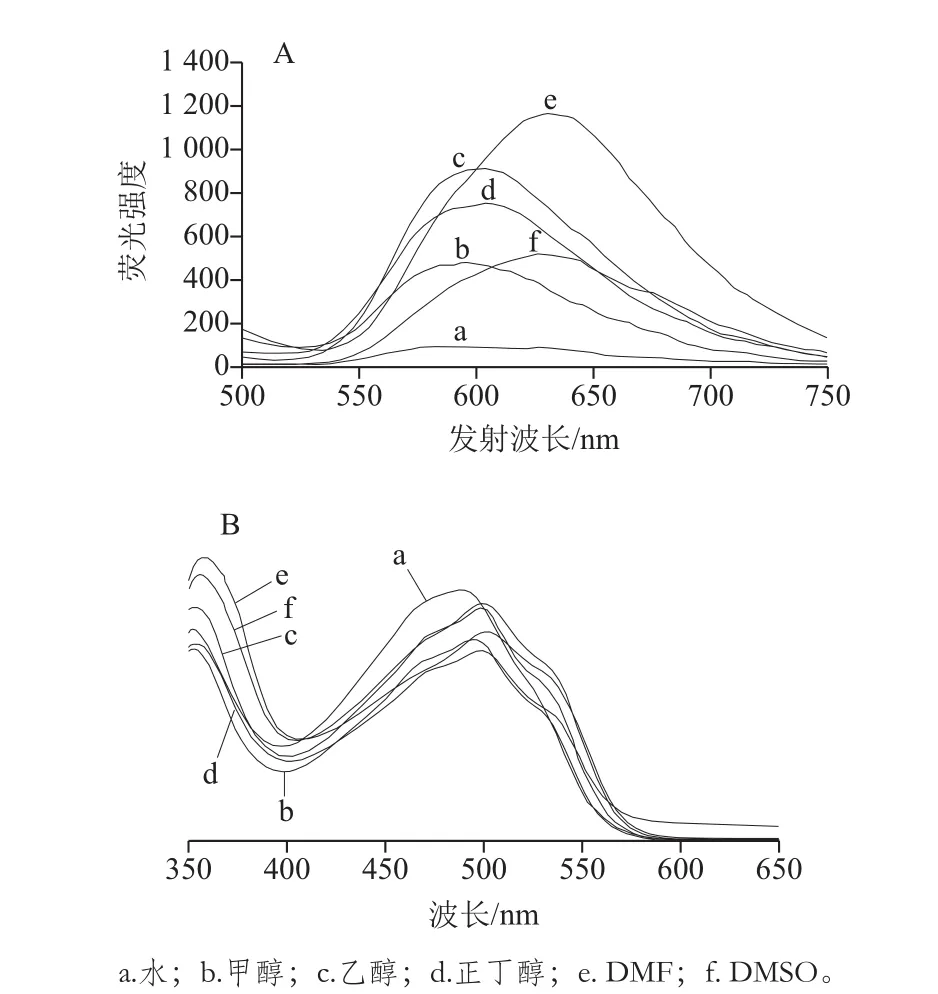
图2 溶剂对紫胶色酸A的荧光(A)和吸收(B)光谱的影响Fig. 2 Fluorescence (A) and absorption (B) spectra of laccaic acid A in different solvents
如图2所示,紫胶色酸A在不同的溶剂中其荧光强度由小到大的顺序为:水<甲醇<DMSO<正丁醇<乙醇<DMF。此外,紫胶色酸A的最大发射波长与溶剂有关,在水和醇中发射波长位于590 nm左右,在DMF和DMSO中发射波长位于630 nm左右。随着荧光强度和发射波长的变化紫胶色酸A在可见光区的最大吸收波长(λmax)发生了改变,最小的是在水中,为488 nm;最大的是在DMF中,为501 nm。究其原因,水和醇属于质子性溶剂,它们与色酸分子容易形成氢键,有助于色酸分子聚集,而水是所考察的所有溶剂中极性最大的,色酸分子的亲水性作用足以克服色酸阴离子之间的静电斥力,从而使其荧光降低,因此,紫胶色酸A在水中的荧光强度最小。DMSO和DMF属于非质子性溶剂,它们与溶质色酸分子容易发生溶剂化作用,同时,由于溶剂中存在S=O或C=O键,在色酸分子的荧光被激发时有助于π→π*跃迁,而DMF中的N原子具有孤对电子,加强了这种作用,因而紫胶色酸A在DMF中的荧光最强。由此可见,紫胶色酸A的荧光强度主要受溶剂本身的化学特性影响,其次,溶剂的极性也有一定程度的影响[24]。紫胶色酸A在水中的溶解度很小,在乙醇中的溶解度较大,而DMSO、DMF等有机溶剂有一定的毒性,因此,考虑到实际应用,选择乙醇-水混合体系作为溶剂较为合适,本实验选择75%的乙醇溶液作溶剂。
2.2 紫胶色酸A浓度对荧光强度的影响
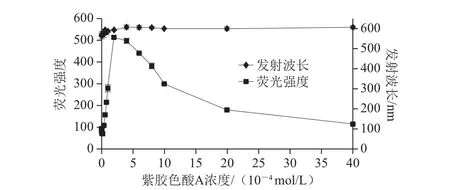
图3 紫胶色酸A浓度对荧光强度和发射波长的影响Fig. 3 Effect of concentrations on the fluorescence intensity and emission wavelength of laccaic acid A
如图3所示,当紫胶色酸A浓度在2×10-6~2×10-4mol/L范围内,紫胶色酸A的荧光强度和发射波长均随浓度的增大而增大,当溶度为2×10-4mol/L时荧光最强,发射波长从585 nm增大至598 nm;继续增大紫胶色酸A的浓度,体系的荧光强度会急剧减小直至猝灭,发射波长基本保持在600 nm左右。这可能是由于荧光分子在低浓度范围内聚集形成二聚体或多聚体是有助于荧光增强的,但是当荧光分子浓度增大到一定程度,激发态的分子与处于基态的分子相互碰撞导致激发态分子失活的概率增大,荧光分子发生能量自吸收从而引起了荧光减弱甚至猝灭[25-26]。因此,探究紫胶色酸A的其他荧光性质时,选择其浓度为2.0×10-4mol/L。
2.3 pH值对紫胶色酸A荧光强度的影响
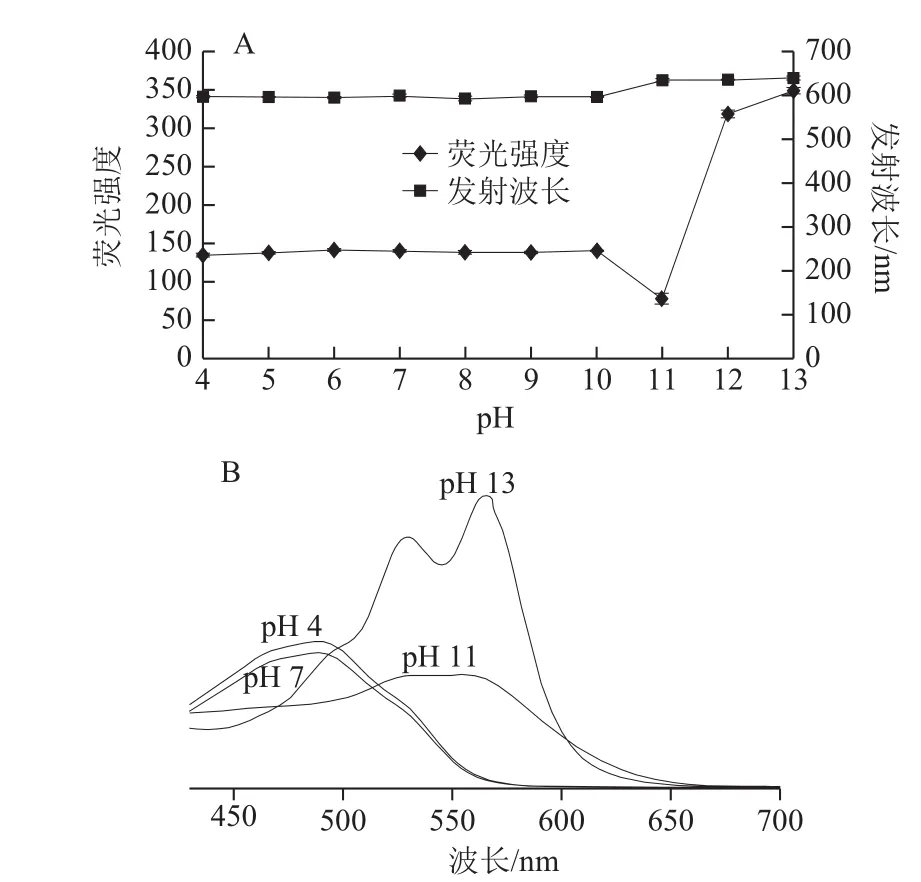
图4 pH值对紫胶色酸A荧光强度(A)和吸收光谱(B)的影响Fig. 4 Fluorescence intensity (A) and absorption spectra (B) of laccaic acid A at different pH values
将紫胶色酸A溶解于pH值不同的水溶液中,当溶液的pH值小于或等于3时,紫胶色酸A的溶解度很小,小于2×10-4mol/L,导致其荧光强度极低。如图4所示,当溶液的pH值在4~10之间,紫胶色酸A的荧光强度受pH值的影响较小,几乎保持不变,吸收光谱也没有明显差异。当溶液pH值达到11时,溶液的颜色变为紫红色,荧光几乎猝灭,可见光谱中出现了一个平而宽的吸收峰。当pH值大于11时,紫胶色酸A荧光强度迅速显著增加,可见光区出现双吸收峰,最大吸收波长分别为530 nm和565 nm。紫胶色酸A在不同pH值范围内呈现出荧光强度变化的差异性可能与其分子结构中的羧基、羟基(酚)的电离有关[27-28],pH值在4~10之间,紫胶色酸A主要以分子形态存在;pH值在11左右,分子中的两个羧基发生电离;当pH值大于11时,羟基(酚)开始电离,紫胶色酸A主要以离子形态存在。因此,考察其他因素对紫胶色酸A的荧光影响时可选择pH值为4~10之间的溶液。
2.4 紫胶色酸A对金属离子的选择性识别
如图5A所示,在75%乙醇溶液体系中加入Na+、K+、Cd2+、Ag+、NH4+、Mn2+和Hg2+等金属离子对紫胶色酸A的荧光强度几乎没有产生影响,Cu2+、Fe3+、Fe2+和Pb2+四种离子均使紫胶色酸A的荧光几乎完全猝灭,而Mg2+使其荧光略有增加,Zn2+和Al3+却使紫胶色酸A荧光强度显著增强。究其原因,可能是紫胶色酸A分子中的酚羟基、羧基都是金属离子的良好配体,易与金属离子形成配合物从而发生电子、能量转移等作用[29-30]。同时,受金属离子的核外电子排布和电荷的影响,不同的金属离子对紫胶色酸A的荧光产生的作用效果出现了差异[29-30]。
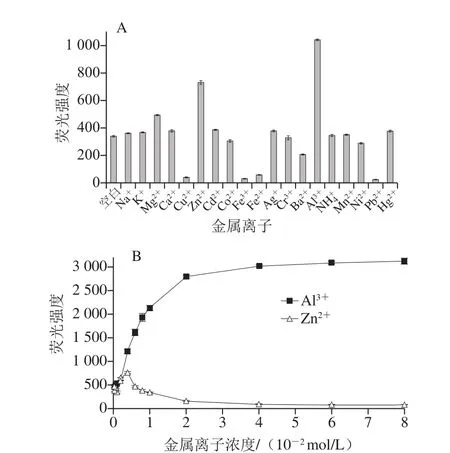
图5 紫胶色酸A在75%乙醇溶液中对金属离子的荧光识别(A)和Al3 +、Zn2+浓度对荧光强度的影响(B)Fig. 5 Fluorescence recognition of metal ions by laccaic acid in 75% ethanol solution (A) and effects of Al3+ and Zn2+ concentration on fluorescence intensity(B)
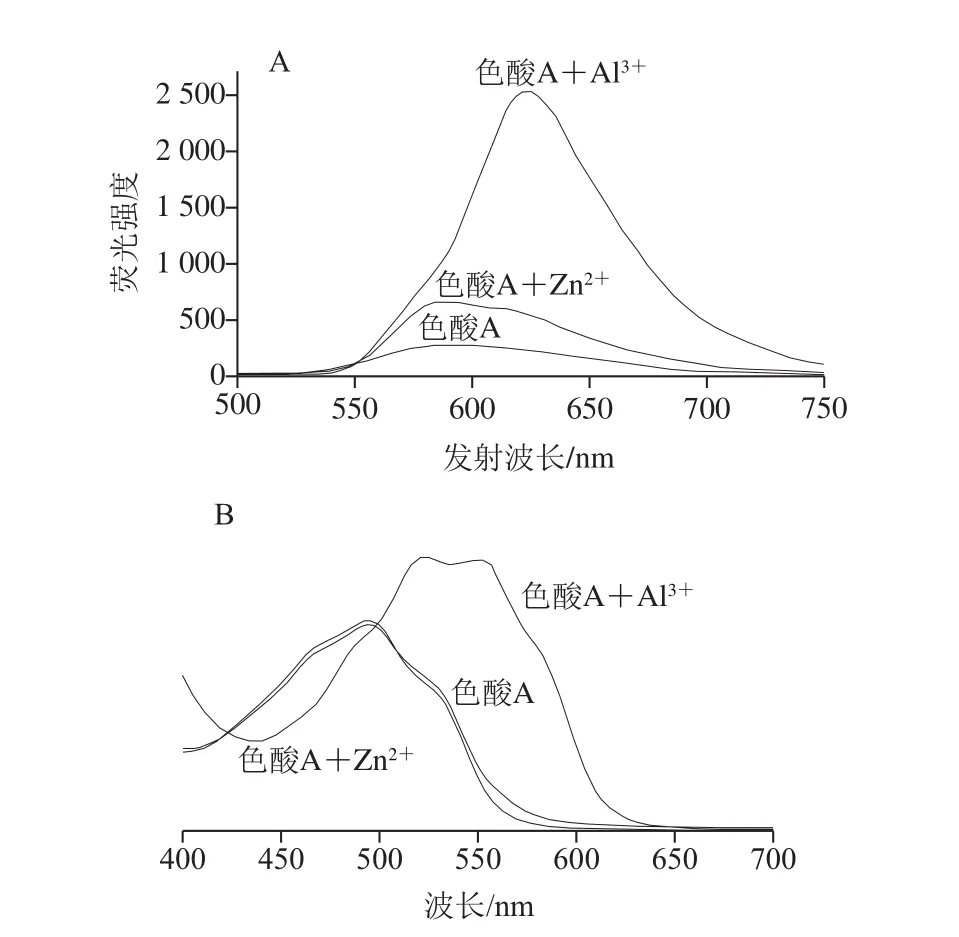
图6 荧光光谱(A)和可见光光谱(B)Fig. 6 Fluorescence spectrum (A) and visible spectrum (B)
进一步考察Zn2+或Al3+与紫胶色酸A荧光强度的关系,如图5B所示,当Zn2+的浓度小于4×10-3mol/L时,紫胶色酸A的荧光强度随Zn2+的浓度增加而增加,但是继续增加Zn2+的浓度,溶液中开始产生不溶物,荧光逐渐减弱直至完全猝灭。与加入Zn2+的变化不同,当Al3+的浓度小于2.0×10-2mol/L 时,紫胶色酸A的荧光强度随Al3+浓度的增加而明显增加,继续增加其浓度,紫胶色酸A的荧光强度几乎保持不变。由此可见,二者增强紫胶色酸A荧光的机理可能是不一样的,这个推论可由荧光光谱和紫外-可见光光谱得到进一步验证。如图6所示,紫胶色酸A溶液加入Zn2+时,其发射波长和可见光区的最大吸收波长基本没变化,然而,加入Al3+时,紫胶色酸溶液的发射波长由590 nm移动至625 nm左右,同时,可见光谱由488 nm向长波长方向移至522 nm,同时出现另一个吸收峰,其可见光区的最大吸收波长为562 nm。据此,可推测Zn2+增强紫胶色酸A荧光的原因可能是Zn2+与色酸分子中的N原子和—OH作用下发生光致电子转移,而Al3+与色酸分子中多个位点的—OH和—COOH形成不同的配合物,发生荧光能量共振转移[29-30]。综合以上,在所考察的金属离子中,只有Al3+显现出显著增强紫胶色酸A的荧光强度的特异性。
2.5 抗干扰性实验结果
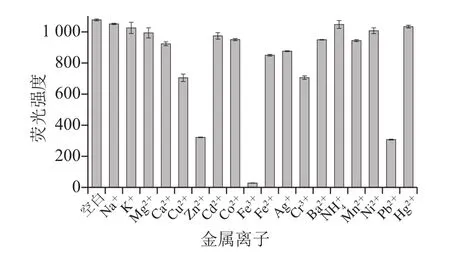
图7 其他金属离子对探针识别Al3+的影响Fig. 7 Effect of other metal ions on Al3+ recognition by fluorescence probes
如图7所示,在含有Al3+的紫胶色酸A的75%乙醇溶液中加入其他金属离子,Fe3+与Al3+共存时体系的荧光猝灭,Zn2+和Pb2+与Al3+共存时体系的荧光强度有所降低,而其他金属离子共存时并未明显改变体系的荧光强度。结果表明,在没有Fe3+、Zn2+和Pb2+离子的环境中,紫胶色酸A对Al3+选择性识别的抗干扰性较强、选择性较好,紫胶色酸A具有开发成为荧光探针用于检测Al3+的潜在应用。
2.6 紫胶色酸A浓度与其荧光强度的关系
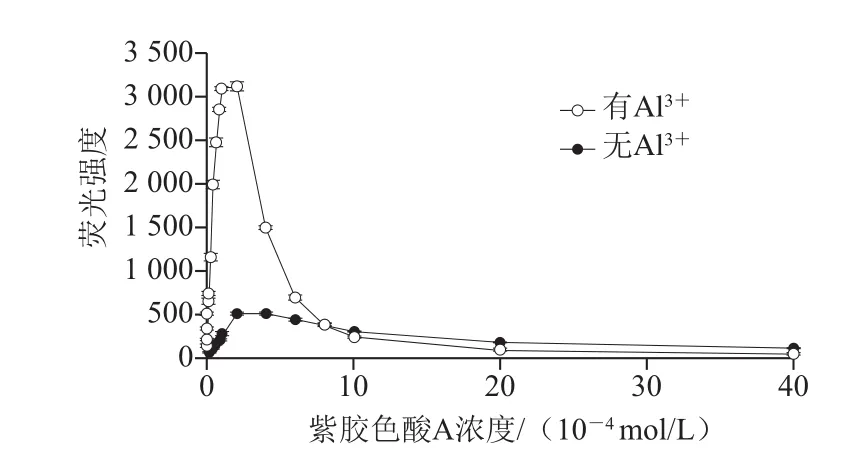
图8 紫胶色酸A浓度与荧光强度的关系图Fig. 8 Relationship between laccaic A concentration and fluorescence intensity
如图8所示,在紫胶色酸A的75%乙醇溶液中,无论溶液中是否加入Al3+,紫胶色酸A的荧光强度都随其浓度的增加呈现先增后减的变化。然而,在未加Al3+时,紫胶色酸A的荧光强度很低,若用荧光法检测其浓度,误差较大,而加入Al3+后其荧光强度最大可增强6 倍多,因此,可考察Al3+存在的条件下,紫胶色酸A的荧光强度与其浓度的关系。结果表明,紫胶色酸A在Al3+(0.04 mol/L)存在的条件下,其在1×10-5~8×10-5mol/L浓度范围内与其荧光强度呈良好的线性关系,对线性进行拟合得到方程y=326.2x+467.7,线性相关系数R2为0.995 2。

图9 紫胶色酸A在自然光(A)和紫外光365 nm波长处(B)的照片Fig. 9 Pictures of laccaic acid A in natural light (A) and UV light (365 nm, B)
如图9所示,在Al3+(0.04 mol/L)存在的条件下,紫胶色酸A的75%乙醇溶液在自然光下,溶液颜色由浅变深,紫红色变为红色再变为暗红色;荧光呈现淡紫色至橙色再到红色直至无荧光的变化。
2.7 应用实验结果
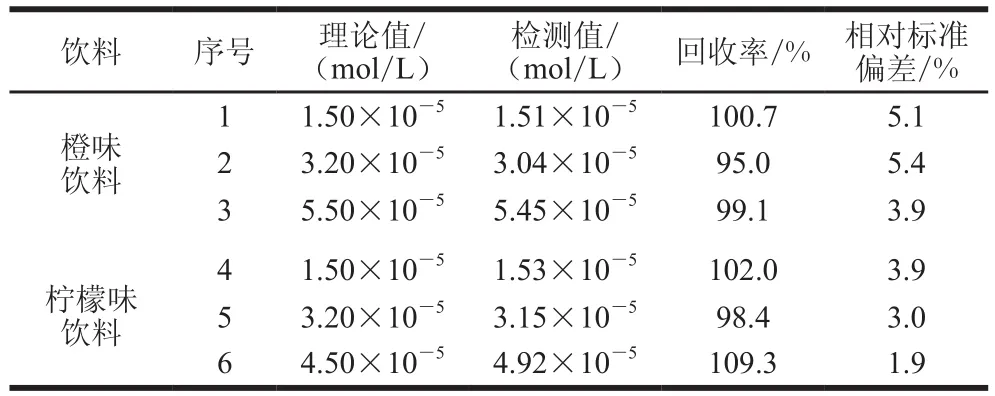
表1 紫胶色酸A检测应用实验结果(n= 3)Table 1 Application of the fluorescence method for laccaic acid A detection in beverages (n= 3)
如表1所示,以Al3+为标准液,用荧光法检测两种不同饮料中添加的紫胶色酸A含量,样品回收率在95.0%~109.3%之间,相对标准偏差在1.9%~5.4%之间,结果表明,在Al3+(0.04 mol/L)存在的条件下,可用荧光法检测紫胶色酸A在样品中的含量,该方法具有实际应用价值。
3 结 论
紫胶色酸A可发射较强荧光,溶剂的化学特性和极性、其自身浓度以及溶液的酸碱性都会影响其荧光强度和发射波长。
紫胶色酸A对不同的金属离子具有一定的识别作用,在75%乙醇溶液中,Na+、K+、Cd2+、Ag+、NH4+、Mn2+和Hg2+等金属离子对其荧光强度几乎没有影响,Cu2+、Fe3+、Fe2+和Pb2+四种离子均可猝灭其荧光,而Zn2+和Al3+显著增强了紫胶色酸A的荧光强度。
在75%乙醇溶液中,Al3+显现出显著增强紫胶色酸A荧光强度的特异性;在Al3+(0.04 mol/L)存在的条件下,紫胶色酸A在其浓度为1.0×10-5~8.0×10-5mol/L的范围内与荧光强度呈良好的线性关系。
应用实验结果表明,以Al3+为标准液,用荧光法检测两种不同饮料中添加紫胶色酸A的含量,样品回收率在95.0%~109.3%之间,相对标准偏差在1.9%~5.4%之间,该方法具有实际应用价值。
