高效微波辐射制备Fe-MSB对磷的吸附
2019-01-05,,,,
,,,,
(安徽工业大学能源与环境学院,安徽 马鞍山 243032)
1 前 言
磷作为富营养化的元素之一,排放标准越来越严格,尤其是国家对磷排放标准提高到一级A标准(0.5mg/L)后,各企业和该领域研究者对磷处理更加重视。相比其他除磷方法,吸附法除磷具有无可比拟的优点:高效低耗、操作简单和无二次污染等[1]。
膨润土是以蒙脱石为主要矿物成分的非金属矿产,全球分布甚广,主要以钠基膨润土为常见工业品,且具有良好的吸附性能,价格低廉[2]。但由于膨润土的亲水性极强,致使其对废水中污染物的吸附性能较差,因此通过对膨润土进行改性来改善其吸附性能具有重大意义。微波辐射改性法相比传统的水热合成法[3]具有升温迅速、受热均匀、加热效率高和节约能源等优点[4]。利用微波辐射法制备改性膨润土吸附剂,并将其用于吸附磷的研究已有报道[5-6,8]。宋珍霞等[5]采用先恒温搅拌后微波辐射的方法,利用十六烷基三甲基溴化铵改性膨润土,制得有机改性膨润土,但有机物改性使天然无毒的膨润土附带了毒性,有悖绿色环保这一原则。范恒等[6]采用微波辐射,以季铵盐和Al3+盐为改性剂对钠基膨润土进行改性,制备有机无机复合改性膨润土,研究复合改性膨润土对磷的吸附,但制备过程复杂,而且由于Al3+的存在,在制备过程中可能产生破坏蒙脱石阳离子交换性能的keggin离子,影响膨润土的吸附性能[7]。聂锦旭等[8]先利用搅拌浸泡的方式混合钠基膨润土和FeSO4溶液,再将其烘干后置于微波炉中辐射制得改性膨润土(制备周期约为24h),并用其吸附磷,但制备周期长,且低价铁盐也不稳定。除了以上不足之处,已有的改性膨润土吸附磷研究往往仅限于反应条件对吸附影响的研究,缺乏对磷吸附规律和机理的探讨。
为了制备性能良好且稳定的环保吸附磷材料,探索简化制备过程、缩短制备周期和磷的吸附规律,本研究以较为稳定的三价铁盐作为改性剂,高效利用微波能量直接辐射Fe2(SO4)3和钠基膨润土混合液,制备Fe-MSB(制备周期约为12h),并对改性前后钠基膨润土进行XRD和SEM表征。探讨吸附剂投加量、初始pH、温度和振荡时间对Fe-MSB吸附磷性能的影响,通过吸附动力学和热力学分析,找到吸附规律,阐述吸附机理,为膨润土在含磷废水处理的工业化应用方面提供吸附模型和数据。
2 实 验
2.1 实验材料与仪器
原料与试剂:钠基膨润土为工业级,硫酸铁、磷酸二氢钾、四水合钼酸铵、酒石酸锑氢钾、抗坏血酸、硫酸和氢氧化钠均为分析纯。
主要仪器:722s型可见分光光度计、P70D20N1P-G5型格兰仕微波炉、SHZ-B型水浴恒温振荡器和JW-3021H型高速离心机,Ultima IV型X射线衍射仪和JSM-6490LV型扫描电子显微镜。
2.2 实验方法
2.2.1Fe-MSB的制备方法 取0.8g改性剂Fe2(SO4)3·xH2O溶于50mL蒸馏水中,待改性剂溶解后形成溶液A,然后向溶液A中投加10g钠基膨润土(经105℃烘1.5h预处理后的钠基膨润土),摇匀使其完全溶解形成溶液B,静置30min,将溶液B置于微波炉中,经微波低火辐射6min后,水洗3~4次直到洗出液澄清,随后将其置于干燥箱中,在110℃烘干,研细。
2.2.2表征方法 采用Rigaku Ultima IV型XRD对吸附材料进行表征,测定条件:入射光源为Cu-Kα靶,入射波长λ=1.54178Å,电压V=40kV,电流I=120mA,扫描速率v=10°/min,扫描范围(2θ)3~50°。
取少许吸附材料,置于喷铂金的小铜片上,于JSM-6490LV型SEM下,放大2000倍,观察吸附材料的微观形貌。
2.2.3吸附实验 (1)操作步骤与测定方法 取50mL模拟含磷废水(用磷酸二氢钾和蒸馏水配制,其pH≈6、磷含量C=25mg/L,现配现用)置于250mL锥形瓶中,加入若干吸附剂,置于水浴恒温振荡器中,在一定水浴温度下,振荡一段时间。取出部分吸附后的溶液移入15mL离心管中,在离心机转速为4000r/min下离心5min,取上清液,依据《钼酸铵分光光度法》(GB 11893-89)测定溶液中残余磷浓度。
按下式计算去除率R(%)及平衡吸附量qe(mg/g):
R=[(C0-Ce)/C0]×100%
(1)
qe=(C0-Ce)V/m
(2)
式中,C0为磷的初始浓度(mg/L),Ce为平衡浓度(mg/L),V为溶液体积(L),m为吸附剂投加量(g)。
(2)吸附实验方案 采用单因素实验探讨Fe-MSB投加量、pH值、温度和振荡时间对去磷效果的影响。各因素具体水平取值见表1。

表1 吸附实验方案设计Table 1 Adsorption experiment scheme
2.2.4吸附等温实验 分别取50mL初始浓度为20、25、30、40和50mg/L的模拟含磷废水置于250mL锥形瓶中,向每个锥形瓶中加入1.0g Fe-MSB,将锥形瓶放入水浴恒温振荡器中,分别在水浴温度为293、303、313和323K下,振荡120min。取出部分吸附后的溶液移入15mL离心管中,在离心机转速为4000r/min下离心5min,取上清液测定溶液中的残余磷浓度。
3 结果与讨论
3.1 吸附剂的表征
3.1.1XRD分析 由图1可以看出,Fe-MSB和钠基膨润土的XRD图谱相似,说明Fe3+的引入并没有破坏钠基膨润土内部原有的基本构架[9]。但可以看出Fe-MSB的d001处峰所对应的2θ比钠基膨润土的d001处峰所对应的2θ明显减小。
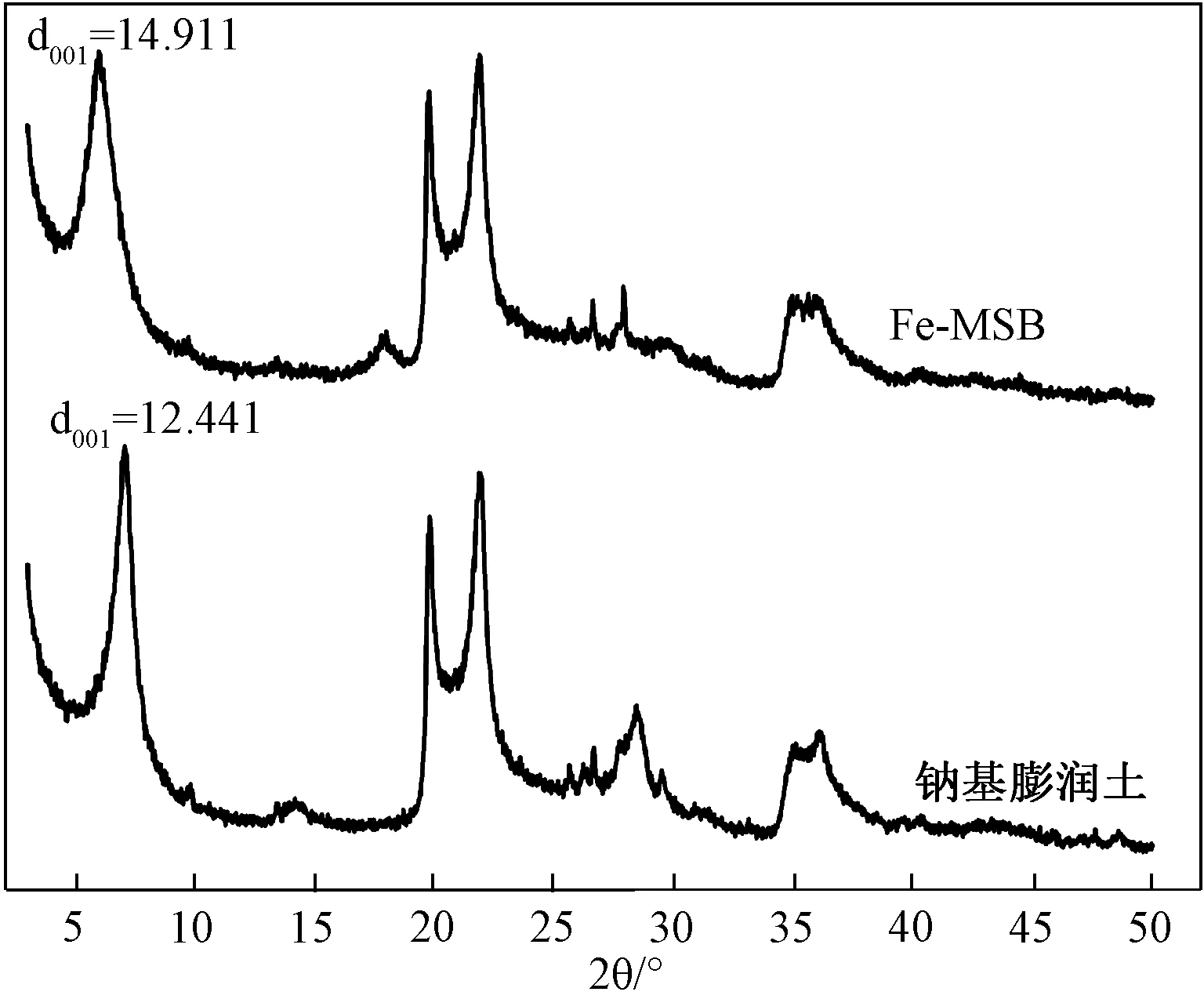
图1 吸附剂的XRD图谱Fig.1 XRD patterns of adsorbents
根据Bragg公式[10]:
2dsinθ=nλ
(3)
式中:d为晶面间距(Å),θ为入射X射线与相应晶面的夹角(°),n为衍射级数。由图1得到的Fe-MSB的d001=14.911大于钠基膨润土d001=12.441。d001越大,说明钠基膨润土的分子层间被撑得越开,吸附性能就越好[11]。XRD表征表明Fe3+进入到了钠基膨润土的分子层间,成功改性了钠基膨润土,改变了钠基膨润土的层状结构[12],使钠基膨润土层间距变大,可使其吸附性能提高[11]。
3.1.2SEM观察 分别对钠基膨润土和Fe-MSB进行SEM表征,分析其微观结构,结果如图2所示。图2(a)中钠基膨润土表面光滑,而图2(b)中Fe-MSB表面粗糙、疏松、多孔,其原因可能是因为Fe3+取代钠基膨润土中的钠离子导致钠基膨润土表面电荷发生变化,负电性增强;此外在改性过程中,将Fe2(SO4)3、膨润土和蒸馏水混合溶解,除了大部分Fe3+取代了钠离子连接在钠基膨润土表面外,一小部分的Fe3+可与水形成Fe—OH键,插入钠基膨润土层间,产生片层翻起的现象,经微波辐射,在钠基膨润土层间进行了阳离子交换,钠基膨润土中杂质以及无定性相被置换出来,因此钠基膨润土的插层和其中无定形相减少,造成了改性后的Fe-MSB的片层与孔隙[13]。这样的结构改变可使吸附剂的吸附能力得到增强[9,14-15]。结合XRD分析进一步说明Fe3+成功进入到了钠基膨润土的分子层间,改善了钠基膨润土的孔道和孔隙结构[16],从而提高了钠基膨润土的吸附性能。

图2 吸附剂的SEM图像 (a) 钠基膨润土;(b) Fe-MSBFig.2 SEM patterns of adsorbents (a) Sodium bentonite; (b) Fe-MSB
3.2 Fe-MSB吸附磷的影响因素
3.2.1Fe-MSB投加量对吸附的影响 由图3可知,随着Fe-MSB投加量的增加,磷的去除率先迅速增加后趋于稳定。在Fe-MSB投加量在10~20g/L内,去除率随投加量的增加而迅速增大;此后继续增加投加量,磷的去除率趋于稳定。当Fe-MSB投加量为20g/L时,Fe-MSB对磷的去除率高达98.72%,此时出水磷浓度为0.32mg/L,已达到排放标准(0.5mg/L),继续增加投加量对磷的去除率提高并不明显。胡凤杰等[17]向100mL模拟含磷废水(C0=5mg/L)添加6.0g 改性膨润土,对磷的去除率为70.21%。本研究与胡凤杰相比,膨润土投加量明显减少。因此,将Fe-MSB投加量设定为20g/L。
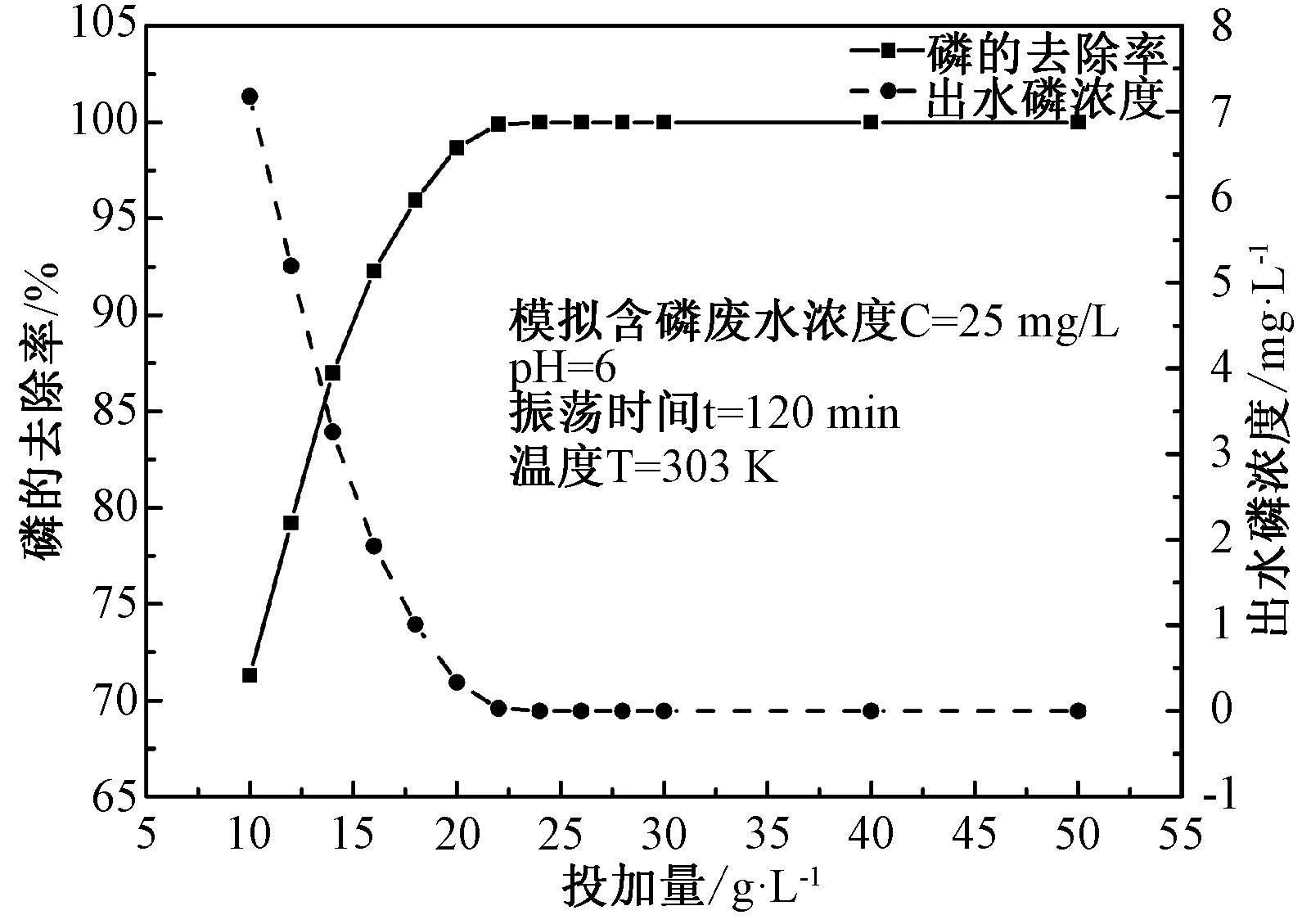
图3 Fe-MSB投加量对磷吸附的影响Fig.3 Effect of Fe-MSB dosage on adsorption

图4 初始pH值对磷吸附的影响Fig.4 Effect of initial pH on adsorption
3.2.2初始pH值对吸附的影响 由图4可知,磷的去除率随初始pH值的增加先增大,后略有降低。在初始pH=2时,Fe-MSB对磷的去除率较低,根据不同pH条件下磷酸盐的形态分布,当pH≤2时,在强酸环境中,磷酸盐的主要存在形式为H3PO4,溶液中的H+较多,占据了膨润土的吸附点位[17],使Fe-MSB对磷的吸附效果下降,吸附后溶液的H+减少导致平衡pH升高;在初始pH=3时,磷去除率达到峰值;初始pH在3~6之间,磷的去除率维持在较高水平;当初始pH>6时,随着溶液处于的碱性环境越强,溶液中OH-越多,与磷酸根负离子形成竞争吸附,此外由于Fe3+作为Lewis酸酸位点,在溶液的pH值增大时,溶液中OH-与其作用,导致Fe-MSB吸附活性降低,磷去除率降低,同时溶液中OH-就会减少,致使吸附后平衡pH值降低[18]。
由此分析可知,初始pH维持在3~6之间,Fe-MSB对磷的吸附效果较好,Fe-MSB适用于处理弱酸性废水,而本研究模拟含磷废水pH≈6,为节约吸附剂,可省去实验用水pH值的调试。本研究与胡凤杰[17]和顾伟[19]等的研究结果一致。胡凤杰[17]等将pH调至6,改性膨润土对磷的去除率达到最大,为78.41%。顾伟[19]等研究Al3+改性膨润土对磷的吸附,研究表明在pH为6时,吸附剂对模拟含磷废水中磷的去除效果最好,为95.1%。
3.2.3温度对吸附磷的影响 由图5可知,随着反应温度升高,Fe-MSB对磷的去除率先快速增加后趋于平缓。当温度<303K时,去除率随着温度升高明显增大,当温度T=303K时,磷的出水浓度已在0.5mg/L以下。继续升高温度,Fe-MSB对磷的去除率增加幅度较小。综合节约能耗和磷含量达标两因素,实验将温度控制在303K。
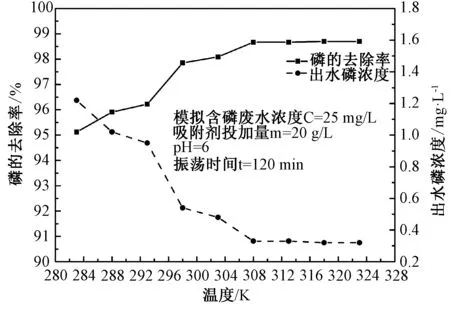
图5 温度对磷吸附的影响Fig.5 Effect of temperature on adsorption
3.2.4振荡时间对吸附的影响及吸附动力学分析 由图6可见,随着吸附时间延长,Fe-MSB对磷的吸附量先迅速增加后趋于稳定。吸附过程大致分为两个阶段:第一阶段5~60min为快速反应,第二阶段60~240min为慢速反应。在t=120min时,吸附基本达到平衡,此时水中磷浓度降至0.32mg/L。因此将吸附时间确定为120min。
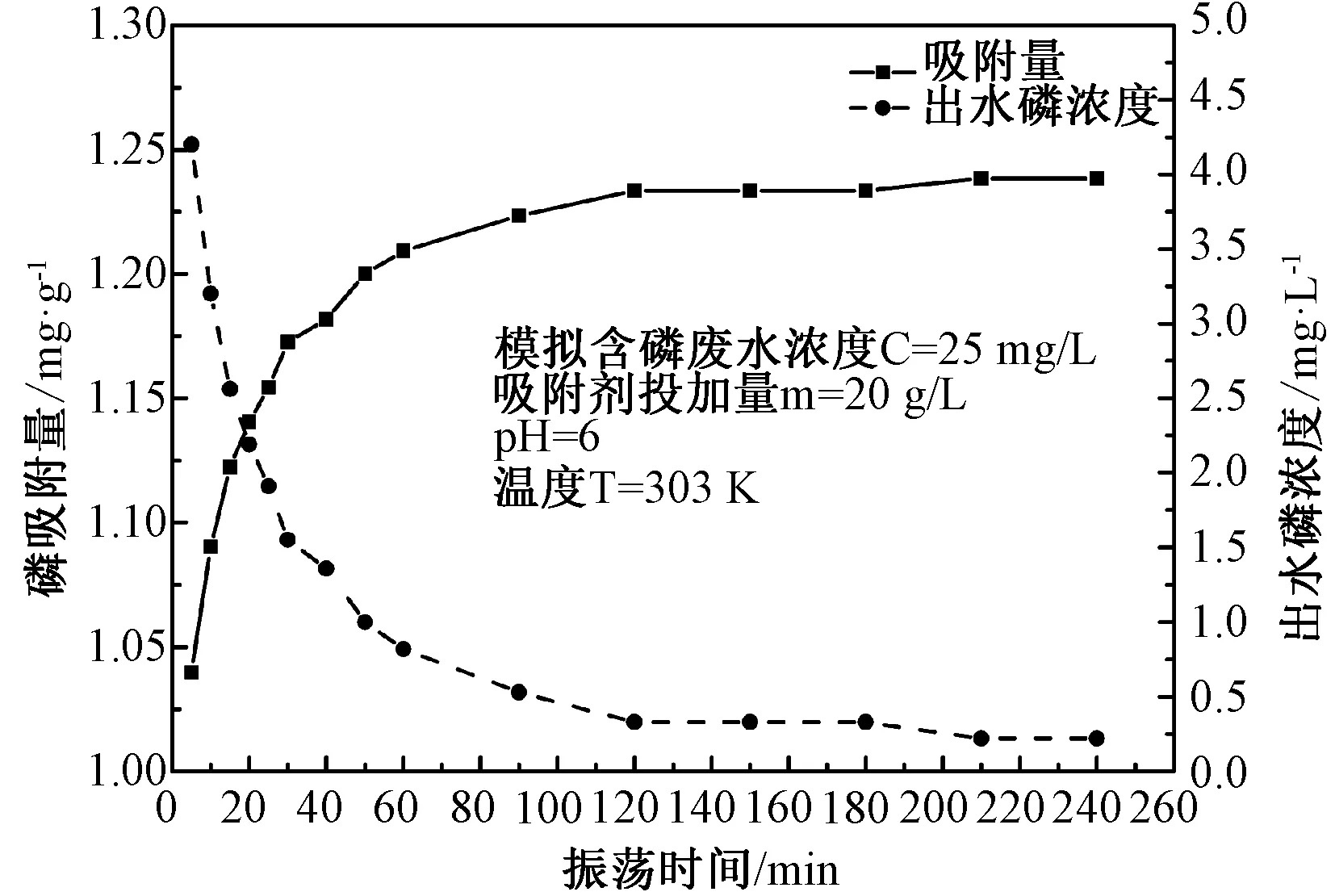
图6 振荡吸附时间对磷吸附的影响Fig.6 Effect of reaction time on adsorption
根据图6中实验数据对吸附过程的动力学进行拟合,主要采用3个动力学模型方程,包括:
一级动力学模型[20]:
log(qe-qt)=logqe-Kf/2.303t
(4)
准二级动力学模型[21]:
t/q=Ks-1qe-1+qe-1t
(5)
颗粒内扩散模型[22]:
qt=Kidt1/2+C
(6)
式中:qe为平衡吸附量(mg·g-1);qt为t时刻的吸附量(mg/g);Kf为一级吸附速率常数(min-1);Ks为准二级吸附速率常数[(g/mg·min)];Kid为传质扩散速率[mg/(g·min2)],C为截距(mg/g)。
分别用动力学方程(4)、(5)和(6)对吸附过程中快速反应阶段、慢速反应阶段和整个吸附过程进行拟合,根据线性化的R2值来判断拟合的优劣。表2所示的拟合结果表明:以准二级动力学方程描述Fe-MSB吸附磷的吸附过程为最优,且其拟合出的qe与实验结果极为接近,说明该过程以化学吸附为主[18]。陈泳[18]等在吸附磷的研究中也得到了同样的结果。

表2 吸附动力学方程及相关系数Table 2 Adsorption kinetic parameters and correlation coefficients
3.3 吸附热力学分析
吸附等温线的拟合采用Langmuir和Freundlich两个吸附等温方程[23-26]。
Langmuir吸附等温方程:
(7)
Freundlich吸附等温方程:
lnqe=lnKF+(1/n)lnCe
(8)
式中:qe为平衡吸附量(mg/g);Ce为吸附平衡浓度(mg/L);qm为最大吸附容量(mg/g);KL为Langmuir常数(L/mg);KF、n为 Freundlich 吸附等温方程的经验参数,可以将KF看作是与吸附剂吸附容量有关的参数,n是与吸附质和吸附剂表面作用强度有关的参数。
由图7可见,随着磷酸根吸附平衡浓度增大,Fe-MSB对磷的平衡吸附量也随之增加。采用方程(7)和方程(8)对图7中实验数据进行回归处理,得到表3中Langmuir和Freundlich 等温方程的相关参数R2,表明Langmuir等温模型拟合的效果优于Freundlich。Langmuir 方程中参数 KL值随着温度的升高而升高,表明吸附是吸热过程[18]。
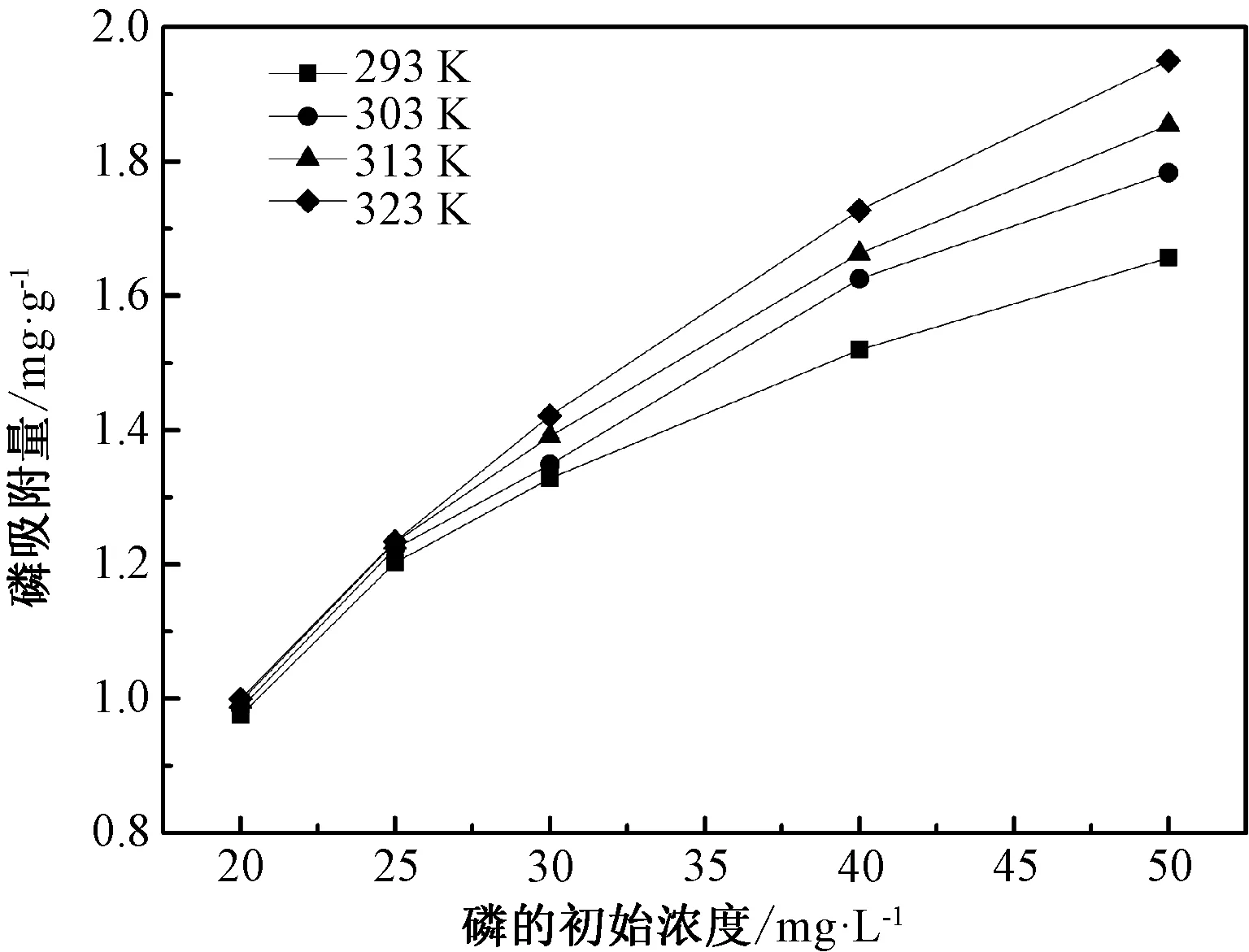
图7 Fe-MSB吸附磷的等温吸附线Fig.7 Adsorption isotherm of Fe-MSB uptake P
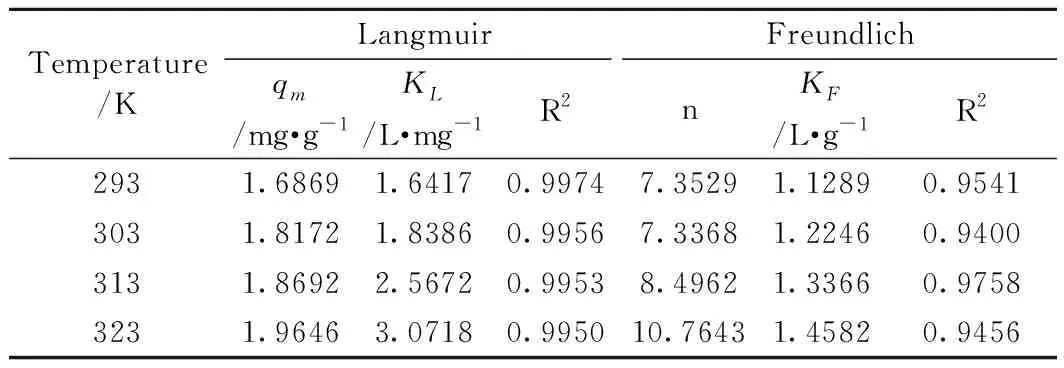
Temperature/KLangmuirFreundlichqm/mg·g-1KL/L·mg-1R2nKF/L·g-1R22931.68691.64170.99747.35291.12890.95413031.81721.83860.99567.33681.22460.94003131.86922.56720.99538.49621.33660.97583231.96463.07180.995010.76431.45820.9456
根据范特霍夫方程[27-29]:
ΔG=-RTlnKa
(9)
(10)
式中:ΔG为标准自由能(kJ·mol-1),ΔH为吸附焓(kJ·mol-1),ΔS为吸附熵(J·mol-1.K-1),R为标准摩尔气体常数(数值等于8.314J·mol-1·K-1),T为温度(K),Ka为Langmuir常数,Ka=qmKL。
采用线性回归的方法,用lnKa对1/T作图,得到一个线性方程(如图8):lnKa=-2549.9/T+9.6874,R2=0.9831,拟合效果较好。根据式(9)、(10)以及图8中直线的斜率和截距可求得热力学参数,见表4。
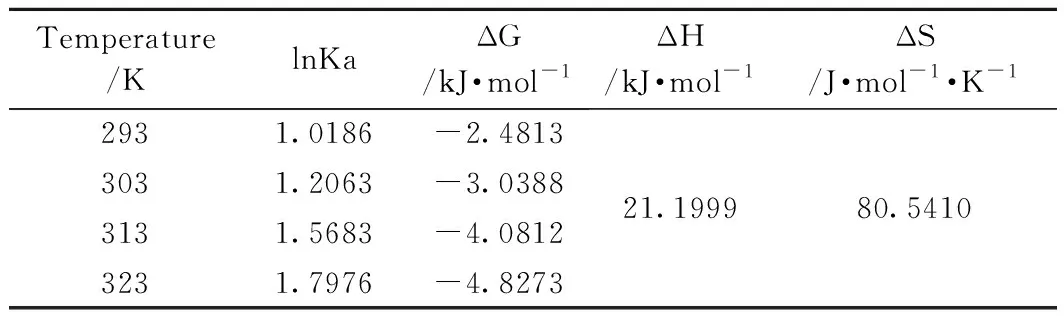
表4 吸附热力学参数Table 4 Values of adsorption thermodynamic parameters
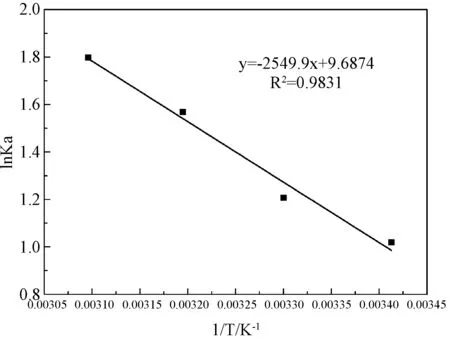
图8 lnKa与1/T的关系曲线Fig.8 lnKa-1/T curve
由表4可知,自由能ΔG为负值,说明在自然条件下吸附能自发进行。焓变ΔH为正值,说明吸附过程是吸热过程,升高温度有利于吸附进行。若焓变ΔH在2.1~20.9kJ/mol之间,吸附为物理吸附;若焓变ΔH在20.9~418.4kJ/mol之间,吸附为化学吸附[30]。Fe-MSB吸附磷的焓变ΔH约为21.2kJ/mol,说明吸附主要以化学吸附为主。离子交换的焓变通常小于8.4kJ/mol[31],Fe-MSB吸附磷的焓变ΔH不在这个范围内,说明吸附反应还存在离子交换之外的吸附机理[27]。各种作用力引起的吸附热范围分别为:范德华力是4~10kJ/mol,偶极间作用力是2~29kJ/mol,氢键力是2~40kJ/mol,疏水键力约为5kJ/mol,配位基交换约为40kJ/mol,化学键力大于60kJ/mol[32]。由此推断吸附过程作用力是以氢键力和偶极作用力为主。ΔS为正值,说明吸附过程不可逆。因此Fe-MSB对磷的吸附主要以化学吸附为主,其吸附过程是一个自发进行、吸热、不可逆过程,随着温度升高,固液界面上的分子运动混乱度会加剧,有利于吸附进行。
4 结 论
采用高效微波辐射法以Fe2(SO4)3为改性剂对钠基膨润土进行改性,制备Fe-MSB,通过该吸附剂的XRD和SEM表征分析其吸附性能。采用单因素实验,探讨吸附剂投加量、初始pH值、温度和振荡时间对吸附过程的影响,确立最佳吸附条件。并对吸附过程进行吸附动力学和吸附热力学分析,探索吸附规律和吸附机理,得出以下结论:
1.采用高效微波辐射的方法,以Fe2(SO4)3为改性剂制备的Fe-MSB层间距变大,表面粗糙、多孔、松弛,吸附性能明显提高;
2.Fe-MSB吸附磷的最佳反应条件为:Fe-MSB投加量为20g/L、初始pH=6、温度为303K和振荡吸附时间为120min,在此条件下Fe-MSB对磷去除率为98.72%;
3.准二级动力学模型能够很好地描述Fe-MSB吸附磷过程,吸附规律符合Langmuir 等温吸附方程,磷在Fe-MSB上的吸附主要以化学吸附为主,吸附过程是一个可自发进行、吸热且不可逆的过程。
