线性探针技术诊断HIV/结核分枝杆菌感染者结核菌耐药性效能评价
2019-01-03韦善求麻秋英罗顺达倪祖彥韦善君
韦善求,麻秋英,罗顺达,倪祖彥,韦善君
结核病是HIV感染者最常见的机会性感染疾病,也是艾滋病患者死亡的重要原因之一。WHO数据显示,2015年约35%的艾滋病相关死亡病例是由于结核病所致,在资源受限地区有近50%患者死亡前没有得到诊断[1-2]。临床研究显示早期诊断和有效的抗结核治疗是降低HIV/结核分枝杆菌(Mycobacterium tuberculosis, MTB)感染者病死率的重要措施[3]。目前传统分离培养和药物敏感(药敏)试验仍然是我国诊断和评判结核病疗效的主要手段与金标准,但过程长达2~3个月,不能满足临床快速诊断需要。近年来DNA测序技术在MTB及其耐药性诊断中得到推广应用,其检验结果直观可靠,能在1周内完成检测,但对实验室设施及技术要求高,难以在基层医疗机构推广应用。线性探针技术(line-probe assay, LipA)是基于核酸杂交的一种检测技术,通过检测MTB耐药特定基因rpoB的8l bp核心区域、katG密码子和inhA启动子的基因突变,预测RFP、INH耐药表型。常用的试剂盒是GenoType MTBDRplus,可以对涂阳痰标本或分离株进行检测,在6 h内获得结核病及耐多药结核病的诊断。该技术操作难度不大,具有二级以上生物安全资质的普通基因检测实验室均可以开展。LipA应用于肺结核病患者的耐药性检测具有较高的敏感度和特异性,是WHO推荐应用的分子生物学方法之一[4]。
HIV感染者免疫系统严重受损,继发MTB感染的病理改变与HIV阴性MTB感染者的表现差异显著。LipA应用于HIV/MTB感染者的MTB耐药检测是否与结核病总体人群一致值得探讨。本研究采用GenoType MTBDRplus试剂盒对HIV/MTB感染者涂阳痰标本及临床分离株进行检测,以评价LipA对HIV/MTB感染者的检测效能,同时进一步了解广西地区HIV/MTB感染者耐药MTB的基因型特征,为抗结核治疗和耐药防控提供理论依据。
1 材料与方法
1.1 标本来源 检测标本取自2012年1月—2017年12月在南宁市第四人民医院、柳州市龙潭医院及广西疾病预防控制中心治疗的HIV/MTB感染者148例,其中107例为药敏试验的临床分离株,41例为涂阳痰标本(金铵“O”或萋尔-尼尔逊染色),质控菌株H37Rv(ATCC27294)由中国疾病预防控制中心结核病参比实验室提供。纳入标准:①HIV感染的诊断依据《艾滋病诊疗指南(第三版)》[5];②MTB的诊断依据《肺结核诊断和治疗指南》[6]。排除标准:排除非结核分枝杆菌感染的患者。
1.2 仪器与试剂 萋尔-尼尔逊及金铵“O”染色液、改良罗氏培养基、药敏试验及菌型鉴定采用的培养基均购自珠海BASO公司,培养基内药物终浓度为异烟肼(isoniazid, INH)1 μg/ml和10 μg/ml, 利 福 平(rifampicin, RFP)50 μg/ml和250 μg/ml,对硝基苯甲酸 500 μg/ml,GenoType MTBDRplus试剂盒购自德国Hain Lifesciences公司;RCR扩增仪购自Biometra;TwinCubator杂交仪购自Hain Lifesciences公司。
1.3 检测方法
1.3.1 分离培养、药敏试验和菌型鉴定依据《结核病实验室标准化操作与网络建设》操作[7],LiPA依据GenoType MTBDRplus试剂盒说明书进行。
1.3.2 耐药判定及其相关定义 rpoB+katG和/或inhA突变判定为耐多药(multi drug resistant,MDR);katG 或inhA突变判定为耐INH;rpoB突变判定为耐RFP;无rpoB、katG和inhA突变判定为敏感;MDR是指对一种以上的抗结核药物至少包括RFP和INH同时耐药。
1.3.3 耐药基因扩增及测序 测序DNA制备与LipA核酸制备方法一致, H37Rv的katG、inhA基因序列来自GeneBank数据库(http://www.ncbi.nlmnih.gov),根据基因序列设计引物(表1)。引物的合成、DNA扩增和测序由上海生工生物公司完成。采用DNAman 8.0软件中的Multiple Alignment将测序结果与H37Rv株基因序列进行比对,确定基因突变位点。

表1 katG、inhA基因片段PCR扩增用的引物序列Table 1 Primers used to amplify fragment of katG and inhA
1.4 质量控制 每批号试剂检测均用H37Rv标准株和阴性对照随标本一起检测。
1.5 统计学处理 运用SPSS 19.0软件对数据进行处理。以药敏试验结果作为参考,2种检测方法的一致性分析采用kappa一致性分析,kappa值表示不同级别的一致性:0~0.20,极低的一致性;0.21~0.40,一般一致性;0.41~0.60,中等一致性;0.61~0.80,高度一致性;0.81~1,几乎完全一致。P<0.05为差异有统计学意义。
2 结 果
2.1 涂阳痰标本及临床分离株耐药MTB检测 在41例涂阳痰标本中,LipA检出MTB 37例,2例阴性,2例结果无法判读;LipA检出的MTB株中,11株显示突变信号,其中MDR 5株、单耐INH 3株、单耐RFP 3株。对痰凃阳标本进行传统培养与鉴定,37例检出MTB,1例检出非结核分枝杆菌,3例无细菌生长,药敏试验检出MDR 5株、单耐INH 3株、单耐RFP 3株。2种耐药检测方法的结果见表2。

表2 37株MTB LipA检测及药敏试验结果(株)Table 2 Results of LipA results and drug sensitivity test from 37 MTB samples(strains)
107株临床分离菌中LipA检出MTB 98株,7例阴性,2例结果无法判读;98株MTB中,24株显示突变信号(MDR 9株、单耐INH 12株、单耐RFP 3株),74株敏感。药敏试验检出MDR 8株,单耐INH 11株,单耐RFP 4株,敏感75株,见表3。

表3 98株MTB LipA检测及药敏试验结果(株)Table 3 Results of lipA and drug sensitivity test from 98 MTB samples(strains)
2.2 LipA与药敏试验结果比较 从临床分离株和涂阳痰标本中均检出MTB 135株。LipA和药敏试验均检出RFP耐药20株。RFP耐药株中,LipA检出MDR 14株、单耐RFP 6株,与药敏试验结果完全一致;INH耐药株中,LipA检出相关突变29株(包括MDR 14株、单耐INH 15株),药敏试验检出耐药菌27株,见表4。
2种检测方法结果不一致4株,其中各有1株LipA检测为rpoB+inhA、inhA及katG突变株而药敏试验显示为INH敏感,1株药敏试验显示INH耐药而LipA未检出katG或inhA突变。2者的一致性分析,LipA检测INH耐药、敏感的边际频率分别是0.21、0.78;药敏试验检测INH耐药、敏感的边际频率分别是0.20、0.80,kappa=0.969(μ=64.17,≥95%标准正态分位数1.96,故P<0.05)。依据一致性强度的参考判断指标,认为2种检测方法结果一致性极高。

表4 LipA和药敏试验检测135株MTB的INH耐药性(株)Table 4 INH-resistance from 135 MTB detected by LipA and drug sensitivity test(strains)
在临床分离株中,LipA检出3株INH耐药相关突变,而药敏试验显示INH敏感(图1)。进一步采用基因测序法进行验证,结果显示12号菌株katG在315位点发生了点突变, AGC>ACC(图2A);13和14号株在inhA启动子-15位点存在C>T突变(图2B)。测序结果表明LipA检测突变基因可信度高。
2.3 耐药菌株基因突变类型、位点与频率 2批标本中,LipA共检测到rpoB突变20株(14.81%),katG或inhA突变29株(21.48%)。rpoB、katG及inhA突变类型、位点与频率见表5。
3 讨 论
LipA是WHO新推荐应用相对快速的耐多药结核病诊断方法。有研究以药敏试验结果为标准,同时用LipA检测武汉地区MTB对RFP和INH的耐药性,2者的kappa值分别为0.94和0.85(P<0.05)[8],说明LipA与药敏试验结果差异无统计学意义。本研究结果显示:LipA检测涂阳痰标本和临床分离株中MTB对RFP的耐药性与药敏试验结果完全一致,对INH耐药的检测一致性强度也达到极高级(kappa=0.969),与文献所报道的结核病总体人群的检测结果一致。说明LipA对HIV/MTB双重感染中MTB的耐药性也具有良好的检测效能,特别是检测痰标本不须要经过分离培养程序,可以提高诊断速度,这对于HIV/MTB双重感染的及时诊断和治疗具有更重要意义。
在结核病总体人群中,INH耐药株中约有34.6%~94.3%与katG 315位点突变相关,2.9%~21.5%在inhA启动子区域发生突变;RFP耐药株中超过95%是在rpoB耐药决定区发生突变[9]。例如,云南和河南省INH耐药株中katG 315、inhA及katG 315+inhA突变的频率是92.80%、11.20%、4.00%和73.50%、35.64%、9.20%[10-11],徐州市、浙江省rpoB突变株中,S531L位点的突变频率是61.0%和64.66%[12-13]。本研究中INH耐药株中katG 315位点和inhA的突变频率分别占82.76%和17.24%,katG 315位点的突变频率与云南省相近,而inhA突变频率远低于河南省,未见katG 315+inhA突变型;在20株 RFP耐药菌中,全部突变均发生于rpoB耐药决定区,其中S531L占80.00%,高于徐州市和浙江省。本研究中INH、RFP耐药的主要基因突变型与结核病总体人群基本一致,但突变类型少于结核病总体人群,可能与样本量少有关;其次HIV/MTB感染者抗结核治疗时间一般较HIV阴性MTB感染者短,发生耐药突变的比率也相对低;此外还可能与不同地区MTB耐药的基因突变类型差异有关。鉴于HIV/MTB感染者MTB耐药性与结核病总体人群相近,当临床难以获得其病原菌耐药性诊断时,治疗用药可适当参考当地结核病总体人群的耐药参数。
本研究中有3例INH耐药相关突变而药敏试验显示INH敏感,1例INH耐药而未检测到katG或inhA突变。MTB对INH产生耐药与多个功能基因(如inhA、kasA、ndh、katG等)和调控因子(如mabA-inh启动子和oxyR-ahpC)的突变、缺失及插入有关,此外还有外排泵机制以及其他未知的机制等。LipA只是针对katG和inhA启动子区域的基因突变检测INH的耐药性,所以出现药敏试验与基因型耐药结果不一至的情况也可以理解。目前使用的基因测序法仅能检测出耐药亚群比例为20%以上的耐药MTB,远不及表型耐药检测达到1%的敏感度[14]。由此推测当耐药亚群比例低于20%时,LipA也同样存在漏检的可能。

图1 LipA检测显示突变信号的INH敏感标本12为katG突变(药敏试验INH敏感);14为inhA突变(药敏试验INH敏感);13为rpoB+inhA突变(药敏试验RFP耐药而INH敏感)Figure 1 Mutation signals of INH-sensitive isolates by LipA

图2 药敏试验与LipA法检测结果不一致菌株的测序结果katG-12株系代表第12号菌株,pinhA-13/14株系代表13和14号菌株Figure 2 Sequencing results of isolates that are inconsistent between LipA and drug sensitivity test
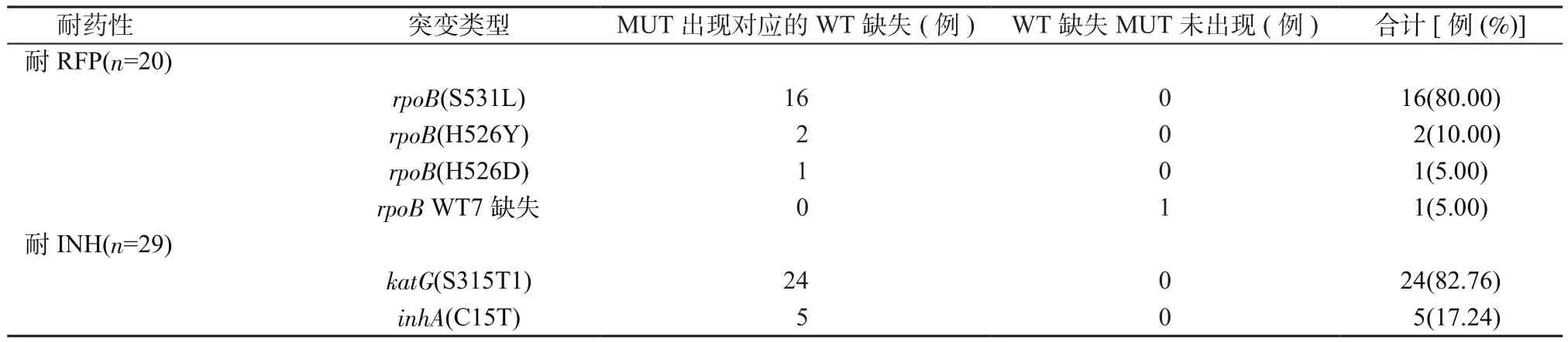
表5 INH和RFP耐药突变位点Table 5 Mutation sites in the INH- and RFP-resistant MTB
而另一项研究发现,在药敏试验中通常耐药性MTB的生长速率较慢,在体外培养中容易被生长速率快的非变异群体掩盖[15],导致耐药株在群体中的比例变小或消失,使药敏试验显示敏感。在分子水平检测的LipA则可以探测到被掩盖的突变基因型,对药敏试验有补充作用。而仅采用一种方法评价MTB耐药特征会存在漏检或评价不全面的可能。
对于HIV/MTB双重感染者而言,及时治疗至关重要,可先采用LipA检测菌株对一线抗结核药物的耐药性,随后还是要采用药敏试验进一步诊断,以指导合理及正确用药。对于具有典型耐药相关基因(如katG和inhA)突变而暂时保持药物敏感性的菌株,要多关注其耐药变化,以便指导及时调整治疗。
由于本研究样本量有限,能观察到的耐药基因突变类型和位点相对欠缺,有待增大标本量进一步观察。本研究中有7株经培养初步鉴定为MTB而LipA检测为阴性的标本,我们未采用其他检测方法进一步验证。由于艾滋病合并结核病患者中非结核分枝杆菌感染的占比可达到40%~50%,而临床实验室主要是采用选择性培养的方法进行鉴定,其结果判定受多种因素影响。因此,对于LipA检测为阴性的菌株应考虑采用基因芯片和测序等其他技术进一步验证。
总之,LipA检测MTB耐药性具有高度敏感性和特异性,可以直接检测涂阳痰标本,适用于HIV/MTB双重感染MTB耐药性的快速筛查,且对药敏试验诊断具有良好的补充作用。
志谢感谢广西疾病预防控制中心结核病防治所覃慧芳老师、广西龙潭医院中心实验室曾蓉老师对本研究的帮助
