基于羧酸酯酶降解伏马毒素研究
2019-01-02陈亭亭张巧艳杨兰花杨胜利袁玉伟
■陈亭亭 张巧艳* 王 坡, 林 琳 杨 华 杨兰花 杨胜利 袁玉伟
(1.浙江省农业科学院农产品质量标准研究所,浙江杭州310021;2.浙江工业大学药学院,浙江杭州310014;3.上海市质量监督检验技术研究院,上海200233;4.义乌出入境检验检疫局,浙江义乌322000)
伏马毒素(Fumonisins,FBs)是由层生镰刀菌(Fusarium proliferatum)、轮状镰刀菌(Fusarium verticillioides)等丝状真菌产生的水溶性代谢产物[1],分子结构见图1。与绝大多数真菌毒素不同的是,它缺乏环状结构,但仍具有很强的毒性[2]。其中,伏马毒素B1(Fumonisin B1,FB1)污染率最高,占伏马毒素总量的70%~80%,且危害最大,具有致畸性、致癌性,可诱发人类食管癌、猪肺水肿、马脑白质软化等症[1-3]。猪长期摄入低剂量伏马毒素污染的饲料还将导致日增重下降和免疫抑制[4]。近年来,调查显示,玉米、大豆、小麦、DDGS饲料和全价饲料中伏马毒素是主要的污染物[5]。2014年,我国华东地区抽检的仔猪配合饲料中伏马毒素检出率为83.3%,雏禽、蛋禽配合饲料污染率达100%[6]。为了减少污染危害,美国FDA规定动物饲料中伏马毒素的限量范围为5~100 mg/kg[7]。我国即将实施的《GB 13078—2017饲料卫生标准》特别新增了伏马毒素的限量要求,其中猪饲料中的限量为5 mg/kg,牛饲料中的限量为50 mg/kg[8]。
饲料中伏马毒素的污染不仅影响畜禽健康养殖,而且将通过食物链长期威胁人类健康。高效安全的脱毒方法受到养殖企业、饲料企业以及兽医专家的广泛关注。大多数物理和化学脱毒法容易破坏饲料的营养成分,改变适口性,从而影响动物产品的品质和产量;一些处理试剂的残留蓄积还会带来二次污染而造成不可估量的安全隐患。生物法脱毒包含微生物法和酶法。酶法因具有专一性强、反应条件温和、操作简单、相对安全等特点而广受青睐,而且酶制剂相对于微生物制剂更容易保存,可直接以饲料添加剂形式用于畜禽生产中。本研究从缓冲体系、反应温度、酶浓度、底物浓度等方面首次探索了一种羧酸酯酶对FB1的降解规律(见图1),旨在为伏马毒素酶法脱毒的实际应用提供科学指导。
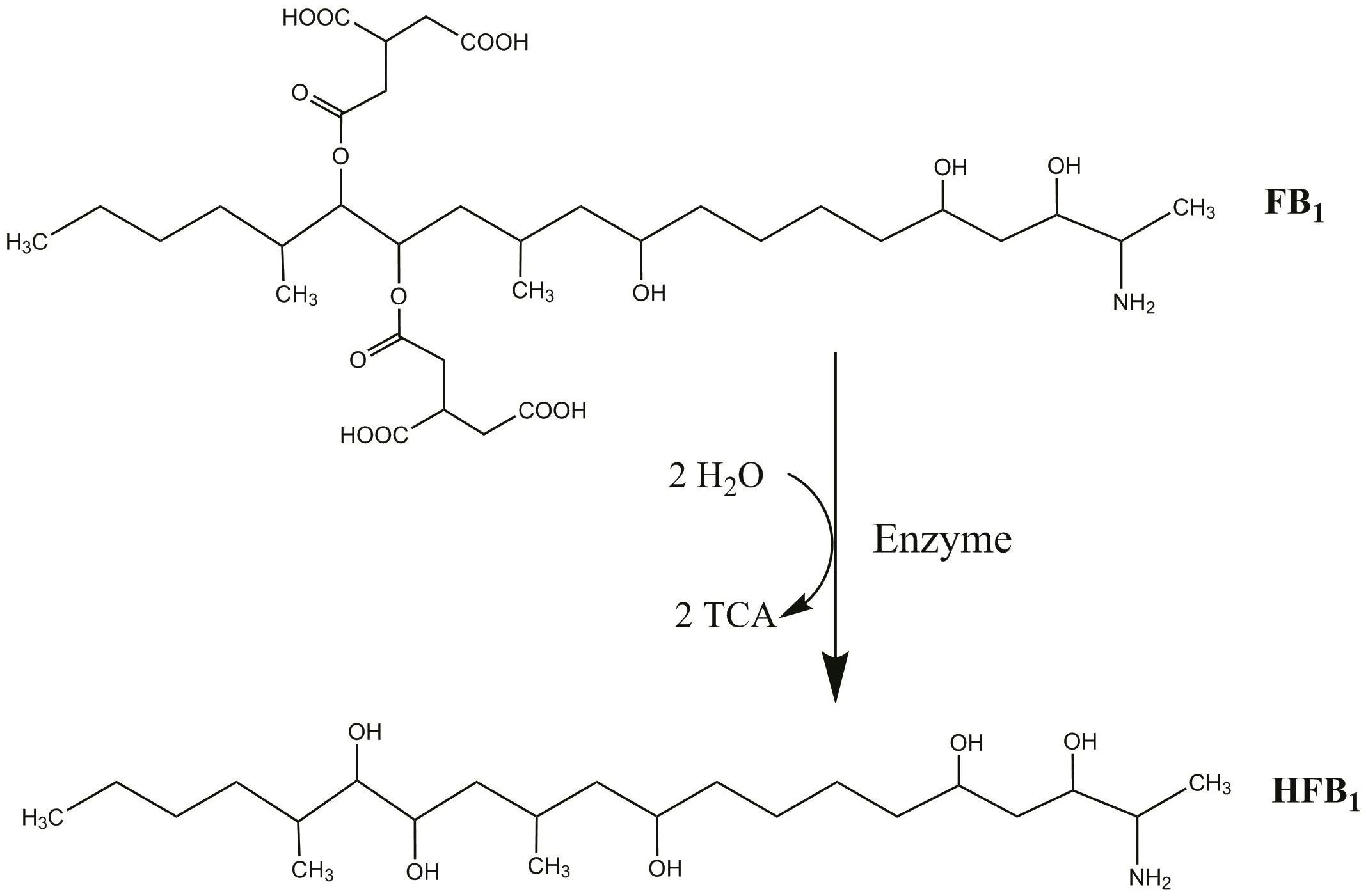
图1 伏马毒素B1酶解示意图
1 材料与方法
1.1 试验材料
FB1标准品购自青岛普瑞邦生物工程有限公司;牛血清白蛋白(BSA)购自上海源叶生物科技有限公司;甲醇、乙腈为色谱纯,购自德国默克公司;其他试剂均为国产分析纯。羧酸酯酶:从养殖场附近的土壤中筛选获得一株革兰氏阴性细菌,具有伏马毒素降解活力,经摇瓶发酵、初步纯化制得粗酶。
1.2 检测方法
1.2.1 仪器条件
采用柱前衍生高效液相色谱-荧光法检测。色谱柱:Agilent HC-C18(250 mm×4.6 mm,5 μm);流动相:A相为0.05 mol/l柠檬酸钠缓冲液(pH值4.0),B相为甲醇;梯度洗脱条件:0~2 min,55%B;2~4 min,55%B~75%B;4~9 min,75%B~90%B;9~9.5 min,90%B;9.5~13 min,90%B~55%B;13~15 min,55%B;流速:1.0 ml/min;激发波长335 nm,发射波长440 nm;进样量:50 μl;柱温:35 ℃。
1.2.2 样品处理
取一定体积的待测液,适当稀释,与反应液Ⅰ和反应液Ⅱ等体积混合衍生,过膜后检测。反应液Ⅰ:14 μl β-巯基乙醇溶于 4 ml 0.1 mol/l硼酸钠缓冲液(pH值9.1);反应液Ⅱ:称取10 mg邻苯二甲醛,溶于1 ml甲醇中,再加入3 ml 0.1 mol/l硼酸钠缓冲液(pH值9.1),混匀。其中反应液Ⅱ在室温下可稳定1周[9]。
1.2.3 HFB1制备
取0.5 ml 200 μg/ml FB1甲醇溶液,与10 ml 1 mol/l KOH溶液混合,70℃孵育1 h,冷却后用2 mol/l HCl溶液将pH值调至4.5。将反应液用HLB柱净化,获得浓度为11.2 μg/ml的HFB1甲醇溶液,用作液相分析HFB1含量的参考标样[10-11]。
1.3 试验方法
1.3.1 相关定义
酶活定义:在30℃、pH值8.0条件下,每分钟从10 μg/ml FB1中降解1 μg FB1所需的酶量定义为1个酶活单位(U)。FB1降解率定义:FB1的降解量与原始添加量之比,用百分比表示。HFB1生成率定义:HFB1的生成量与FB1完全转化成HFB1的理论值之比,用百分比表示。结果均为3次测定的平均值。
1.3.2 缓冲体系
配制磷酸钾缓冲液(20 mmol/l,pH值8.0)、Teorell-Stenhagen缓冲液(20 mmol/l,pH值8.0)[12]、Tris-HCl缓冲液(20 mmol/l,pH值8.0),以及系列不同pH值的20 mmol/l Teorell-Stenhagen缓冲液(pH值3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0),分别在2 ml缓冲体系中加入FB1(10 μg/ml)、BSA(0.1 mg/ml)和酶(20 U/l),30 ℃孵育3 h,沸水浴灭活10 min,取样检测,比较降解效果。
1.3.3 反应温度
制备2 ml反应体系[FB110 μg/ml,BSA 0.1 mg/ml,酶20 U/l,Tris-HCl缓冲液(20 mmol/l,pH值8.0)],分别在20、30、40、50、60、70、80 ℃中孵育3 h,沸水浴灭活10 min,取样检测,比较降解效果。
1.3.4 酶浓度
在 2 ml反应体系[FB110 μg/ml,BSA 0.1 mg/ml,Tris-HCl缓冲液(20 mmol/l,pH值8.0)]中,添加粗酶至终浓度分别为:1、10、20、40、100 U/l,30 ℃孵育0、0.5、1、2、3、4、6、8、12、16、20、24 h,沸水浴灭活10 min,取样检测,比较降解效果。
1.3.5 底物浓度
在2 ml反应体系[BSA 0.1 mg/ml,酶 20 U/l,Tris-HCl缓冲液(20 mmol/l,pH值8.0)]中,添加底物FB1至终浓度分别为:1、5、10、20、50、100 μg/ml,30 ℃孵育0、0.5、1、2、3、4、6、8、12、16、20、24 h,沸水浴灭活10 min,取样检测,比较降解效果。
2 结果
2.1 缓冲体系的影响
缓冲盐和pH值会影响酶、底物的解离程度,从而影响酶分子对底物分子的结合和催化。FB1的酶解在不同的缓冲体系中进行,结果发现,Tris-HCl缓冲液有利于FB1的酶解,3 h的降解率达到47.08%,磷酸钾缓冲液仅次之,Teorell-Stenhagen缓冲液效果最差(降解仅32.32%)。但由于Teorell-Stenhagen缓冲液具有相对较宽的缓冲范围(pH值2.0~12.0)[12],被进一步用于考察酶解反应的最适pH值。由图2可知,该酶最适反应pH值8.0,此时FB1降解率和HFB1生成率基本达到最高值。整体上看,FB1随pH值变化的降解规律与HFB1生成规律基本一致,但降解率曲线与生成率曲线不完全重合,推测FB1酶解过程存在中间产物。Heinl等[1]也曾发现FB1的酶解产物除了HFB1外,还存在两种结构不同的部分水解型伏马毒素B1(pHFB1)。而且,中间产物在降解产物中的比例可能与缓冲体系的pH值紧密相关,碱性条件相比酸性条件显然更有利于FB1的完全转化,可以解释为:FB1通过羧酸酯酶水解生成HFB1、pHFB1和TCA,TCA能与碱发生中和反应,促进整个反应向生成HFB1的方向进行。另外,当缓冲液的pH值小于3.0或大于11.0时,该酶几乎无法降解FB1,可能过酸或过碱的条件不适宜酶与FB1的结合、催化,或者此时酶已变性失活。
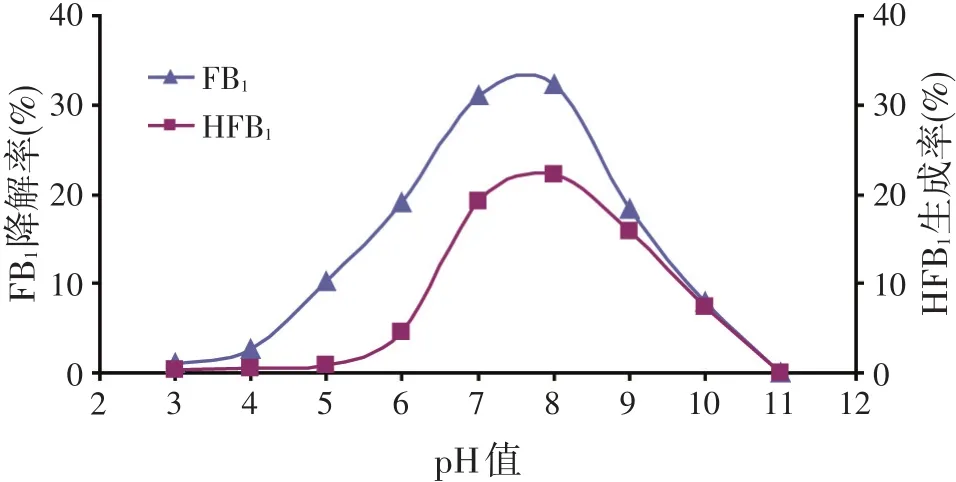
图2 反应pH值对伏马毒素B1酶解的影响
2.2 反应温度的影响
酶促反应具有温度依赖性,因为反应温度会影响分子运动、酶的活力和底物亲和力。一方面,升高温度可以增加酶促反应速度;另一方面,温度过高会导致酶蛋白变性失活。FB1的酶解在不同的温度下进行,由图3可知,最适反应温度为30℃。涉及的羧酸酯酶具有较宽的温度适应性,在20~70℃范围内均有降解活力,高于80℃时,FB1降解率几乎为零,可能高温不利于FB1的水解反应或者此时酶已失活。另外,随反应温度的变化,FB1降解和HFB1生成具有相似的趋势,但降解率与生成率不一致,进一步证实中间产物的存在,并推测中间产物的生成量与反应温度紧密相关。
2.3 酶浓度的影响
通常,当底物分子浓度足够时,酶分子越多,底物转化的速度越快。固定底物浓度为10 μg/ml,在最适条件(pH值8.0、30℃)下进行FB1的酶解反应,考察不同酶浓度下的降解规律。由图4可知,在酶解起始阶段,随着酶浓度的增加,同一时间的降解率增加。计算反应3 h的平均速率,当酶浓度低于40 U/l时,降解速率与酶浓度成正比;当酶浓度为100 U/l时,降解速率增幅较小,可能此时底物分子趋向于被酶分子所饱和。较低的酶浓度(1 U/l)下反应1 d,仍有36.91%的FB1残留。较高的酶浓度(100 U/l)下反应2 h,FB1的降解率已达到91.70%;反应3 h以后,FB1的降解率和HFB1的生成率趋于100%,显然此时FB1被完全转化成HFB1,而HFB1没有进一步降解为其他产物,说明该酶专一性作用于酯键。当酶浓度为20 U/l时,反应8 h就能获得较好的降解效果,此时FB1残留仅剩10%左右。进一步观察发现,在该酶浓度下,反应前期(20 h前),降解率始终大于生成率,说明中间产物的存在;反应后期(20 h后),降解率几乎等于生成率,推测FB1酶解生成HFB1的反应是不可逆的,随作用时间的延长,中间产物pHFB1也能被完全水解成HFB1。

图3 反应温度对伏马毒素B1酶解的影响

图4 酶浓度对伏马毒素B1酶解的影响
2.4 底物浓度的影响
一般随底物浓度升高,酶促反应速度先升高后不变。固定酶浓度为20 U/l,在最适条件(pH值8.0、30℃)下进行FB1的酶解反应,考察不同底物浓度下的降解规律。由图5可知,在酶解过程中,随着FB1浓度的增加,同一时间的降解率降低,可能过多的底物分子阻碍了酶分子的结合、催化。以图5数据计算反应3 h的平均速率,绘制底物浓度(S)与降解速度(V)的关系曲线,发现当FB1浓度低于50 μg/ml时,降解速率随底物浓度的增加而增加,呈正比关系,表现为一级反应;高于50 μg/ml时,降解速率基本保持不变,表现为零级反应,说明此时酶已被底物完全饱和。由米氏方程推出:,绘制1/V-1/S关系曲线,可得:最大降解速率Vmax为0.148 μmol/(l·min),米氏常数Km为33.2 μmol/l。HFB1的生成规律与FB1的降解规律随底物浓度变化的相关性趋势基本一致,但同一时间的生成率几乎都小于降解率,直至反应1 d时FB1才完全转化成HFB1,反映了FB1的酶解程度与作用时间紧密相关。反应8 h,浓度低于20 μg/ml的FB1降解率在90%以上;反应20 h,各种浓度的FB1均能被降解。
2.5 实际应用

图5 底物浓度对伏马毒素B1酶解的影响
从超市、农贸市场、养殖场、饲料企业获得25份玉米粉,用李为喜等[13]的方法进行样品前处理,用柱前衍生高效液相色谱-荧光法检测,筛选获得1份FB1含量为18.26 mg/kg的试样,其液相色谱图见图6(B)。取5 g玉米粉试样,以料液比1∶1.5加入20 mmol/l Tris-HCl缓冲液(pH值8.0)(包含20 U/l酶和0.1 mg/ml BSA),充分混合,在最适条件(pH值8.0、30℃)下静止反应1 d,FB1仍有35.67%残留;静止反应2 d,FB1完全转化成HFB1[图6(C)]。假设玉米粉试样中所有FB1均浸出于缓冲液中,估算底物浓度为12.17 μg/ml。由图5可知,当 FB1浓度为 10 μg/ml时,反应 8 h,降解率为94.57%;反应20 h,降解率达到100%。推测玉米粉酶解过程中,固体基质的存在严重干扰了酶分子与底物分子的作用,从而影响了酶解效率。以后将优化料液比,增加搅拌等措施,使酶分子与底物分子充分接触,缩短完全降解时间。
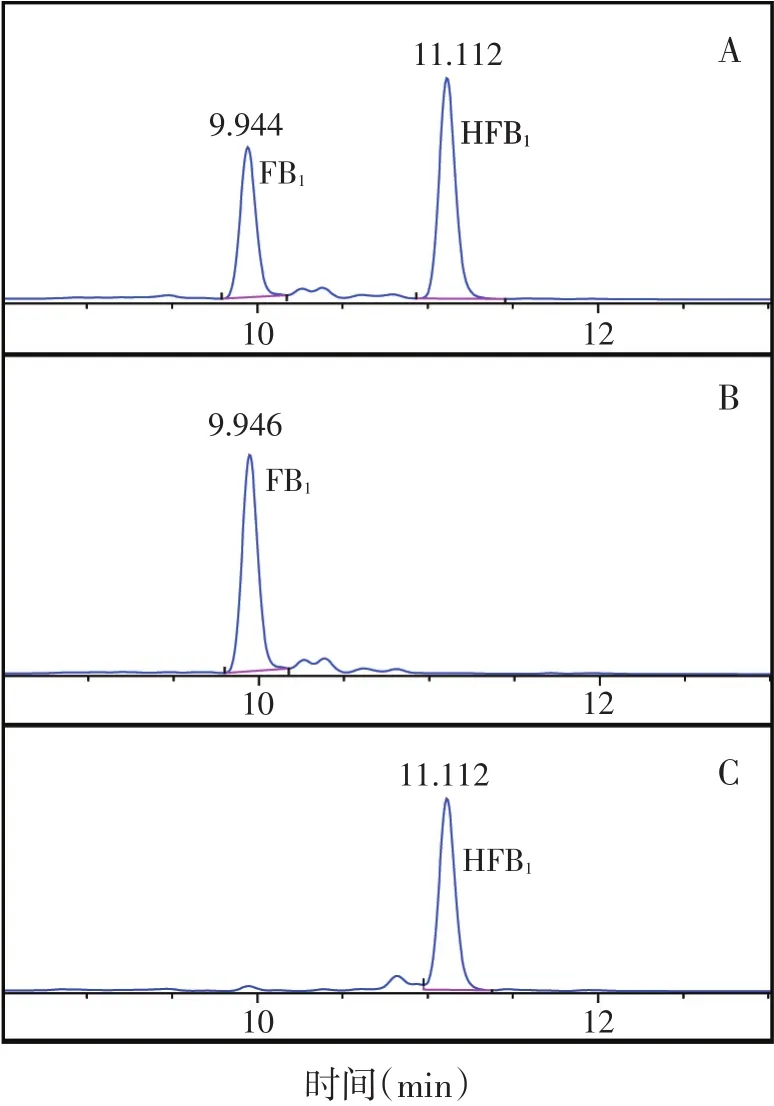
图6 玉米粉伏马毒素B1酶解前后液相色谱图
3 讨论
DDGS(Distillers'dried grains with solubles)是酿酒酵母发酵玉米等谷物生产酒精的主要副产物,蛋白含量高(约30%~35%),营养价值好(富含氨基酸、维生素、矿物质和多糖),且产量较大、成本较低,近几年已逐渐成为一种高需求的动物饲料[14]。然而,玉米原料容易被伏马毒素污染,加上酵母细胞壁和原料中的矿物质会富集真菌毒素(发酵后FB1含量增加1.37~1.94倍),导致DDGS的安全性受到影响[15-16]。在发酵中添加降解毒素的酶制剂,可实现生产过程脱毒。按玉米发酵生产酒精的工艺,一般控制发酵温度在30℃左右;而大多数酵母在微酸性环境中生长最好,发酵pH值一般控制在5.0左右[17]。本研究涉及的羧酸酯酶在pH值5.0条件下可以降解伏马毒素,最适酶解温度为30℃,能够适应发酵环境。应用羧酸酯酶,联合其他酶制剂,开发脱毒DDGS产品,有利于提升国产DDGS品质,应对进口贸易壁垒。
BSA(Bovine serum albumin)是一种常用的载体蛋白,由581个氨基酸残基组成,可与多种阳离子、阴离子和其他小分子物质结合,防止酶的分解和非特异性吸附[18]。Fornasier等[19]报道,BSA可以增加酯酶的提取得率。本研究发现,10 μg/ml FB1在20 U/l酶作用下水解3 h,不添加BSA的降解率仅有添加时的1/3,可见BSA能够显著提高羧酸酯酶的催化活力。Palacharla等[20]曾发现BSA具备捕获脂肪酸的能力。由此推测,其作用机理是:BSA与FB1水解产物TCA结合,从而促进FB1的酶解。此外,聚乙二醇(PEG)、吐温(Tween)等一些非离子型表面活性剂,在促进酶解方面展现了与BSA相当的效果[21-22]。以后将深入研究这些添加剂的作用机理,并结合不同酶浓度、底物浓度下的降解规律,开发复合型酶制剂和饲料脱毒技术,应用于畜禽养殖生产中。
4 结论
本研究涉及的羧酸酯酶具有较强的pH值和温度适应性,最适反应pH值为8.0,最适反应温度为30℃。酶解过程具有时间依赖性,且FB1的降解和HFB1的生成存在不同的规律。较低的酶浓度(1 U/l)下反应1 d,有36.91%的FB1残留;较高的酶浓度(100 U/l)下反应3 h,FB1能被完全降解。当酶浓度为20 U/l时,在最适条件下进行酶解反应,反应8 h时,浓度低于20 μg/ml的FB1降解率在90%以上;反应20 h时,低、中、高浓度的FB1均被降解。最大降解速率Vmax为0.148 μmol/(l·min),米氏常数Km为33.2 μmol/l。该酶作用于玉米粉,反应2 d,能将FB1完全转化成HFB1,应用前景广阔。
