高压均质对二十二碳六烯酸功能因子输送体系稳定性影响
2018-12-29张书文逄晓阳吕加平于景华
王 博,张书文,刘 鹭,逄晓阳,芦 晶,吕加平,*,于景华*
(1.中国农业科学院农产品加工研究所,北京 100193;2.天津科技大学食品工程与生物技术学院,天津 300457;3.甘肃工业职业技术学院,甘肃 天水 741025)
二十二碳六烯酸(docosahexaenoic acid,DHA)俗称“脑黄金”,是ω-3多不饱和脂肪酸家族的重要成员,对人体具有多种重要的生理和药理功能,如提高神经系统活性,促进脑部、视网膜发育,防治心血管疾病、炎性疾病和癌症等[1-3]。此外,DHA对婴幼儿视力完善和智力发育具有重要的意义,据报道母乳脂肪中DHA含量是牛乳的3 倍多,它们在母乳中以磷脂的形式天然存在,而牛乳作为婴幼儿奶粉的主要来源,其所含的DHA含量极少,远不能满足婴幼儿发育的正常需要[4-6]。1994年,联合国粮食及农业组织和世界卫生组织在联合专家报告《脂肪、油脂与人类营养》中推荐在婴幼儿奶粉中添加DHA,用来补充由非母乳喂养婴儿的这种重要营养物质的缺乏。2001年,美国食品药品监督管理局在GRAS Notice No.000080中批准了DHA在婴幼儿配方奶粉中的应用。
微藻油脂是一种从人工培育的海洋微藻中提取、未经食物链传递的纯植物性DHA原料,是目前世界上较纯净、安全的DHA来源。藻油中的DHA以天然的甘油三酯形式存在[7],与母乳中的多不饱和脂肪酸存在形式相同,易被人体消化吸收,生物利用率较高;我国卫生部于2010年发布第3号公告,将DHA藻油列入新资源食品,并允许其在婴幼儿食品中添加[8]。但藻油的水溶性差、密度比胃液小,直接食用易造成反胃,同时还具有令人不愉悦的鱼腥味,限制了其应用范围。另外,其含有多个双键,遇光、氧和热易发生氧化还原反应,产生的过氧化脂质等氧化产物对人体易造成极大的危害[9-10]。基于藻油的这些特点,选用合适的乳化剂制备出O/W、W/O/W型乳状液,作为DHA功能因子传递系统添加到婴幼儿配方奶粉等食品中是最为常见的方式。
美拉德反应制备的蛋白-多糖共价复合物可以提高蛋白质的溶解性、降低蛋白质过敏反应,具有良好的乳化、抗氧化、抑菌、保护心血管疾病和预防肠道炎症等功能特性,可作为多功能食品添加剂应用到食品工业中[11-15]。酪蛋白酸钠(sodium caseinate,NaCN)作为酪蛋白的一种钠盐,是一种安全无害的乳化剂和增稠剂,普遍应用于食品工业,GB/T 2760—2014《食品安全国家标准 食品添加剂使用标准》指出NaCN可作为DHA和花生四烯酸的载体添加到婴幼儿配方食品中[16];而葡萄糖(glucose,glu)是生物体内新陈代谢不可缺少的营养物质,很容易被吸收进入血液中,它的氧化反应放出的热量是人类生命活动所需能量的重要来源,因此被广泛应用于食品、医药工业。
本研究在实验室前期有关NaCN-glu美拉德反应产物(Millard reaction products,MRPs)制备工艺研究的基础上,以NaCN-glu MRPs为乳化剂,结合静态光散射、紫外-可见光谱分析技术和激光共聚焦技术等对不同的均质条件下制备出的O/W型DHA藻油乳状液的物理稳定性、氧化稳定性以及微观结构进行了分析。利用稳定性分析仪对不同均质压力下制备的乳状液的物理稳定性进行快速分析;通过测定乳状液在7、14、21 d和28 d室温贮藏期间的总氧化值(total oxidation value,TOTOX)来反映油脂的氧化程度;以尼罗红为荧光探针,利用激光共聚焦扫描显微镜(confocal laser scanning microscopy,CLSM)对乳状液的微观结构进行观察,以期筛选出制备DHA藻油乳状液的最佳工艺条件,扩大DHA藻油等水不溶性、易氧化敏感物质在婴幼儿配方奶粉等食品中的应用范围。
1 材料与方法
1.1 材料与试剂
NaCN(纯度不小于97%)、D-(+)-葡萄糖(分子质量180 Da)、Life’sTMDHA S40-O400藻油 荷兰皇家帝斯曼集团;尼罗红、过氧化氢异丙苯 美国Sigma Aldrich公司;p-茴香胺 美国Alfa Aesar试剂公司;其他试剂均为国产分析纯。
1.2 仪器与设备
T25 Digital高速剪切仪 德国IKA公司;AH100D高压均质机 ATS工业系统有限公司;SPAKK酶标仪帝肯(上海)贸易有限公司;Turbiscan AGS稳定性分析仪 法国Formulation公司;Andor Revolution XD CLSM 英国牛津仪器公司;小型超高温瞬时灭菌(ultra-high temperature instantaneous sterilization,UHT)设备 北京博华精远科技开发有限公司。
1.3 方法
1.3.1 MRPs的制备
配制质量分数为5%的NaCN溶液,充分水合后按蛋白质与糖质量比1∶1向其中加入葡萄糖,用0.2 mol/L NaOH溶液调节起始pH值为8.0;利用小型UHT设备在130 ℃下热处理15 s,得到NaCN-glu MRPs。
1.3.2 乳状液的制备
将1.3.1节得到的MRPs溶液作为水相,向其中缓慢加入质量分数10% DHA藻油(油相),在中等剪切速率下剪切3 min得初始乳状液,然后经高压均质机在35、65、95、125 MPa的均质压力下均质3 次得到最终的乳状液,冰水浴立即冷却,作为实验组NaCN-glu,4 ℃冷藏备用。以单独的NaCN为水相在相同的条件下制备DHA乳状液,记为对照组NaCN。在95 MPa下对NaCN-glu MRPs制备的初乳状液均质1、2、3、4、5 次,冰水浴立即冷却,4 ℃冷藏备用。
1.3.3 乳状液物理稳定分析
利用Turbiscan AGS稳定性分析仪对乳状液的稳定性进行快速分析。仪器采用近红外作为光源,与透射光检测器和背散射光检测检测器组成测量探头,对样品池从底部到顶部每40 μm扫描一次,在一定时间内连续扫描,获得透射光与背散射光信号对样品高度的函数曲线图,即可反映出样品中颗粒的运动趋势,根据光强度值的偏差计算出样品稳定性指数,进而预测乳状液的稳定性。取1.3.2节中制备的乳状液20 mL于样品瓶中,将样品瓶放入检测池中,检测温度设定为25 ℃,每1 h扫描一次,扫描24 h,记录扫描图谱。实验重复测定3 次。
1.3.4 乳状液氧化稳定性分析
1.3.4.1 PV的测定
参照Zou Long等[17]的方法略作改动测定乳状液的过氧化值(peroxide value,PV)。取0.3 mL样品于2 mL离心管中,加入1.5 mL异辛烷-异丙醇(体积比3∶2)溶液,漩涡振荡30 s后2 000 r/min离心5 min;取0.2 mL上清液于10 mL离心管中(以200 μL异辛烷作为空白),加入2.8 mL甲醇-正丁醇(体积比2∶1)溶液,再加入15 μL硫氰化钾和15 μL FeSO4溶液,漩涡振荡;室温避光反应20 min,用SPAKK酶标仪在510 nm波长处测OD值。PV用过氧化氢异丙苯的标准曲线(5、10、50、100、500、1 000 μmol/L过氧化氢异丙苯溶解在甲醇中)定量,计算公式如式(1)所示。
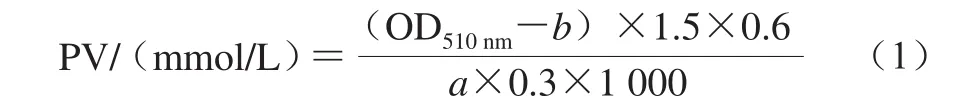
式中:OD510nm为测得样品的OD值;a为标准曲线斜率;b为标准曲线与y轴的截距。
1.3.4.2 p-AnV的测定
p-茴香胺值(p-anisidine value,p-AnV)参照AOCS Official Method Cd 18-90 American oil chemists society及文献[18]的方法测定。取2 mL样品于25 mL容量瓶中,用异辛烷定容混匀后转移到50 mL离心管中,漩涡振荡20 s后5 000 r/min离心10 min;取上清液(空白组为异辛烷),在350 nm波长处测吸光度A1。取上清液5 mL(空白组为5 mL异辛烷)于10 mL离心管中,加入1 mL p-茴香胺溶液,漩涡振荡10 s,室温下孵育10 min,350 nm波长处测吸光度A2,p-AnV计算公式如式(2)所示。
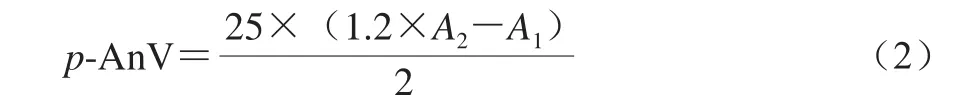
1.3.4.3 TOTOX的测定
PV和p-AnV分别表征油脂一级和二级氧化产物的含量,乳状液的TOTOX程度包括对一级和二级氧化产物的检测。用TOTOX表示乳状液中油脂的氧化程度更为全面[19],其计算公式如式(3)所示。
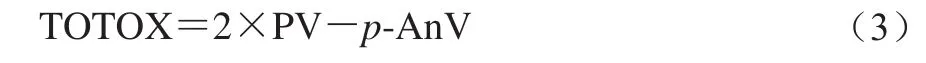
1.3.5 乳状液的微观结构观察
参照Gallier等[20]的方法略作改动。将制备好的乳状液稀释100 倍,取0.5 mL稀释乳状液加入10 μL荧光染料尼罗红,轻轻翻转混匀后避光染色20 min。取染色后的样品100 μL与琼脂(10 g/L)按体积比1∶1混合,迅速充分混匀后取10 μL染色后样品滴在载玻片上,并迅速盖上盖玻片。用CLSM观察,He/Ne激光器为激发光源,尼罗红激发波长为514 nm。
1.4 数据分析
2 结果与分析
2.1 均质压力对乳状液稳定性的影响分析
2.1.1 乳状液物理稳定性分析
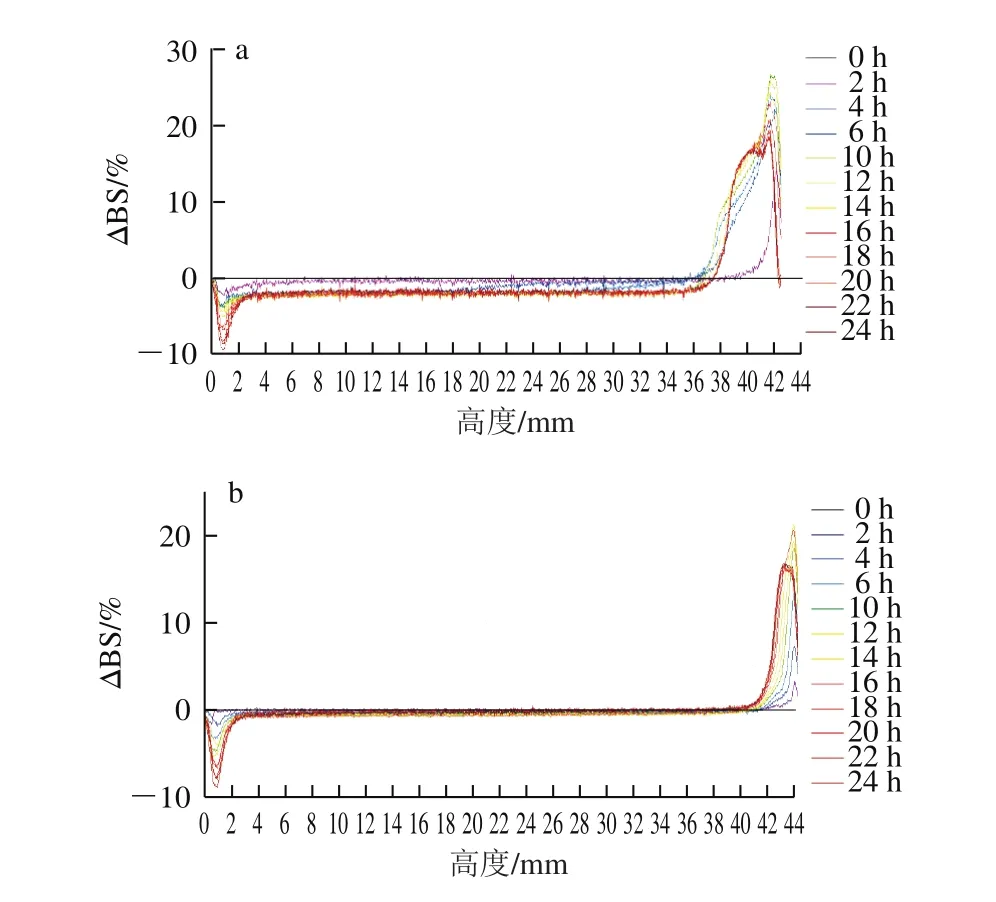
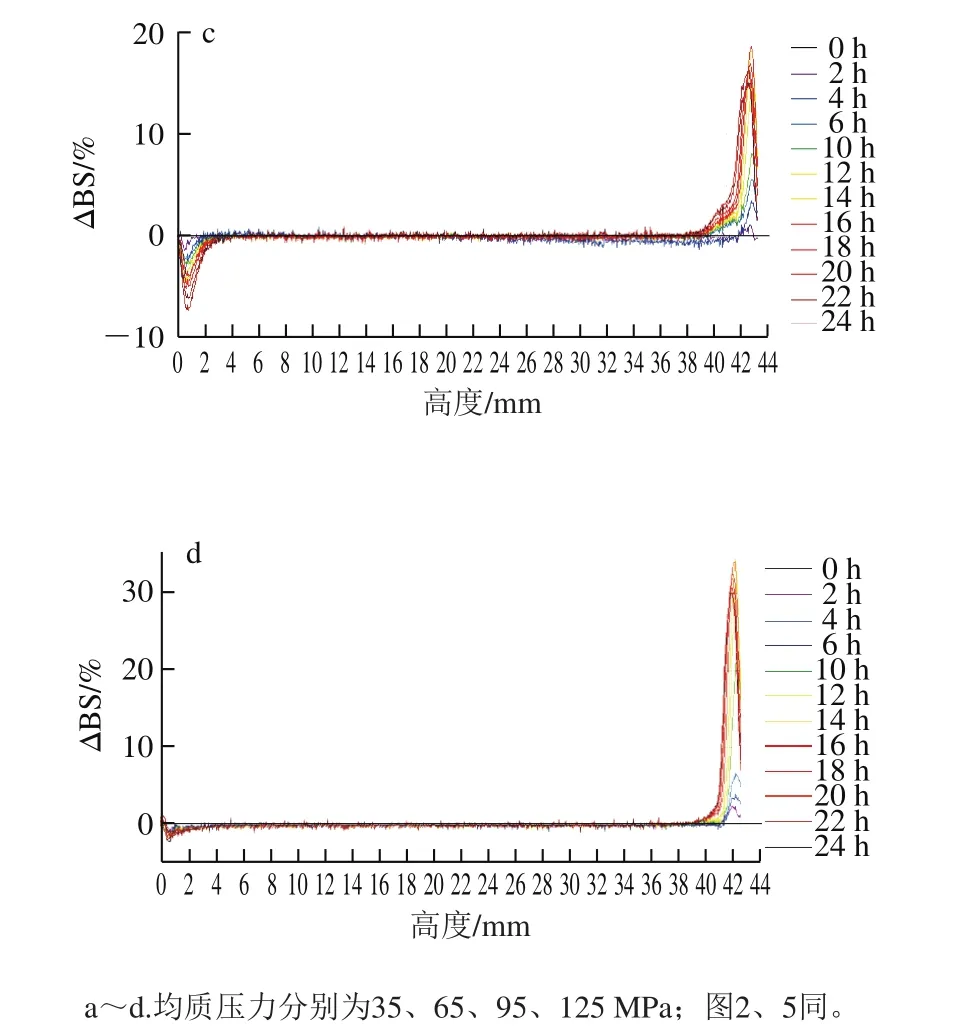
图1 不同均质压力下NaCN-glu制备的DHA藻油乳状液Turbiscan扫描图谱Fig.1 Turbiscan test of DHA algae oil emulsions prepared by NaCN-glu under different homogeneous pressures
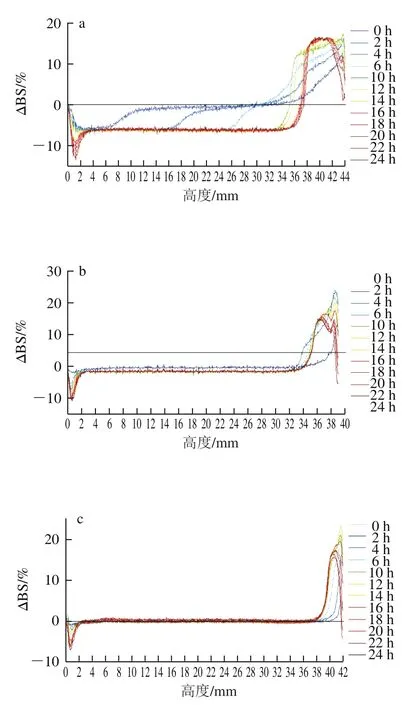
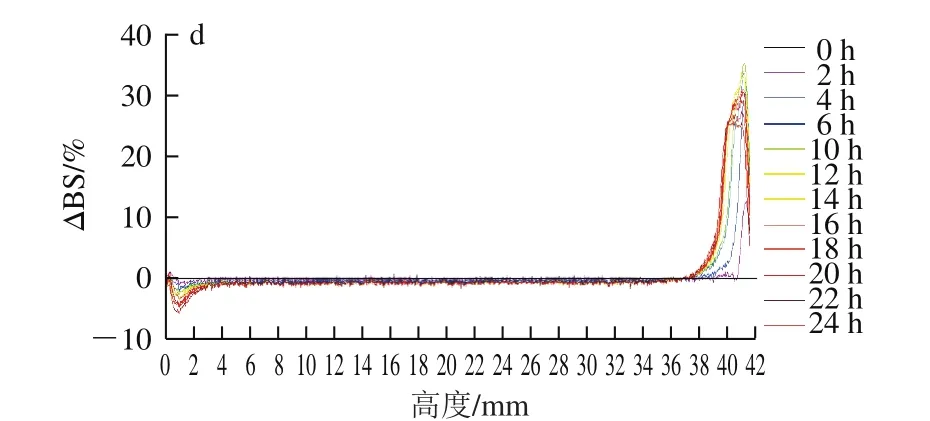
图2 不同均质压力下NaCN制备的DHA藻油乳状液Turbiscan扫描图谱Fig.2 Turbiscan analysis of DHA algae oil emulsions prepared with NaCN under different homogenization pressures
本研究制备的DHA藻油乳状液总固形物含量较高,几乎没有透射光,所以选择背散射光强度(backscattering,BS)对样品进行分析。图1、2中横坐标从左到右代表样品瓶底部、中部和顶部,纵坐标为BS差(ΔBS,以第一次扫描结果为参比)。所有样品均呈现底部的ΔBS逐渐减小后增加,顶部的ΔBS先增加后减小的趋势。根据BS随体系浓度的减小而减小的理论[21],实验组和对照组样品均在底部出现澄清层,在顶部出现脂肪上浮层,并且顶部脂肪上浮后颗粒之间发生了絮凝,使ΔBS减小;图中的峰宽代表澄清层和脂肪上浮层的厚度[22],可以看出两组样品的澄清层和脂肪上浮层的厚度在一定均质压力范围内与压力的大小成反比。
在相同的条件下,实验组NaCN-glu的顶部和底部的ΔBS、澄清层和脂肪上浮层厚度均小于对应的对照组NaCN样品,证明NaCN经美拉德反应改性后的乳化性有明显提高;图1a和图2a、b的中部BS不重合,说明颗粒粒径变化明显,但与图1a、2b相比,图2a的BS波动幅度更大,即图2a的粒径变化更大,乳状液更不稳定。实验组中,随均质压力的增加,底部ΔBS绝对值的最大值从8.24%减小到2.58%,ΔBS的绝对值越小体系越稳定,所以在一定的压力范围内,均质压力越大,样品的底部越稳定,出现底部澄清的情况越不明显,对照组也表现为同样的趋势。对于实验组,样品顶部的稳定性表现为随均质压力的增加先增大后减小的趋势,ΔBS从26.72%减小到18.77%又增大到34.38%;对照组中除图2a的底部、中部和顶部的稳定性都较差外,图2b~d的顶部稳定性与实验组表现出相同的趋势。
为更直观地对比组间、组内样品稳定性的差异,利用TurbiSoft Lab软件计算得到Turbiscan稳定性系数(Turbiscan stability index,TSI)对乳状液的整体稳定性进行分析。TSI值综合反映样品在整个放置时间浓度和颗粒粒径的变化幅度,变化幅度越大,TSI值就越大,体系就越不稳定。图3为不同均质压力下实验组和对照组样品的TSI值。实验组所有样品的TSI值均小于对照组,分别为4.75、1.70、1.55和2.10,说明NaCN-glu制备的乳状液的稳定性明显优于单独的NaCN。随着均质压力的增大,实验组样品的TSI值先减小后增大,即样品稳定性先增大后减小,与Turbiscan扫描图谱的结果一致。当均质压力大于95 MPa时,样品的稳定性减小,可能是因为均质压力过大,使油相形成的油滴过小,比表面积急剧增大,体系内的乳化剂并不足以包埋全部的油滴或不能在油滴外形成良好的保护层,没有足够的静电排斥或空间位阻作用,导致油滴间易发生絮凝、聚结和分层,甚至是相分离[23-24],所以均质压力过大反而使体系更不稳定,当均质压力为65、95 MPa时,两个样品的TSI值较小,但差异并不明显,所以均质压力控制在65~95 MPa间较好;对照组也表现出相同的趋势。
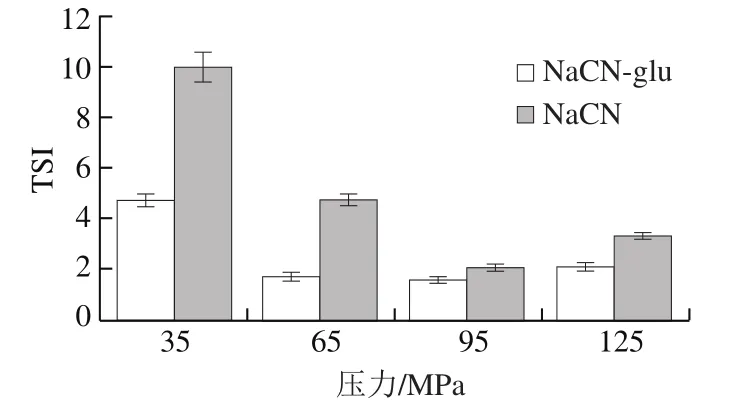
图3 均质压力对DHA藻油乳状液TSI值的影响Fig.3 Effect of homogenization pressure on TSI of DHA algae oil emulsion
2.1.2 乳状液氧化稳定性分析
油脂氧化的初级产物是不稳定的氢过氧化物,易分解生成具有不愉快气味的小分子醛、酮、醇和酸等二级氧化产物,这些氧化产物不但会对食品的外观、口感、营养价值和货架期产生不良的影响,而且氧化过程中产生的自由基也会严重危害人体健康,导致机体损伤、细胞破坏、人体衰老等[25]。藻油因含有大量的多不饱和脂肪酸,易氧化变质,因此测定DHA藻油乳状液的氧化稳定性具有重要的意义。

图4 NaCN与NaCN-glu制备的DHA藻油乳状液在28 d室温贮藏期间的TOTOXFig.4 TOTOX of DHA algae oil emulsions prepared with NaCN and NaCN-glu during 28 d room temperature storage
由图4可知,实验组所有样品的TOTOX在同一时期均低于相应的对照组,并随时间的延长差异逐渐变大,说明NaCN与葡萄糖的MRPs除具有良好的乳化性外,还具有一定的抗氧化作用,与Augustin等[26]的报道一致;对照组样品在贮藏第14天时TOTOX明显升高,在21 d时35 MPa处理组样品的TOTOX已超过8,此时油脂已经氧化变质[27],而实验组样品的TOTOX在28 d时才有明显的增长,直到28 d时所有样品的TOTOX均未出现大于8的情况。
各组样品的TOTOX随均质压力的增大,呈先减小后增大趋势,这与其物理稳定性有一定的关系。当体系内的乳化剂在油滴外形成致密的界面层时,油滴与氧气、促氧化剂等接触的机会大大减少,在一定程度上抑制或延迟了油脂氧化,从而表现出良好的氧化稳定性[28]。其中实验组95 MPa处理的样品TOTOX在7、14、21 d和28 d始终为同一时期样品的最低值,分别为0.095、0.331、0.570、6.280,所以可以进一步确定95 MPa为本研究制备DHA藻油乳状液较为合适的均质压力。
2.1.3 乳状液的微观结构分析
乳状液属于多分散体系,当乳状液中大、小液滴共同存在时,小液滴有自动减小(溶解)的趋势,大液滴有增大的趋势;因此液滴分布均匀的乳状液比相同平均粒径但液滴分布不均匀的乳状液更稳定。由图5可知,随均质压力的增大,样品粒径明显减小,压力在35~95 MPa时,油滴呈现为完整的脂肪球形态;当压力达到125 MPa时,部分油滴已经呈碎片状,说明均质压力对乳状液的粒径形态、大小和分布具有明显的影响,进而影响乳状液的稳定性。在35 MPa和65 MPa压力下,油滴的粒径较大,分布并不均匀,而125 MPa的样品油滴粒径过小使体系的表面自由能明显增大,有明显的聚集现象。对于95 MPa处理的样品,油滴呈现较好的状态,大小、分布较为均匀,不易絮凝或聚集,乳状液相对稳定。由此可见,在一定的压力范围内,提高均质压力可以带来更好的乳化效果,但均质压力过大反而使乳状液更易发生不稳定现象,易出现聚集、絮凝、分层甚至破乳。

图5 不同均质压力下NaCN-glu制备的DHA藻油乳状液中油滴分布情况Fig.5 Oil droplet size distribution of DHA algae oil emulsions prepared with NaCN-glu under different homogenization pressures
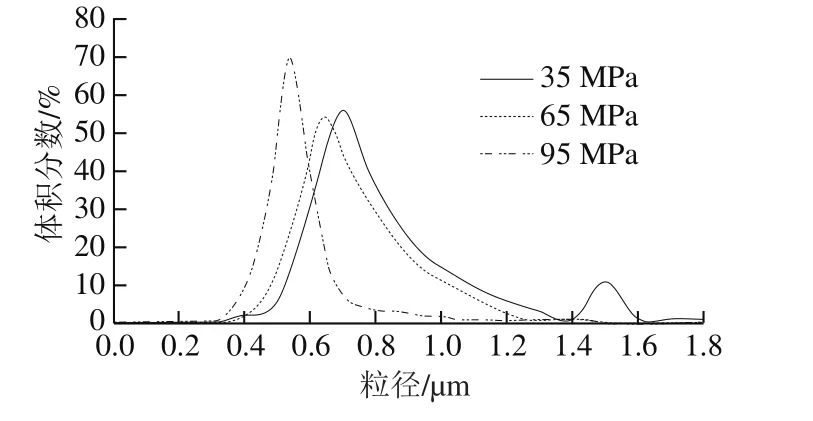
图6 不同均质压力下DHA藻油乳状液中油滴的粒径分布Fig.6 Particle size distribution curves of DHA algae oil emulsions under different homogenization pressures
在CLSM下随机选择200 个油滴,对其粒径大小、分布进行分析(125 MPa的样品已经成为较小的碎片或聚集成团,失去统计意义)。由图6可知,样品粒径呈正态分布趋势,随均质压力的增大,粒径分布曲线逐渐左移,即粒径逐渐从0.69 μm减小到0.53 μm,同时峰宽逐渐变窄,从双峰分布变成单峰分布。这是因为在一定均质压力范围内,随着均质压力的增加,机械作用变大,油相被分散,原先未被细化的大颗粒或小颗粒聚集体被分散,粒径不断下降,大小趋向均一,此变化趋势同毕爽等[29]的报道一致。由此,乳状液的微观结构再次证明95 MPa的均质压力下,DHA藻油乳状液的稳定性更好,与2.1.2节结论一致。
2.2 均质次数对乳状液稳定性的影响分析
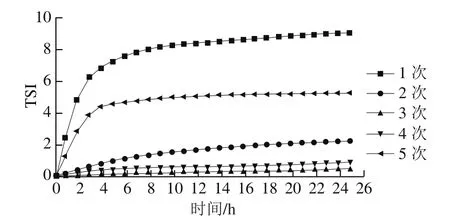
图7 均质次数对DHA藻油乳液TSI值的影响Fig.7 Effect of homogenization cycles on TSI of DHA algae oil emulsion
以NaCN-glu作为乳化剂在95 MPa的均质压力下,均质1、2、3、4、5 次制备DHA藻油乳状液,利用Turbiscan稳定性分析仪对其TSI值变化进行分析。由图7可知,样品的TSI值随均质次数的增加,呈先减小后增大趋势,均质3 次时样品的TSI值最小,稳定性最好;均质4 次时样品的TSI值有轻微的增加;而均质1 次和5 次的样品在开始扫描的1 h内,TSI值就明显升高,样品较不稳定,说明均质次数过少或过多都会明显影响DHA藻油乳状液的稳定性。
均质次数过少,机械力作用时间短,油相未被良好地分散,体系内依旧存在很多大油滴或小油滴聚集体,稳定性较差,TSI值较大;当均质次数达到3 次时,油相被分散为较小的油滴,通过吸附体系内的蛋白质乳化剂,使蛋白质乳化剂的疏水基与油相结合,亲水基与水相结合,从而在两相间形成界面膜,得到稳定性较好的包埋结构,粒径较小且分布均匀,稳定性较好,TSI值减小,与Floury等[30]的报道一致;若继续增加均质次数,油相被分散的程度过大,比表面积的增大使体系内有限的乳化剂不能覆盖新增加的界面,并且对已形成的相对稳定的乳化体系造成不利影响,严重时会使油相、水相彻底分离,发生破乳;同时均质时产生的热效应会对蛋白质乳化剂的乳化性质、构象产生一定的影响,使蛋白质间的疏水相互作用增加,易发生桥联絮凝[31],导致体系稳定性降低,TSI值增加,与毛立科等[32]的报道一致。综上,本研究选择的均质次数为3 次,此时得到的DHA藻油乳状液稳定性较好,且能耗较少。
3 结 论
根据稳定性分析仪分析、贮藏期间乳状液的氧化程度分析和CLSM观察对NaCN-glu MRPs在不同均质条件下制备的DHA藻油乳状液的稳定性和微观结构进行研究,以相同条件下单独NaCN制备的DHA藻油乳状液作为对比,进一步证实了NaCN-glu MRPs优良的乳化性和抗氧化活性,确定NaCN-glu MRPs制备DHA藻油乳状液的最佳工艺条件为均质压力95 MPa、均质3 次,此时Turbiscan稳定性分析仪24 h的扫描结果显示DHA藻油乳状液的稳定性优于其他各组,ΔBS变化较小,只有轻微的脂肪上浮和底部澄清;室温贮藏28 d期间的TOTOX处于较低水平,CLSM观察乳状液中油滴的粒径较小,主要分布在0.47~0.59 μm之间,且形态完整、较为均一。
本研究利用小型UHT设备制备NaCN-glu MRPs,避免水浴、油浴等实验方法的弊端,提高生产效率的同时获得了工业生产所需的实验数据,加速和推进实验室成果走向工业化生产。同时,本研究为DHA等敏感易氧化的功能因子输送体系的制备及其在婴幼儿配方奶粉等食品中的应用提供技术支持。
