大承气汤合大柴胡汤加芒硝外敷联合乌司他丁对重症急性胰腺炎患者腹内压及血清炎性因子的影响
2018-11-30郑惠之
黄 梅 郑惠之 赵 荣
(四川省南充市中心医院,四川 南充 637000)
急性胰腺炎(AP)是临床上较为多发的急腹症之一,按病情严重程度可分为轻症急性胰腺炎(MAP)、中症急性胰腺炎 (MSAP)和重症急性胰腺炎 (SAP)[1]。MAP和MSAP给予及时治疗后,大多预后良好,而SAP病程进展十分迅速,早期即可出现全身炎症反应综合征 (SIRS),进而发展为多器官功能障碍综合征(MODS),预后较为凶险[2]。 近年来,西医在 SAP 的临床诊断、病情评估、发病机制的研究、重要脏器功能的维护以及治疗方式的选择等方面虽获得了长足的进步,但SAP的病死率仍未得到明显改善。中医对SAP的发病机制和病理变化有着深入而广泛的研究,且经过多年的临床研究和观察,积累了丰富的治疗经验。中医学认为,本病多因饮食不节,外感六邪等,导致中焦气滞血瘀,闭塞不通,治法应为清热攻下、行气开结,治疗方法常采用中药内服和(或)外敷,不仅能够快速缓解患者临床症状,促进胃肠道功能恢复,还显著提高了SAP的临床治愈率,疗效确切。目前,中西医结合治疗SAP在实际临床工作中逐渐得到推广,其既能发挥西医靶向治疗的优势,又能体现中医注重整体的观念,显著缩短了治疗时间,减少了并发症和死亡病例的发生。本观察中,笔者采用大承气汤合大柴胡汤加芒硝外敷联合乌司他丁对SAP患者进行治疗,通过观察治疗对患者腹内压及血清炎性因子表达的影响,评价本方案治疗SAP的疗效并探讨其作用机制。现报告如下。
1 资料与方法
1.1 病例选择 所选病例临床西医诊断均符合《中国急性胰腺炎诊治指南》对SAP的诊断规定[3]。中医诊断符合《中药新药临床研究指导原则》对胃肠实热证的规定[4]。排除标准:坏死性AP或出现局部并发症需采用手术治疗者;爆发性胰腺炎或慢性胰腺炎急性发作者;合并严重原发性疾病者或合并其他急腹症病变 (如肠梗阻、胃肠穿孔等)者;妊娠待产者;合并精神疾病者。
1.2 临床资料 选择2016年6月至2017年6月在本院住院治疗的SAP患者90例,按随机数字表法将患者随机分为治观察组与对照组各45例。两组患者临床资料差异均无统计学意义(P>0.05)。见表1。

表1 两组临床资料比较
1.3 治疗方法 两组患者均给予禁食、禁水、液体补充、胃肠道减压、电解质纠正、常规抗感染等临床基础治疗。对照组在以上常规治疗基础上给予乌司他丁(广东天普生化医药股份有限公司,国药准字H19990133,规格:5万u/支)治疗,取5万u本品加入500 mL 5%葡萄糖注射液中,静滴2 h,每日1次,连续治疗2周。观察组根据“禁食不禁中药”的原则,在对照组治疗基础上给予大承气汤合大柴胡汤。方药组成:白芍15 g,柴胡、黄芩、法半夏、枳实、厚朴各10 g,大黄、芒硝各6 g,生姜3片,大枣6枚。上方加水煎煮,收汁200 mL,早晚分服,2周为1个疗程,共治疗1个疗程。在此基础上给予芒硝腹部外敷治疗:芒硝1000 g研磨成细末,缝制2个白布布袋(40 cm×22 cm),将研磨好的芒硝装入布袋中,平铺于中上腹部,袋内芒硝发硬结晶时应及时更换,连续外敷至腹部变软。两组均治疗2周后,评估疗效。
1.4 观察指标 观察两组临床疗效;观察两组治疗前后临床症状变化,并对腹痛腹胀、恶心呕吐、发热、身目发黄、大便不畅等主要症状进行积分。比较两组治疗后血淀粉酶、尿淀粉酶、血脂肪酶及白细胞等主要生化指标恢复时间。检测患者治疗前后腹内压改善和细胞间黏附分子-1(ICAM-1)、肿瘤坏死因子-α(TNF-α)、白细胞介素-8(IL-8)血清炎性因子水平变化。
1.5 疗效标准 疗效标准参照《中药新药临床研究指导原则》[4]中制定。治愈:临床症状、阳性体征消失,腹痛等主要症状完全消失,血、尿淀粉酶等生化指标恢复正常。显效:临床症状、阳性体征基本消失,腹痛等主要症状得到显著改善,血、尿淀粉酶等生化指标恢复至正常水平。有效:临床症状、阳性体征得到一定改善,腹痛等主要症状得到一定缓解,血、尿淀粉酶等生化指标得到一定改善。无效:临床症状、体征无任何改善,腹痛等主要症状以及血、尿淀粉酶等生化指标均未出现好转趋势。总有效率=治愈率+显效率+有效率。
1.6 统计学处理 应用SPSS23.0统计软件。计量资料以(±s)表示,数据呈正态分布,方差齐时采用t检验,计数资料采用χ2检验。P<0.05为差异有统计学意义。
2 结 果
2.1 两组临床疗效比较 见表2。观察组总有效率显著高于对照组(P<0.05)。
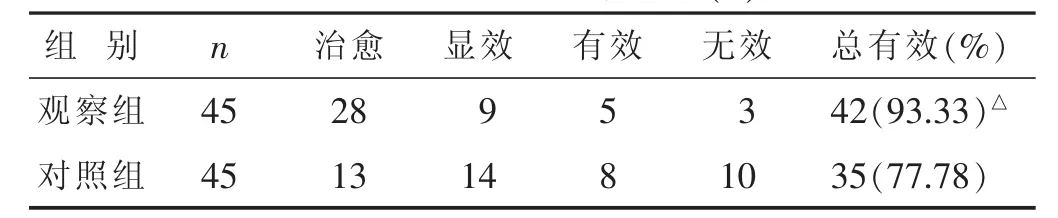
表2 两组临床疗效比较(n)
2.2 两组治疗前后主要临床症状积分比较 见表3。两组治疗后腹痛腹胀、恶心呕吐、发热、身目发黄、大便不畅等症状积分均较治疗前显著降低(P<0.05);两组比较,治疗组各项症状积分改善更加明显(P<0.05)。
2.3 两组临床生化指标恢复时间比较 见表4。观察组血淀粉酶、尿淀粉酶、血脂肪酶及白细胞恢复时间均明显低于对照组(P<0.01)。
2.4 两组治疗前后腹内压及血清炎性因子水平比较见表5。两组治疗后腹内压和血清ICAM-1、TNF-α、IL-8水平均显著降低(P<0.01),且治疗组降低更加明显(P<0.01)。
表3 两组治疗前后主要临床症状积分比较(分,±s)
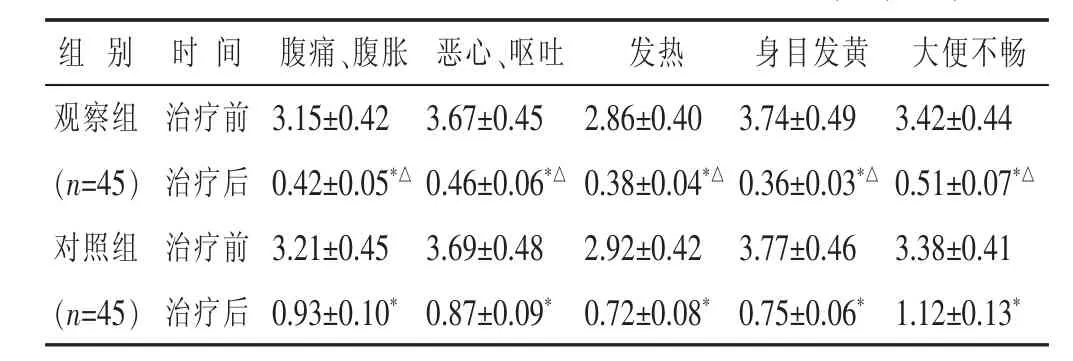
表3 两组治疗前后主要临床症状积分比较(分,±s)
与本组治疗前比较,*P<0.05;与对照组治疗后比较,△P<0.05。下同
组别 时间腹痛、腹胀 恶心、呕吐 发热身目发黄 大便不畅观察组 治疗前(n=4 5) 治疗后对照组 治疗前3.1 5±0.4 2 3.6 7±0.4 5 2.8 6±0.4 0 0.4 2±0.0 5*△ 0.4 6±0.0 6*△ 0.3 8±0.0 4*△3.2 1±0.4 5 3.6 9±0.4 8 2.9 2±0.4 2 3.7 4±0.4 9 3.4 2±0.4 4 0.3 6±0.0 3*△ 0.5 1±0.0 7*△3.7 7±0.4 6 3.3 8±0.4 1(n=4 5) 治疗后0.9 3±0.1 0*0.8 7±0.0 9* 0.7 2±0.0 8*0.7 5±0.0 6*1.1 2±0.1 3*
表4 两组临床生化指标恢复时间比较(d,±s)

表4 两组临床生化指标恢复时间比较(d,±s)
组 别 血脂肪酶 白细胞观察组 8.1 2±0.9 2△ 7.8 7±0.8 7△对照组 1 0.3 2±1.0 9 1 2.3 5±1.3 3 n 4 5 4 5血淀粉酶 尿淀粉酶6.1 1±0.7 2△ 7.6 1±0.8 7△7.8 2±0.8 6 9.3 9±1.0 2
表5 两组治疗前后腹内压及血清炎性因子水平比较(±s)
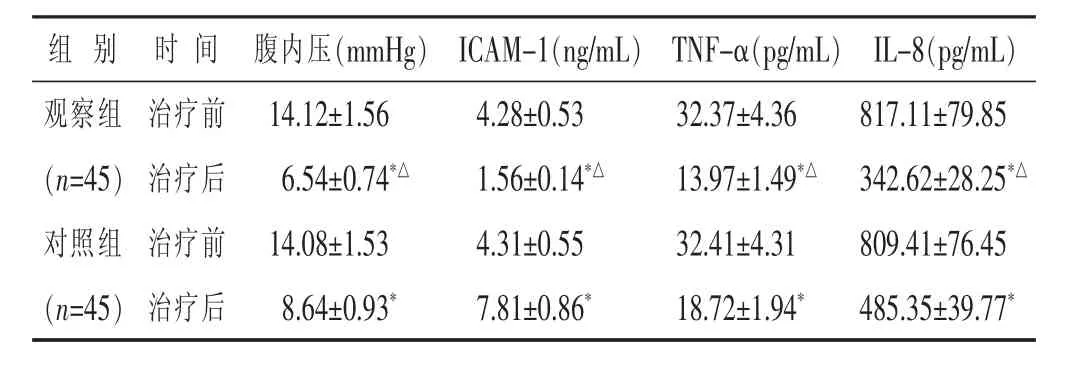
表5 两组治疗前后腹内压及血清炎性因子水平比较(±s)
组别 时间腹内压(m m H g) I C A M-1(n g/m L) T N F-α(p g/m L) I L-8(p g/m L)观察组 治疗前(n=4 5) 治疗后对照组 治疗前1 4.1 2±1.5 6 4.2 8±0.5 3 3 2.3 7±4.3 6 8 1 7.1 1±7 9.8 5 6.5 4±0.7 4*△ 1.5 6±0.1 4*△ 1 3.9 7±1.4 9*△ 3 4 2.6 2±2 8.2 5*△1 4.0 8±1.5 3 4.3 1±0.5 5 3 2.4 1±4.3 1 8 0 9.4 1±7 6.4 5(n=4 5) 治疗后8.6 4±0.9 3* 7.8 1±0.8 6* 1 8.7 2±1.9 4* 4 8 5.3 5±3 9.7 7*
3 讨 论
SAP是指AP出现坏死、脓肿(或假性脓肿)等局部并发症,或伴有脏器功能障碍,或同时存在上述两种情形,且APACHⅡ≥8分,Balthazar的CT分级≥Ⅱ级[5]。西医学研究认为SAP的发病机制十分复杂,其具体机制目前尚未阐明,但无论何种原因引起的SAP,最终均可引发局部及全身性的炎症反应,而炎症介质和炎性因子在这一病理生理过程中发挥着重要的桥梁作用[6]。TNF-α是一种由单核-巨噬细胞激活后分泌产生的小分子蛋白,具有多重生物学效应,是机体炎症反应的启动因子,能够促进其他炎性因子产生,进而放大或连锁全身炎症反应。彭晟研究表明,AP病情的严重程度与血清TNF-α的表达水平密切相关,TNF-α水平越高,则AP病情越严重[7]。IL-8是一种白细胞趋化因子,能够诱导T淋巴细胞、中性粒细胞、嗜性粒细胞向病灶部位趋化。在AP病程初期,IL-8能够促进和加重炎症反应,最终导致局部胰腺损害发展为全身性的脏器功能障碍。ICAM-1是一种跨膜糖蛋白,其通过介导细胞间与细胞外基质间的黏附参与机体炎症反应过程。余珊等研究发现,AP患者血清ICAM-1的表达水平显著高于健康人群,且ICAM-1浓度的高低与AP病情的发展和预后具有密切的关系[8]。由此可见,TNF-α、IL-8、ICAM-1炎性因子的释放能够引起炎症级联放大效应,在SAP的病程发展中起着非常重要的作用。若给予阻断上述炎性因子释放的药物治疗,可成为临床治疗SAP的重要机制之一。本研究结果显示,观察组治疗后TNF-α、IL-8、ICAM-1水平改善状况显著优于对照组,这可能是通过此机制对SAP患者起到相对更好的治疗作用。
AP归属中医学“腹痛”“脾心痛”“胁痛”等范畴,多因饮食不节、酗酒、蛔虫上扰、外感六邪、情志不畅所致。本病病位在胃和肝,中医学认为,胃与脾相合,肝与胆相合。胃属六腑之一,主水谷腐熟,食物受纳,以降为顺;脾主运化,生气血,以升为和。脾胃位于中焦,为气机升降之中枢,若中焦脾胃受损,则升降失调,湿热内蕴,导致中焦郁结。肝胆功主疏泄,肝属木,胃属土,若肝胆气息郁滞,则木郁犯土,导致脾胃、肝胆功能紊乱。湿热内蕴互结,久而化热,最终导致气滞血瘀,内蕴成毒。湿、热、瘀、毒互结,致血脉经络受损,胰脏组织出血,阴伤及阳,正虚邪陷,患者出现虚脱甚至猝死。故临床治疗应以清热攻下、行气开结为法。大承气汤和大柴胡汤均出自《伤寒论》,其中大承气汤主治脘腹痞满、频转矢气、大便不通、里热实证之症,由大黄、芒硝、厚朴、枳实组成;大柴胡汤主治少阳阳明合病,由柴胡、黄芩、枳实、大黄、白芍、法半夏、生姜、大枣组成。本研究将两方合用,以柴胡、大黄、黄芩为君药,其中柴胡升阳举陷、疏肝解热;大黄清热解毒、泻下攻积;黄芩泻火解毒、清热燥湿。枳实、芒硝共为臣药,其中枳实破气消积、化痰散痞;芒硝消肿止痛、润肠通便。白芍、法半夏、厚朴共为佐药,其中白芍凉血止痛、清热散瘀;法半夏降逆止呕、燥湿化痰、消痞散结;厚朴行气止痛、燥湿消积。生姜、大枣配伍既能缓和大黄、枳实泻下伤胃之弊,又能助法半夏增强和胃止呕之功,同时能调和诸药,为使药。诸药配伍,共奏清热攻下、行气开结之功。现代药理学研究证实,柴胡具有增强胃肠蠕动,促进胃排空和肠道推进的作用;大黄能够通过刺激黏膜和肠壁肌层内的神经丛增强肠蠕动能力,同时,大黄能促进肠腔内渗透压增高和肠腔容积增大,从而改善腹腔脏器的灌注功能[9];黄芩苷能够有效抑制AP大鼠体内炎症因子的释放,有助于改善AP大鼠的病死率[10];枳实具有增强胃肠动力、促进胃肠内容物、胆汁及胰腺排出的作用;芒硝能够促进腹腔渗出液吸收,增强胃肠道蠕动,促进胃肠黏膜修复,清除内毒素,改善肠黏膜表面微循环,有助于胰腺组织尽快修复[11];白芍能够加快肠壁组织的血流速度,有助于改善胰腺组织微循环以及肠道细菌移位和肠内毒素吸收;半夏能够有效抑制由组胺、乙酰胆碱及氯化钡诱导的肠管收缩;厚朴能够促进胃肠蠕动,增强胃肠道的排泄和收缩功能,改善胃肠道潴留。
《急性胰腺炎中医诊疗专家共识意见》[12]和《重症急性胰腺炎中西医结合诊治指南》[13]中均提及腹部芒硝外敷可用于AP的治疗中,其临床疗效已得到大量临床资料证实,如韩小勇等研究表明,芒硝外敷能够显著减轻AP患者的临床症状,增强胃肠道的蠕动能力[14]。王巧瑜将100例AP患者随机分为治疗组和对照组,治疗组患者在对照组常规治疗基础上,加用芒硝腹部外敷治疗,结果显示治疗组在促进血尿淀粉酶降低和胃肠功能恢复方面效果更为明显[15]。现代医学研究表明,腹部芒硝外敷治疗能够有效摄取腹腔渗液,促进局部炎症反应吸收,并能有效刺激肠道内血管扩张,降低血流阻力,从而改善肠道内的血液灌流[16]。同时,芒硝外敷还能够刺激大肠内形成高渗盐溶液,增加肠内水分,增强肠蠕动力,促进胃肠功能和排便功能恢复[17]。由于芒硝价格低廉,简单易得,疗效显著,因而被广泛用于AP的辅助治疗中。
本研究结果显示,观察组治疗后临床疗效显著高于对照组,临床症状(腹痛腹胀、恶心呕吐、发热、身目发黄、大便不畅)积分、主要生化指标(血淀粉酶、尿淀粉酶、血脂肪酶、白细胞)的恢复时间、腹内压以及血清炎性因子(ICAM-1、TNF-α、IL-8)水平均显著低于对照组。结果提示大承气汤合大柴胡汤加芒硝外敷联合乌司他丁治疗SAP,能够降低ICAM-1、TNF-α及IL-8的表达水平,改善腹内压,促进胃肠功能恢复,改善临床预后。
