化学核心素养视域下的教学问题解析
2018-11-13严业安
严业安
(三明第一中学,福建 三明 365001)
化学核心素养是学生在认知活动中解答有关化学问题时呈现出来的关键素养,是学生用化学的眼光审视客观事物时表现出来的一种能力水平,这是伴随和影响学生一生的东西。那么,如何培养高中化学核心素养呢?清华大学化学系张希教授在中国化学奥林匹克(决赛)暨冬令营上说:“化学不只出现在书本上,也不仅停留在实验室里,更是与我们的社会和生活息息相关。”高中化学核心素养应立足于具体的课堂教学或课外活动展开。提炼出一些贴近生活的具体情境的问题,让学生有意识地关注身边所发生的化学现象,思考如何利用学过的知识解答化学问题和解释身边的化学现象,不失为提升自身化学核心素养的一种途径。以下14个具体问题的解答正是基于这一想法的尝试。
【问题1】为什么喝水解辣的效果并不显著,而喝牛奶却可以很快消退辣觉?
【解答】辣的味觉来自于辣椒中所含有的辣椒素分子,这种分子通过与神经元末梢的受体蛋白质发生作用,激活钙离子通道而产生辣的感觉。由于辣椒素的水溶性差、脂溶性好,利用牛奶中的脂肪成分溶解辣椒素,可降低辣椒素的浓度。简单的相似相溶原理可帮助我们巧妙地解决生活中的问题。
【问题2】臭豆腐“闻起来臭、吃起来香”,其背后蕴含着什么化学道理?
【解答】研究表明,豆腐在发酵过程中,蛋白质在酶的作用下发生水解,其中含有的甲硫氨酸和半胱氨酸降解,产生易挥发的硫化氢气体,因而“闻着臭”。同时,蛋白质水解产生的其他氨基酸,有的具有鲜美的滋味,因而“吃着香”。简单的生物化学知识成功地运用到烹饪过程中,造就了这种家喻户晓的美食。
【问题3】为什么冷的米饭显得很硬且营养价值低?
【解答】大米的主要成分为淀粉,淀粉是葡萄糖单体脱水而成的聚合体,每个分子大约含有几百到几千个葡萄糖单元。其中直链淀粉的分子盘旋呈一个螺旋,每转一圈,约含六个葡萄糖单元。葡萄糖单元含有若干羟基,螺旋内羟基间形成氢键,无法再与水分子形成氢键。所以淀粉在冷水中溶解度较低,人体消化系统中的淀粉酶无法分解它。煮饭时,大米在热水中吸收水分,使淀粉分子体积膨胀,部分氢键被破坏,淀粉就溶在热水中。刚煮好的米饭显得粘稠、柔软,有利于人体消化和吸收营养。
米饭放置一段时间变冷后,淀粉分子中原来断裂的氢键再次形成,使米饭变得很硬。时间放置越长,米饭就显得越硬,越来越不利于消化,吸收率下降,营养价值缺失。即使把冷饭放在锅里或用微波炉重新蒸煮,其消化吸收率已无法与刚煮好的媲美,营养价值必然降低。
【问题4】“水滴石穿”是物理变化还是化学变化?
【解答】“水滴石穿”是一句成语,大意是“水不停地滴下来,能把下面的石头滴穿”,比喻力量虽小,但功到自然成。水滴石穿既有物理变化的原因,也有化学变化的原因。水滴石穿的原因之一是水从高处滴落,其冲击力比较大,冲击力给石头带来磨损,水滴日复一日、年复一年,一滴一磨,石头就被磨穿了。这一过程只是石头的形状发生了变化,没有产生新的物质,是物理变化。水滴石穿也可能是由于水和空气中的二氧化碳共同作用的结果。二氧化碳能溶于水,在通常状况下,1体积水约能溶解1体积的二氧化碳,二氧化碳和水作用形成碳酸,水滴可看成是碳酸溶液,呈弱酸性。大理石、石灰石这类石块的主要成分是碳酸钙(CaCO3),水滴落下来时,发生如下反应:CaCO3+CO2+H2O=Ca(HCO3)2,Ca(HCO3)2可溶于水,导致石块局部慢慢溶解而损失。溶洞现象是水滴石穿的一个典型例子。水滴石穿还有一种原因是受酸雨的腐蚀。
【问题5】什么是丁达尔现象?
【解答】当可见光通过胶体时,在入射光侧面可观察到光亮的通路(微弱闪光集合而成的光柱),该现象称为丁达尔效应,也叫丁达尔现象。实验室中常利用丁达尔现象来区分溶液与胶体。波长为400~750 nm的光为可见光,可见光在胶体的分散质微粒表面发生散射,形成丁达尔现象。胶体中分散质粒子直径(为1~100 nm)小于可见光的波长,光波可以绕过粒子前进,并从粒子向各方向传播,这就是散射现象,散射的光环组成了光柱。溶液中分散质粒子很小,散射很弱,看不到闪光和光柱。粗分散体系(悬浊液和乳浊液)中,分散质粒子大于光波波长,在光照射下产生反射作用,可看到颗粒的形状而呈浊状。
【问题6】晴朗的天空为什么是呈蓝色的?车辆在雾天行驶时为什么要用黄色灯?
【解答】散射光的强度可用雷利(Rayleigh)公式来表示。由雷利公式得知,散射强度和入射光的波长的4次方成反比,即入射光若波长越短就越容易发生散射,波长越长的光越容易透过。可见光中,黄色光的波长为580~600 nm,蓝色光的波长为450~480 nm。大气层可看成是一种气溶胶,当白光照射在大气层上时,蓝色光几乎都发生散射,而黄色光大体都透过,只有极少被散射,所以晴朗的天空显示蓝色,车辆在雾天行驶时用黄色灯。
【问题7】“鬼火”究竟是什么?
【解答】磷的拉丁文原意是发光物,我国古代典籍中就有燐这个词,俗称鬼火,按统一命名原则现在命名为磷,所以“鬼火”就是“磷火”。动物的牙齿和骨骼中含有元素磷,尸体在腐烂过程中发生复杂的生物变化、化学变化和物理变化,产生少量的P2H4和PH3气体。P2H4比PH3更活泼,能够自燃,火焰显暗淡的蓝绿色。空气流动形成风,火焰就随风飘荡。有关反应方程式为:
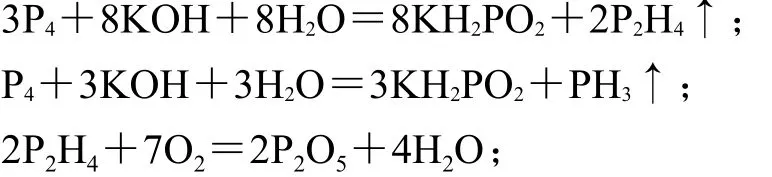
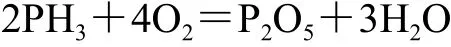
【问题8】烧砖过程中,如果从窑顶喷水得到的是青砖,不喷水则得到红砖,这是什么原因?
【解答】粘土是烧砖用的原料,主要成分为含水硅酸铝(xAl2O3·ySiO2·nH2O),同时还掺有赤铁矿(Fe2O3为主)、菱铁矿(FeCO3为主)、黄铁矿(FeS2为主)或褐铁矿(Fe2O3·2Fe(OH)3为主)等矿物杂质。当砖坯在砖窑中高温煅烧时,若氧气充足,则上述铁的化合物都转化为Fe2O3,得到红砖。铁元素的含量越多,砖的颜色就越红。砖坯烧制过程中,如果从窑顶向下喷适量的水,水会转化为水蒸气,水蒸气和焦炭在高温下反应生成H2和CO。H2和CO在高温下将Fe2O3还原成Fe3O4或FeO,得到的砖就显青灰色。
【问题9】为什么液化石油气罐在用完之后再摇一摇或浇一点热水又可使用一会儿?
【解答】目前家庭使用的液化石油气的主要成分是丙烷、丙烯、丁烷和丁烯等低级烃的混合物。常温下它们是气体,通过加压转化为液体装在钢罐中。使用时旋开阀门,由于压强突然减小,这些烃类化合物会立即气化而喷出,点燃即可使用。当这些烃类化合物都气化逸出后,火苗就逐渐变小了。这时把一些热水浇在液化气罐上,或者稍用力摇一摇液化气罐,火苗就会突然变大起来。这是因为目前使用的液化石油气中含有少量戊烷,常温下戊烷是液体,升高温度时其蒸气压增大,摇一摇或加热有利于戊烷气化。戊烷的数量虽然不多,但其产生的气体可维持一段时间。应注意的事项,严禁使用明火对着液化气罐直接加热,否则会有爆炸的危险。
【问题10】实验室蒸馏石油时要在蒸馏烧瓶中加入一些沸石或碎瓷片,其原理是什么?
【解答】在常压下仔细观察加热纯水的过程,会发现:把水加热到100℃时,水并没有沸腾;当温度超过100℃以后一段时间,水却突然沸腾了。为什么水会存在这种过热现象呢?因为对液体加热,沸腾时内部将有小气泡生成,小气泡充当“气化核”的角色,液体在其周围气化。而小气泡在纯液体内难以形成,导致加热时液体不容易沸腾,就产生过热现象。化学工作者必须注意防止过热现象的发生,因为过热程度越大,沸腾的发生越剧烈,即暴沸,液体往往大量喷出,构成安全隐患。特别是在处理酒精、石油、乙醚等这些易燃液体时,伴随气泡喷溅出来的液体如果遇到明火就会燃烧起来。碎瓷片(或沸石)是一种多孔的硅酸盐,通常内孔中存储着气体,加热时这些气体逸出,形成“气化核”,跳过了形成微小气泡的阶段,这样就大大地降低了液体的过热程度。搅拌也有利于气化核的形成。因此,加入碎瓷片(或沸石)和搅拌可以有效地减少过热现象的产生。
【问题12】为什么油不溶于水?
【解答】溶解过程是溶剂分子拆散、溶质分子拆散、溶剂与溶质分子相结合(溶剂化)的过程。根据溶解过程的自由能变化公式△G=△H-T△S可知,如果△G<0,溶解易于进行;△G>0,溶解难于进行。油不溶于水(疏水效应)通常用“相似相溶”经验规律来解释。凡溶质与溶剂的结构越相似,溶解前后分子周围作用力的变化越小,这样的过程就越容易发生。若将油溶于水,需要破坏油分子间的弱的范德华力、水分子间的范德华力及部分氢键,再形成油分子与水分子之间相对较弱的范德华力。一般认为,后者不足以弥补前者损失的能量,故整个过程应吸热,即焓变应为正值(△H>0)。而由于两相混合,混乱度增加,熵应增加(△S>0)。故通常的解释是焓变驱动了疏水效应的发生。近年来研究发现,在油分子周围的水化层中,水分子间可形成比水相更强更有序的氢键,故将导致熵减(△S<0),因此熵变(△S<0)是油不溶于水的决定性因素。由此可见,油不溶于水这个看似简单的现象,普遍而又复杂。疏水效应与很多重要的自然现象相关,如生物膜的结构、洗涤剂的去污原理、表面活性剂的作用、相转移催化剂等。
【问题11】凝固点降低原理在生活和生产中的常见应用有哪些?
【解答】非挥发性、非电解质的稀溶液的蒸气压比纯溶剂低,并且溶液浓度越大,蒸气压下降越多。在101 kPa下纯液体和它的固相达平衡的温度就是该液体的正常凝固点,此时液相的蒸气压与固相的蒸气压相等。纯溶剂的凝固点为,但在溶液的蒸气压低于纯溶剂的,所以溶液在不凝固。当温度继续下降到Tf,溶液的蒸气压和纯溶剂固相的蒸气压相等,达到平衡,该温度(Tf)即为溶液的凝固点。就是溶液凝固点的降低,它和溶液的质量摩尔浓度(m)成正比。冬天,撒一些盐,会使覆盖在马路上的积雪较快地融化。松树叶子在寒冬里能常青而不冻,是由于入冬前松树叶内存储了大量的糖分,降低了叶液的凝固点。在冬季,常常将一定量的甲醇或乙二醇加到汽车散热器的冷却水中,由于冰盐浴的凝固点低于冰浴,可防止水的冻结。上述这些常见应用都利用了凝固点降低原理。在基础有机化学实验中,常采用测定物质熔点的方法来检验其纯度。由于含杂质的有机物可看成是一种溶液,其中有机物为溶剂,杂质为溶质,故有机物含杂质时其熔点会比纯有机物低。
【问题13】为什么医院给病人作静脉点滴用的输液是0.9%的生理食盐水、5%的葡萄糖注射液?渗透压与生命现象关系密切吗?
【解答】有关渗透压的系统研究表明,生物细胞膜具有半透膜的性质。人体内的毛细血管壁和细胞膜就是半透膜,其渗透平衡与生命现象密切相关。临床上给病人作静脉点滴时,各种输液的浓度需要仔细调节,确保它与血液的渗透压相同,即需要用等渗溶液,如质量分数为0.9%的生理食盐水、5%的葡萄糖注射液。这是医学上需要遵守的原则,否则可能导致红细胞中的水分子向高渗盐水中渗透使红细胞皱缩,或是水分子向红细胞内渗透使红细胞膨胀以致破裂。
人体的肾可看成特殊渗透器,代谢过程中产生的废物通过它经渗透随尿排出,有用的蛋白质仍留在肾小球内,故肾功能受损时尿中会出现蛋白质。淡水鱼和海鱼的鱼鳃渗透功能有所差异,水和鱼体液之间的渗透平衡通过鱼鳃来调节,故淡水鱼无法生活在海水中,淡水不能用来养殖海鱼。树根的渗透压可高达1×106Pa,植物需要的养分和水分正是借助渗透作用输送到树叶末端。
【问题14】农田中施肥太浓时植物会被烧死,盐碱地的农作物长势不良,甚至枯萎,试解释原因。
【解答】施肥太浓时或盐碱地里,当土壤中肥料(或盐类)的浓度超过在植物中的浓度时,水分会通过植物细胞膜从植物反渗透到土壤中,导致植物枯萎或“烧死”。
