亮菌口服液对慢性萎缩性胃炎大鼠胃黏膜及PDCD4表达的影响
2018-11-07朱耀东
胡 磊,朱耀东,李 平,张 梅
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)是一种胃癌前病变,研究证明胃癌前病变患者有着10倍的患癌风险[1]。CAG是胃癌发病模式Correa 级联反应中较常见病理阶段[2]。目前临床常用防治萎缩性胃炎的措施有质子泵抑制剂、胃黏膜保护剂及幽门螺杆菌根治、内镜手术等手段[3]。近年中医药被广泛用于防治CAG[4],为胃癌前病变治疗拓展了治疗思路。亮菌是我国最初发现并拥有自主知识产权的一种真菌。中医认为,该菌对胃肠道有保健功能[5]。目前经亮菌发酵提取的亮菌口服液(Armillariella oral solution, AOS)被临床常用于慢性肝炎、迁延性肝炎、慢性胆管炎和胆囊炎以及慢性胃炎的治疗。对AOS前期研究[6-8]显示,AOS对返流液诱发胃黏膜损伤以及化疗引起胃肠道副反应有着改善作用,其机制可能通过调节超氧化物歧化酶(SOD)、白细胞介素-8(IL-8)以及5-羟色胺(5-HT)的活性改变胃肠活动节律。但对治疗CAG的作用机制,尚未完全清楚。
程序性细胞死亡因子4(programmed cell death 4, PDCD4)是一种抑癌基因,研究[9]表明该基因通过在胃癌黏膜组织中表达下调及缺失,促进肿瘤增殖。同时既往研究[10]也表明胃癌前病变组织中较正常胃黏膜也存在PDCD4低表达,PDCD4可作为评估胃癌前病变及其转归的特异性指标。本研究拟制备CAG大鼠模型,观测AOS对CAG大鼠胃黏膜腺体萎缩及PDCD4表达的影响,初步探讨治疗CAG的可能作用机制。
1 材料与方法
1.1实验动物及主要试剂SD雄性大鼠(安徽医科大学实验动物中心,Sprague-Dawley),SPF级,体质量140~180 g,5周龄,共40只。处于室温24 ℃,湿度50%,通风良好环境中。AOS(合肥诚志生物制药有限公司,批号为20161109);胃复春片(杭州胡庆余堂药业有限公司生产,批号为16066146),称取药物溶于蒸馏水配成0.06 g/ml溶液。胃蛋白酶测试盒(南京建成生物工程研究所,批号为20170503);兔抗大鼠PDCD4多克隆抗体(美国Proteintech公司,批号12587-1-AP); N-甲基-N硝基-N-亚硝基胍(N-methyl-N′-nitro-N-nitrosoguanidine,MNNG)(山东西亚化学工业有限公司,批号为Q94510);小鼠/兔聚合物法检测系统(北京中衫金桥生物技术有限公司,批号17G37D07);10%水合氯醛(安徽省立医院,批号20170706)。
1.2仪器DHG-9070型电热恒温鼓风干燥箱(上海齐欣科学仪器有限公司);GFL1008型水浴锅(深圳市朗诚科技股份有限公司);SPX-250-2型生化培养箱(上海赫田科学仪器有限公司);Thermo Muitioken MK3型酶标仪(瑞士TECAN公司);5424R型高速冷冻离心机(德国艾本德公司);BX53型光学显微镜(日本奥林巴斯公司);RM2235型切片机(德国莱克公司)。
1.3方法所有SD鼠随机分为对照组10只,模型制备组30只;对照组自由饮食水,模型制备组自由饮用100 μg/ml MNNG联合饥饱失常(饱食2 d,饥饿1 d)9周[11];随机从两组各取2只SD鼠颈椎脱臼法处死,通过肉眼及HE染色镜下观察模型制备情况。模型成功标准:肉眼可见胃黏膜缺损,黏膜层变薄,胃黏膜由正常的橘红色变为红白相间,黏膜下血管透见;镜下观可见胃黏膜腺体数目减少,细胞核固缩且深染,肠上皮化生出现。模型制备过程中2只SD鼠死亡, 从制备组剩余26只鼠中随机取25只,依次分为模型组、AOS低剂量组、中剂量组、高剂量组、胃复春组,每组各5只。从对照组8只鼠中随机取5只为正常组。其中正常组及模型组用生理盐水灌胃,剂量为10 ml/kg;AOS低剂量组、中剂量组、高剂量组用亮菌口服液灌胃,剂量依次为0.5、1.0、2.0 ml/kg ;胃复春组用胃复春灌胃,剂量为10.0 ml/kg。干预期间以上6组正常饮食水,每天灌胃1次,疗程28 d。
1.4检测
1.4.1大鼠一般情况观察 观察大鼠情绪、毛发颜色及外观、饮食、体质量及眼睛的变化,观察大鼠刺激后的反应能力,呼吸的频率、节律,大便是否带血、黏液等。
1.4.2胃液pH、分泌量及胃蛋白酶效价测定[12]灌药28 d后,10%水合氯醛 (0.03 ml/kg)腹腔注射麻醉大鼠,取头高脚低仰卧位幽门部下端约5 mm处结扎。静置4 h,收集胃液。胃液于4 000 r/min离心15 min, 吸上清液于2.0 ml EP管,13 000 r/min离心10 min,吸取上清液。计胃液总量并用精密pH试纸测胃液pH值,依据ELISA试剂盒步骤测胃蛋白酶效价。
1.4.3胃组织形态肉眼及镜下观察 取胃液后,距贲门部5 mm处切断,从整个胃部取部分胃体,沿胃小弯切开,缓慢冲洗干净,肉眼观察胃体形态后,4%中性福尔马林浸没2 d后剪取约15 mm×8 mm长条状组织。胃组织常规HE染色镜下观察胃病理结构。
1.4.4免疫组化测PDCD4蛋白表达 按照免疫组化SP法,依次脱蜡脱水,柠檬酸钠缓冲液(pH 6.0)抗原修复,过氧化物酶阻断剂温育10 min,洗涤,PDCD4兔抗大鼠多克隆一抗(1 ∶300),HRP标记的山羊抗小鼠/兔IgG聚合物二抗,DAB显色4 min,复染细胞核,脱水、封片。结果判断以光镜下观察视野中呈棕黄色或棕褐色颗粒为阳性,视野中染色程度分级:无染色0分,浅黄色1分,棕黄色2分,棕褐色3分。每张载玻切片随机选取6个视野光镜观察,以阳性细胞占视野比例分级:无阳性细胞0分,<25%为1分,25%~75%为2分,>75%为3分。计视野染色程度分级及阳性细胞占视野比例分级数值的乘积为总分进行分析比较(总分=PDCD4表达阳性细胞比例分级×染色程度)。
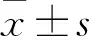
2 结果
2.1大鼠一般情况对照组大鼠情绪稳定,刺激后反应灵敏,动作灵活,呼吸规律,毛发细腻光泽,眼睛红润,大便正常。模型制备早期大鼠躁动与淡漠情绪交替,刺激后反应迟钝,呼吸稍急促,毛发暗黄粗糙,眼睛黯淡,活动少,食少;模型制备后期大鼠情绪淡漠,几乎不活动,常蜷曲伴颤抖,乍毛,大便灰褐色稀稠样。经药物干预后,与模型组比较,AOS中剂量组、高剂量组与胃复春组明显好转;较正常组毛发颜色稍有差异,其他无明显差异。但AOS低剂量组大鼠反应仍迟钝,活动及食量介入正常组与模型组之间,呼吸稍急促。药物干预期间未发生大鼠死亡。各组体质量变化见表1。

表1 治疗期间各组大鼠体质量变化比较
与模型组比较:*P<0.05;与正常组比较:##P<0.01
2.2胃液pH、分泌量及胃蛋白酶效价各组结果比较28 d后,与正常组比较,模型组大鼠胃液pH值升高(P<0.01),胃液分泌量及胃蛋白酶效价明显减少(P<0.01)。与模型组比较,AOS中剂量组、高剂量组及胃复春组胃液pH值降低(P<0.01),胃液分泌量增加及胃蛋白酶效价增多(P<0.05)。见表2。
2.3病理形态变化
2.3.1肉眼观察 正常组胃黏膜层表面完整、光滑、无出血点,呈肉红色;皱襞完整凸起、无序交错、厚薄均一、皱襞表面有适量透明黏液。与正常组比较,模型组黏膜层表面粗糙呈细颗粒状、少量出血点,色泽红白相间;皱襞明显变浅、皱襞间交错不连续、厚薄不均一;部分皱襞变浅,甚至消失;黏膜层厚度薄、表面黏液量少、黏膜下血管透见。与模型组比较,AOS中剂量组、高剂量组及胃复春组胃表面较完整、出血点极少、色泽淡红色;皱襞多见,其表面有大量黏液附着。AOS低剂量组胃黏膜层厚薄不均一;黏膜表面仍有粗糙且少许出血点,局部色泽红白相间。见图1。
2.3.2镜下观察 正常组胃体部腺体排列整齐、 腺体大小一致;黏膜层厚度及胃小凹深度适中;固有层偶见少量炎性细胞;细胞间界限清晰,细胞核正常,核浆比正常。模型组胃腺体缩小且腺管排列紊乱扭曲,腺体减少;黏膜层变薄且肠上皮化生,胃小凹变浅;黏膜层及固有层有大量炎性细胞、散在分布;细胞核深染固缩,核浆比例失调。与模型组比较,AOS中剂量组、高剂量组及胃复春组腺体排列及大小明显改善,细胞核浆比基本正常;肠型腺上皮与炎性细胞减少。但AOS低剂量组改善不明显,腺管排列仍紊乱,细胞核浆比有异常。见图2。
2.4免疫组化测胃组织PDCD4蛋白表达胃组织中有PDCD4蛋白表达呈棕色,无PDCD4蛋白表达呈蓝色。与正常组比较,模型组PDCD4表达量明显下调(P<0.01)。与模型组比较,AOS中剂量组、高剂量组PDCD4蛋白表达量上调(P<0.05);同时AOS高剂量组及胃复春组表达多于低剂量组及中剂量组。见表2、图3。

表2 治疗后各组大鼠胃液pH值、分泌量、胃蛋白酶效价及胃黏膜组织PDCD4表达比较
与正常组比较:##P<0.01;与模型组比较:*P<0.05,**P<0.01

图1 AOS对大鼠胃黏膜大体形态的影响A:正常组;B:模型组;C:AOS低剂量组;D:AOS中剂量组;E:AOS高剂量组;F:胃复春组

图2 AOS对大鼠胃组织病理变化的影响 HE染色×200A:正常组;B:模型组;C:AOS低剂量组;D:AOS中剂量组;E:AOS高剂量组;F:胃复春组
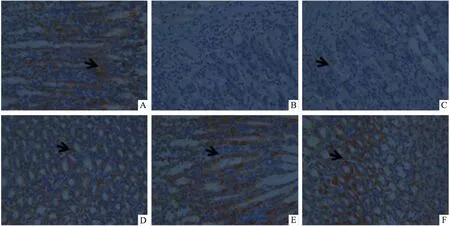
图3 AOS对CAG大鼠PDCD4表达的影响 免疫组化×400A:正常组;B:模型组;C:AOS低剂量组;D:AOS中剂量组;E:AOS高剂量组;F:胃复春组
3 讨论
慢性萎缩性胃炎作为胃癌前病变的一种,是目前的治疗热点,不断探索最有效治疗手段缓解CAG消化道症状及改善生活质量。亮菌口服液在临床上用于慢性萎缩性胃炎患者治疗有着显著的疗效,但其长期缺乏基础研究及作用机制不明。本研究制备CAG大鼠模型,观察AOS对胃液pH值、分泌量、胃蛋白酶效价、胃黏膜腺体萎缩及PDCD4蛋白表达的影响。CAG胃黏膜病变过程中黏膜腺体萎缩,甚至消失,表面黏液层逐渐减少。正常胃黏膜表面由黏液及碳酸氢盐形成约0.5 mm凝胶黏液屏障保护层,具有缓解食物机械性损伤、细菌生物损害及H+化学侵蚀作用。而黏液及碳酸氢盐由胃黏膜层分泌,其中随着黏膜萎缩加重,分泌细胞减少,从而直接影响盐酸、胃蛋白酶原不同程度的缺乏,进一步干扰胃部消化、杀菌、营养等功能。因此,本研究通过胃液pH值、分泌量、胃蛋白酶效价间接反映AOS治疗后CAG大鼠病理转归,同时经肉眼及镜下直接观察AOS可抑制黏膜萎缩。
研究[13]发现PDCD4在人类胃癌组织存在下调,萎缩性胃炎黏膜中PDCD4也低表达。PDCD4基因低表达可能与miRNA的3′-UTR位点被干扰影响基因转录调控有关。胃癌组织中miR-208a-3p表现尤为突出,随着表达增加PDCD4基因表达下调,促进胃组织细胞增殖加快及细胞核的特定变化[14-15]。本研究证实CAG PDCD4基因蛋白表达少,随着AOS抑制CAG胃黏膜萎缩后PDCD4基因蛋白表达增多。因此,CAG的转归机制可能与PDCD4基因表达有关。通过对PDCD4研究,探讨与CAG病情转归的相关性,可通过对结合其他相关基因多靶点监测判断AOS改善CAG治疗疗效有着一定临床意义。也对AOS的深入研究,探讨其更多的作用机制及临床适应症提供坚实的基础依据。
