人类表皮细胞衰老相关的microRNA差异性表达与信号通路分析
2018-11-02韩银淑
韩银淑
(厦门医学院,厦门 361023)
人类的表皮是非常重要的天然屏障,用来抵御环境中化学、物理和微生物的影响。位于真皮与表皮连接处的基底层分布有干细胞,它不断的分化成新的角质形成细胞(keratinocytes, KC)以更新表皮,而这些角质形成细胞在表层脱落的过程中分化、死亡。尽管表皮处于不断更新的状态,但随着角质形成细胞更新速率的下降,衰老即产生。衰老与诸如表皮变薄、弹性组织缺失、黑色素细胞损失与皮肤苍白和透明度增加以及屏障功能降低相关。相反,角质形成细胞过度活化会引起的表皮过度增生及炎症细胞的浸润导致的局部炎症。如银屑病,癌前期病变如光线性角化病,原位癌如Bowen病,皮肤癌如基底细胞癌,鳞状细胞癌。角质形成细胞的分子机制和信号传导途径在很大程度上是未知的,本研究试图通过基因调控的视角揭示参与人类表皮组织衰老的分子机制与信号通路。
miRNA是内源性22个核苷酸的小非编码RNA,其通过靶向mRNAs并触发翻译抑制或RNA降解来控制基因表达[1]。这些非编码RNA与靶mRNA的3’端结合,其结合的特异性主要由miRNA的启动区域(从核苷酸2~8位)决定。通常情况下miRNA可同时调控数百个相同途径的靶基因,并且为了增加这种转录后调节的复杂性,几种miRNA可以靶向相同的转录物[2]。miRNAs是生物过程所必需的[3-4]。许多miRNA以组织特异性方式表达[5]。在横纹肌中,miRNA参与其生理过程,如肌形成、纤维类型转换和再生[6-8]。因此,miRNA表达水平的失调与病理状态有关[9-10]。例如,SOD1G93 A转基因小鼠中miRNA-206的抑制诱导严重萎缩[11]。然而,miRNA在人类表皮组织中的参与情况和所调控的信号通路很大程度上是未知的。
为了确定哪些miRNA和其调控的信号通路与表皮组织衰老过程相关,本课题组选择了年轻人和老年人的表皮组织GEO芯片,检查不同年龄下miRNA表达的差异,通过Cytoscape软件(v.3.5.1)预测分析下游靶基因并筛选出关键基因分析其参与的细胞活动和参与的信号通路。总之,这些结果在一定程度上提示与衰老相关的miRNA在表皮细胞衰老过程中潜在的调控作用,为进一步治疗和抵抗衰老提供新的理论依据和方法。
1 材料和方法
1.1 微阵列芯片分析
本研究使用二种芯片,包括基因芯片、miRNA芯片。使用GEO2R软件(https://www.ncbi.nlm.nih.gov/geo/geo2r/)分析芯片数据。在所有实验组中,差异表达的基因,miRNA均通过显着性水平P< 0.05或|logFC| > 1来鉴定。
1.2 功能富集分析
可视化集成数据库v.6.8(DAVID v.6.8)用来进行基因注释。“京都基因和基因组百科全书”(KEGG)和基因本体论(GO)用来对基因进行生物功能及通路分析。GO分析仅限用于生物过程分析。Cytoscape(v.3.5.1)平台上的ClueGO和CluePedia插件用于可视化分析。GO术语基于共享基因的功能性进行连接,并根据功能相似性进行分组。
1.3 网络建设和分析
关于蛋白质-蛋白质相互作用(PPI)的信息来源于检索相互作用的基因/蛋白质数据库的搜索工具(https://string-db.org/)。选择经实验验证,并且得分≥0.4的基因。关于miRNA基因相互作用的信息是使用Cytoscape上相互作用的miRNA基因的检索工具(v.3.5.1)推导。
2 结果
2.1 通过生物信息学分析鉴定了年轻与老年表皮组织micRNA芯片
使用GEO2R方法的GEO数据库筛选老年(55~66岁)和年轻人(20~25岁)角质形成细胞中差异表达的miRNA的分层聚类基因芯片(GSE101493)。结果显示11个miRNA上调,18个miRNA下调(表1)。
2.2 通过生物信息学分析鉴定年龄差异的基因芯片
使用GEO2R方法的GEO数据库筛选来自年轻人和老年人的表皮组织差异表达基因芯片(GSE18876)。筛查结果显示,基于倍数变化(FC)或P值(| logFC |> 0.8或P< 0.05),不同年龄表皮组织基因芯片中有105个差异表达基因。其中,有17个年龄相关基因共同上调,17个年龄相关基因共同下调。使用火山图来显示二种微阵列上所有基因的差异(图1)。
2.3 年龄差异的miRNA与年龄差异基因的相互作用
为了提高预测的准确性,使用Cytoscape软件(v.3.5.1),选择了差异最大的前5个上调的miRNA和前5个下调的miRNA,预测与它们相互作用基因。然后筛选了与基因芯片共表达的基因,为基因芯片中上调的基因与下调的miRNA预测的基因以及下调的基因与上调的miRNA预测基因的交集(图3)。选择差异最大的前5个下调的miRNA和前5个上调的miRNA用于互作网络分析(图4)。上调的miRNA预测靶基因与差异基因(下调)交集,如表2显示,GO分析的结果为这些差异基因主要与ω羟化酶P450途径、NO生物合成过程、氧化还原酶活性、芳香化酶活性、凋亡过程的正调控、氧结合、细胞增殖负调控等相关。下调的miRNA预测靶基因与差异基因(上调)交集,GO分析的结果显示与细胞成分运动的调节、凋亡过程、蛋白质磷酸化、细胞或亚细胞的运动、程序性细胞死亡等功能相关,见表3。

表1 上、下调差异表达的miRNA在年轻与老年表皮组织中的表达差异

表2 差异基因的功能富集分析(下调基因)
注:18个下调的基因参与的生物学进程。Note. Enrichment biological process analysis of 18 down-regulated genes.

注:A:由无监督聚类产生的热图,其将样品分成年轻人和老年人。B:两个芯片所有基因的火山图。
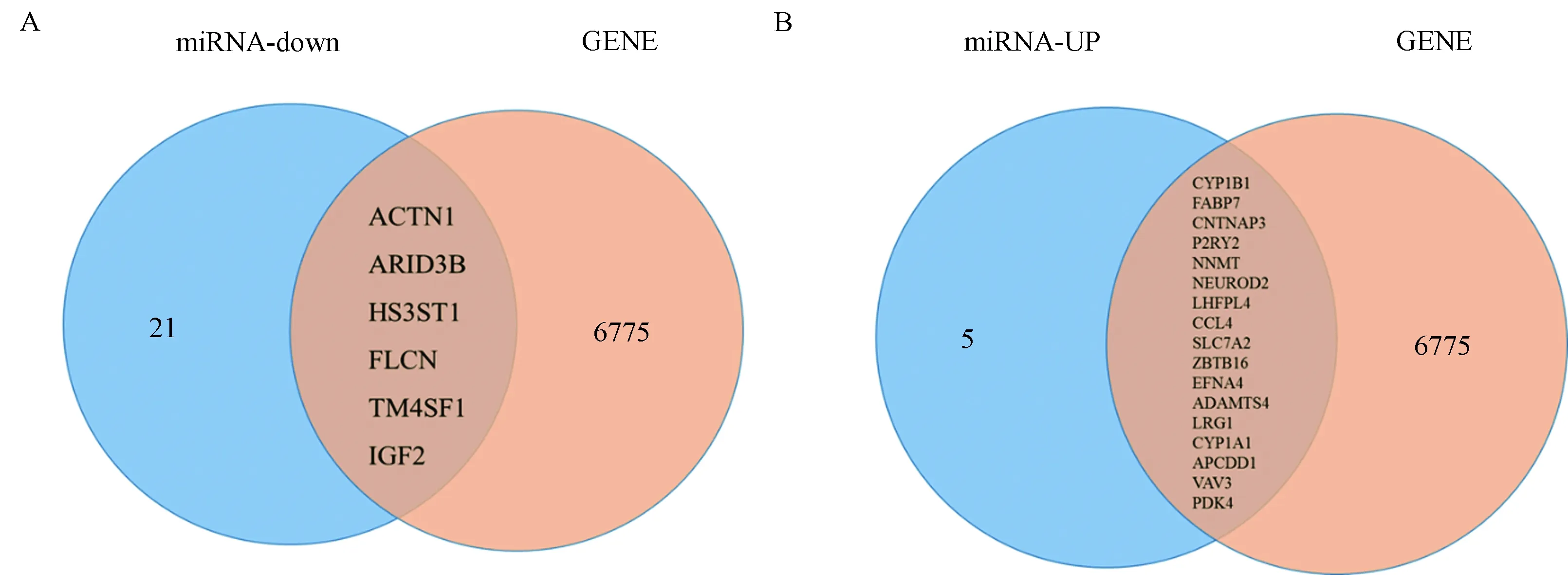
注:A:下调的micRNA与基因芯片中上调基因的交集。B:上调的micRNA和基因芯片中下调基因的交集。
2.4 核心基因相互作用和通路富集分析
将共表达的基因使用在线蛋白质相互作用预测软件(https://string-db.org/)筛选核心基因。随后,使用DAVID在线分析数据库对筛选的核心基因进行KEGG通路分析。保留P< 0.05的通路用于PPI作图。下调miRNA调控靶基因KEGG途径富集分析结果显示,该基因主要富集在局灶性粘连、PI3K/AKT信号通路、mTOR信号通路、蛋白质多糖的代谢通路。上调miRNA调控靶基因KEGG途径富集分析PPAR信号通路、趋化因子信号通路、PI3K/AKT信号通路、色氨酸代谢通路等。

表3 差异基因的功能富集分析(上升基因)
注:11个上调基因参与的生物学进程。Note. Enrichment biological process analysis of 11 up-regulated genes.

注:A:18个下调基因的KEGG通路分析。B:11个上调基因的KEGG通路分析。
3 讨论
这些发现表明,microRNA参与了人类表皮衰老的微调。最近的研究结果表明,miRNA作为一种新型基因表达调控因子在银屑病中发挥重要作用[12]。miRNA的成熟涉及多个步骤,此过程中依次生成两种中间形式的miRNA,即原代(pri)和前体(前)miRNA。同时,RNase III酶Drosha和配偶双链RNA(dsRNA)结合蛋白Dgcr8切割pri-miRNAs,其被Exportin5识别并随后从细胞核转运到细胞质的发夹形前pre-miRNA。另一个RNase III酶Dicer切割pre-miRNA以释放22nt核苷酸(nt)dsRNA双链体,即具有2nt 3’突出端的miRNA / miRNA双链体。miRNA双链中的一条链保存在RISC复合物中,另一条链则排出复合物外并迅速降解[13]。关于银屑病皮肤中异常表达的小ncRNAs(sncRNAs)的研究结果提示sncRNA在牛皮癣中的功能作用[12],大量实验结果显示在皮肤早期发育中占重要部分的miRNA也可以在银屑病中以关键的方式起作用。这与“生命早期出现错误可能会在生命后期再次出现错误”的理念是一致的。
为了解这些miRNA控制的机制,本课题组同时筛选了不同年龄表皮的mRNA表达谱。在与差异的miRNA预测的基因取交集之后,研究结果显示上调的miRNA调控的靶基因主要与细胞运动功能的调节、细胞凋亡、蛋白质磷酸化、细胞程序性死亡、有机氮化合物生物合成过程、RNA代谢过程的正调控、信号转导的正调控、大分子代谢调控等。下调的miRNA调控的靶基因主要与ω羟化酶P450途径、(NO)生物合成过程、氧化还原酶活性、芳香化酶活性、凋亡过程的正调控、氧结合、细胞增殖负调控等相关。特别值得注意的是上述信号通路往往是肿瘤组织异常激活的通路。上述结果提示衰老与肿瘤的发生发展有共同的信号通路参与。上调miRNA调控靶基因KEGG途径富集分析结果显示其主要富集在局灶性粘连、PI3K/AKT信号通路、mTOR信号通路、蛋白质多糖的代谢通路。上调miRNA调控靶基因KEGG途径富集分析PPAR信号通路、趋化因子信号通路、PI3K/AKT信号通路、色氨酸代谢通路等。值得注意的是,上调与下调miRNA调控的靶基因均对PI3K/AKT信号通路具有调控作用,同时mTOR信号通路、PPAR信号通路、趋化因子信号通路均在肿瘤的发生发展中起重点作用。这在某种程度上解释了皮肤肿瘤的发生发展病因。
目前在人类表皮衰老领域的miRNA研究较少,二代测序在鉴定miRNA并分析其在皮肤形态发生和体内平衡中的特定功能方面取得了重大进展。此研究从基因水平和miRNA水平多维度确定了参与并调控衰老的潜在原因,所预测的结果为衰老疾病的治疗和预测以及皮肤肿瘤疾病发生发展的机制研究提供了理论依据。
