重视ICU患者医院获得性急性肾损伤
2018-10-31史忠
史 忠
(陆军军医大学新桥医院急诊部,重庆 400037)
医院获得性急性肾损伤(hospital-acquired acute kidney injury,HA-AKI)是指患者入院后因某些医源性因素导致的急性肾损伤(AKI),在重症监护病房(ICU)发病率及病死率高,是导致患者预后不良的独立危险因素。遗憾的是,目前国内对HA-AKI的诊断被严重低估,漏诊率高达74.2%[1],对慢性肾脏病(CKD)和终末期肾病(end-stage renal disease,ESRD)的发生、发展将产生较大影响。因此,重视ICU患者HA-AKI的预防和诊治将成为重要任务,也是针对国际肾脏病学会(International Society of Nephrology,ISN)提出的急性肾损伤“0 by 25”的倡议,旨在实现至2025年无1例患者死于可预防的AKI的重大挑战[2]。
1 ICU患者HA-AKI流行病学现状
由于诊断AKI的标准和来源不同,不同时期不同文献所报道的ICU患者HA-AKI流行病学资料有很大差异,导致对HA-AKI发病率及严重性认识上存在较大偏差。
1.1AKI的概念及诊断标准 AKI的概念是从急性肾衰竭(acute renal failure,ARF)演变而来,目的是便于早期发现肾的病理生理变化及损伤过程。自2002年急性透析质量倡议(Acute Dialysis Quality Initiative,ADQI)指导组提出RIFLE分期诊断标准以来,2005年急性肾脏损伤网络(Acute Kidney Injury Network,AKIN)专家组在RIFLE基础上进行了修订和简化,建立了AKIN标准,确定了AKI的定义。2012年,改善全球肾脏病预后组织(Kidney Disease:Improving Global Outcome,KDIGO)又在RIFLE和AKIN基础上,提出了目前为止AKI最新的KDIGO诊断标准和分级标准[3],即48 h内血肌酐升高大于或等于26.5 μmol/L或血肌酐升高在7 d内超过基础值的1.5倍或尿量持续6 h少于0.5 mL·kg-1·h-1便可诊断为AKI。若血肌酐超过基础值1.5~1.9倍或尿量小于0.5 mL·kg-1·h-1持续6~12 h为1期AKI;血肌酐超过基础值2~2.9倍或尿量小于0.5 mL·kg-1·h-1持续12 h及以上为2期AKI;血肌酐超过基础值3倍或大于或等于354 μmol/L,尿量小于0.3 mL·kg-1·h-1持续24 h及以上或无尿大于或等于12 h,以及开始肾替代治疗者为3期AKI。这3个诊断标准及分期均是以血肌酐和尿量为主要指标,依据一定时间内在基线值上发生血肌酐的增高或尿量减少的程度来确定AKI诊断。事实上,AKI是一个由实质性损伤到功能性损伤的过程,血肌酐是反映肾功能性的指标,在已经有肾实质性损伤而肾小球滤过率(glomerular filtration rate,GFR)尚处在正常水平时血肌酐可不增高,只有在GRF严重下降时才发生明显变化,因此,它不是诊断AKI的敏感指标,其滞后性是导致AKI诊断延误或漏诊的主要因素。此外,在我国临床尿量监测管理中,通常计算24 h尿量,而忽略每小时公斤体质量尿量的变化,在早期诊断AKI的敏感性和准确性上存在客观的不足。尽管如此,这些诊断标准的提出,对目前AKI流行病学研究的同质性和可比性方面起到了促进作用。
1.2ICU患者HA-AKI流行病学现状 HA-AKI是ICU患者常见而严重的并发症,准确了解其流行病学资料对制订有效的预防措施、质量控制指导和临床研究方法设计均很重要。按照RIFLE、AKIN和KDIGO诊断标准,已经有一些ICU患者的HA-AKI流行病学资料,但多为单中心的研究。近几年,以KDIGO标准进行多中心队列研究已有不少报道,总体看,ICU患者的HA-AKI发病率远高于其他住院患者,增加了ICU患者处理的难度。
2015年,HOSTE等[4]首次以KDIGO分期标准进行了国际多中心AKI流行病学前瞻性调查(AKI-EPI),该研究涉及33个国家的97个综合ICU,研究结果表明,在1 802例入住ICU的患者中,1 032例在入住第1天便出现了AKI,发生率为57.3%,其中1期AKI为18.4%,2期AKI为8.9%,3期AKI为30.0%;随着AKI严重性增加其病死率逐步上升,死亡优势比(odds ratio,OR)值1、2、3期分别为2.19、3.88、7.18;在研究观察的1周期间,有23.5%的AKI患者接受了肾脏替代治疗,且大部分采用的是持续肾脏替代治疗(CRRT)。提示ICU中有50%以上患者发生AKI,由于肾损伤等级高,多需启动肾脏替代治疗,导致ICU患者HA-AKI伴发的病死率、住院时间及出院时肾功能未恢复的比率明显增加,这些结果对AKI患者将产生重要的经济和社会影响。
国内在HA-AKI流行病学调查方面,2013年南方医院在全国9家三级甲等医院开展了一项多中心回顾性AKI流行病学调查,AKI诊断及分期采用KDIGO标准,发现在14 305例入选的ICU患者中,AKI的发生率为30.04%,低于HOSTE等[4]报道的发生率,AKI 1、2、3期患者占比分别为52.1%、19.7%及28.2%,在出院时诊断为AKI者仅占5.4%,AKI病死率为16.7%,是非AKI患者的7.59倍,AKI 1、2、3期的死亡OR值分别为2.02、3.94和6.19,有58.75%的AKI患者肾功能没有恢复,其中8.6%的患者作了透析治疗[5]。2014年北京市30个ICU参与的多中心前瞻性AKI流行病学研究中,共纳入3 107例ICU重症患者,AKI诊断及分期分别采用RIFLE、AKIN和 KDIGO标准,发现AKI的发病率分别为46.9%、38.4%和51.0%,病死率分别为27.8%、32.2%和27.4 %[6]。2015年YANG等[1]在柳叶刀杂志上报道了国内多中心AKI流行病学的横断面研究,指出在住院患者中AKI的发病率为1%~2%,病死率为12.4%,AKI漏诊率为74.2%,未报道ICU患者AKI相关的流行病学资料。最近,以哈尔滨医科大学附属第二医院牵头的中国ICU成人AKI最大的横断面研究方案已经公布,该方案为全国性多中心前瞻性随机临床研究,涉及23个省、4个直辖市及5个自治区的35家医院约6 147例患者,将从中国ICU成人AKI的流行病学、病因、危险因素、预后与治疗及ICU医务人员的策略与认知5个方面进行调查,期待该研究将为我国AKI的诊断、治疗提供更科学的理论基础和标准的方法,解决AKI被低估和预后不良的问题[7]。
2 ICU患者HA-AKI危险因素评估
AKI是入住ICU危重患者致命和致残的严重并发症。一些研究已经确认小量血肌酐增加与肾不良事件发生的关系,提出准确识别存在发生AKI风险的人群及早期认识AKI的发生将可能为AKI的诊断、预防和治疗干预提供机会。在如何评估ICU患者发生HA-AKI风险方面,过去10年虽然有一些在特殊临床情况下预测AKI风险分层的评分,也有为数不多的针对ICU人群发生AKI的临床危险因素,但多为单中心研究或样本量太小,缺乏有效的验证。血肌酐和尿量是临床常用反映肾功能状态的指标,但在预测AKI方面并不敏感,诊断AKI需要重复的血肌酐测定,也常受许多因素的限制和干扰,难以早期准确反映AKI发生的风险。因此,寻求新的评估AKI风险和早期诊断的方法对早期肾保护非常重要。
2.1肾脏损伤生物标志物 近几年,利用肾损伤生物标志物来预测AKI增加的风险成为了研究的热点,目前这些新的肾损伤标志物包括:代表肾脏细胞周期停滞的标志物胰岛素样生长因子结合蛋白7(insulin-like growth factor-binding protein 7,IGFBP 7)及组织抑制剂金属蛋白酶-2(tissue inhibitor of metalloproteinases-2,TIMP-2);代表肾小管损伤的标志物肾损伤分子-1(kidney injury molecule-1,KIM-1)、中性粒细胞明胶酶相关脂蛋白(neutrophil gelatinase-associated lipocalin,NGAL)、白细胞介素-18(interleukin-18,IL-18)、脂肪酸结合蛋白(lipid acid-binding protein,L-FABP)及β2-微球蛋白(β2-microglobulin);代表GFR的标志物半胱氨酸蛋白酶抑制剂(cystatin C)等。不少Meta分析研究认为,这些新的标志物对早期预测ICU患者AKI的风险具有良好价值,预测成人AKI的曲线下面积(AUROC)≤0.8,预测儿童AKI的AUROC≥0.95,即在儿童预测方面更具有优势,预测的敏感性和特异性范围取决于标志物的性质、标本的类型(血浆或尿)及定义AKI的阈值水平[8]。尽管如此,以诊断AKI为目的,目前尚无有关联肾损伤标志物的随机对照研究,且单独基于标志物的预测策略价格高昂,难以被临床常规使用,并因存在患者个体的临床异质性容易出现预测失败。因此,目前尚不推荐应用肾脏标志物用于早期诊断AKI。BASU等[9]认为将标志物与临床资料结合,可提高ICU患者严重AKI风险预测的准确性。
2.2临床危险因素评估 最近,MALHOTRA等[10]通过前瞻性多中心的队列研究,提出了ICU中AKI危险因素预测评分。该研究对象选自美国加州大学外科(UCSD)ICU和内科ICU的1 117例及梅奥诊所综合ICU的1 486例患者,在ICU入住48 h内利用血肌酐作为标志物按照KDIGO标准进行筛查,排除CKD 5期、血液透析及已明确有AKI的患者后,美国加州大学有717例、梅奥诊所有1 300例患者入选。研究终点为患者入选后7 d内发生AKI的情况,以48 h内肌酐上升超过0.016 7 mmol/L或7 d内肌酐上升超过50%定义为AKI。通过对25项急慢性临床危险因素的筛选,最终选定了10项急慢性指标作为发生AKI的高危因素(表1),设定的最大积分为21分,最小积分为0分,并以截断分值大于或等于5分确定为最有可能发生AKI的最佳分值。在这个评分系统中,有些危险因素在既往的研究报道中已经确认,如CKD、慢性肝脏疾病、充血性心力衰竭、高血压、肾毒性药物暴露及脓毒症等,在此基础上,该研究又提出了酸中毒、粥样冠状血管疾病、机械通气和贫血作为预测ICU患者AKI风险的指标,认为酸中毒和贫血是潜在可调节的危险因素,可以作为治疗纠正的目标。在这项队列研究中,利用该危险评分系统,发现了40%的ICU患者存在AKI高风险,其中23%可能在24 h内发生AKI,而分值小于5分的患者96%未发生AKI,预测的准确性在UCSD和梅奥队列研究中的AUROC分别为0.79和0.81,优于BASU等[9]报道的肾脏绞痛指数(renal angina index,RAI)的预测价值(AUROC为0.74),后者对预测已有AKI患者从普通病房到ICU,以及预测入住ICU的中度AKI开始向重度AKI转变的可能性是有效的[11]。因此认为,该评分是预测ICU患者早期AKI风险简单可靠的实用工具,特别是血肌酐值未达到诊断标准时,若能结合AKI相关标志物的检测结果,对ICU患者AKI的早期识别、诊断、干预和预后的改善有很大的帮助。
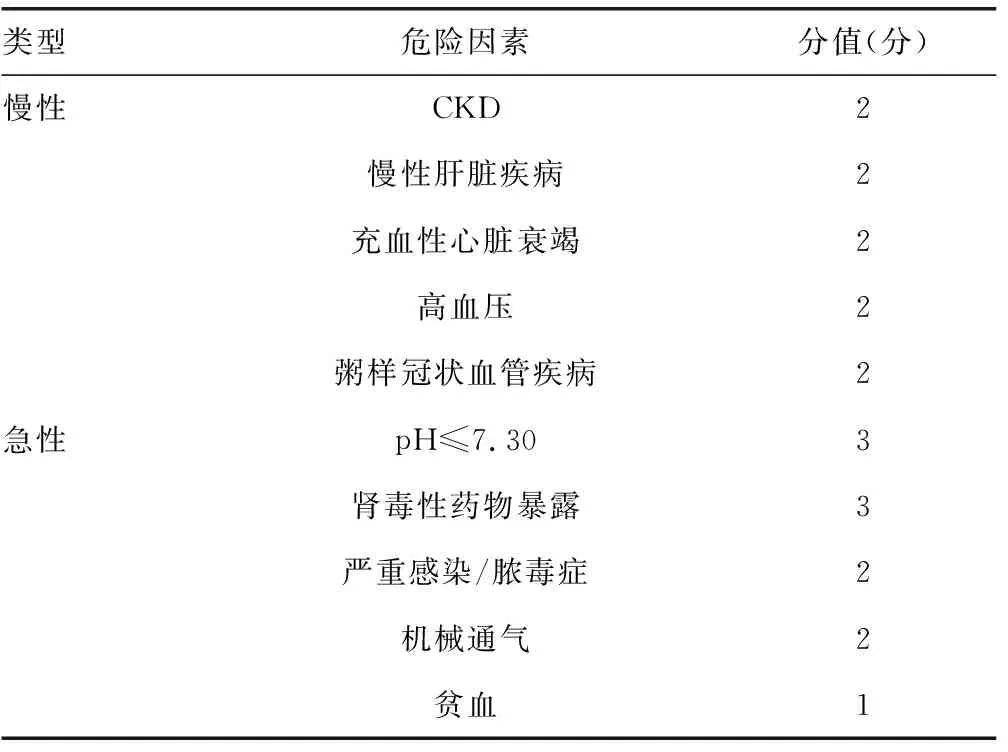
表1 ICU中AKI危险因素预测评分
最小积分:0分;最大积分:21分
3 ICU患者HA-AKI的预防及肾功能保护
ICU患者发生HA-AKI涉及多种因素,包括在原有疾病基础上增加的肾前性、肾性和肾后性高危因素。目前认为,危重患者中导致AKI最常见的原因是脓毒症、低血容量和肾毒性药物。在如何预防ICU患者HA-AKI发生及保护肾功能方面,《Intensive Care Medicine》杂志发布了2017新指南[12]。该指南系统评价了MEDLINE (1966-2017)、EMBASE (1980-2017)、CINAHL(1982-2017)、Web (1955-2017)及PubMed等数据库收集的关于预防AKI及保护肾功能方面的随机对照研究(RCT)和Meta分析,以相关理论基础和临床研究为依据,提出了预防ICU患者AKI和保护肾功能的推荐意见,为有效预防AKI的发生提供了帮助。
3.1适当扩容治疗可降低AKI风险 各种原因引起机体相对或绝对的容量不足是发生AKI的重要危险因素,适时地扩容治疗能恢复循环血量和肾脏灌注,降低肾毒性和AKI的风险。扩容治疗中应严密监测,避免容量负荷过度,减少因液体成分、肾间质水肿和肾实质压力增加促使AKI发生的风险。在液体的选择上,由于存在渗透性肾病、组织胺释放及凝血病发生的可能,不推荐使用羟乙基淀粉、明胶和右旋糖酐液体用于液体复苏。低血容量或脱水时,对比剂的使用潜在增加AKI的风险,对接受血管内造影的患者,推荐使用等渗晶体液纠正低血容量或脱水。高氯性酸中毒有使肾皮质血管收缩导致AKI的可能,当使用含氯液体(如生理盐水、复方氯化钠等)时应常规监测血氯和酸碱水平。若大量液体复苏建议使用平衡晶体液。当脓毒症休克确实需要用胶体液治疗时建议使用人血清蛋白,但不单独用于扩容治疗。低血容量也有利于药物性肾损伤的发生,为预防使用某些药物如两性霉素B、抗病毒药物膦甲酸钠、西多福韦和阿德福韦及引起晶体肾病的药物茚地那韦、阿昔洛韦和磺胺嘧啶等引起的AKI,建议使用晶体液进行预防性容量扩张。对急诊增强扫描,建议不要因为存在潜在AKI风险而延误检查。
3.2科学合理使用救治药物 少尿时ICU医生经常使用髓袢利尿剂,其目的是通过预防肾小管梗阻、降低肾髓质氧耗、增加肾血流及降低液体超负荷和静脉充血来改善AKI。曾有研究表明,给予1~1.5 mg/kg呋塞米后至少利出超过100 mL/h的尿量,预测可降低分级较高AKI少尿患者的进展。但在多个RCT研究及Meta分析中,没有证实利尿剂能改善AKI的结局,如肾功能恢复和死亡率,还伴随较大的药物副作用风险[13]。对心力衰竭患者,大剂量利尿剂虽可明显缓解症状,但以降低肾功能为代价,因此,不推荐单纯以预防AKI为目的使用髓袢利尿剂,为控制或避免液体超负荷,可对利尿剂有反应的患者使用利尿剂。
理论上,液体复苏、正性肌力药、肾血管扩张剂、血管升压药能达到保护或改善肾灌注的效果。在升压药的使用上,如何选择理想目标平均动脉压(MAP)是关键点。针对脓毒症休克复苏的多中心RCT研究表明,将目标MAP设定为80~85 mm Hg和65~70 mm Hg,其死亡率、AKI 2期或需要肾替代治疗的发生率两组没有差异,但80~85 mm Hg组有更多的房颤发生;而在严重高血压伴发急性脑出血的RCT研究表明,收缩压140~179 mm Hg组肾功能恶化的发生率较110~130 mm Hg组低。因此,对于脓毒性休克患者推荐滴定升压药物维持目标MAP于65~70 mm Hg,而存在慢性高血压的脓毒性休克患者应将目标MAP维持在80~85 mm Hg,以利于肾脏保护;对严重高血压伴急性脑出血患者,推荐将入院收缩压控制在140~190 mm Hg;若需要升压药物治疗低血压,推荐去甲肾上腺素(同时纠正低血容量)作为首选升压药保护肾功能;而对心脏手术后血管麻痹性休克患者建议给予血管加压素,并根据发病前的血压制订个体化目标血压[14-15]。
缺血性AKI早期,交感神经系统的激活及血管收缩物质的释放,如内皮素、血管紧张素Ⅱ和前列腺素均可使肾血流量(RBF)下降。而脓毒性AKI,总的肾血流量并无改变,灌注不足主要发生在髓质外微血管区域。当以肾保护为目的使用血管扩张剂时,应首先考虑有无因抵消代偿性血管收缩使隐蔽的低血容量暴露,加重肾灌注损伤的问题;其次,因内皮细胞损伤选用依赖一氧化氮作用的血管扩张剂可能无效;此外,微循环已闭塞时的延迟给药会降低有效性。至于小剂量多巴胺具有肾保护的观点已趋于否定,无论是预防还是改善AKI方面均无益处。不推荐纯多巴胺A1受体激动剂非诺多巴、钙增敏剂左西孟旦及利钠肽用作对心脏手术及危重患者的肾功能保护[16-17]。
丙泊酚和右美托咪定是ICU患者常使用的镇静药。动物研究发现,丙泊酚能降低肾氧化应激,右美托咪定能降低血管加压素分泌,通过增加肾血流量和GFR具有肾保护作用。但RCT研究提示,二者肾保护效果轻微且不完全确定,同时,也存在“丙泊酚输注综合征”即输注后发生肌病、横纹肌溶解、高钾血症及AKI的问题,因此,建议丙泊酚的使用时间最多48 h,最大剂量4 mg·kg-1·h-1[18-19]。
在ICU患者的代谢性干预中,目标血糖应控制在10 mmol/L以下,避免高血糖或低血糖对肾脏产生的危害。类固醇激素或促红细胞生成素(EPO)虽对某些肾脏疾病有一定作用,但不建议用于AKI的预防。对所有AKI或有AKI风险的患者,适当的营养支持有助于肾的保护和改善,最好选择肠内途径。作为营养辅助因子,谷氨酰胺前体N-乙酰半胱氨酰由于存在过敏反应、降低心排量或涉及脓毒症休克等副作用,不建议用于预防危重患者造影对比剂相关性AKI,也不推荐大剂量静脉使用硒剂作为危重患者的肾保护[20-21]。他汀类药物具有抗氧化、抗炎和抗血栓的作用,RCT研究认为,对暴露于血管造影对比剂的高风险患者可能有助于肾保护,建议对冠状动脉血管造影高风险患者,短期使用阿托伐他汀或瑞舒伐他汀预防对比剂相关性AKI,但不推荐心脏手术围术期高剂量使用他汀类药物预防术后AKI[22-23]。
3.3加强对肾毒性药物的监测与调控 ICU患者药物性AKI发生率较高,多与药物的不合理使用及缺乏监测有关。常见肾毒性药物包括放射性造影剂、抗生素(氨基糖甙类、头孢、磺胺类、两性霉素、阿昔洛韦)、非甾体抗炎药、血管紧张素转换酶抑制剂和受体抑制剂、抗肿瘤药物(甲氨蝶呤、顺铂)、免疫抑制剂(环孢素、他克莫司)、高渗性药物(甘露醇)等[24]。对AKI高风险患者,应高度重视药物的选择,对药物的代谢、药代动力学/药效学(PK/PD)特点、药物剂量、疗程、合并用药的相互作用等应充分了解,加强对特殊药物的监测,适时合理调控,早发现、早治疗。
4 结 语
ICU中HA-AKI是导致患者结局不良的重要因素,在当前面临对HA-AKI评估和诊断不足的情况下,重视和加强ICU患者的风险评估、识别和预防措施,对减少AKI的发生和发展,降低肾替代治疗需求率和时间,控制CKD的发生将有重要意义。
