原子吸收标准加入法测定硫酸铝中的铁
2018-10-29章文华应琦琰马凯迪徐锡梅赵赛君UlrikeStadtmller刘洪波
章文华,应琦琰,马凯迪,徐锡梅,彭 慧,赵赛君,Ulrike Stadtmüller,刘洪波
(1.苏州工业园区清源华衍水务有限公司 水质检测中心,江苏苏州 215021;2.上海理工大学环境与建筑学院,上海 200093;3.莱茵美茵应用技术大学工程学院,德国吕塞尔斯海姆 65428)
液体硫酸铝是一种重要的水处理剂,其作为净化水质的原材料,被广泛应用于污水处理厂和自来水厂[1]。硫酸铝中铁的质量分数是一个重要的技术指标[2]。溶液中铁离子的测定方法有原子吸收法、极谱法、重铬酸钾法、容量法、分光光度法等[3-5]。目前,国家标准规定的测定硫酸铝中铁含量的方法是邻菲罗啉分光光度法[6]。该方法具有取样少、分析快、简便、准确和灵敏度高等优点[7-8]。但该法所用试剂种类多,对反应的pH条件要求比较高,操作步骤多,而显色剂邻菲罗啉有效期短,需要经常配制[9]。采用火焰原子吸收法测定铁含量, 样品预处理方法简便, 有较好的精密度和回收率, 且与邻菲罗啉分光光度法相比,结果无差异,可作为测定水处理剂硫酸铝中铁的首选方法[10]。原子吸收法中标准曲线法最为常用, 使用也方便,但是只有当基体对响应值完全没有影响时才能采用标准曲线法[11]。试验证明,该水厂使用的硫酸铝在测定铁含量时基体干扰严重,故采用标准加入法测定液体硫酸铝中的铁[12-18]。测定结果与国标法无显著差异,且预处理方法简单,精密度、准确度都符合测定要求,只是分析速度慢,不适合分析大批量的样品。
1 试验材料与方法
1.1 试验仪器
原子吸收分光光度计ICE3500(赛默飞公司);紫外可见分光光度计E300(赛默飞公司);赛多利斯电子天平BSA6202S(d=0.01);纯水器Milli-Q Direct 8(密理博公司);可调低温电炉;铁空心阴极灯。
1.2 试验药品
样品A:本司水厂所用液体硫酸铝。
样品1~6∶6种不同的液体硫酸铝,其中铁的质量分数为0.000 8%~0.001 5%。
试液A:称取36.39 g液体硫酸铝样品A,精确至0.01 g,置于250 mL烧杯中。加入100 mL水和2 mL浓盐酸,加热并煮沸5 min,取下冷却,纯水定容于500 mL容量瓶,摇匀,备用。
铁标准溶液(500 mg/L,环境保护部标准样品研究所GSB 07-1286-2000批次102508);铁标准使用液(10 mg/L);盐酸溶液(优级纯);乙酸钠溶液(272 g/L);氯化锌标准滴定溶液(0.025 mol/L);乙二胺四乙酸二钠(EDTA)标准溶液(0.05 mol/L);二甲酚橙指示液(2 g/L);纯水(产自Milli-Q纯水器)。
1.3 试验原理
(1)原子吸收法试验原理
铁空心阴极灯发射出的一定强度和一定波长的特征谱线的光,通过含有铁基态原子蒸气的火焰时,部分特征谱线的光被基态原子吸收,而未被吸收的光经单色器照射到光电检测器上被检测,根据该特征谱线光被吸收的程度,可测得试样中铁的含量。
仪器条件:灯电流为 9 mA;波长为248.3 nm;狭缝宽为0.2 nm;点灯方式为 BGC-D2。
(2)原子吸收标准加入法测定原理
将不同量的标准溶液分别加入数份等体积的试液中,其中一份试液不加标准溶液,均稀释至相同体积后测定(同时制备样品空白)。以测定溶液中外加的标准溶液的浓度为横坐标,以吸光度为纵坐标对应作图,然后将直线延长使之与浓度轴相交,交点对应的浓度绝对值即为试液中待测元素的浓度Cx。
1.4 试验方法
(1)分别用邻菲罗啉分光光度法、原子吸收标准曲线法和原子吸收标准加入法测定试液A中铁的含量,对比试验结果。发现,原子吸收标准加入法测定试液A中铁含量结果与国标法邻菲罗啉分光光度法的结果均符合测定偏差,而标准曲线法有较大偏差。
(2)通过分析原子吸收标准曲线与标准加入法曲线,探究样液基体对吸光度的干扰。
(3)取样品1~6进一步分析原子吸收标准加入法的准确性及优劣势。
2 结果与讨论
2.1 三种方法测定试液A中的铁含量
2.1.1 邻菲罗啉分光光度法测定试液A中的铁含量
按国家标准GB 31060—2014中的邻菲罗啉分光光度法测定液体硫酸铝中的铁含量,测得铁的质量分数为0.001 2%。因此36.39 g硫酸铝定容于500 mL容量瓶中后,换算得到容量瓶中试液A的铁含量为0.873 mg/L。本文以国标法测得的数据,即0.873 mg/L作为真值参与讨论。
2.1.2 原子吸收标准曲线法测定试液A中的铁含量
(1)原子吸收标准曲线法
通过将试液A稀释不同的倍数测定其铁含量。分别将试液A于容量瓶中稀释1、2、5、10、20倍,用1%硝酸溶液定容,摇匀。原子吸收分光光度计分别连续测定3次,取平均值,结果如表1所示。
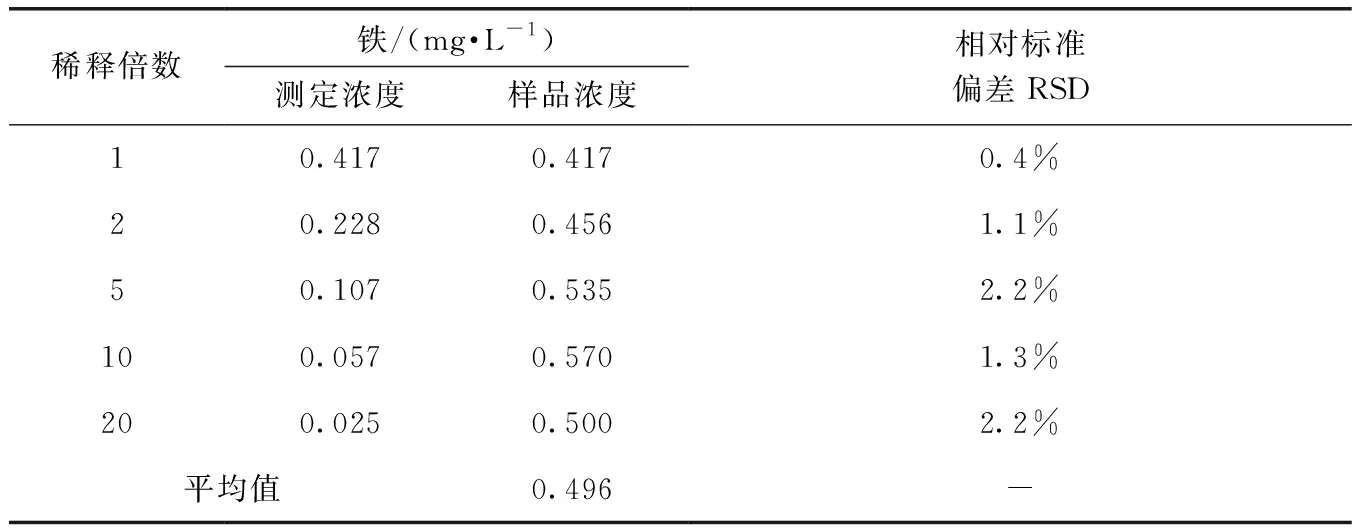
表1 试液A不同稀释倍数下的铁含量Tab.1 Iron Content of Test Solution A at Different Dilution Times
由表1可知,标准曲线法测得的铁含量平均值(0.496 mg/L)与国标法邻菲罗啉分光光度法测得的真值(0.873 mg/L)的绝对误差为0.377 mg/L,相对误差达43.2%。说明,试样内存在基体干扰,需要做加标回收试验进一步确认。
(2)加标回收率试验
分别取试液A 20 mL于8个100 mL容量瓶中,依次加入0.00、1.00、2.00、2.50、4.00、6.00、8.00、12.00 mL的铁标准使用液,其加标浓度依次是0.00、0.10、0.20、0.25、0.40、0.60、0.80、1.20 mg/L。用1%盐酸定容至100 mL,摇匀,测定,结果如表2所示。
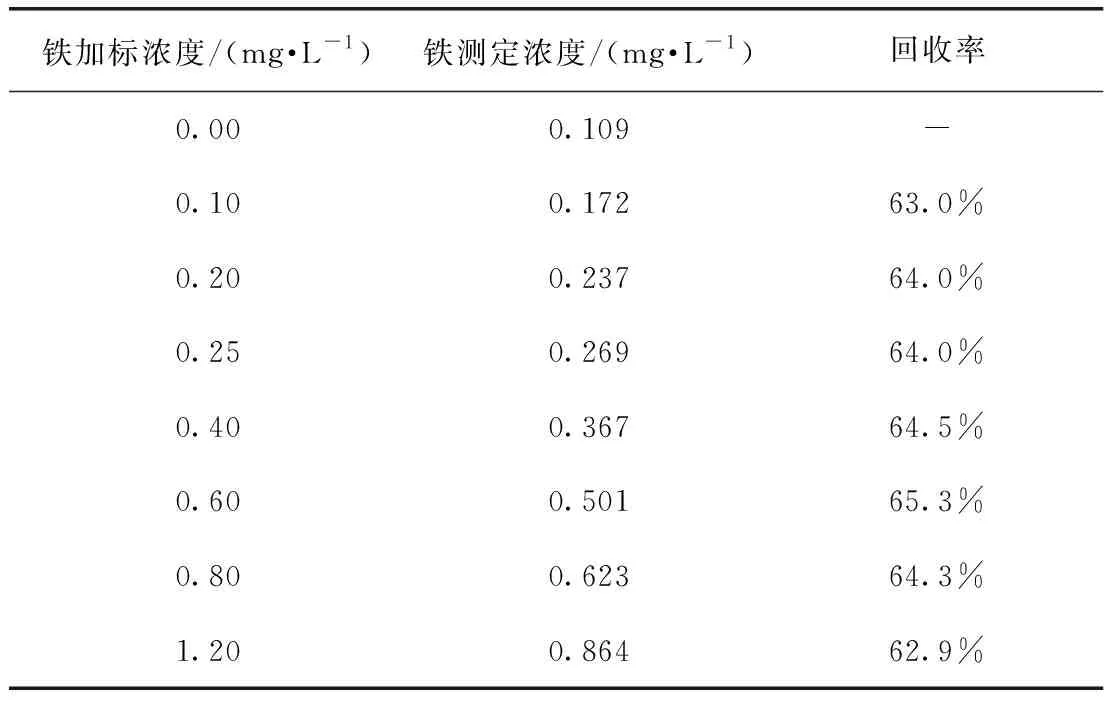
表2 加标回收率试验Tab.2 Standard Addition Recovery Test
由表2可知,加标回收率均低于85%,进一步说明试样内存在基体干扰,标准曲线法测得的试验结果与实际结果有较大偏差。因此,标准曲线法不适用于测定液体硫酸铝中的铁含量。
2.1.3 原子吸收标准加入法测定试液A中的铁含量
标准加入法曲线制作:分别吸取试液A 20 mL于5个100 mL容量瓶中,再依次加入0、2、4、6、8 mL的铁标准使用液,用1%的硝酸溶液定容至刻度线,摇匀。原子吸收操作软件的校正方法里选择“标准加入:线性最小二乘法拟合”,根据系统提示,依次进样、测定。得到标准加入法曲线回归方程为y=0.050 39x+0.008 70,线性相关系数r=0.999 9。由此得到试液A中的铁浓度为0.890 mg/L,如图1所示。该法与国标法邻菲罗啉分光光度法测得的真值(0.873 mg/L)相对偏差为1.0%,因此标准加入法符合硫酸铝中铁含量的分析检测要求。
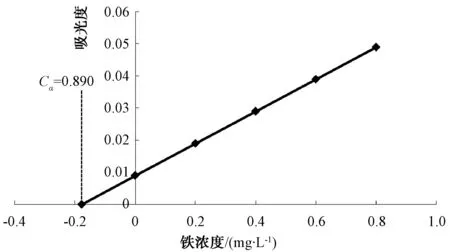
图1 试液A中铁浓度的标准加入法曲线Fig.1 Standard Addition Curve of Iron Content of Test Solution A
2.2 样液基体对吸光值的影响
标准曲线的制作:以10 mg/L的铁标准使用液,配制7个浓度分别为0.00、0.10、0.20、0.40、0.60、1.00、1.25 mg/L的标准溶液,用1%盐酸溶液分别定容于100 mL的容量瓶中,摇匀。采用火焰原子吸收分光光度计测定标准溶液。原子吸收操作软件的校正方法里选择“一般:线性最小二乘法拟合”。根据系统提示,依次进样,以铁的浓度对吸光值作图绘制标准曲线,测定完毕得到回归方程为y=0.095 69x+0.001 40,线性相关系数r=0.999 9。将上述标准曲线与标准加入法曲线(y=0.050 39x+0.008 70,r=0.999 9)绘制比较,如图2所示。
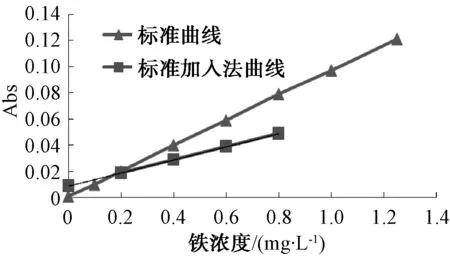
图2 试液A中铁浓度的标准曲线和标准加入法曲线Fig.2 Standard Curve and Standard Addition Curve of Iron Content of Test Solution A
由图2可知:(1)两者线性相关系数均为0.999 9,说明铁浓度与吸光度近似完全线性相关;(2)标准加入法分析曲线表现出线性相关性,说明所获取的分析数据信息真实且可靠[12-13];(3)标准曲线的斜率大于标准加入法曲线的斜率,说明硫酸铝溶液基体对铁元素的测定干扰很大,且样液基体
对吸收产生负干扰。
一般常见元素对测定铁无干扰,只有硅浓度大于20 mg/L时对铁有负干扰[19]。说明该水厂所使用的液体硫酸铝中可能含有浓度较高的硅,对标准曲线的测定产生干扰。当标准曲线法与标准加入法的斜率基本相同时, 不必应用标准加入法;如果两者的斜率有极大的不同, 则标准曲线法无效, 应使用标准加入法[11]。为了克服基体干扰对测定的影响,可采用原子吸收的标准加入法来测定硫酸铝中的铁含量。宋寅生等[20]和周虹等[21]同样应用火焰原子吸收法测定水处理剂硫酸铝中的铁,但使用标准曲线就得到了与国标法相似的结果,表明其使用的硫酸铝中基体的干扰影响不大,说明不同厂家生产的水处理剂硫酸铝成分存在差异。这对于不同地区不同厂家生产的硫酸铝具有实际意义,若基体干扰不影响,可只用标准曲线得到结果;若基体干扰影响严重,则可用标准加入法消除干扰,得到准确结果。
2.3 原子吸收标准加入法
2.3.1 原子吸收标准加入法测定铁浓度
分别称取6种不同的液体硫酸铝样品1~6,每种样品称取约37 g,精确至0.01 g,置于250 mL烧杯中,加入100 mL纯水和2 mL盐酸,加热并煮沸5 min,取下冷却,定容于500 mL容量瓶,摇匀,备用。
从上述制备好的试液中每种分别吸取 20 mL于5个100 mL容量瓶中,再依次加入0、2、4、6、8 mL的铁标准使用液,用1%的盐酸定容至刻度,摇匀。其余5种试液的操作步骤相同。在248.3 nm波长下,用火焰原子吸收的标准加入法分别测定6个系列溶液的吸光度,每个溶液重复测定6次,取平均值后从上述标准加入法曲线上得出铁含量,结果如表3所示。
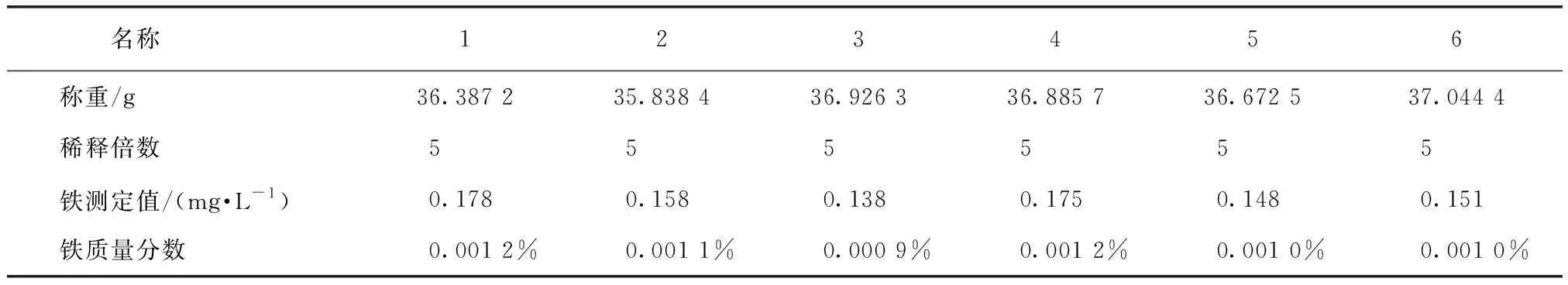
表3 标准加入法测定6种样品的试验结果Tab.3 Experimental Results of Six Samples Determined by Standard Addition Method
2.3.2 邻菲罗啉分光光度法测定铁浓度
分别取2.3.1中制备好的6种硫酸铝样品试液10 mL于100 mL容量瓶中,加水至40 mL左右,加0.5 mL H2SO4,调pH值接近2,加3 mL抗坏血酸,10 mL乙酸-乙酸钠,5 mL邻菲罗啉,用水稀释至刻度,摇匀,放置15 min,在波长510 nm处用30 mm比色皿测定。结果如表4所示。
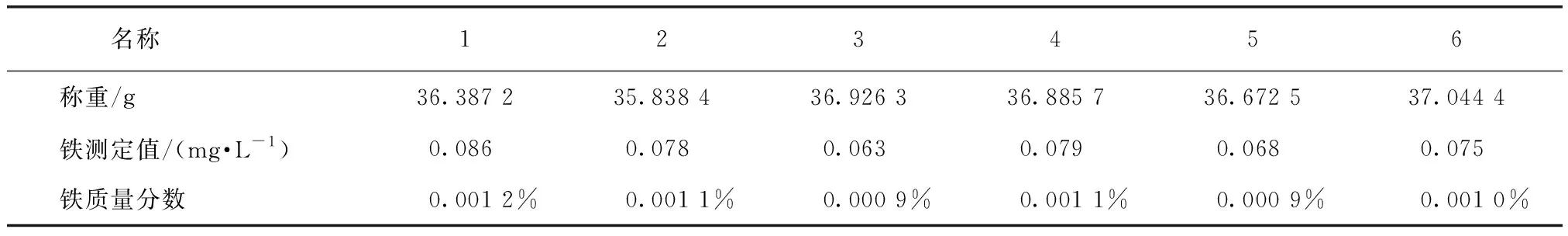
表4 邻菲罗啉法测定6种样品的试验结果Tab.4 Experimental Results of Six Samples Determined by Phenanthroline Method
2.3.3 两种方法的测定结果比较
根据试验结果比对,采用火焰原子吸收法中的标准加入法测得的铁质量分数与邻菲罗啉分光光度法测得的数据无显著差异。比较两种方法的试验过程可以发现,标准加入法试验操作方法简便,而邻菲罗啉分光光度法所用试剂种类多,对反应的pH条件要求比较高,操作步骤多。说明,标准加入法在测定该水厂硫酸铝中铁的质量分数中,可一定程度上替代国标法邻菲罗啉分光光度法。
2.3.4 标准加入法的精密度试验
选用样品浓度为0.10、0.20、0.40、0.60、1.00、1.25 mg/L的6种铁溶液,重复测定6次,直接从电脑上读出标准偏差及相对标准偏差的值,结果如表5所示。
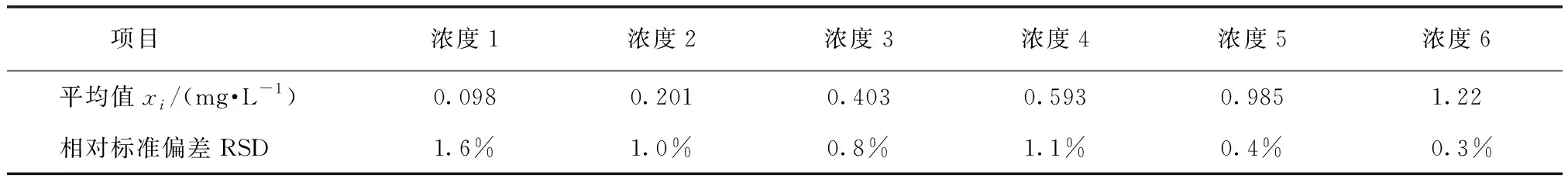
表5 精密度测定结果Tab.5 Results of Precision Experiment
由表5可知,标准加入法测定铁的相对标准偏差<5%,满足分析要求,说明标准加入法的精密度较好,可获得准确的试验结果。
2.3.5 标准加入法的分析速度
标准加入法一般用于测定低浓度的样品,为了得到准确的结果和较好的精密度,分析每个样品都必须进行2~3次加标试验,因此标准加入法的分析速度比标准曲线法慢得多。在测定该水厂硫酸铝中铁含量时,若样品数量较少,标准加入法明显优于邻菲罗啉分光光度法;但若样品数量较大,标准加入法的分析速度慢,不适合分析大批量的样品。
3 结论
采用原子吸收法测定水处理剂液体硫酸铝中铁的质量分数时,若液体硫酸铝样品中的基体干扰严重,原子吸收法中的标准曲线法不能用于测其铁含量。选用原子吸收标准加入法则可消除基体干扰,获得准确的结果和较好的精密度,与国标法邻菲罗啉分光光度法测定结果相比无显著差异,且操作方法简便,成本较低。但是原子吸收标准加入法分析速度慢,不适合分析大批量样品。在非大批量样品分析的前提下,优先考虑使用原子吸收标准加入法测定液体硫酸铝中的微量铁含量,不仅简化试验过程,且节约试验成本,可保证结果的准确性。
